Hoofdstuk 2 Paragraaf 6 Een nieuwe eenheid de


























- Slides: 31

Hoofdstuk 2 Paragraaf 6 Een nieuwe eenheid: de mol

De wetenschappelijke notatie. In de wetenschappelijke notatie schrijf je een getal in de vorm: a. . 10 b Hierin is a een getal met één cijfer vóór. . . de komma Voorbeelden: 235, 6 =. . . . 2, 356. 102 0, 00000345 =. . . 3, 45. 10⁻ 6 61 6, 1. 101 =. . . 1, 470. 10⁻ 2 = 0, 01470. . .

Iets wat je kunt meten, noem je een. . . . grootheid Een grootheid geef je weer met een getal, gevolgd door de eenheid. . . . stelsel is een internationaal stelsel van Het SI eenheden (zie Binas, tabel 3 en 4) Voorbeelden: kilogram is een grootheid / eenheid oppervlak is een grootheid / eenheid temperatuur is een grootheid / eenheid tijd is een grootheid / eenheid seconde is een grootheid / eenheid

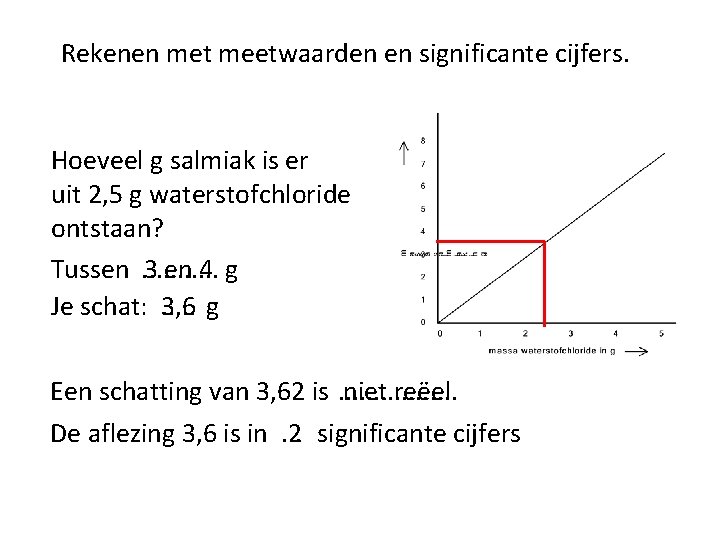
Rekenen met meetwaarden en significante cijfers. Als je ammoniak met waterstofchloride laat reageren, ontstaat salmiak: NH 3(g) + HCl(g) In een diagram is het aantal gram waterstofchloride uitgezet tegen het aantal gram salmiak: NH 4 Cl(s)

Rekenen met meetwaarden en significante cijfers. Hoeveel g salmiak is er uit 2, 5 g waterstofchloride ontstaan? Tussen. . . 3 en 4 g Je schat: . . . 3, 6 g Een schatting van 3, 62 is. . . . niet reëel De aflezing 3, 6 is in. . . 2 significante cijfers

Rekenen met meetwaarden en significante cijfers. Het getal 803, 0 is in. . . 4 significante cijfers Het getal 0, 00045 is in. . . 2 significante cijfers

Rekenen met meetwaarden en significante cijfers. Bij vermenigvuldigen of delen wordt het antwoord afgerond in het aantal significante cijfers van de meetwaarde met de minste. . significantie 8, 0 x 3, 4567 =. . . 28 0, 0045 x 3, 6789 = 0, 017. . Bij optellen of aftrekken is het aantal decimalen van het antwoord gelijk aan de meetwaarde met het minste. . . aantal decimalen. . . 3, 825 – 0, 4 = 3, 4 2100 + 0, 4 =. . 2100

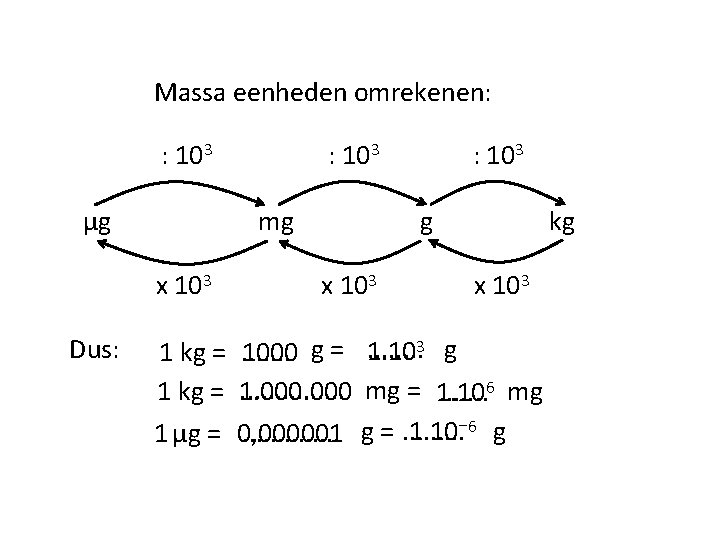
Massa eenheden omrekenen: : 103 μg mg x 103 Dus: : 103 1 kg = 1 μg = : 103 g x 103. . . . 1000 g =. . . . 1. 000 0, 000001. . . kg x 103 . . . . 3 g 1. 10 mg = 1. 10. . . . 6 mg g =. . 1. 10⁻ 6 g

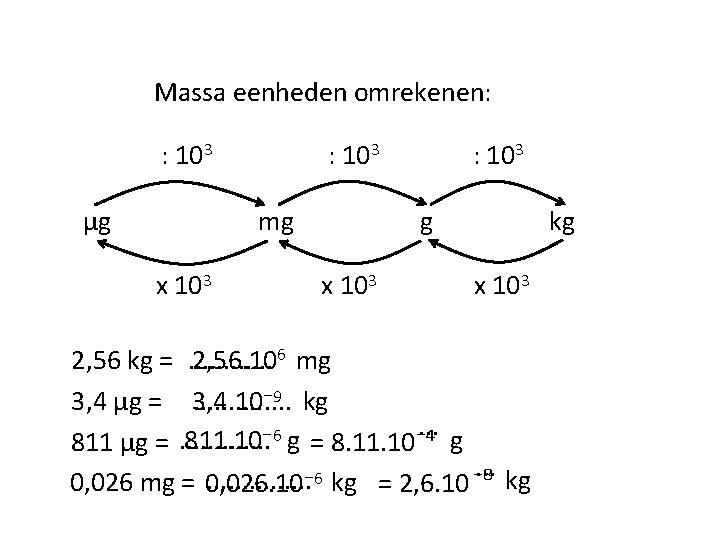
Massa eenheden omrekenen: : 103 μg : 103 mg x 103 : 103 g x 103 kg x 103 2, 56. 106 mg 2, 56 kg =. . . 9 kg 3, 4 μg = 3, 4. 10⁻. . . . 6 811. 10⁻ g = 8. 11. 10⁻ 4 g 811 μg =. . . . 6 kg = 2, 6. 10 ⁻. . . 8 kg 0, 026 mg = 0, 026. 10⁻

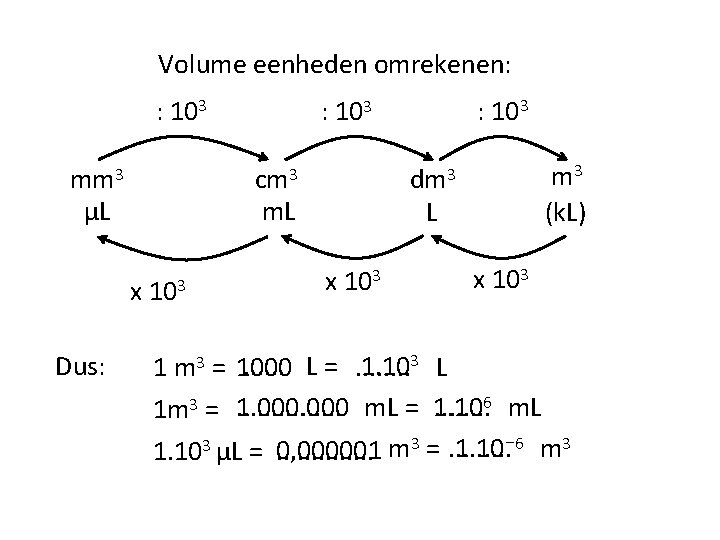
Volume eenheden omrekenen: : 103 mm 3 μL cm 3 m. L x Dus: 103 : 103 m 3 (k. L) dm 3 L x 103 1. 103 L. . . L =. . . . 1 m 3 = 1000. . . . m. L = 1. 10. . . . 6 m. L 1 m 3 = 1. 000 1. 10⁻ 6 m 3 0, 000001 m 3 =. . 1. 103 μL =. . .

Reken om: 2, 3. 109 μL 2, 3 m 3 =. . . 1, 23 m. L = 1, 23. 10⁻. . . 6 m 3 2, 50 μL = 2, 50. 10⁻. . . 6 dm 3 ⁻ 5 m 3 11, 4 m. L = 11, 4. 10⁻. . . . 6 m 3 = 1, 14. 10. . . 616 μL = 616. 10⁻. . . 6 L = 6, 16. 10⁻. . 4 L 11. . . 9 3. . . 411. 10 μL = 4, 11. 10 411 m = 0, 079 L = 0, 079. 10⁻ ⁻ 5 m 3. . . . 3 m 3 = 7, 9. 10. . .

In 6 weken tijd groeit je haar 3 cm. Bereken hoeveel μm je haar per seconde groeit 3 cm = 3. 10. . . . 4 μm 6 weken = 42 1008 uur = 3, 6. 10. . . dagen =. . . . 6 sec. Je haar groeit dan 3. 104. . . 3, 6. 106. . . 8. 10⁻ 3. . μm s⁻ 1 =. .

De MOL !!!!! • • • 1 dozijn = 12 1 gros = 144 Dus: …………………. . (? ? ? ). . . 23 1 mol = 6, 02. 10 Dit noemen we de. . . . . chemische hoeveelheid 6, 02. 1023 heet de constante van. . . . Avogadro (NA) Zie Binas, tabel 7

Waarom is 1 mol 6, 02. 1023 ? Tabel 7 B: . . . . 24 g 1 u = 1, 66. 10⁻ 27 kg = 1, 66. 10⁻ Hoeveel u is dan 1, 00 gram? x= u x 1, 00 gram 1, 66. 10⁻ 24 1, 00. . . . 1, 00 23 u = 6, 02. 10. . . 24 1, 66. 10⁻ Dus 1 gram = 6, 02. 1023 u 6, 02. 1023 is dus een omrekeningsfactor van gram u. . . . naar. .

1 molecuul H 2 O heeft massa: 2 x 1, 008 + 16, 00 = 18, 016. . . . . u Wat is de massa van 1 mol (= 6, 02. 1023) moleculen H 2 O? 6, 02. 1023 moleculen H 2 O hebben massa. . . . 6, 02. 1023 x 18, 016 = 1, 50. 10. . . 27 u Hoeveel gram is dit? 1, 50. 1027 u 1, 00 gram 1, 66. 10⁻ 24 x . . . . 1, 66. 10⁻ 24 x 1, 50. 1027 = 18, 016. . . gram x=. . . . 1, 00 Dus 1 mol (=6, 02. 1023) H 2 O moleculen hebben massa 18, 016 g

1 molecuul H 2 O heeft massa: 2. . . . . x 1, 008 + 16, 00 = 18, 02. . . u 1 moleculen H 2 O hebben massa 18, 02. . . g Het getal is dus hetzelfde, maar de eenheid is verschillend: De massa van een molecuul wordt uitgedrukt in. . . u De massa van 1 moleculen wordt uitgedrukt in. g. .

Dus: 1 mol = M gram !!! Waarin M de. . . atoom- of molecuulmassa. . . is De massa van 1 moleculen / atomen heet de MOLAIRE MASSA. . . . De molaire massa van CO 2 is 44, 010 g. . mol⁻ 1 Dit wil zeggen dat de massa van. . . . 1 mol CO 2 44, 010 g is

Bereken de molaire massa van CH 3 CH 2 OH. De molecuulmassa van CH 3 CH 2 OH is: 2 x 12, 01 u + 6. . . . x 1, 008 u +. . . 16, 00 u = 46, 07. . . . u 1 molecuul CH 3 CH 2 OH heeft dus massa 46, 07. . u. . g 1 mol CH 3 CH 2 OH moleculen hebben massa: 46, 07 Maar: kijk een naar tabel 98 !

Tabel 98 mol⁻ 1 De molaire massa van CH 3 OH is 32, 042. . g. . Dus: 1 mol CH 3 OH moleculen hebben massa. . . 32, 042 g Wat is de massa van 0, 0325 mol CH 3 OH moleculen? 0, 0325 aantal mol 1 aantal gram 32, 042 x 0, 0325 x 32, 042 = 1, 0414 x= 1. . . g De massa van 0, 0325 mol CH 3 OH moleculen is 1, 04

Tabel 98 mol⁻ 1 98, 079 g. . De molaire massa van H 2 SO 4 is. . . Dus: 1 mol H 2 SO 4 moleculen hebben massa. . . 98, 079 g Hoeveel (mol) H 2 SO 4 moleculen zitten in 2, 45 mg H 2 SO 4 ? aantal mol 1 x aantal gram 98, 079 2, 45. 10⁻ 3 1 x 2, 45. 10⁻ 3 x= = 2, 49799. 10⁻ 5 98, 079 In 2, 45 mg H 2 SO 4 zitten. . . . 2, 50. 10⁻ 5 moleculen

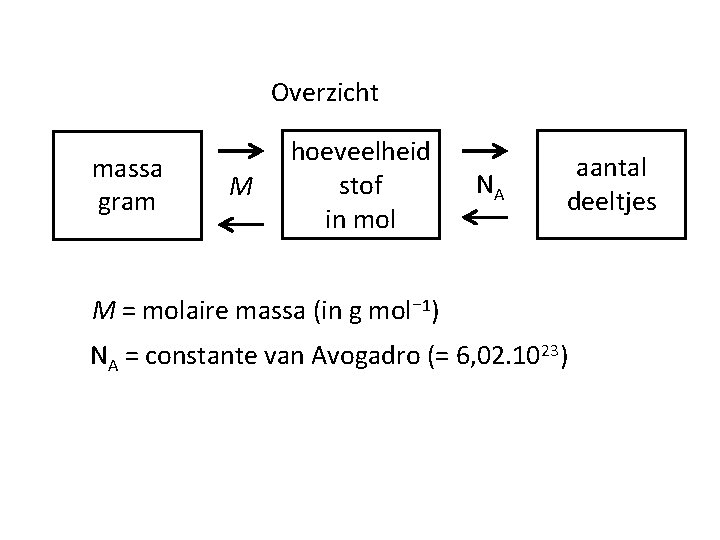
Overzicht massa gram M hoeveelheid stof in mol NA aantal deeltjes M = molaire massa (in g mol⁻ 1) NA = constante van Avogadro (= 6, 02. 1023)

En nu zelf: 1. Bereken de massa van 5, 13 mmol KMn. O 4 2. Hoeveel moleculen zitten in 0, 918 mg H 2 CO ? 3. Bereken de massa van 2, 80 kmol HNO 3 4. Hoeveel moleculen zitten in 3, 18. 103 kg HCl? Antwoorden: 1. 811 mg (0, 811 g) 2. 3, 06. 10⁻ 5 mol H 2 CO moleculen 3. 1, 76. 105 g (176 kg) 4. 8, 72. 104 mol HCl moleculen (872 kmol)

1. Bereken de massa van 5, 13 mmol KMn. O 4 Tabel 98: de molaire massa van KMn. O 4 = 158, 03 g mol⁻ 1 Dus 1 mol KMn. O 4 = 158, 03 g 5, 13 mmol KMn. O 4 = 5, 13. 10⁻ 3 mol KMn. O 4 is dan: 5, 13. 10⁻ 3 mol 1 massa 158, 03 g xg 5, 13. 10⁻ 3 x 158, 03 = 0, 811 g (= 811 mg) x= 1 iets handiger is het zó te doen:

1. Bereken de massa van 5, 13 mmol KMn. O 4 Tabel 98: de molaire massa van KMn. O 4 = 158, 03 g mol⁻ 1 Dus 1 mol KMn. O 4 = 158, 03 g Maar ook: 1 mmol KMn. O 4 = 158, 03 mg 5, 13 mmol KMn. O 4 is dan: mmol 1 massa 158, 03 mg x= 5, 13 x 158, 03 1 5, 13 x mg = 811 mg

2. Hoeveel moleculen zitten in 0, 918 mg H 2 CO ? Tabel 99: de molaire massa van H 2 CO = 2 x 1, 008 + 12, 01 + 16, 00 = 30, 026 g mol⁻ 1 Dus 1 mol H 2 CO = 30, 026 g 0, 918 mg H 2 CO = 9, 18. 10⁻ 4 g mol massa 1 30, 026 g 1 x 9, 18. 10⁻ 4 x= 30, 026 x 9, 18. 10⁻ 4 g = 3, 06. 10⁻ 5 mol H 2 CO moleculen

3. Bereken de massa van 2, 80 kmol HNO 3 Tabel 98: de molaire massa van HNO 3 = 63, 013 g mol⁻ 1 Dus 1 mol HNO 3 = 63, 013 g 2, 80 kmol HNO 3 = 2, 80. 103 mol HNO 3 is dan: 2, 80. 103 mol 1 massa 63, 013 g xg 2, 80. 103 x 63, 013 = 1, 76. 105 g (= 176 kg) x= 1 iets handiger is het zó te doen:

3. Bereken de massa van 2, 80 kmol HNO 3 Tabel 98: de molaire massa van HNO 3 = 63, 013 g mol⁻ 1 Dus 1 mol HNO 3 = 63, 013 g Maar ook: 1 kmol HNO 3 = 60, 013 kg 2, 80 kmol HNO 3 is dan: kmol 1 massa 63, 013 kg x= 2, 80 x kg 2, 80 x 63, 013 = 176 kg 1

4. Hoeveel moleculen zitten in 3, 18. 103 kg HCl? Tabel 99: de molaire massa van HCl = 36, 461 g mol⁻ 1 Dus 1 mol HCl = 36, 461 g 3, 18. 103 kg H 2 CO = 3, 18. 106 g mol massa 1 36, 461 g 1 x 3, 18. 106 x= 36, 461 x 3, 18. 106 g = 8, 72. 104 mol HCl moleculen

Nog een keer zelf 5. Bereken de massa (in g) van 2, 31. 1024 moleculen CO 2 6. Bereken hoeveel moleculen er in 3, 02 g water zitten Antwoorden: 5. 169 g 6. 1, 01. 1023 moleculen H 2 O

5. Bereken de massa (in g) van 2, 31. 1024 moleculen CO 2 1 mol CO 2 bevat 6, 02. 1023 moleculen CO 2 Hoeveel mol CO 2 is dan 2, 31. 1024 moleculen CO 2? mol 1 x aantal 6, 02. 1023 2, 31. 1024 24 2, 31. 10 x= = 3, 837 mol CO 2 moleculen 23 1 x 6, 02. 10 Binas, tabel 98: de molaire massa van CO 2 = 44, 010 g mol⁻ 1 3, 837 mol CO 2 moleculen hebben massa: 3, 837 x 44, 01 = 169 g

6. Bereken hoeveel moleculen er in 3, 02 g water zitten Binas, tabel 98: de molaire massa van H 2 O = 18, 015 g mol⁻ 1 Hoeveel mol H 2 O moleculen zitten in 3, 02 g H 2 O? mol 1 x massa 18, 015 g 3, 02 g 1 x 3, 02 x= = 0, 1676 mol H 2 O moleculen 18, 015 1 mol H 2 O is 6, 02. 1023 moleculen H 2 O 0, 1676 mol H 2 O bevat dan: 0, 1676 x 6, 02. 1023 = 1, 01. 1023 moleculen H 2 O