Europos direktorato vaist kokybei veikla J Petroit 2006

Europos direktorato vaistų kokybei veikla J. Petrošiūtė 2006 -06 -13
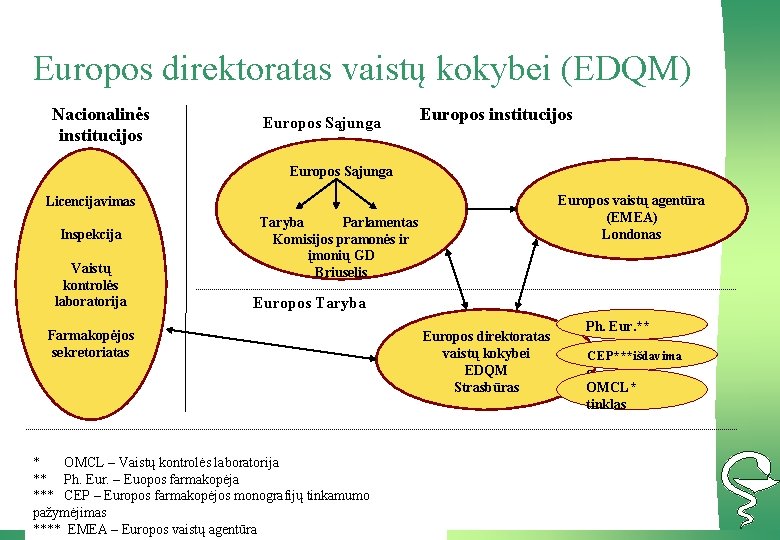
Europos direktoratas vaistų kokybei (EDQM) Nacionalinės institucijos Europos Sąjunga Europos vaistų agentūra (EMEA) Londonas Licencijavimas Inspekcija Vaistų kontrolės laboratorija Taryba Parlamentas Komisijos pramonės ir įmonių GD Briuselis Europos Taryba Farmakopėjos sekretoriatas * OMCL – Vaistų kontrolės laboratorija ** Ph. Eur. – Euopos farmakopėja *** CEP – Europos farmakopėjos monografijų tinkamumo pažymėjimas **** EMEA – Europos vaistų agentūra Europos direktoratas vaistų kokybei EDQM Strasbūras Ph. Eur. ** CEP***išdavima s OMCL* tinklas
EDQM veikla Ph. Europos direktoratas vaistų kokybei EDQM CEP išdavimas OMCL tinklas

1. Europos farmakopėja
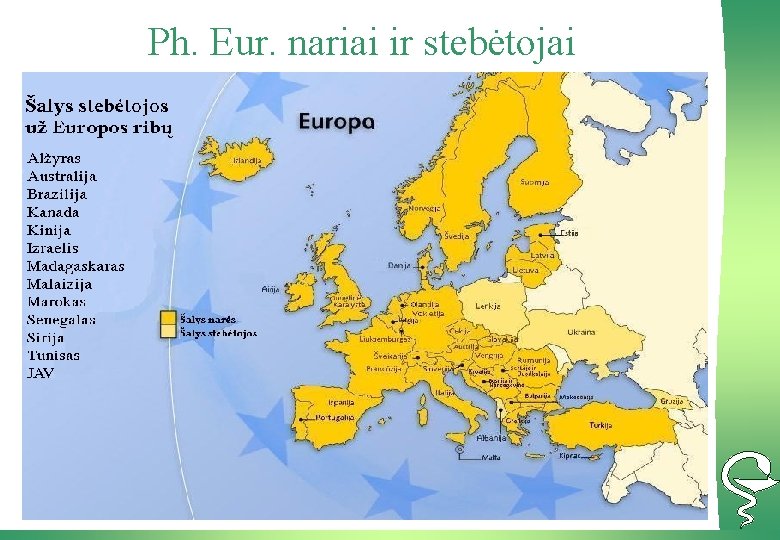
Ph. Eur. nariai ir stebėtojai

Konvencijos ratifikavimas Lietuvoje

Lietuva ratifikuoja konvenciją dėl Europos farmakopėjos rengimo

Organizacijos, dalyvaujančios Ph. Eur. rengime • • Europos farmakopėjos komisija Ekspertų grupės Farmakopėjos sekretoriatas Nacionalinės farmakopėjos institucijos

Europos farmakopėjos rengimas
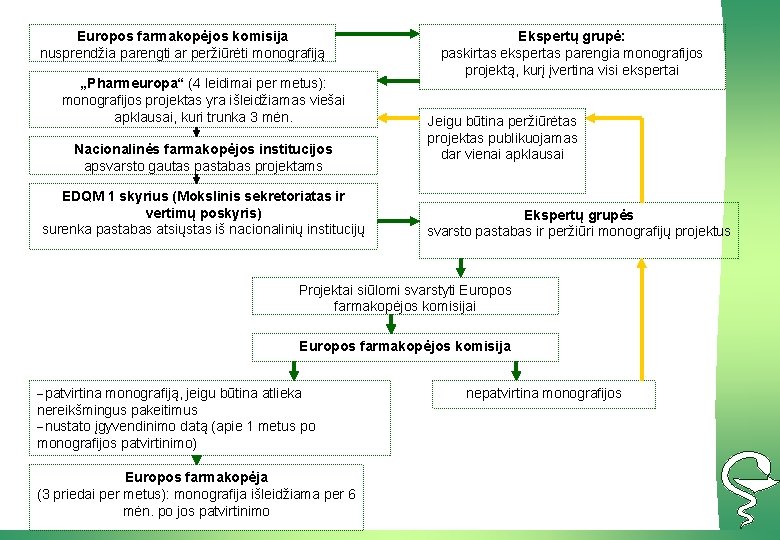
Europos farmakopėjos komisija nusprendžia parengti ar peržiūrėti monografiją „Pharmeuropa“ (4 leidimai per metus): monografijos projektas yra išleidžiamas viešai apklausai, kuri trunka 3 mėn. Nacionalinės farmakopėjos institucijos apsvarsto gautas pastabas projektams EDQM 1 skyrius (Mokslinis sekretoriatas ir vertimų poskyris) surenka pastabas atsiųstas iš nacionalinių institucijų Ekspertų grupė: paskirtas ekspertas parengia monografijos projektą, kurį įvertina visi ekspertai Jeigu būtina peržiūrėtas projektas publikuojamas dar vienai apklausai Ekspertų grupės svarsto pastabas ir peržiūri monografijų projektus Projektai siūlomi svarstyti Europos farmakopėjos komisija -patvirtina monografiją, jeigu būtina atlieka nereikšmingus pakeitimus -nustato įgyvendinimo datą (apie 1 metus po monografijos patvirtinimo) Europos farmakopėja (3 priedai per metus): monografija išleidžiama per 6 mėn. po jos patvirtinimo nepatvirtina monografijos
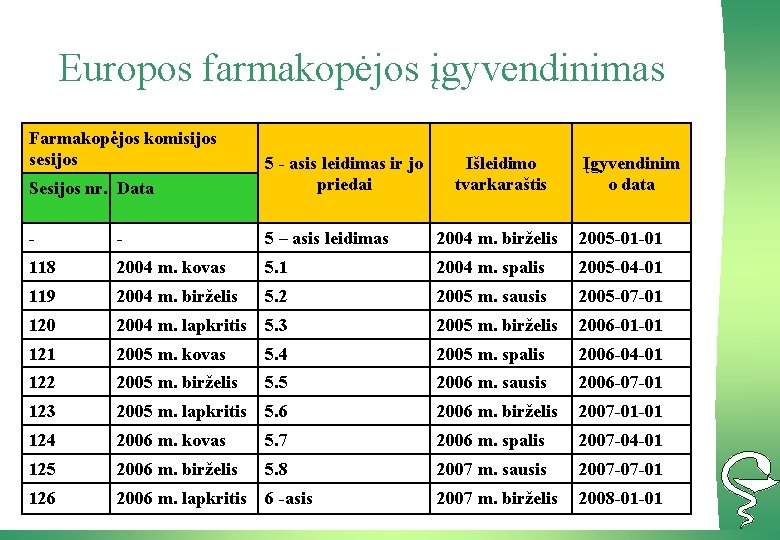
Europos farmakopėjos įgyvendinimas Farmakopėjos komisijos sesijos Sesijos nr. Data 5 - asis leidimas ir jo priedai Išleidimo tvarkaraštis Įgyvendinim o data - - 5 – asis leidimas 2004 m. birželis 2005 -01 -01 118 2004 m. kovas 5. 1 2004 m. spalis 2005 -04 -01 119 2004 m. birželis 5. 2 2005 m. sausis 2005 -07 -01 120 2004 m. lapkritis 5. 3 2005 m. birželis 2006 -01 -01 121 2005 m. kovas 5. 4 2005 m. spalis 2006 -04 -01 122 2005 m. birželis 5. 5 2006 m. sausis 2006 -07 -01 123 2005 m. lapkritis 5. 6 2006 m. birželis 2007 -01 -01 124 2006 m. kovas 5. 7 2006 m. spalis 2007 -04 -01 125 2006 m. birželis 5. 8 2007 m. sausis 2007 -07 -01 126 2006 m. lapkritis 6 -asis 2007 m. birželis 2008 -01 -01

Rengimo etapų žymėjimas duomenų bazėse • 0 = darbo programoje, projekto nėra • 1 = 1 -asis projektas (nauja ar peržiūrima monografija) • 2 = paskelbta “Pharmeuropa” • 3 = pateikta komisijai • 4 = patvirtinta, paruošta išleisti • 5 = publikuojama * www. pheur. org Knowledge Database

2. CEP išdavimas

Europos farmakopėjos monografijų tinkamumo pažymėjimai (CEP) 1. Pripažįsta 34 Europos farmakopėjos konvenciją pasirašiusios, ES ir kitos šalys (pvz. Australija, Naujoji Zelandija, Kanada). 2. CEP gali būti pateikiamas kartu su vaistinio preparato registravimo paraiška, įrodant, kad vaistinė medžiaga, esanti preparato sudėtyje, atitinka Ph. Eur. monografijas ir 2001/83/EC direktyvą.

CEP pateikimas su registracijos paraiška Bendroji tvarka 1 modulis − VM pavadinimas ir adresas − Pažymima, kad pateikta CEP / Europinė VM gamybos byla (ASMF) / visa informacija 3. 2. S modulis 3. 2. S. 1 bendra informacija; 3. 2. S. 2 gamyba; 3. 2. S. 3 apibūdinimas; 3. 2. S. 4 veikliosios vaistinės medžiagos kontrolė specifikacijos ir analizės procedūros): − mokslinis specifikacijų pagrindimas; − analizės procedūrų patvirtinimas; − gamybos serijos analizės rezultatai; 3. 2. S. 5 referenciniai standartai ir medžiagos: 3. 2. S. 6 talpyklės uždarymo sistema; 3. 2. S. 7 tinkamumo laikas (re-test period) ir stabilumo duomenys. CEP 1 modulis − VM pavadinimas ir adresas − Pažymima, kad pateiktas CEP 3. 2. S modulis 3. 2. S. 4 veikliosios vaistinės medžiagos kontrolė specifikacijos ir analizės procedūros): − mokslinis specifikacijų pagrindimas; − analizės procedūrų patvirtinimas; − gamybos serijos analizės rezultatai; 3. 2. S. 5 referenciniai standartai ir medžiagos: 3. 2. S. 6 talpyklės uždarymo sistema; 3. 2. S. 7 tinkamumo laikas (re-test period) ir stabilumo duomenys, jeigu nenurodyti CEP kopija, su patvirtinimu, kad gamybos metoduose nebuvo esminių pakeitimų
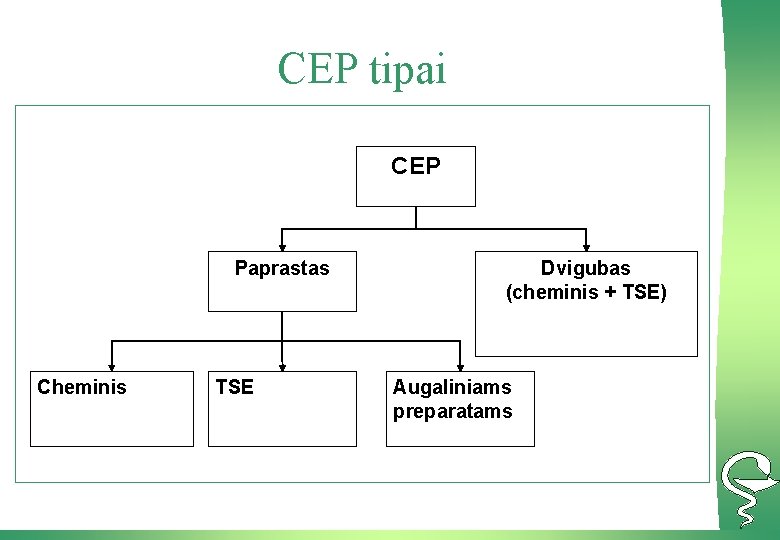
CEP tipai CEP Paprastas Cheminis TSE Dvigubas (cheminis + TSE) Augaliniams preparatams

CEP išdavimo procedūra • Rezoliucija AP-CSP (99) 4 (Resolution AP-CSP (99) 4, adopted by the Public Health Committee (Partial Agreement) (CD-P-SP) on 22 December 1999) http: //www. pheur. org/medias/fichiers/APCSP 9904 E. pdf
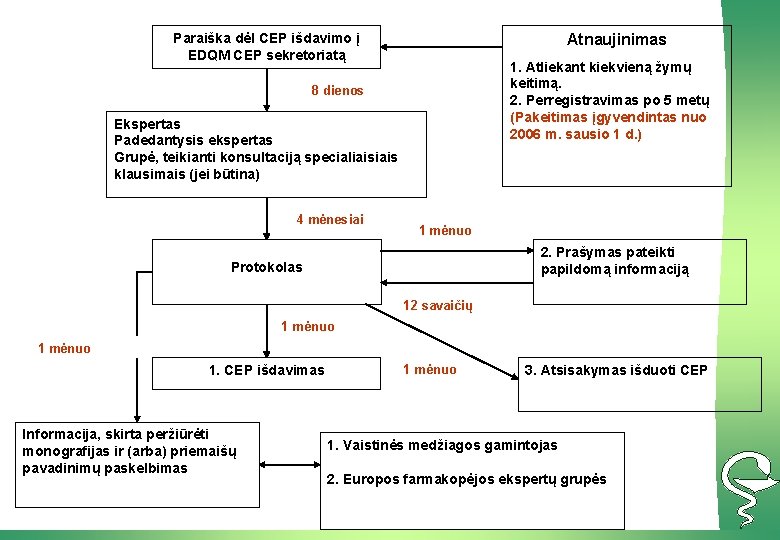
Paraiška dėl CEP išdavimo į EDQM CEP sekretoriatą Atnaujinimas 1. Atliekant kiekvieną žymų keitimą. 2. Perregistravimas po 5 metų (Pakeitimas įgyvendintas nuo 2006 m. sausio 1 d. ) 8 dienos Ekspertas Padedantysis ekspertas Grupė, teikianti konsultaciją specialiais klausimais (jei būtina) 4 mėnesiai 1 mėnuo 2. Prašymas pateikti papildomą informaciją Protokolas 12 savaičių 1 mėnuo 1. CEP išdavimas Informacija, skirta peržiūrėti monografijas ir (arba) priemaišų pavadinimų paskelbimas 1 mėnuo 3. Atsisakymas išduoti CEP 1. Vaistinės medžiagos gamintojas 2. Europos farmakopėjos ekspertų grupės

CEP peržiūros ir perregistravimo procedūra • CEP peržiūros / perregistravimo reikalavimų vadovas (Guideline on requirements on revision /renewal of CEPs (PA/PH/CEP (04) 2) • Naujos CEP peržiūros / perregistravimo valdymo procedūros (New procedures for management of revision / renewal of CEPs (PA/PH/Exp. CEP/T (04) 18) Įgyvendinimas: 2004 m. rugsėjo 1 d. Tikslas: suvienodinti CEP keitimų ir procedūrų klasifikaciją su vaistinių preparatų registravimo keitimų ir procedūrų klasifikacija (Komisijos reglamentai (EC) 1084/2003 (MRP) ir (EC) 1085/2003 (CP)).
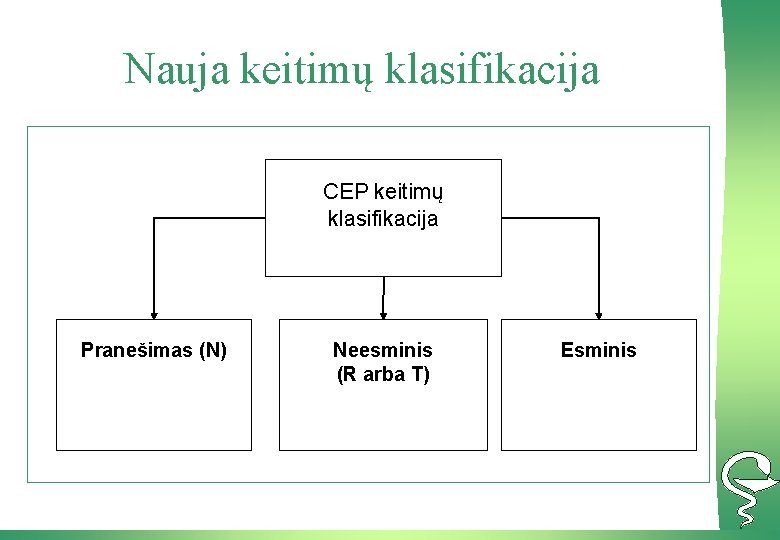
Nauja keitimų klasifikacija CEP keitimų klasifikacija Pranešimas (N) Neesminis (R arba T) Esminis

Kas nesikeitė procedūroje • Privalu pranešti Europos direktoratui vaistų kokybei (EDQM) apie bet kurį (administracinį ar specialųjį) bylos turinio pakeitimą, kuris turi būti patvirtintas. • CEP išduodamas 5 metams (paraišką perregistravimui pateikti ne vėliau kaip 6 mėnesiai prieš CEP galiojimo pabaigą). • Ph. Eur. monografijų / bendrinių straipsnių peržiūra tiesiogiai siejasi su vaistinės medžiagos kontrolės ir CEP bylos atnaujinimu.

Europos farmakopėjos 5 leidimo įgyvendinimas Visų CEP peržiūra buvo atlikta tam, kad atitiktų išvardintų Ph. Eur. tekstų reikalavimus: • bet kurios peržiūrėtos monografijos; • bendrinio straipsnio „Vaistinės medžiagos” (2034); • bendrojo teksto apie priemaišas (5. 10); • peržiūrėto bendrojo teksto dėl gyvūnų spongiforminės encefalopatijos plitimo rizikos sumažinimo (5. 2. 8).

Peržiūrėjus CEP • CEP kopija pateikiama pareiškėjams • Atnaujinama vaistinių preparatų registravimo paraiška (dažniausiai pateikiama I A tipo variacija)

CEP paieška www. pheur. org skiltyje Certification paieškos duomenų bazėje Certification Search online database

3. Standartinių terminų rengimas

Standartinių terminų naudojimo įvadas ir vadovas Standard terms Introduction and Guidance for use * EDQM leidinyje Standard Terms 2004 * www. pheur. org Publications Special Theme Issues List of standard terms • Standartinių terminų sąrašų naudojimo bendrieji principai ir taisyklės • Standartinių terminų įtraukimo, išbraukimo ir pakeitimo standartinių terminų sąraše procedūra

Standartinių terminų įtraukimo, išbraukimo ir pakeitimo procedūra Šalis narė / Europos Komisija / EMEA pateikia paraiškos formą EDQM 1 sav. Ph. Eur. komisijos standartinių terminų darbo grupė pateikia pasiūlymus 6 mėn. Šalis narė, Europos Komisija ar EMEA pateikia pastabas 1 mėn. Ph. Eur. komisijos Ekspertų grupė Nr. 12 Standartinio termino įtraukimas, išbraukimas ar termino pakeitimas Standartinių terminų sąrašo atnaujinimas ir standartinių terminų atitikmenų rengimas įvairiomis kalbomis nacionalinėse institucijose Susijusios Ph. Eur. monografijos peržiūra ar naujos monografijos rengimas

Sudėtiniai standartiniai terminai • Sudėtinis standartinis terminas = standartinis terminas /standartinio termino elementas + standartinis terminas /standartinio termino elementas • Šalies narės atsakinga institucija / EMEA praneša EDQM • Terminas tinkamas į Sudėtinių standartinių terminų sąrašą www. pheur. org

Informacija • www. pheur. org • Knowledge Database • Help. Desk

Ačiū už dėmesį
- Slides: 30