Enjeux conomiques et dfis technologiques du transfert de








































- Slides: 55

Enjeux économiques et défis technologiques du transfert de gène en thérapie génique

Petit Robert : Sens du mot soigner : - S’occuper de rétablir la santé - Faire ce qu’il faut pour guérir Petit du Robert : Sens mot guérir : - Aller mieux et sortir de la maladie - Débarrasser d’un mal

Soigner et guérir sont donc deux mots dont le sens va dépendre du contexte, donc des outils thérapeutiques disponibles, des acteurs impliqués et de l’environnement. Pour un thérapeute, l’objectif du soin pourra donc être de plusieurs natures: - Aller mieux (augmenter le confort de vie) - Rétablir la santé (ramener le confort à la normale) - Débarrasser le patient de son problème Les principes thérapeutiques peuvent donc avoir des objectifs différents. Leur émergence en temps que nouveau principe va donc dépendre du contexte.

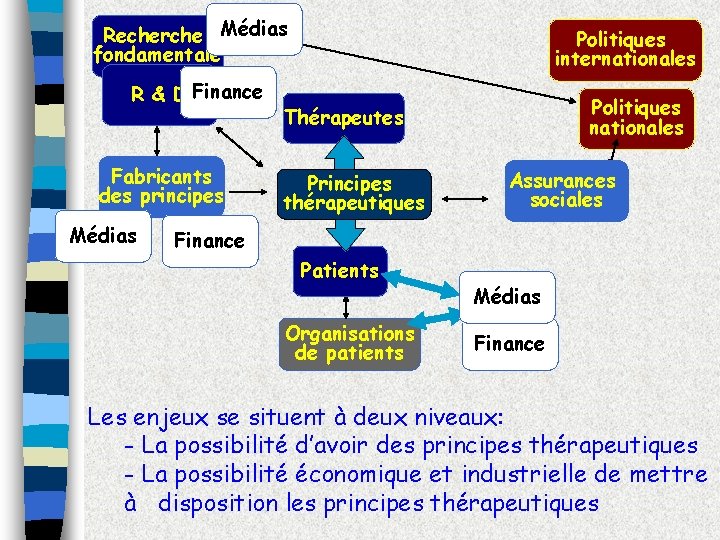
Recherche Médias fondamentale R & D Finance Fabricants des principes Médias Politiques internationales Politiques nationales Thérapeutes Principes thérapeutiques Assurances sociales Finance Patients Organisations de patients Médias Finance Les enjeux se situent à deux niveaux: - La possibilité d’avoir des principes thérapeutiques - La possibilité économique et industrielle de mettre à disposition les principes thérapeutiques

Contours des principes en thérapie génique 1 - Désordres génétiques 2 - Concepts thérapeutiques utilisables en thérapie génique 3 - Possibilités et limites des thérapies in vivo et ex vivo 4 - Entendement et impact de l’assurance qualité en TG

Contours des principes en thérapie génique 1 - Désordres génétiques = Altérations génétiques = Modifications de l’ADN dans le chromosome Sain X Héréditaires Acquises Certains cancers Cancers Diabètes de type 2 X X Certains cancers Maladies génétiques Cancers

Contours des principes en thérapie génique 1 - Désordres génétiques * * * Vecteurs synthétiques : Synthe. Gene Transfert

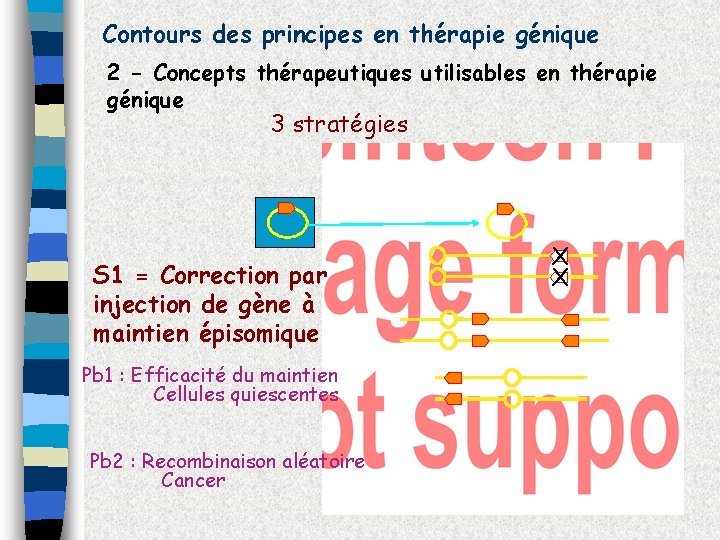
Contours des principes en thérapie génique 2 - Concepts thérapeutiques utilisables en thérapie génique 3 stratégies S 1 = Correction par injection de gène à maintien épisomique Pb 1 : Efficacité du maintien Cellules quiescentes Pb 2 : Recombinaison aléatoire Cancer X X

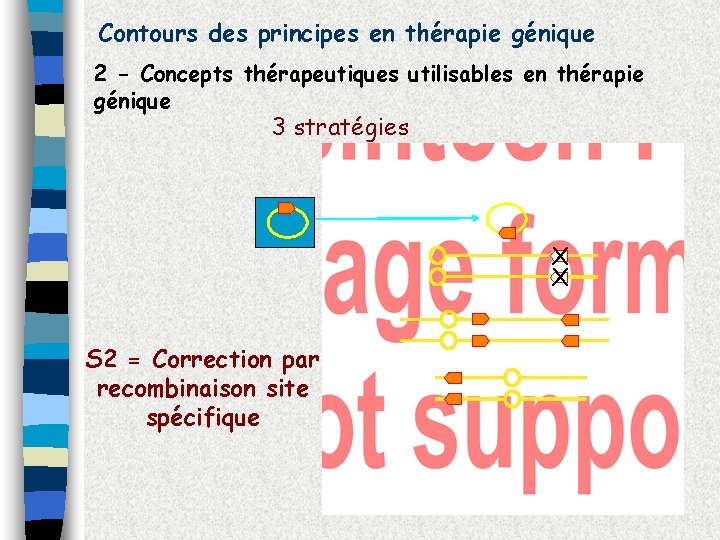
Contours des principes en thérapie génique 2 - Concepts thérapeutiques utilisables en thérapie génique 3 stratégies X X S 2 = Correction par recombinaison site spécifique

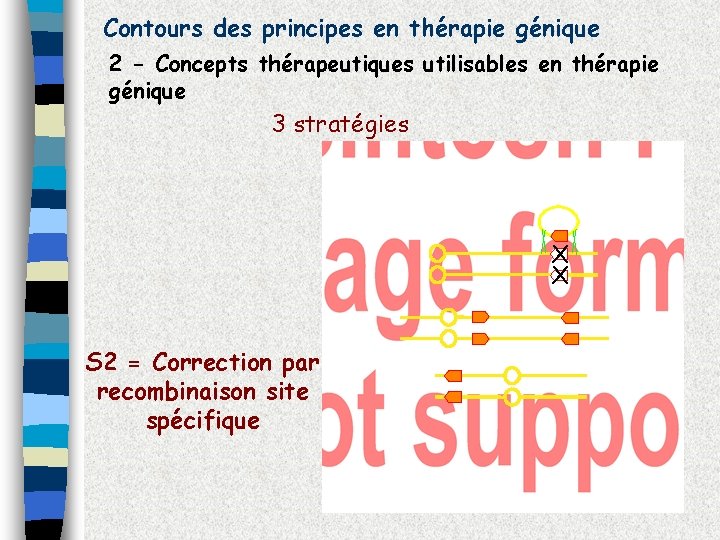
Contours des principes en thérapie génique 2 - Concepts thérapeutiques utilisables en thérapie génique 3 stratégies X X S 2 = Correction par recombinaison site spécifique

Contours des principes en thérapie génique 2 - Concepts thérapeutiques utilisables en thérapie génique 3 stratégies S 2 = Correction par recombinaison site spécifique Pb 1 : Efficacité Pb 2 : Recombinaison aléatoire Cancer X

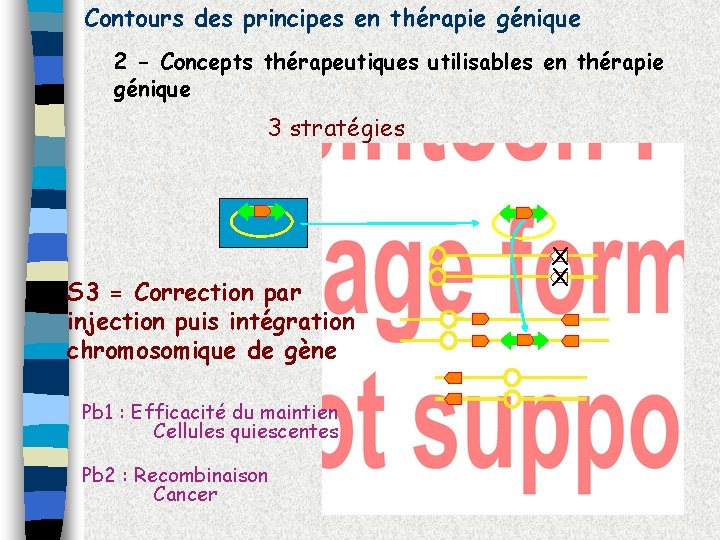
Contours des principes en thérapie génique 2 - Concepts thérapeutiques utilisables en thérapie génique 3 stratégies S 3 = Correction par injection puis intégration chromosomique de gène Pb 1 : Efficacité du maintien Cellules quiescentes Pb 2 : Recombinaison Cancer X X

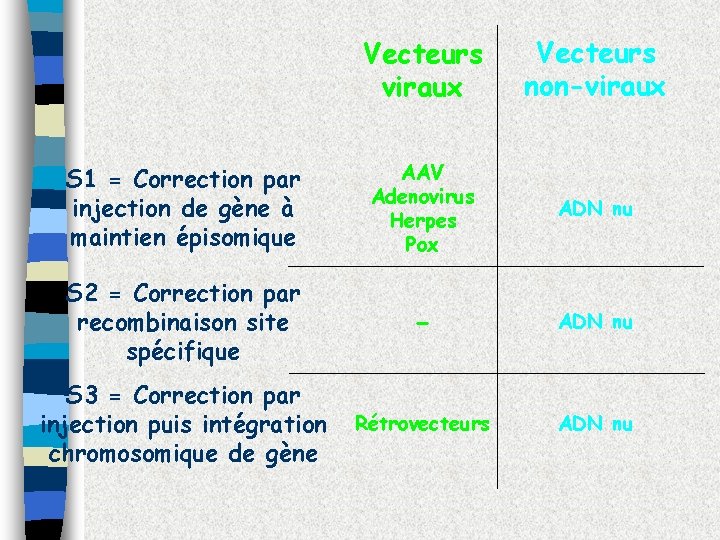
Vecteurs viraux Vecteurs non-viraux S 1 = Correction par injection de gène à maintien épisomique AAV Adenovirus Herpes Pox ADN nu S 2 = Correction par recombinaison site spécifique - ADN nu S 3 = Correction par injection puis intégration chromosomique de gène Rétrovecteurs ADN nu

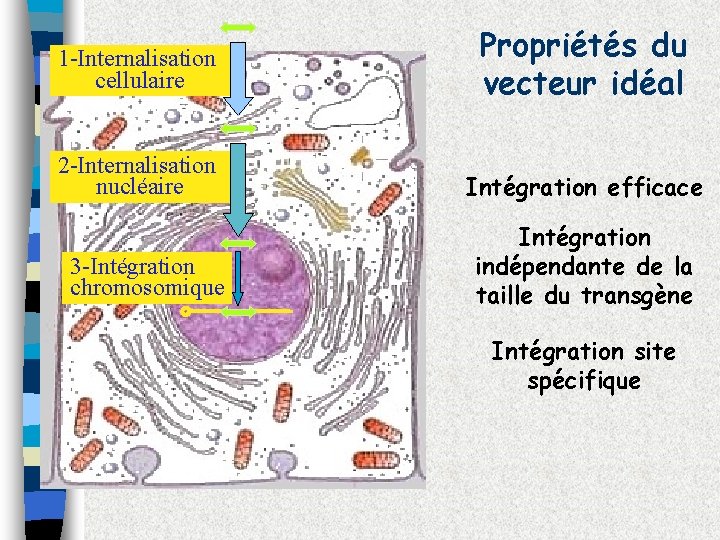
1 -Internalisation cellulaire Propriétés du vecteur idéal 2 -Internalisation nucléaire Intégration efficace 3 -Intégration chromosomique Intégration indépendante de la taille du transgène Intégration site spécifique

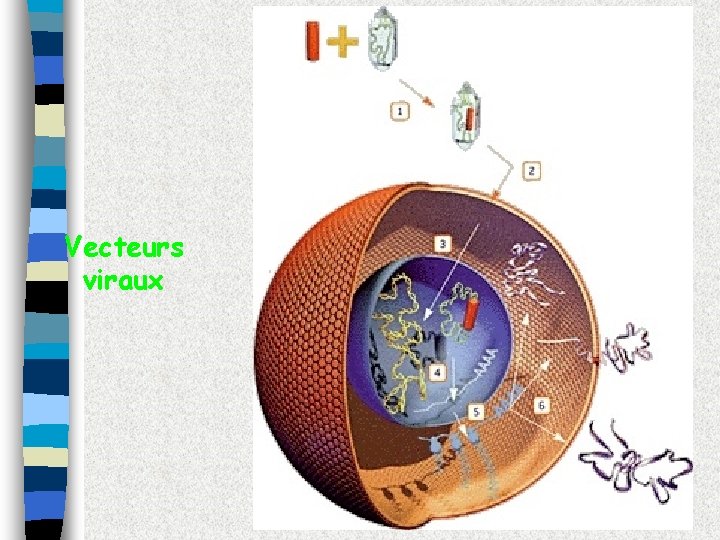
Vecteurs viraux

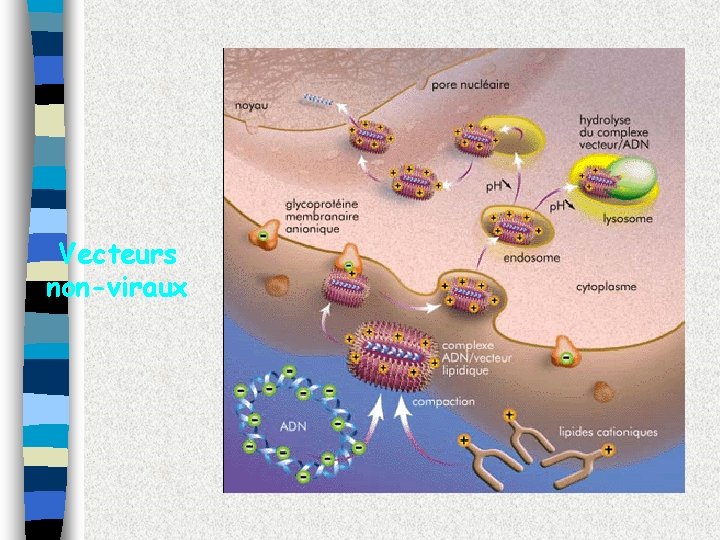
Vecteurs non-viraux

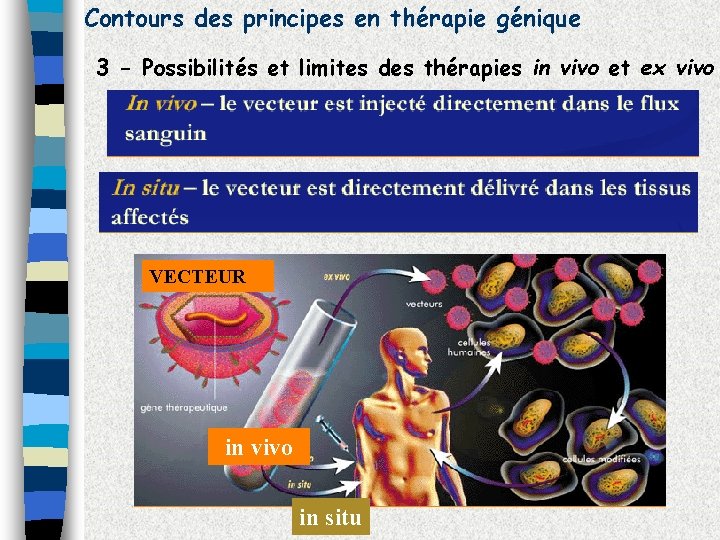
Contours des principes en thérapie génique 3 - Possibilités et limites des thérapies in vivo et ex vivo VECTEUR in vivo in situ

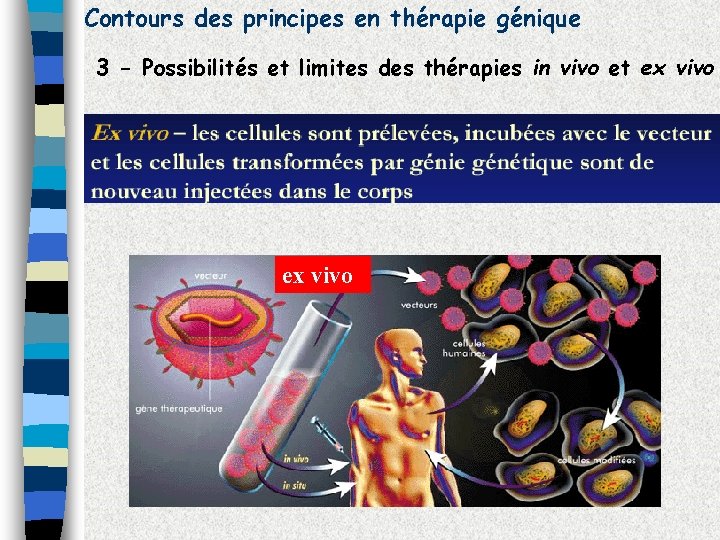
Contours des principes en thérapie génique 3 - Possibilités et limites des thérapies in vivo et ex vivo

3 - Possibilités et limites des thérapies in vivo et ex vivo Peut-on traiter directement les tissus d’un individu ? Ca dépend ! Doit-on traiter tous les tissus ? Doit-on traiter toucher toutes les cellules? Est il possible de cibler les vecteurs vers un tissu particulier ? Les tissus sont formés de cellules quiescentes et/ou en division. Impact de cette différence ? Effet du vecteur sur l’organisme ?

* * * Cahier des charges : lourd *

Vecteurs viraux Transfert d’ADN efficace Taille variable Immunogène Intégration mutagène Possibilité de recombinaison Pas facile à produire et à stocker La Recherche : Des virus bricolés pour transférer des gènes Déc 1998

Vecteurs viraux Ciblage tissulaire = Bof Atteindre un ou une série d’organes entiers dans un individu (muscles) = Pas si mal Très Immunogènes

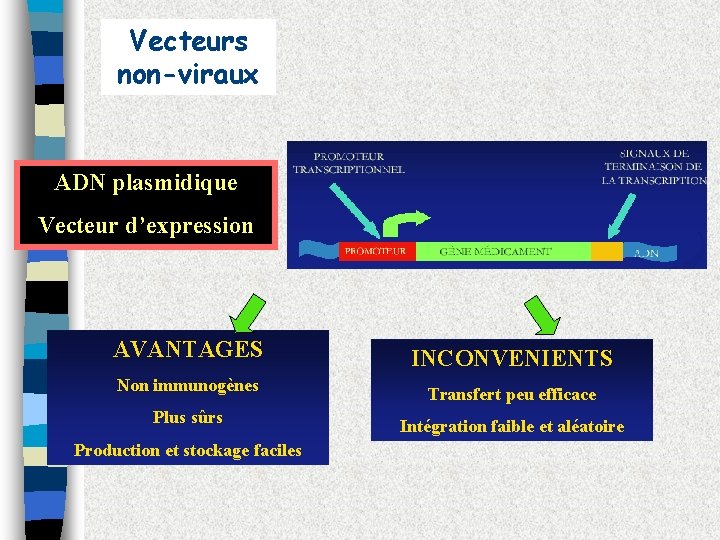
Vecteurs non-viraux ADN plasmidique Vecteur d’expression AVANTAGES INCONVENIENTS Non immunogènes Transfert peu efficace Plus sûrs Intégration faible et aléatoire Production et stockage faciles

Vecteurs non-viraux Ciblage tissulaire = Bof, Bof Atteindre un ou une série d’organes entiers dans un individu (muscles) = re-Bof Pas ou peu immunogènes

Conclusion: Les traitements directs in vivo sont pour l’instant une stratégie peu fiable. pb 1: Ciblage pb 2: Immunogénicité pb 3: Spécificité d’intégration du gène médicament pb 4: Mutagenèse insertionnelle aléatoire (Cancer) Alternative: Les traitements ex vivo (initié par Fisher)

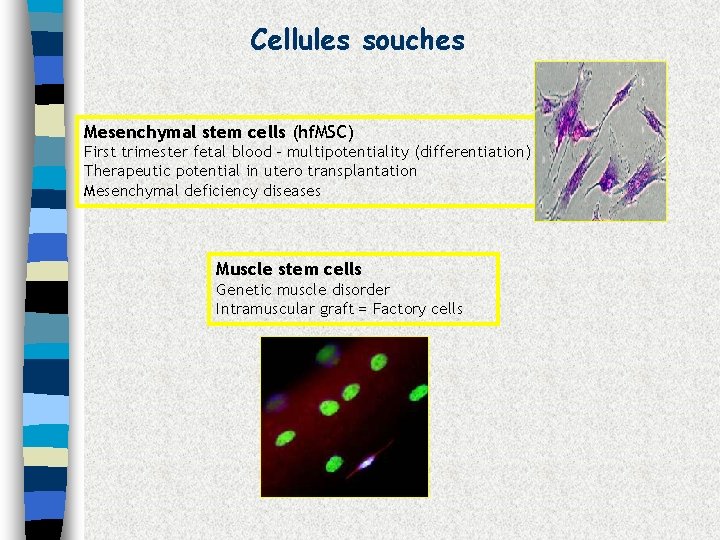
Cellules souches Mesenchymal stem cells (hf. MSC) First trimester fetal blood - multipotentiality (differentiation) Therapeutic potential in utero transplantation Mesenchymal deficiency diseases Muscle stem cells Genetic muscle disorder Intramuscular graft = Factory cells

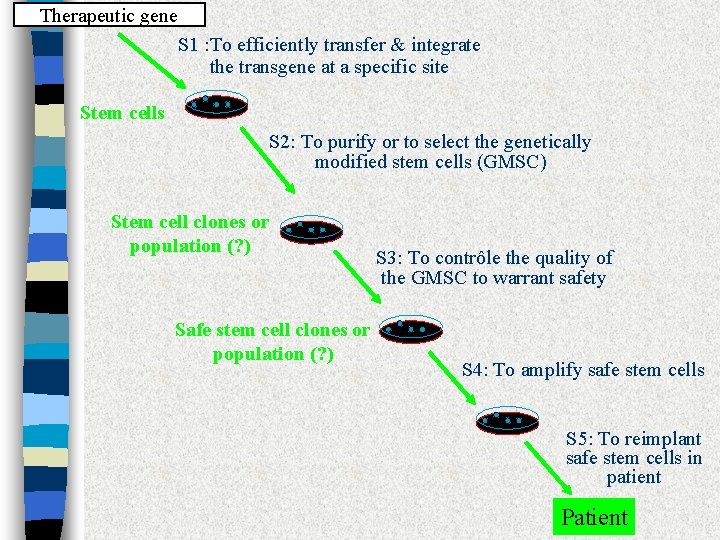
Therapeutic gene S 1 : To efficiently transfer & integrate the transgene at a specific site Stem cells S 2: To purify or to select the genetically modified stem cells (GMSC) Stem cell clones or population (? ) Safe stem cell clones or population (? ) S 3: To contrôle the quality of the GMSC to warrant safety S 4: To amplify safe stem cells S 5: To reimplant safe stem cells in patient Patient

Stratégie thérapeutique Diagnostic prénatal Récupération des cellules souches mésenchymateuses du cordon Tranformation génétique et sélection clonale Réimplantation dans le patient nouveau né

Problème posé par les cellules souches Elles aiment bien qu’on leur fiche la paix et vivrent tranquillement dans le coin Alternative: les cellules souches embryonnaires Elles aiment bien se multiplier et se différencier Conclusion: les stratégies ex vivo offrent de réelles possibilités de thérapies contrôlées

Contours des principes en thérapie génique 4 - Entendement et impact de l’assurance qualité en TG Les pb 3 et 4 évoqués pour les traitements in vivo sont aussi d’actualité ex vivo. pb 3: Spécificité d’intégration du gène médicament pb 4: Mutagenèse insertionnelle aléatoire (Cancer) Concept de vecteur propre -l’insertion site spécifique du transgène - Garantit l’expression du transgène - Prévient les risques de cancers prolifératifs Pb 5: Définition d’un bon site d’insertion

Alternative Diagnostic prénatal Récupération des cellules souches mésenchymateuses du cordon Transformation génétique et sélection clonale Fabrication d’un implant Réimplantation dans le patient nouveau né

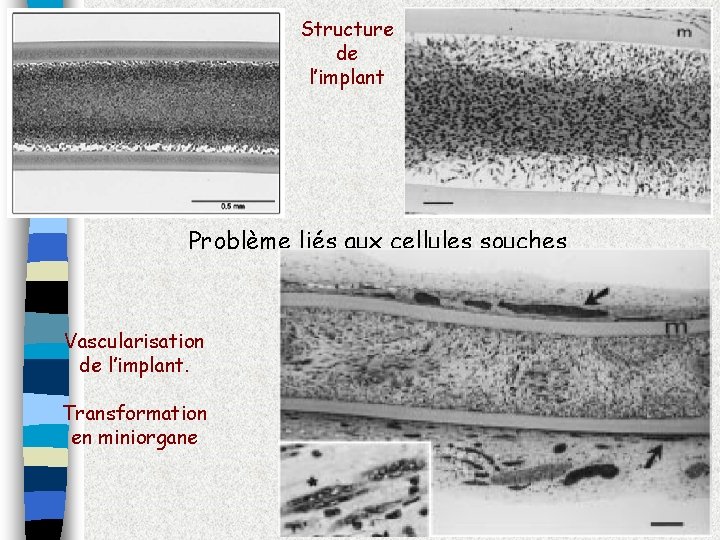
Structure de l’implant Problème liés aux cellules souches Vascularisation de l’implant. Transformation en miniorgane

Conclusions sur les contours des principes en thérapie génique Constat 1 : Nombreuses maladies génétiques « acquises » ou « innées » Nombreux gènes médicament qui ont chacun des conditions d’utilisation propres (tissus, vecteurs, …) Différentes stratégies de vectorisation avec des faisabilités de mise en œuvre (en temps et en besoin de connaissances) très différentes. Constat 2 : Il est possible de hiérarchiser a priori la faisabilité des stratégies Constat 3 : Le coût pour faire aboutir chacune de ces stratégies est très élevé. De plus l’outil industriel n’existe « pas » .

Sens du mot guérir : Pourra-t on développer ces thérapies pour au moins guérir en - Améliorant simplement la vie du patient Ou doit on tout miser pour l’instant dans l’objectif de le - Débarrasser d’un mal

Thérapie génique ex vivo Concept de cellule usine productrice de protéines médicaments Concept d’implant thérapeutique

Points communs et différences des enjeux 1 - Les associations de patients Mettre en œuvre un maximum de solutions thérapeutiques Paradoxe Organisation de patients/société civile et « morale » Ethique et moralité des projets

Points communs et différences des enjeux 2 - Les états, l’Europe - 35 000 de diabétiques en Europe (25) - 100 000 personnes concernées par des neuro-dystrophie en Europe (25) - des hémophiles, ………. . - Les cancers sont la première maladie en France Les systèmes d’assurances santé sont à l’asphyxie, quel que soit le système Paradoxe Etats/Industries La santé est un domaine dans lequel l’industrie fabrique des produits d’exportation. Si un produit est cher et demandé, son exportation permet des entrées de devises importantes

Les abus : Le dopage Le dépistage génétique et assurance ou travail

Le dopage Jusqu’au milieu du XXième siècle Produits anti-fatigue & anti douleur Cafeine, strychnine, cocaïne, arsenic nitroglycerine, alcool, morphine…. 1960: Amphétamines, dopage sanguin Maxiton, Tonedron, Ritaline, … 1970: Anabolisants Testosterone, Dianabol, … 1990: Hormones peptidiques EPO, GH, IGF-1, Insuline…

2008: Thérapie Génique ? The Times February 02, 2006 Apocalypse now: fears of gene doping are realised By Owen Slot A new substance has emerged that suggests the next stage in the drugs battle has started Détournements possibles de la thérapie génique à des fins de dopage - Stimuler (ou bloquer) la production endogène d’une hormone - Faire produire une hormone spécifique par une cellule non programmée pour ce faire en modifiant son génome - Renforcement tissulaire spécifique grâce aux cultures de cellules - Sélection génétique

Augmenter la capacité de transport de l’oxygène par le sang par l’utilisation de vecteurs viraux: EPO • CIBLES : myoblastes ou fibroblastes Agir sur les muscles squelettiques: GH, IGF 1, Myostatine - augmenter la croissance et la différentiation des myoblastes - stimuler la croissance musculaire, l’hypertrophie, le métabolisme anabolique H. Lee Sweeney Gene Doping Scientific American July 2004

EPO

Inhiber la production de la MYOSTATINE

Modifier l’utilisation de l’énergie en agissant au niveau des mitochondries: PPAR - δ L’activation du PPARδ dans le muscle squelettique de la souris - augmente le nombre de fibres musculaires - augmente la performance physique - protège contre l’obésité Augmenter le débit sanguin en stimulant la formation de nouveaux vaisseaux: VEGF Augmenter le seuil de la douleur: endorphines

Prévenir les blessures , accélérer leur guérison muscle squelettique, cartilage articulaire, os, tendons et ligaments De la réparation d’un tendon blessé à l’amélioration de sa résistance en prévision d’une compétition, quelle sera la limite? Efficacité : La thérapie génique dans le sport ?

DEPISTAGE • Réponse immunitaire au vecteur viral • Recherche du DNA artificiel • Marquage du transgène : codage du DNA • Modification de l’expression de gènes suite au traitement par thérapie génique (bio puces, RT-PCR) RISQUE Dépend de la technique utilisée Risques propres à la protéine produite

Profil génétique et assurance ou travail votre profil pour… 1000 $ www. 23 andme. com (Mountain View, Californie) www. decodeme. com (Reykjavik, Islande) www. navigenics. com (Redwood Shores, New York) Services fournis : calcul du risque génétique pour une vingtaine de maladies ou traits physiques, généalogie et comparaisons génétiques, conseil génétique. On peut se tenir au courant des découvertes relatives aux SNP (polymorphismes nucléotidiques simples) via le site SNPedia (Bethesda) www. snpedia. com

Profil génétique individuel : qu’en attendre ? Exemple de résultat (Navigenics, online): Alzheimer’s Yourself 8% Average population 17% Breast cancer Yourself 14% Average population 13% Bénéfices attendus: - financement de la recherche (retour sur investissement), - encouragement à une éthique de la responsabilité, par la conscience du risque (‘un homme averti en vaut deux’) - amélioration thérapeutique (maladies infectieuses, certains cancers*) - thérapie génique ? ? *Milano Gérard, ‘Pharmacogénétique et sensibilité tumorale aux agents anticancéreux. L’exemple du cancer colorectal’, Revue du praticien, 31 mai 2008.

Profil génétique individuel : que craindre ? débat sur la « généticisation » de la médecine et de la culture (années 1990), - reproches faits à la recherche génétique (et au conseil génétique) . idéologie réductionniste (je ne me réduis pas à mon génome !) . tyrannie du ‘génétiquement correct’. risque de discrimination (assurances, employeurs, police) si la confidentialité n’est pas assurée arguments en réponse aux reproches . mieux vaut savoir qu’ignorer . « diversité n’est pas maladie » (Canguilhem, 1943). une procréation responsable…

(i) tri des embryons. exemple du dépistage de la bêta-thalassémie à Chypre (1980 -82). objectif: empêcher la naissance d’enfants atteints d’une maladie sévère. le gène n’est pas éradiqué (ii) « faire la chasse aux gènes hétérodoxes » (Canguilhem, 1966). exemple du diagnostic de la maladie de Huntington. objectif: éradication du gène (iii) choisir un enfant possédant une caractéristique donnée. enfant sourd cependant … . exemple des maladies psychiatriques . que faire de nos vulnérabilités génétiques ?

«For the first time in history, there is now a realistic prospect that we will have the power to radically improve or alter human nature. [. . . ] Of course we are not there yet» (Herman de Dijn, in: Gastmans, 2002, p. 20). «Following Richard Dawkins, we would like to reassert that we indeed live as disposable somas, slaves of our germline genome, but could soon start rebelling against such slavery» (Weill & Radmann, 2003). le principe de justice peut-il être étendu jusqu’à inclure des injustices naturelles qu’il faudrait compenser - devons-nous à nos enfants un « minimum génétique décent » ?

«the feasibility of genetic intervention requires a profound expansion of the domain of justice» (Buchanan et al. , From Chance to Choice. Genetics and Justice, Cambridge: Univ Press, 2000) «The ideal of parental design which is accommodated by the genetic supermarket is attractive, because it overcomes certain worries about a particular group of people controlling genetic policy» (Matthew Clayton, in: Burley & Harris, p. 198) Note: discussion sur le genetic enhancement - Kennedy Institute of Ethics Journal, 2005, 15 (1)

Protéger le génome humain ? Convention concerning the protection of the world cultural and natural heritage UNESCO, 1972. protéger, conserver, transmettre le double patrimoine Convention de Rio de Janeiro, UN, 1992. préserver la biodiversité et la diversité culturelle - le pool génétique humain global est une réalité dynamique : le protéger ne saurait signifier le figer et le mettre dans un reposoir - la protection du patrimoine culturel n’empêche pas la création artistique, la protection du patrimoine génétique humain n’interdit pas d’explorer des possibilités que la nature n’a pas actualisées ________

