Elektronu transports mitohondriju elpoanas d struktra elektronu transporta





- Slides: 26

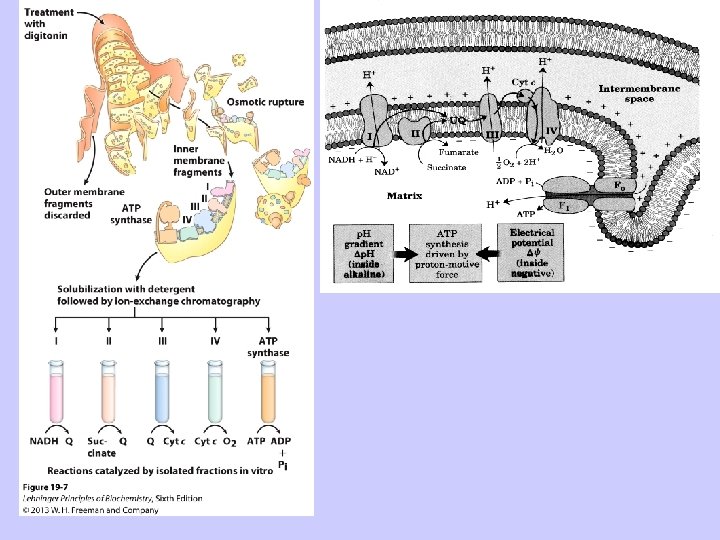
Elektronu transports mitohondriju elpošanas ķēdē: struktūra, elektronu transporta kompleksi un redoks kofaktori Elektronu transportu veic red-oks kofaktori (prostētiskās grupas), kas saistīti pie noteiktām energosajūdzošo membrānu proteīnu struktūrām – elektronu transporta kompleksiem


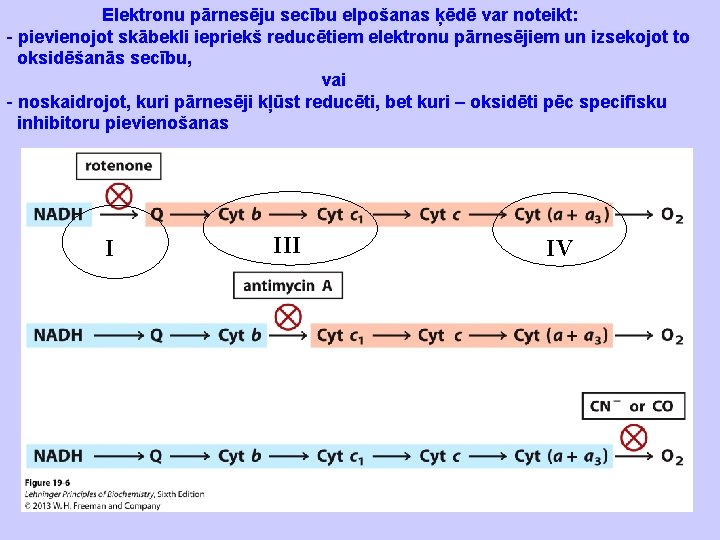
Elektronu pārnesēju secību elpošanas ķēdē var noteikt: - pievienojot skābekli iepriekš reducētiem elektronu pārnesējiem un izsekojot to oksidēšanās secību, vai - noskaidrojot, kuri pārnesēji kļūst reducēti, bet kuri – oksidēti pēc specifisku inhibitoru pievienošanas I III IV

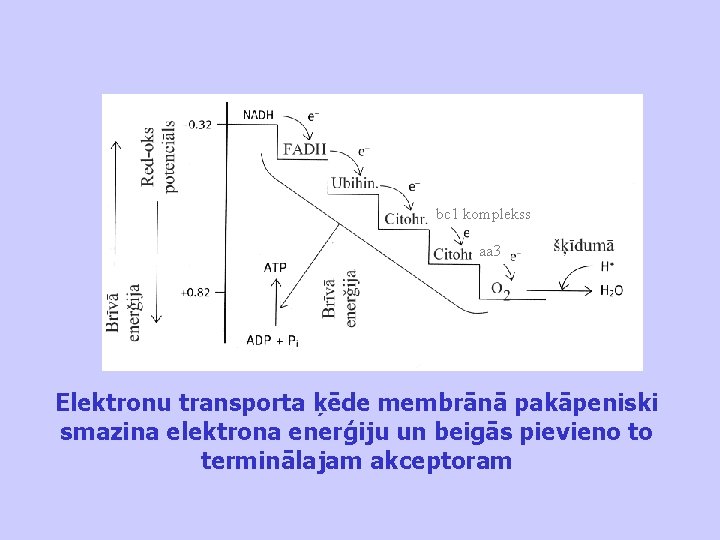
bc 1 komplekss aa 3 Elektronu transporta ķēde membrānā pakāpeniski smazina elektrona enerģiju un beigās pievieno to terminālajam akceptoram

Red-oks kofaktora vietu elpošanas ķēdē nosaka tā red-oks potenciāls Elektroni tiek pārnesti no kofaktora ar zemāko (negatīvāko) red-oks potenciālu uz kofaktoru ar augstāko (pozitīvāko) red-oks potenciālu Standarta red-oks potenciāli elpošanas ķēdē: E’ 0 [NAD+/NADH] = -320 m. V E’ 0 [UQ/UQH 2] = 45 m. V E’ 0 [1/2 O 2/H 2 O] = 816 m. V E’ 0 ķēdē =1. 14 V, kas atbilst G = 220 k. J uz 1 molu oksidēta NADH Ja mitohondrijos Gp = 57 k. J uz 1 molu sintezējamā ATP, tad oksidējot NADH molekulu izdalās enerģija, kas pietiek 3 ATP molekulu sintēzei

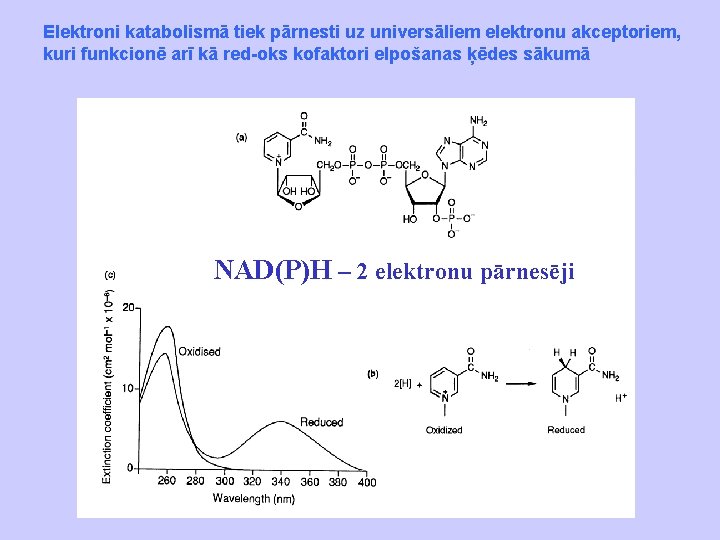
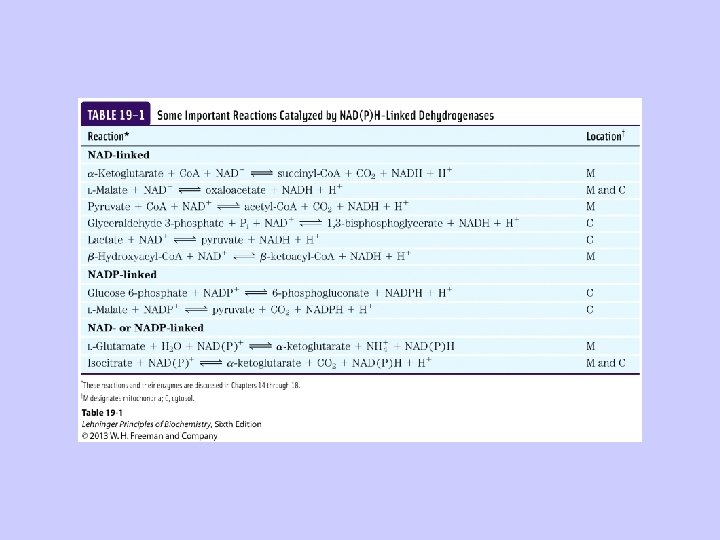
Elektroni katabolismā tiek pārnesti uz universāliem elektronu akceptoriem, kuri funkcionē arī kā red-oks kofaktori elpošanas ķēdes sākumā NAD(P)H – 2 elektronu pārnesēji


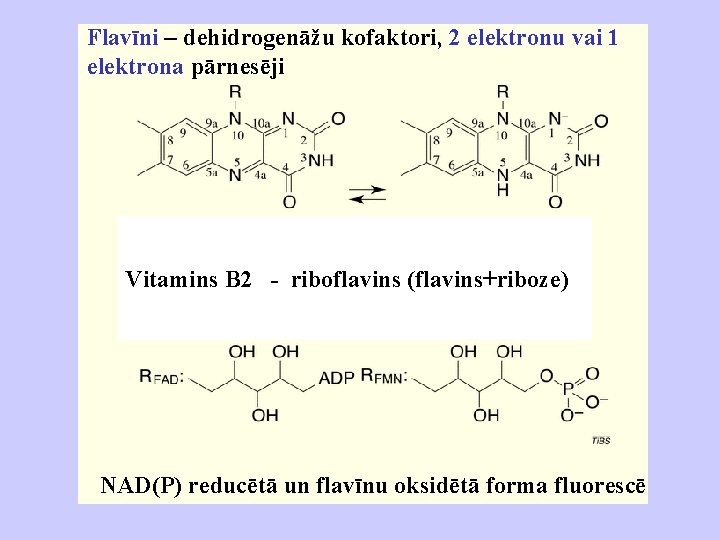
Flavīni – dehidrogenāžu kofaktori, 2 elektronu vai 1 elektrona pārnesēji Vitamins B 2 - riboflavins (flavins+riboze) NAD(P) reducētā un flavīnu oksidētā forma fluorescē

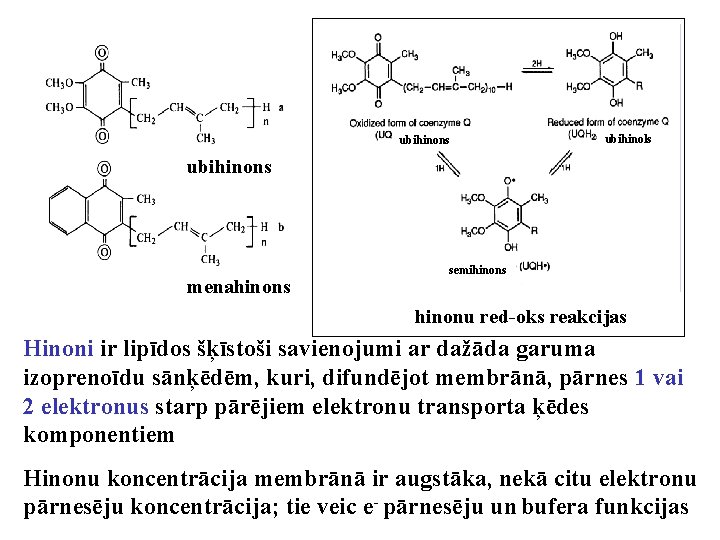
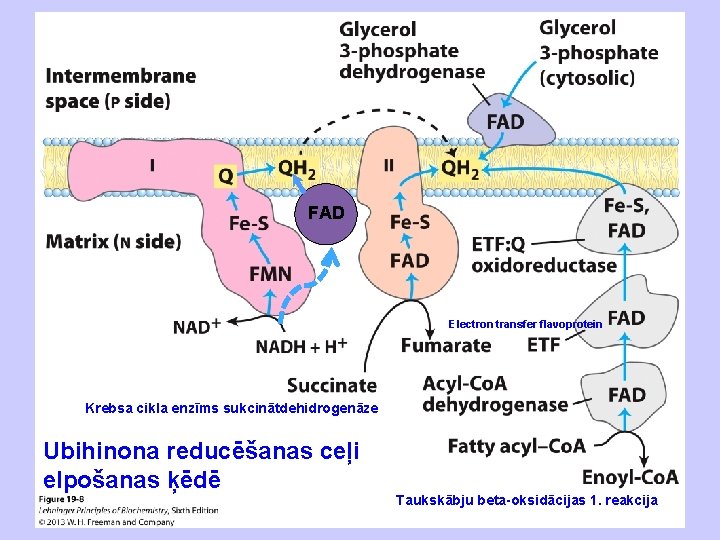
ubihinons ubihinols ubihinons menahinons semihinons hinonu red-oks reakcijas Hinoni ir lipīdos šķīstoši savienojumi ar dažāda garuma izoprenoīdu sānķēdēm, kuri, difundējot membrānā, pārnes 1 vai 2 elektronus starp pārējiem elektronu transporta ķēdes komponentiem Hinonu koncentrācija membrānā ir augstāka, nekā citu elektronu pārnesēju koncentrācija; tie veic e- pārnesēju un bufera funkcijas

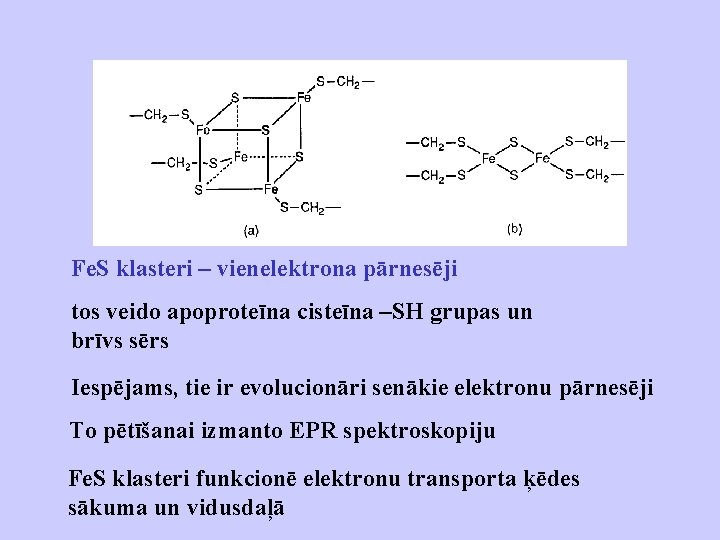
Fe. S klasteri – vienelektrona pārnesēji tos veido apoproteīna cisteīna –SH grupas un brīvs sērs Iespējams, tie ir evolucionāri senākie elektronu pārnesēji To pētīšanai izmanto EPR spektroskopiju Fe. S klasteri funkcionē elektronu transporta ķēdes sākuma un vidusdaļā

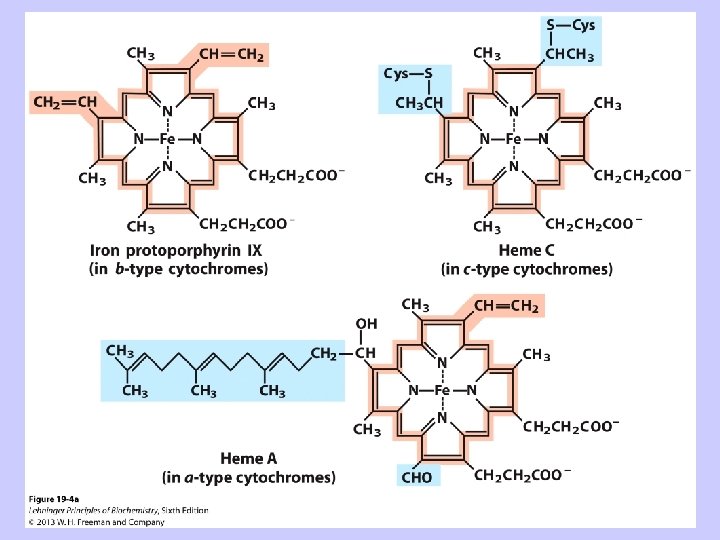
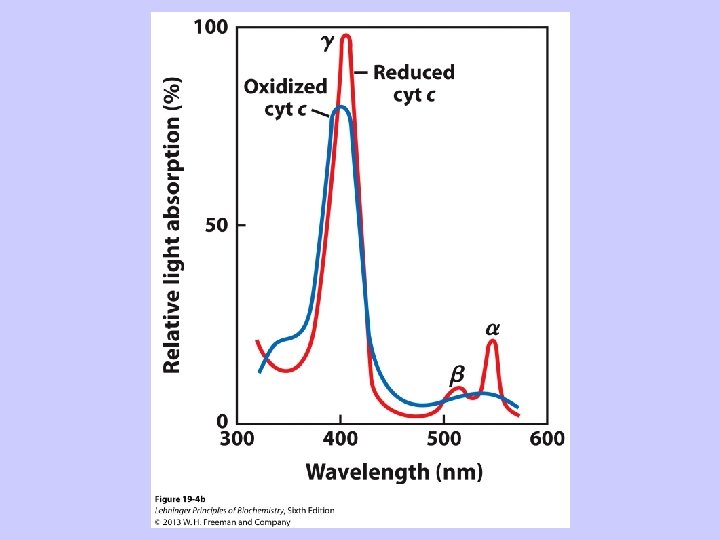
Citohromi funkcionē kā redoks kofaktori elpošanas ķēdes vidusdaļā un beigās Prostētiskā grupa – hems, jeb tetrapirola (porfirīna) gredzens ar dzelzs jonu centrā dažādu citohromu hemi atšķiras pēc aizvietotājgrupām pie porfirīna gredzena Reducētiem citohromiem raksturīga gaismas absorbcija redzamajā diapazonā: a – ap 605 nm, b – ap 560 nm, c – ap 550 nm, d – ap 630 nm (sastopams baktērijās) Kā Fe. S klasteros, tā citohromos Fe jonam saņemot un atdodot elektronus, tā oksidācijas pakāpe mainās starp Fe 2+ un Fe 3+: tie ir vienelektrona pārnesēji



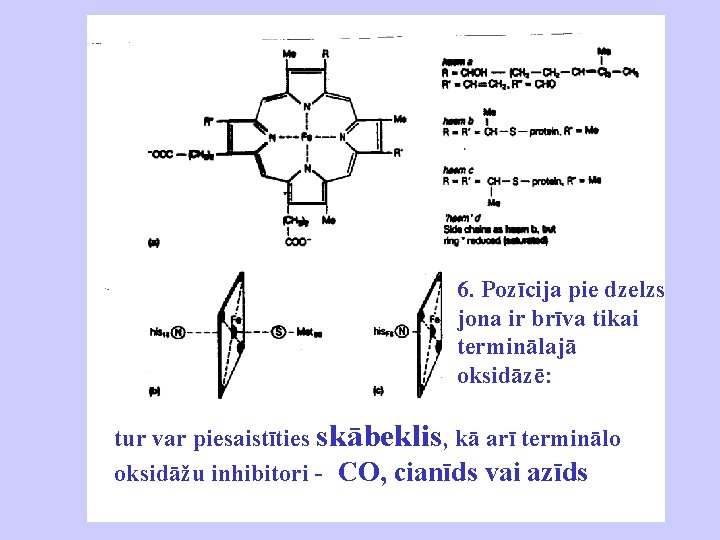
6. Pozīcija pie dzelzs jona ir brīva tikai terminālajā oksidāzē: tur var piesaistīties skābeklis, kā arī terminālo oksidāžu inhibitori - CO, cianīds vai azīds

FAD Electron transfer flavoprotein Krebsa cikla enzīms sukcinātdehidrogenāze Ubihinona reducēšanas ceļi elpošanas ķēdē Taukskābju beta-oksidācijas 1. reakcija

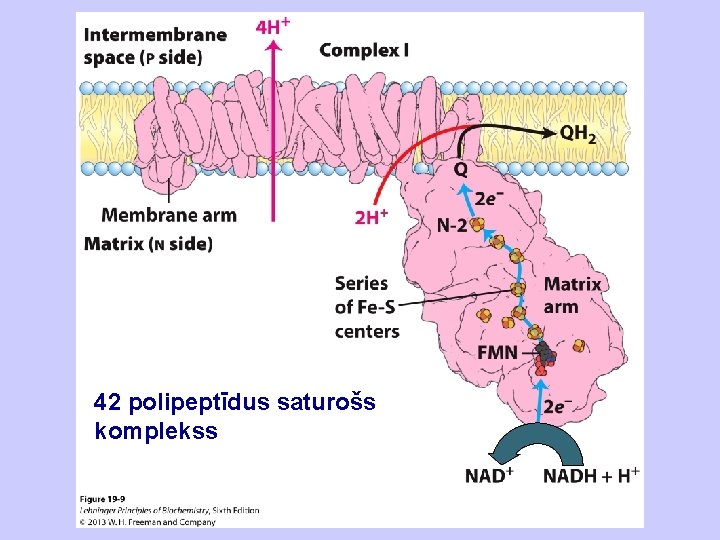
42 polipeptīdus saturošs komplekss

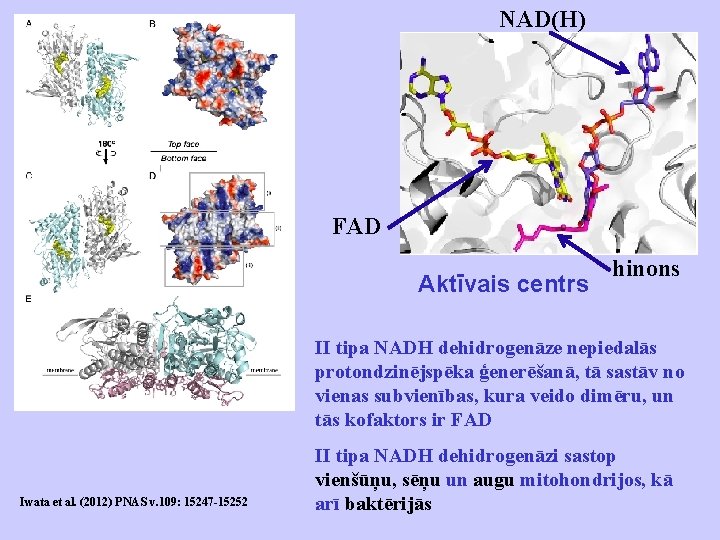
NAD(H) FAD Aktīvais centrs hinons II tipa NADH dehidrogenāze nepiedalās protondzinējspēka ģenerēšanā, tā sastāv no vienas subvienības, kura veido dimēru, un tās kofaktors ir FAD Iwata et al. (2012) PNAS v. 109: 15247 -15252 II tipa NADH dehidrogenāzi sastop vienšūņu, sēņu un augu mitohondrijos, kā arī baktērijās

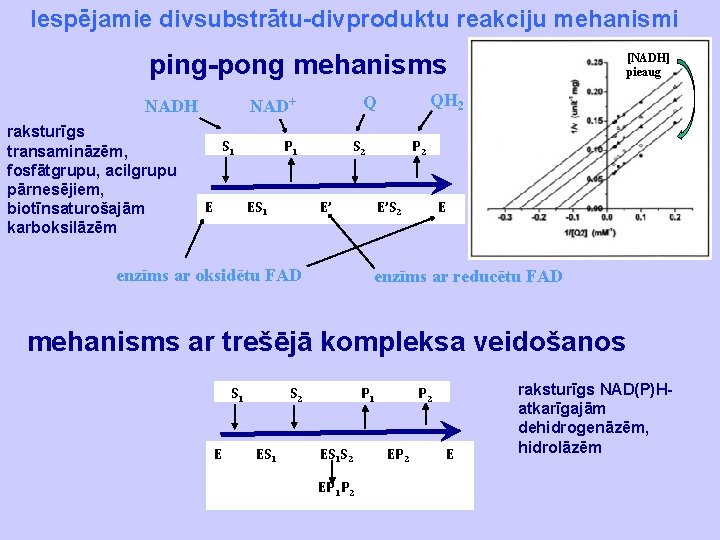
Iespējamie divsubstrātu-divproduktu reakciju mehanismi ping-pong mehanisms raksturīgs transamināzēm, fosfātgrupu, acilgrupu pārnesējiem, biotīnsaturošajām karboksilāzēm S 1 E P 1 ES 1 QH 2 Q NAD+ NADH S 2 P 2 E’ enzīms ar oksidētu FAD [NADH] pieaug E’S 2 E enzīms ar reducētu FAD mehanisms ar trešējā kompleksa veidošanos S 1 E S 2 ES 1 P 1 ES 1 S 2 EP 1 P 2 EP 2 E raksturīgs NAD(P)Hatkarīgajām dehidrogenāzēm, hidrolāzēm

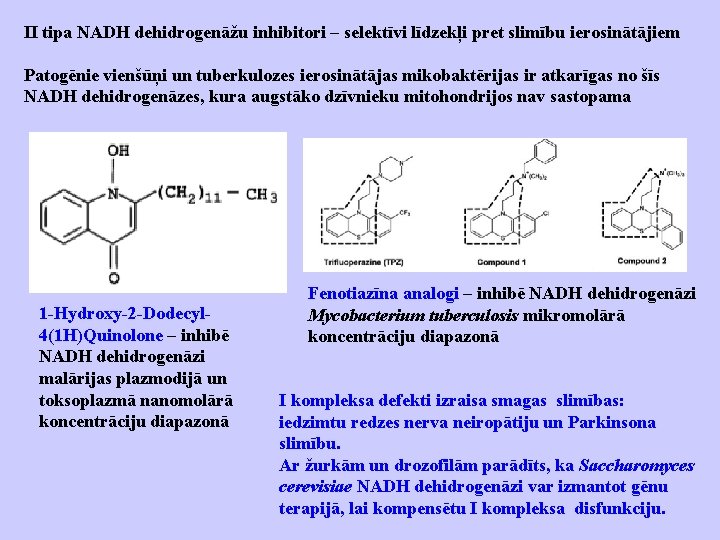
II tipa NADH dehidrogenāžu inhibitori – selektīvi līdzekļi pret slimību ierosinātājiem Patogēnie vienšūņi un tuberkulozes ierosinātājas mikobaktērijas ir atkarīgas no šīs NADH dehidrogenāzes, kura augstāko dzīvnieku mitohondrijos nav sastopama 1 -Hydroxy-2 -Dodecyl 4(1 H)Quinolone – inhibē NADH dehidrogenāzi malārijas plazmodijā un toksoplazmā nanomolārā koncentrāciju diapazonā Fenotiazīna analogi – inhibē NADH dehidrogenāzi Mycobacterium tuberculosis mikromolārā koncentrāciju diapazonā I kompleksa defekti izraisa smagas slimības: iedzimtu redzes nerva neiropātiju un Parkinsona slimību. Ar žurkām un drozofilām parādīts, ka Saccharomyces cerevisiae NADH dehidrogenāzi var izmantot gēnu terapijā, lai kompensētu I kompleksa disfunkciju.

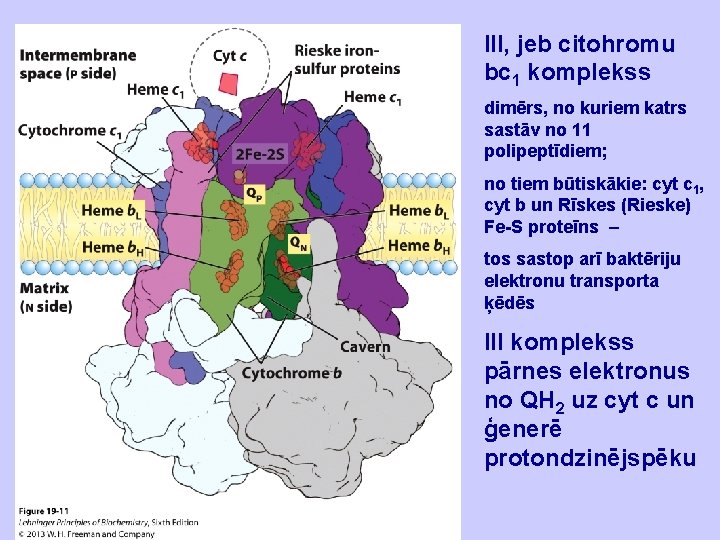
III, jeb citohromu bc 1 komplekss dimērs, no kuriem katrs sastāv no 11 polipeptīdiem; no tiem būtiskākie: cyt c 1, cyt b un Rīskes (Rieske) Fe-S proteīns – tos sastop arī baktēriju elektronu transporta ķēdēs III komplekss pārnes elektronus no QH 2 uz cyt c un ģenerē protondzinējspēku

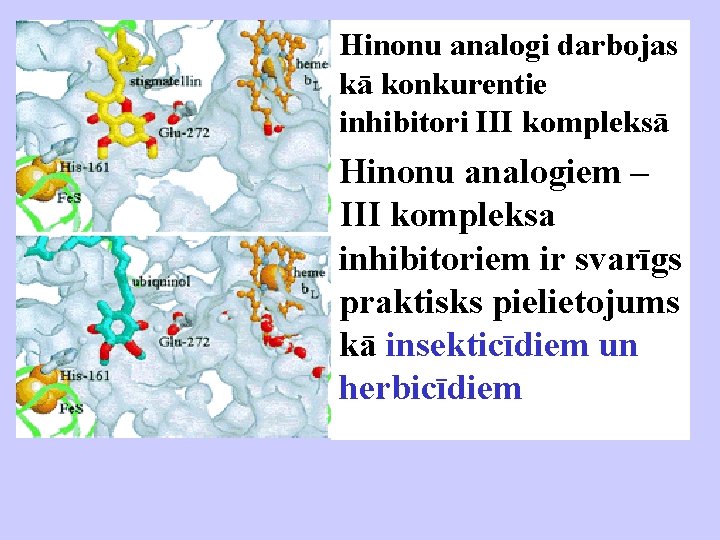
Hinonu analogi darbojas kā konkurentie inhibitori III kompleksā Hinonu analogiem – III kompleksa inhibitoriem ir svarīgs praktisks pielietojums kā insekticīdiem un herbicīdiem

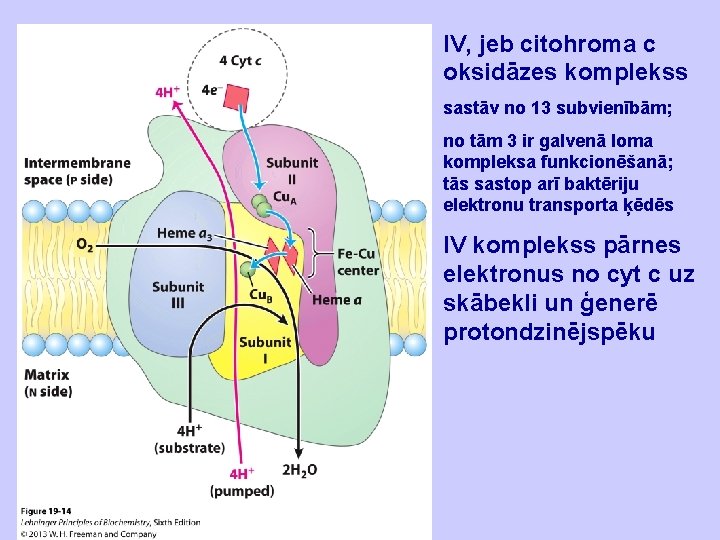
IV, jeb citohroma c oksidāzes komplekss sastāv no 13 subvienībām; no tām 3 ir galvenā loma kompleksa funkcionēšanā; tās sastop arī baktēriju elektronu transporta ķēdēs IV komplekss pārnes elektronus no cyt c uz skābekli un ģenerē protondzinējspēku

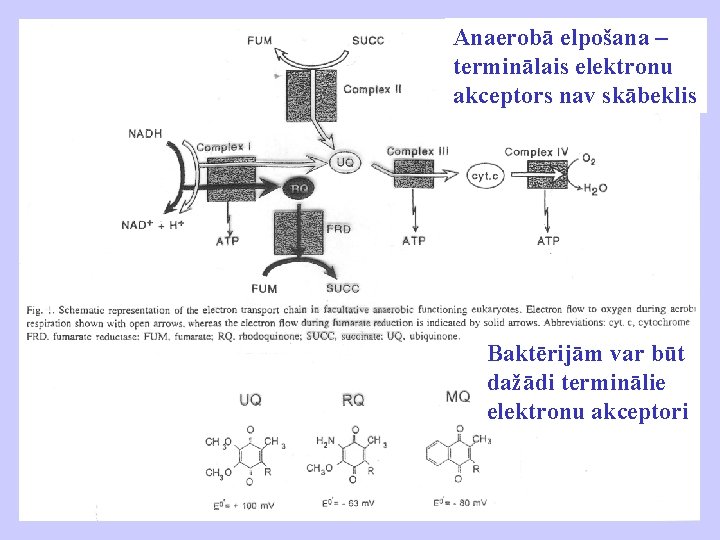
Anaerobā elpošana – terminālais elektronu akceptors nav skābeklis Baktērijām var būt dažādi terminālie elektronu akceptori

Lenaz and Genova (2007) Am. JPhysiol. Cell. Physiol v. 292 C 1221 C 1239 Vai elpošanas ķēdes kompleksi savstarpēji mijiedarbojoties veido superkompleksus, kuru iekšienē elektronu pārnese ir stingri ‘kanalizēta’ (Chance and Williams (1955) JBiol. Chem v. 217: 409 -427) vai elektronu pārnesi var izskaidrot tikai ar brīvu kompleksu un hinona molekulu difūziju lipīdu dubultslānī un to nejaušām sadursmēm (Hackenbrock et al. (1986) JBioenerg. Biomembr v. 18: 331 -368) ?

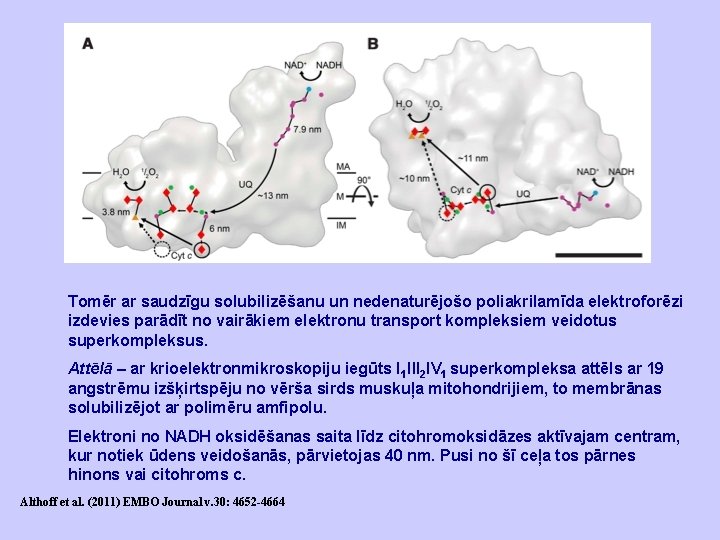
Tomēr ar saudzīgu solubilizēšanu un nedenaturējošo poliakrilamīda elektroforēzi izdevies parādīt no vairākiem elektronu transport kompleksiem veidotus superkompleksus. Attēlā – ar krioelektronmikroskopiju iegūts I 1 III 2 IV 1 superkompleksa attēls ar 19 angstrēmu izšķirtspēju no vērša sirds muskuļa mitohondrijiem, to membrānas solubilizējot ar polimēru amfipolu. Elektroni no NADH oksidēšanas saita līdz citohromoksidāzes aktīvajam centram, kur notiek ūdens veidošanās, pārvietojas 40 nm. Pusi no šī ceļa tos pārnes hinons vai citohroms c. Althoff et al. (2011) EMBO Journal v. 30: 4652 -4664

Elektronu transports notiek: • pateicoties pārnesēju (hinonu) difūzijai • kā tunelēšana (elektronu “pārlekšana”) starp 2 paralēli orientētām un ne tālāk kā 20 Å vienu no otras situētām red-oks (piem. citohromu hema) grupām e • elektronu transporta kompleksu proteīnu subvienības tieši nepiedalās elektronu pārnesē; to funkcija ir nodrošināt atbilstošu red-oks grupu orientāciju un mikrovidi ap tām