IEVADS NAS BIOLOIJ I DZVBAS MIJA ATOMA UZBVE

IEVADS ŠŪNAS BIOLOĢIJĀ I DZĪVĪBAS ĶĪMIJA ATOMA UZBŪVE, ELEMENTU PERIODISKĀ SISTĒMA, ĶĪMISKĀS SAITES, ŪDENS ĪPAŠĪBAS, p. H

2. LEKCIJA ATOMA UZBŪVE, ELEMENTU PERIODISKĀ SISTĒMA, ĶĪMISKĀS SAITES, ŪDENS ĪPAŠĪBAS, p. H · Atomu uzbūves principi. · Elementu periodiskā sistēma. Biogēnie elementi. · Ķīmiskās saites un starpmolekulu mijiedarbības: jonu saite; kovalentā saite; Van-der-Valsa spēki; ūdeņraža saite · Ūdens bioloģiski nozīmīgās īpašības · p. H, skābes un sārmi
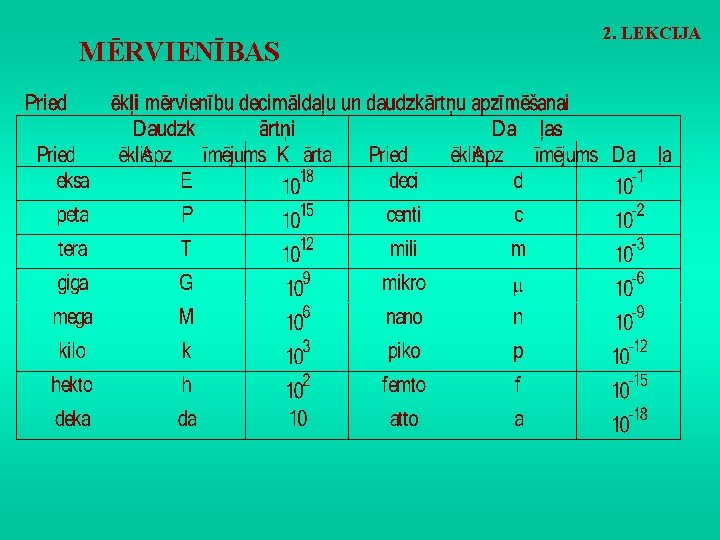
MĒRVIENĪBAS 2. LEKCIJA

MĒRVIENĪBAS 2. LEKCIJA Dažu bioloģijā izmantojamo ārpussitēmas mērvienību izcelsme: Atmosfēra – zemes atmosfēras spiediens jūras līmenī. Kalorija – siltuma daudzums, kas jāizlieto, lai uzsildītu vienu gramu ūdens par vienu grādu celsija.

Atomu uzbūves principi. 2. LEKCIJA Atomu veidojošās daļiņas Protoni + neitroni = atoma kodols, pozitīvs elektriskais lādiņš. Elektroni veido atoma apvalku, negatīvs elektriskais lādiņš.

Atomu uzbūves principi. 2. LEKCIJA Atoma skaitlis – protonu vai elektronu skaits atomā Atoma masas skaitlis – protonu un neitronu kopskaits atoma kodolā http: //biology. wright. edu/faculty/krane/112/lectures/96/lec 2. html#hy
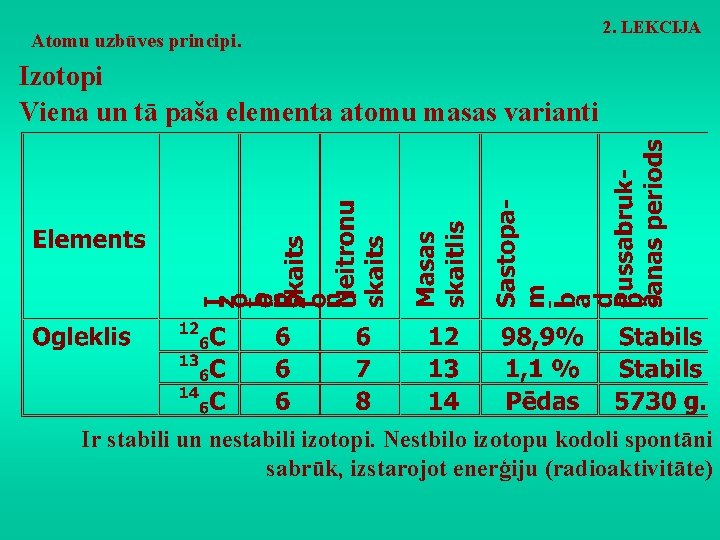
Atomu uzbūves principi. 2. LEKCIJA Izotopi Viena un tā paša elementa atomu masas varianti Ir stabili un nestabili izotopi. Nestbilo izotopu kodoli spontāni sabrūk, izstarojot enerģiju (radioaktivitāte)

Atomu uzbūves principi. 2. LEKCIJA Atoma masas vienība – viena divpadsmitā daļa no oglekļa atoma masas, aptuveni vienlīdzīga protona masai. Molekulas masa - molekulu veidojošo atomu masas summa. Atoma masas vienības ekvivalents gramos: Daltons (Da) ~ 1, 66 x 10 -24 grami.

2. LEKCIJA Ķīmiskā saite: mola jēdziens Veidojot ķīmiskās saites atomi mijiedarbojas noteiktās veselu skaitļu attiecībās: viens atoms ar vienu, diviem, trim, utt. , bet ne ar pusotru citu atomu (stehiometrija). Atomu (arī molekulu un jonu) daudzuma mērvienība ir mols. Viens mols jebkura atoma (molekulas, jonu) satur 6, 02 x 1023 daļiņu.

2. LEKCIJA Ķīmiskā saite: mola jēdziens 6, 02 x 1023 = Avogadro skaitlis, ķīmiska konstante: oglekļa atomu skaits, kuru kopējā masa ir 12 grami. Avogadro skaitlis norāda atomu vai molekulu skaitu molā. Amadeus Avogadro (1776 - 1856) - itāļu ķīmiķis, kurš ievēroja, ka gāzes savā starpā reaģē noteiktās tilpuma attiecībās. 22, 4 litri = gāzu molārais tilpums, ko aizpilda viens mols jebkuras gāzes atomu vai molekulu http: //dbhs. wvusd. k 12. ca. us/Mole/Molar. Mass. html http: //ask. yahoo. com/ask/19991123. html

2. LEKCIJA Ķīmiskā saite: mola jēdziens GRAMMOLS Jebkuru 6, 02 x 1023 atomu vai molekulu masa gramos, kas ir skaitliski vienāda ar viena atoma vai molekulas masu, kas aprēķināta atoma masas vienībās.
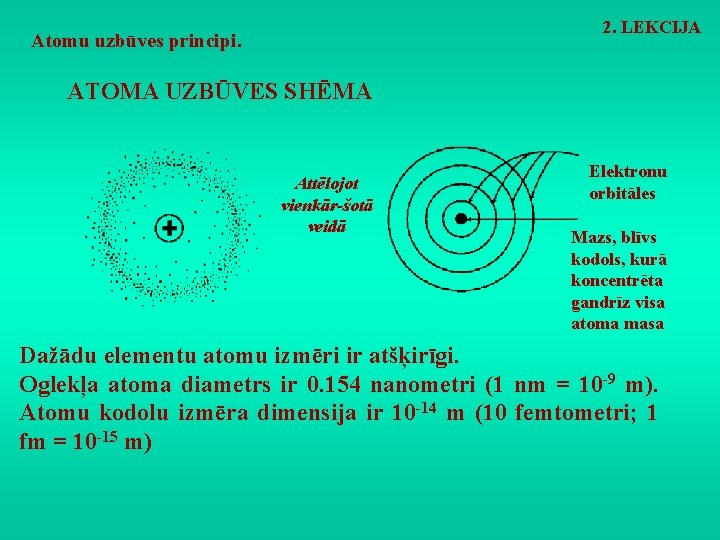
2. LEKCIJA Atomu uzbūves principi. ATOMA UZBŪVES SHĒMA Attēlojot vienkār-šotā veidā Elektronu orbitāles Mazs, blīvs kodols, kurā koncentrēta gandrīz visa atoma masa Dažādu elementu atomu izmēri ir atšķirīgi. Oglekļa atoma diametrs ir 0. 154 nanometri (1 nm = 10 -9 m). Atomu kodolu izmēra dimensija ir 10 -14 m (10 femtometri; 1 fm = 10 -15 m)

Atomu uzbūves principi: kvantu ķīmija 2. LEKCIJA ATOMA ELEKTRONU APVALKA UZBŪVE Elektroni ap atoma kodolu izvietoti noteiktos enerģijas līmeņos, kurus apzīmē ar burtiem: K; L; M, utt. Vienu enerģijas līmeni veido viens vairāki apakšlīmeņi, kurus apzīmē ar burtiem: s; p; d, utt. Katru enerģijas apakšlīmeni aizpilda raksturīgas un noteikta skaita formas elektronu orbitāles (čaulas).

Atomu uzbūves principi: kvantu ķīmija 2. LEKCIJA ATOMA ELEKTRONU APVALKA UZBŪVE Telpas daļu, kurā ar noteiktu varbūtību atrodas elektrons, sauc par elektrona orbitāli. Vienā orbitālē vienlaikus var atrasties divi elektroni ar pretējiem magnētiskajiem griezes momentiem - spiniem. Orbitāles un apakšlīmeņi aizpildās pakāpeniski, maksimāli izmantojot zemākos enerģētiskos līmeņus.

2. LEKCIJA Atomu uzbūves principi: kvantu ķīmija BIOGĒNO MAKROELEMENTU ATOMU UZBŪVE Viens enerģijas līmenis - ūdeņradis, 1 H. Divi enerģijas līmeņi ogleklis, 6 C; slāpeklis, 7 N; skābeklis, 8 O. Trīs enerģijas līmeņi fosfors, 15 P; sērs, 16 S.
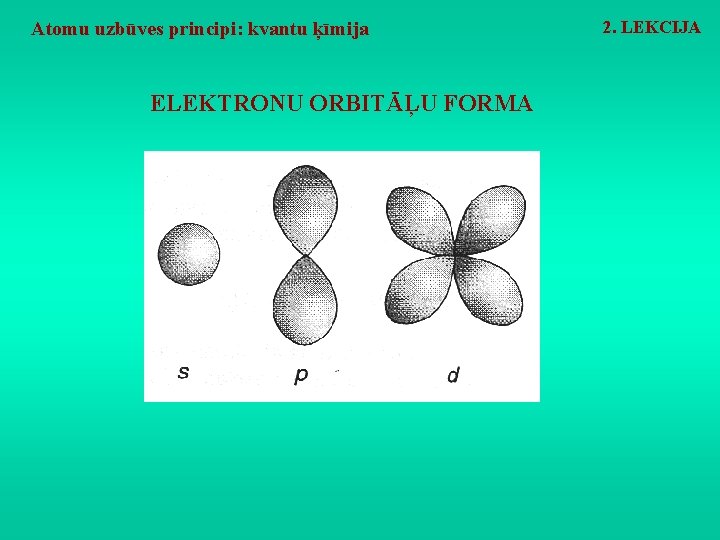
Atomu uzbūves principi: kvantu ķīmija ELEKTRONU ORBITĀĻU FORMA 2. LEKCIJA
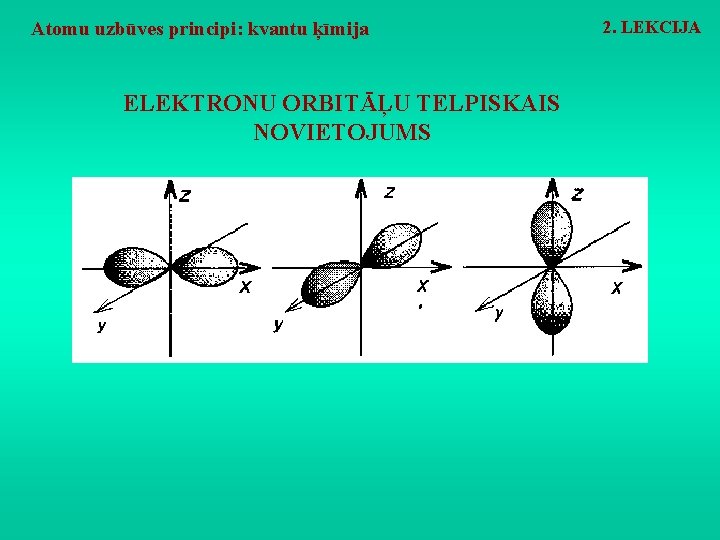
Atomu uzbūves principi: kvantu ķīmija ELEKTRONU ORBITĀĻU TELPISKAIS NOVIETOJUMS 2. LEKCIJA
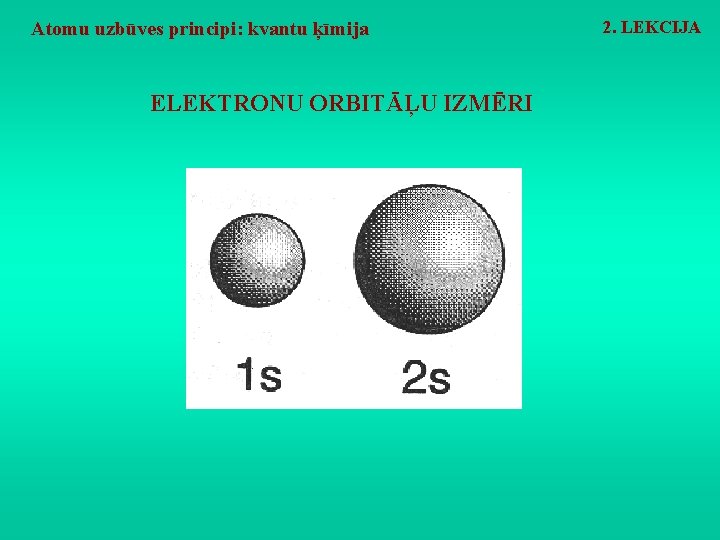
Atomu uzbūves principi: kvantu ķīmija ELEKTRONU ORBITĀĻU IZMĒRI 2. LEKCIJA
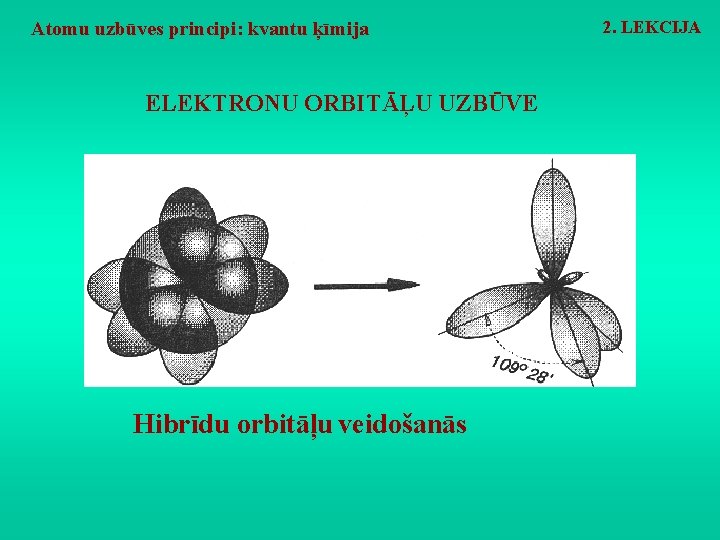
Atomu uzbūves principi: kvantu ķīmija ELEKTRONU ORBITĀĻU UZBŪVE Hibrīdu orbitāļu veidošanās 2. LEKCIJA

Atomu uzbūves principi. 2. LEKCIJA ELEMENTU ĪPAŠĪBAS NOSAKA TO ELEKTRONU APVALKU UZBŪVE, ĪPAŠI ĀRĒJĀ ELEKTRONU ENERĢĒTISKĀ LĪMEŅA AIZPILDĪJUMS SAKĀRTOJOT ELEMENTUS ELEKTRONU ENERĢĒTISKO LĪMEŅU SKAITA PIEAUGUMA UN ŠO LĪMEŅU AIZPILDĪJUMA SECĪBĀ, IEGŪSTAM ELEMENTU PERIODISKO SISTĒMU
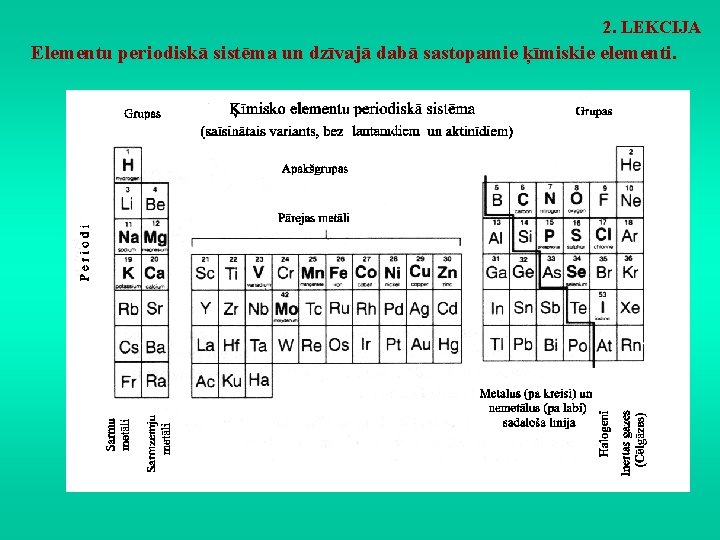
2. LEKCIJA Elementu periodiskā sistēma un dzīvajā dabā sastopamie ķīmiskie elementi.

2. LEKCIJA ŠŪNAS ĶĪMISKAIS SASTĀVS, GALVENIE BIOGĒNIE ELEMENTI. Dabā satopami 92 ķīmiskie elementi, vēl 17 elementi (109. – meitnerijs) iegūti laboratorijas apstākļos. Dzīvās dabas objektus veido 25 – 26 elementi; vēl 10 – 15 elementi ir sastopami toksisko savienojumu vai ārstniecisko preparātu sastāvā.

2. LEKCIJA Elementu periodiskā sistēma un dzīvajā dabā sastopamie ķīmiskie elementi. Sr
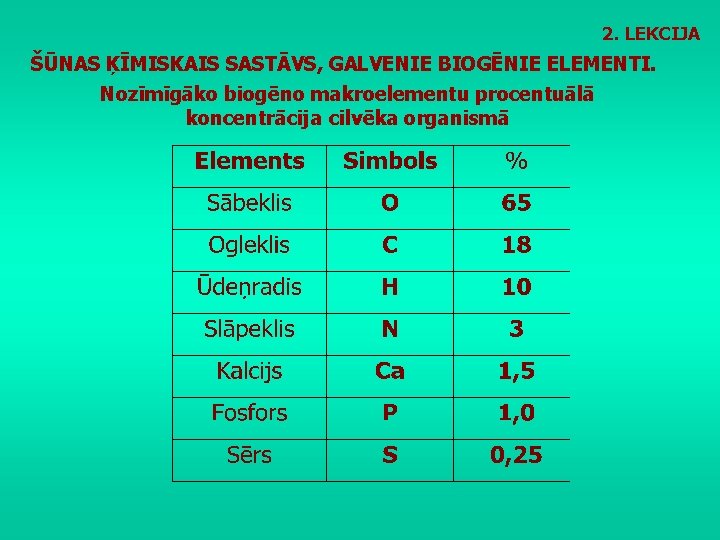
2. LEKCIJA ŠŪNAS ĶĪMISKAIS SASTĀVS, GALVENIE BIOGĒNIE ELEMENTI. Nozīmīgāko biogēno makroelementu procentuālā koncentrācija cilvēka organismā

2. LEKCIJA ŠŪNAS ĶĪMISKAIS SASTĀVS, GALVENIE BIOGĒNIE ELEMENTI. Šūnas masas lielāko daļu veido ūdens. Šūnas karsējot, ūdens iztvaiko, paliek šūnas sausne.
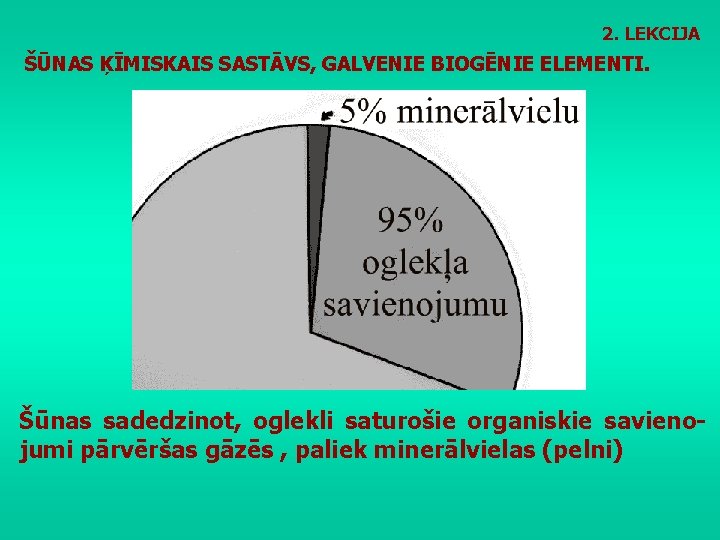
2. LEKCIJA ŠŪNAS ĶĪMISKAIS SASTĀVS, GALVENIE BIOGĒNIE ELEMENTI. Šūnas sadedzinot, oglekli saturošie organiskie savienojumi pārvēršas gāzēs , paliek minerālvielas (pelni)

2. LEKCIJA ŠŪNAS ĶĪMISKAIS SASTĀVS. Citu nozīmīgāko elementu procentuālā koncentrācija cilvēka organismā

2. LEKCIJA ŠŪNAS ĶĪMISKAIS SASTĀVS. Nozīmīgāko mikroelementu procentuālā koncentrācija cilvēka organismā Mikroelementi atrodami organismā koncentrācijā, kas mazāka par vienu procenta simtdaļu (0, 01 %) Kopumā tie veido ap 0, 1% no organisma masas Dzelzs (Fe) – biežāk sastopamais mikroelements 0, 0050 – 0, 0075 % cilvēka masas jeb 4 – 5 g 70 kg smaga cilvēka organismā.
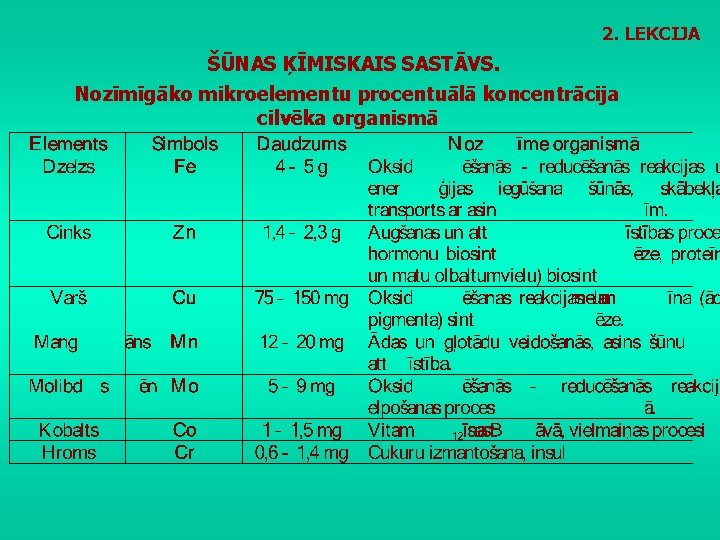
2. LEKCIJA ŠŪNAS ĶĪMISKAIS SASTĀVS. Nozīmīgāko mikroelementu procentuālā koncentrācija cilvēka organismā

2. LEKCIJA ŠŪNAS ĶĪMISKAIS SASTĀVS. Nozīmīgāko mikroelementu procentuālā koncentrācija cilvēka organismā Citi nozīmīgākie mikroelementi: litijs (Li) selēns (Se) fluors (F) jods (I) regulēšana. – nervu darbības regulēšana; – olbaltumvielu biosintēze, mati; – kaulu un zobu attīstība; – hormonu sintēze, nervu darbības Ultramikroelementi: arsēns (As) un kadmijs (Cd) – augšanas un vielmaiņas regulēšana.

2. LEKCIJA ĶĪMISKĀ SAITE Atomi veido molekulas, izmantojot mijiedarbību starp ārējā enerģētiskā līmeņa elektroniem. Ārējā enerģētiskā līmeņa elektroni = valences elektroni, nosaka, cik ķīmisko saišu spēj veidot atoms.

2. LEKCIJA ĶĪMISKĀ SAITE Mijiedarbības starp atomiem aizpilda elektronu ārējos enerģētiskos līmeņus. Ārējos enerģētiskos līmeņus var aizpildīt: • atdodot • pievienojot elektronus; • veidojot kopējus elektronu pārus.

2. LEKCIJA ĶĪMISKĀ SAITE Elektronus atdod atomi, kuru ārējais enerģetiskais līmenis ir maz aizpildīts, tipiski: 1 - 2 elektroni. Elektronus pievieno atomi, kuru ārejais enerģētiskais līmenis gandrīz pilns, tipiski: 6 - 7 elektroni. Kopējus elektronu pārus veido atomi, kuru ārējais enerģetiskais līmenis ir vidēji aizpildīts, tipiski: 3 - 5 elektroni.

2. LEKCIJA ĶĪMISKĀ SAITE Atomi, kuru ārejais enerģetiskais līmenis ir pilns ( 8 elektroni) ķīmiskās saites neveido. Jo tālāk no atoma kodola ir elektronu ārējais līmenis (lielāks atoms), jo vieglāk atņemt tajos esošos elektronus. Jo tuvāk atoma kodolam ir elektronu ārējais līmenis (mazāks atoms), jo aktīvāk tas piesaista elektronus.

2. LEKCIJA Daļiņas, kuras veidojas atomiem atdodot vai piesaistot elektronus sauc par JONIEM.

2. LEKCIJA Ķīmiskā saite : jonu saite - e-- Atomi ar maz aizpildītu elektronu ārējo enerģētisko līmeni elektronus viegli atdod. Elektrona atdošana - oksidēšanās
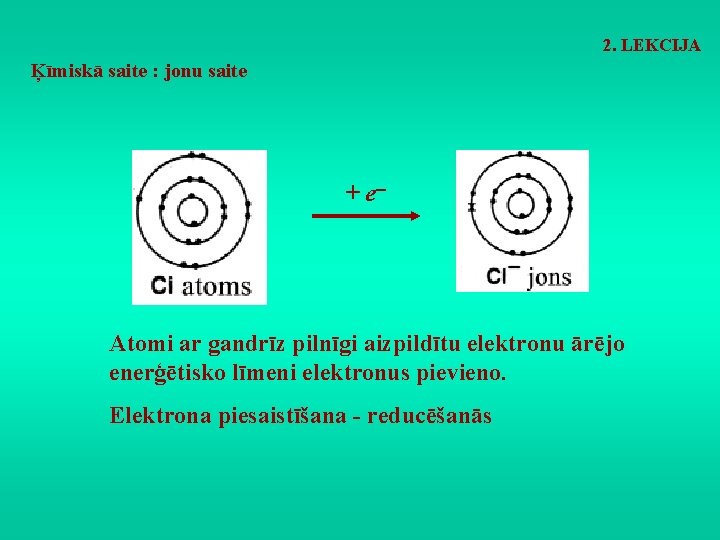
2. LEKCIJA Ķīmiskā saite : jonu saite + e-- Atomi ar gandrīz pilnīgi aizpildītu elektronu ārējo enerģētisko līmeni elektronus pievieno. Elektrona piesaistīšana - reducēšanās

2. LEKCIJA Ķīmiskā saite : jonu saite Oksidēšanās un reducēšanās reakcijas vienmēr ir saistītas Red-oks reakcijas. Oksidētājs reducējas, reducētājs oksidējas

2. LEKCIJA Ķīmiskā saite : jonu saite Oksidēšanās vai reducēšanās procesos atomi atdod vai pievieno elektronus OKSIDĒŠANĀS - elektrona (e-) atdošana REDUCĒŠANĀS - elektrona (e-) pievienošana
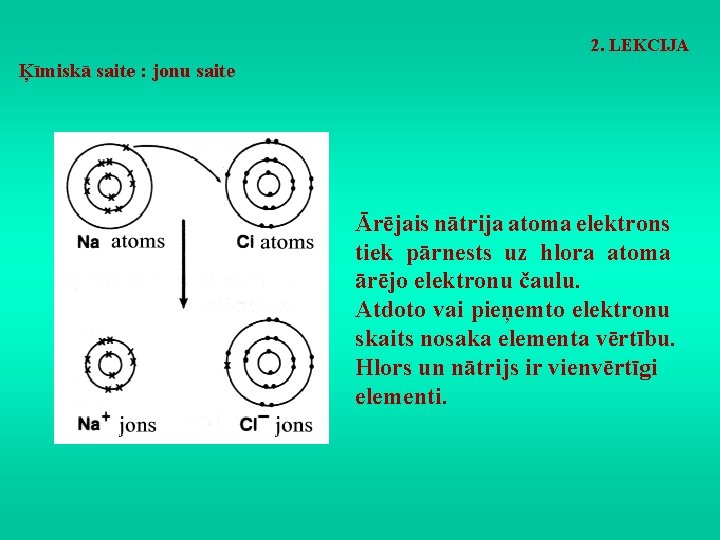
2. LEKCIJA Ķīmiskā saite : jonu saite Ārējais nātrija atoma elektrons tiek pārnests uz hlora atoma ārējo elektronu čaulu. Atdoto vai pieņemto elektronu skaits nosaka elementa vērtību. Hlors un nātrijs ir vienvērtīgi elementi.

2. LEKCIJA Ķīmiskā saite : jonu saite Cietā agregātstāvoklī nātrija hlorīda struktūru veido elektrostatiskas mijiedarbības starp pretēji lādētiem joniem. Elektrostatisku mijiedarbību starp pretēji lādētiem joniem sauc par JONU SAITI Enerģija: 4 – 7 kcal/mols

2. LEKCIJA Ķīmiskā saite : jonu saite Oksidēt vai reducēt var arī atomus, kas atrodas molekulu sastāvā. Molekulu daļas oksidējas vai reducējas, ja mainās elektronu skaits tās veidojošajiem atomiem.

2. LEKCIJA Ķīmiskā saite : jonu saite UZ MOLEKULAS OKSIDĒŠANOS norāda: Ūdeņraža atdošana Skābekļa pievienošana UZ MOLEKULAS REDUCĒŠANOS norāda: Ūdeņraža pievienošana Skābekļa atdošana
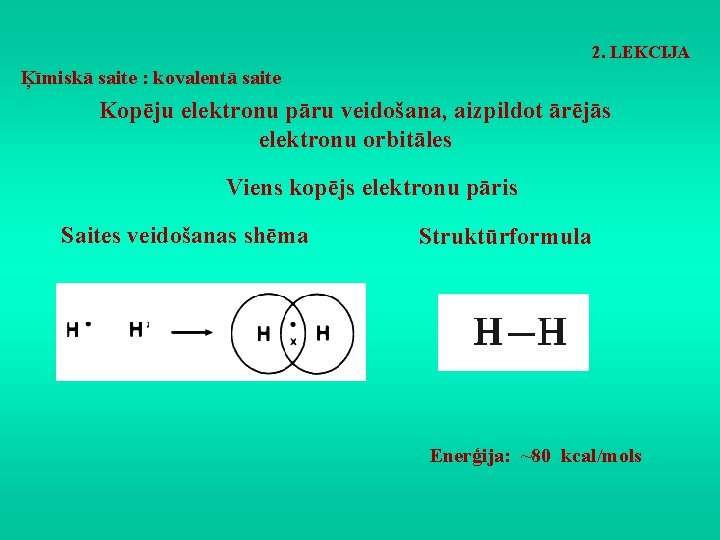
2. LEKCIJA Ķīmiskā saite : kovalentā saite Kopēju elektronu pāru veidošana, aizpildot ārējās elektronu orbitāles Viens kopējs elektronu pāris Saites veidošanas shēma Struktūrformula Enerģija: ~80 kcal/mols

2. LEKCIJA Ķīmiskā saite : kovalentā saite Kopēju elektronu pāru veidošana, aizpildot ārējās elektronu orbitāles Divi kopēji elektronu pāri Saites veidošanas shēma Struktūrformula Enerģija: ~150 kcal/mols

2. LEKCIJA Ķīmiskā saite : kovalentā saite Kopēju elektronu pāru veidošana, aizpildot ārējās elektronu orbitāles Trīs kopēji elektronu pāri Saites veidošanas shēma Struktūrformula Enerģija: ~200 kcal/mols
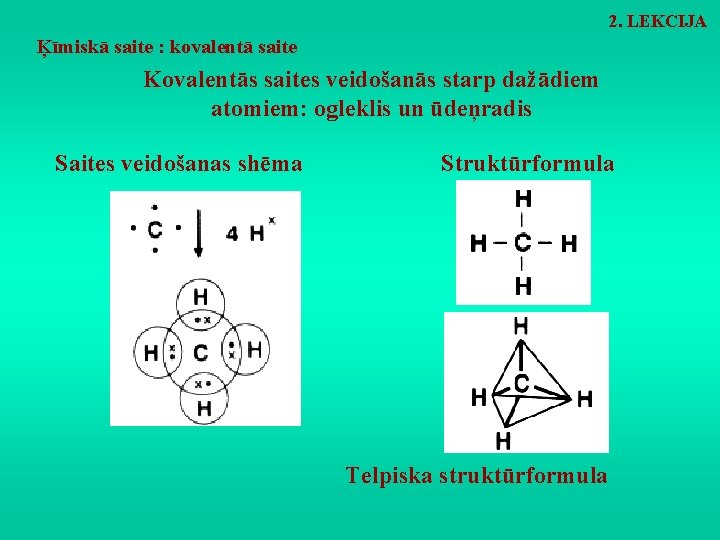
2. LEKCIJA Ķīmiskā saite : kovalentā saite Kovalentās saites veidošanās starp dažādiem atomiem: ogleklis un ūdeņradis Saites veidošanas shēma Struktūrformula Telpiska struktūrformula

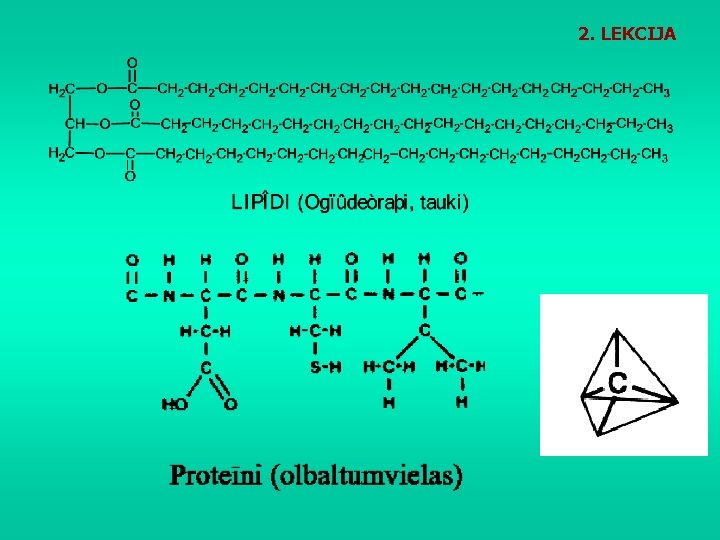
2. LEKCIJA Dzīvībai raksturīgo savienojumu molekulas sastāv lielākoties no garām oglekļa atomu ķēdēm
2. LEKCIJA

Ķīmiskās saites 2. LEKCIJA Jonu saiti veidojot, atomu ķīmisko vērtību (valenci) nosaka atdoto vai pārņemto elektronu skaits. Kovalento saiti veidojot, atomu ķīmisko vērtību (valenci) nosaka kopējo elektronu pāru skaits. Nepolārās kovalentās saites – elektronu pāris atrodas vidū starp saiti veidojošajiem atomiem. Polārās kovalentās saites – elektronu pāris nobīdīts tuvāk elektronegatīvākajam atomam. Kovalentās saites veido bioloģisko makromolekulu struktūras pamatu.

2. LEKCIJA Starpmolekulu mijiedarbības spēki Mijiedarbības starp molekulām stabilizē elektrisko lādiņu sadalījumu.
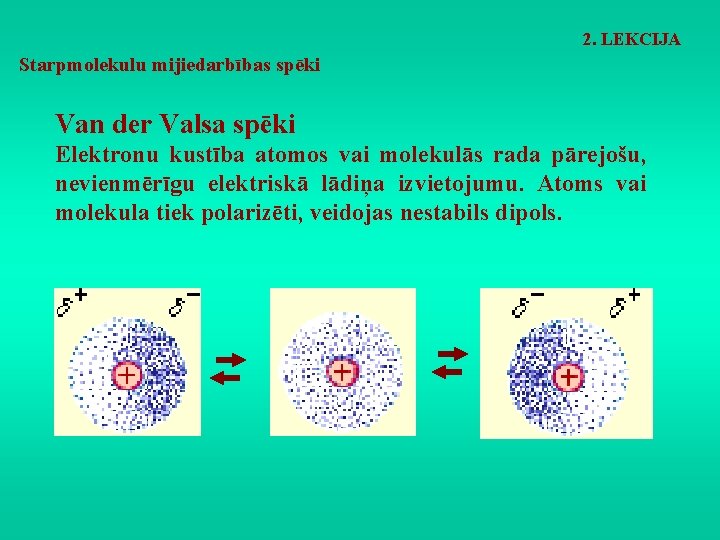
2. LEKCIJA Starpmolekulu mijiedarbības spēki Van der Valsa spēki Elektronu kustība atomos vai molekulās rada pārejošu, nevienmērīgu elektriskā lādiņa izvietojumu. Atoms vai molekula tiek polarizēti, veidojas nestabils dipols.
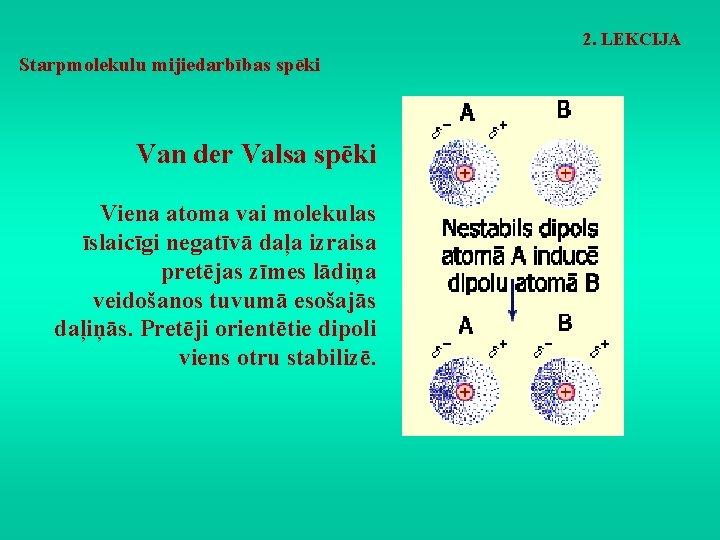
2. LEKCIJA Starpmolekulu mijiedarbības spēki Van der Valsa spēki Viena atoma vai molekulas īslaicīgi negatīvā daļa izraisa pretējas zīmes lādiņa veidošanos tuvumā esošajās daļiņās. Pretēji orientētie dipoli viens otru stabilizē.

2. LEKCIJA Starpmolekulu mijiedarbības spēki Van der Valsa spēki Lielās molekulās (polimeros) šādu mijiedarbību spēks var būt ļoti liels. Bioloģisko makromolekulu struktūru veidošanā Van der Valsa spēkiem ir būtiska loma. Enerģija: 1 - 2 kcal/mols

2. LEKCIJA Starpmolekulu mijiedarbības spēki Ūdeņraža saite elektrostatiska mijiedarbība starp polāru molekulu vai molekulu funkcionālo grupu daļēji elektronegatīviem atomiem (O, N, P) un daļēji elektropozitīvu ūdeņraža atomu. H R OH N R H R OH O R
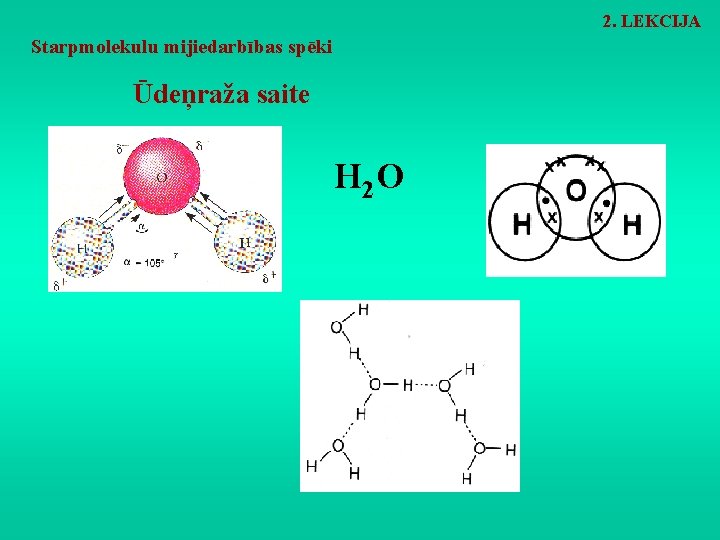
2. LEKCIJA Starpmolekulu mijiedarbības spēki Ūdeņraža saite H 2 O

2. LEKCIJA Starpmolekulu mijiedarbības spēki Ūdeņraža saite Enerģija: 3 - 5 kcal/mols

3. LEKCIJA Bioloģiski nozīmīgās ūdens īpašības Siltumietilpība, dzišana iztvaikojot

2. LEKCIJA Bioloģiski nozīmīgās ūdens īpašības Blīvuma samazināšanās sasalstot

2. LEKCIJA Bioloģiski nozīmīgās ūdens īpašības Spēja šķīdināt polārus savienojumus: ūdens molekulas, hidratējot polārus savienojumus vai jonus, vājina to elektrostatisko mijiedarbību. Ūdens ir dielektriķis.

Bioloģiski nozīmīgās ūdens īpašības 2. LEKCIJA Spēja šķīdināt polārus savienojumus Polāri savienojumi ir hidrofīli

2. LEKCIJA Bioloģiski nozīmīgās ūdens īpašības Atgrūšanās no nepolāru savienojumu virsmas Nepolāri savienojumi ir hidrofobi
- Slides: 62