Elektronu transports baktrijs ievads Elektronu transportu veic redoks

Elektronu transports baktērijās: ievads Elektronu transportu veic red-oks kofaktori (prostētiskās grupas), kas saistīti pie noteiktām energosajūdzošo membrānu proteīnu struktūrām – elektronu transporta kompleksiem Red-oks kofaktori: NAD(P)H, flavīni, hinoni, Fe. S klasteri, hema grupas, Cu+
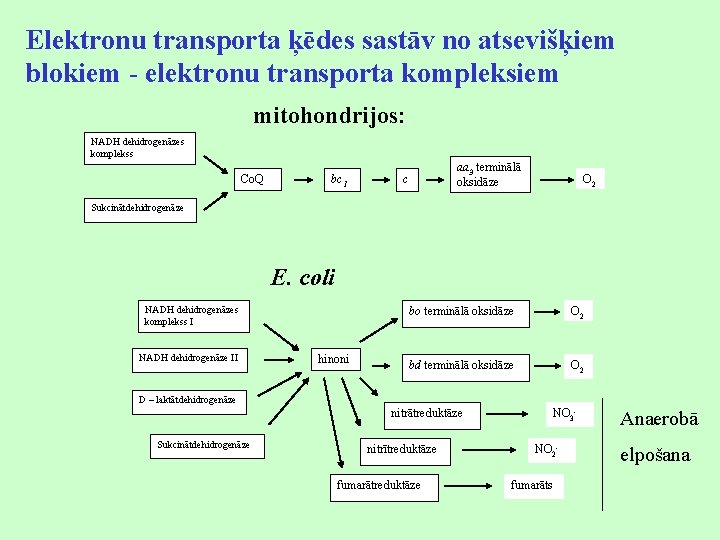
Elektronu transporta ķēdes sastāv no atsevišķiem blokiem - elektronu transporta kompleksiem mitohondrijos: NADH dehidrogenāzes komplekss Co. Q bc 1 aa 3 terminālā oksidāze c O 2 Sukcinātdehidrogenāze E. coli NADH dehidrogenāzes komplekss I NADH dehidrogenāze II hinoni bo terminālā oksidāze O 2 bd terminālā oksidāze O 2 D – laktātdehidrogenāze nitrātreduktāze Sukcinātdehidrogenāze nitrītreduktāze fumarātreduktāze NO 3 NO 2 fumarāts Anaerobā elpošana

Elektroni tiek pārnesti no kofaktora ar zemāko (negatīvāko) red-oks potenciālu uz kofaktoru ar augstāko (pozitīvāko) red-oks potenciālu Standarta red-oks potenciāli elpošanas ķēdē: E’ 0 [NAD+/NADH] = -320 m. V E’ 0 [UQ/UQH 2] = 45 m. V E’ 0 [1/2 O 2/H 2 O] = 816 m. V E’ 0 ķēdē =1. 14 V, kas atbilst G = 220 k. J uz 1 molu oksidēta NADH Ja mitohondrijos Gp = 57 k. J uz 1 molu sintezējamā ATP, tad oksidējot NADH molekulu izdalās enerģija, kas pietiek 3 ATP molekulu sintēzei
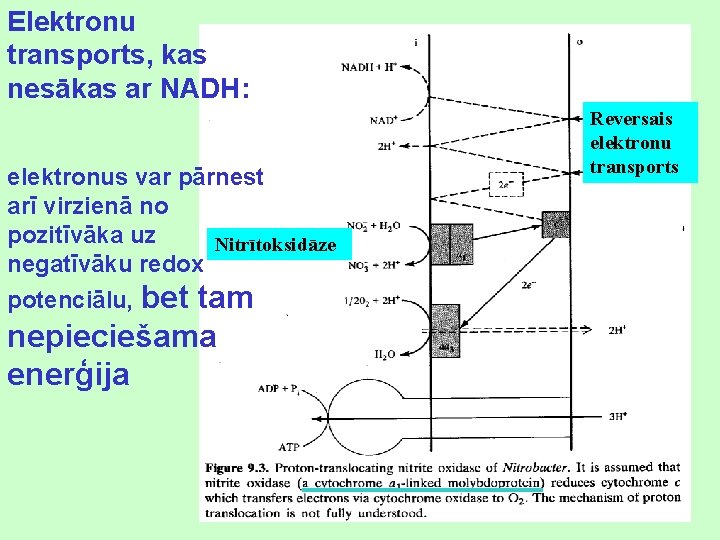
Elektronu transports, kas nesākas ar NADH: elektronus var pārnest arī virzienā no pozitīvāka uz Nitrītoksidāze negatīvāku redox potenciālu, bet tam nepieciešama enerģija Reversais elektronu transports
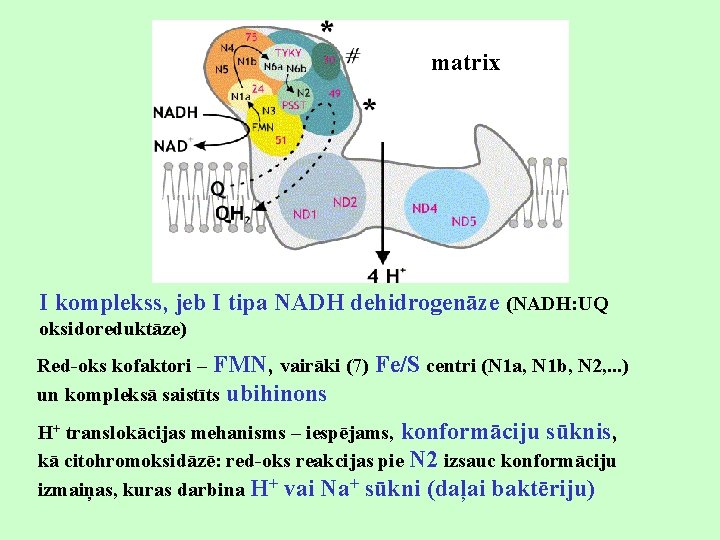
matrix I komplekss, jeb I tipa NADH dehidrogenāze (NADH: UQ oksidoreduktāze) Red-oks kofaktori – FMN, vairāki (7) Fe/S centri (N 1 a, N 1 b, N 2, . . . ) un kompleksā saistīts ubihinons H+ translokācijas mehanisms – iespējams, konformāciju sūknis, kā citohromoksidāzē: red-oks reakcijas pie N 2 izsauc konformāciju izmaiņas, kuras darbina H+ vai Na+ sūkni (daļai baktēriju)

Alternatīva - II tipa NADH dehidrogenāzes: • sastāv no vienas subvienības (ap 50 k. Da) • kofaktors FAD vai FMN; pārnes elektronus no NAD(P)H uz hinonu • nepiedalās protondzinējspēka veidošanā • rezistentas pret I kompleksa inhibitoriem piericidīnu, kapsaicīnu un rotenonu sastop kā baktērijās, tā arhejos; raugiem tās ir vienīgās NADH: hinona oksidoreduktāzes
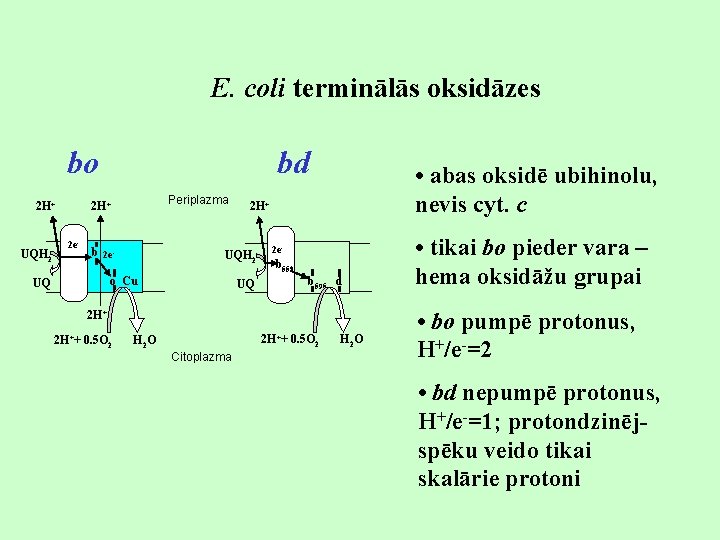
E. coli terminālās oksidāzes bo 2 H+ UQH 2 UQ bd 2 H+ 2 e- b 2 e o Cu Periplazma 2 H+ UQH 2 UQ 2 e- b 558 b 595 d 2 H++ 0. 5 O 2 H 2 O Citoplazma • abas oksidē ubihinolu, nevis cyt. c • tikai bo pieder vara – hema oksidāžu grupai • bo pumpē protonus, H+/e-=2 • bd nepumpē protonus, H+/e-=1; protondzinējspēku veido tikai skalārie protoni
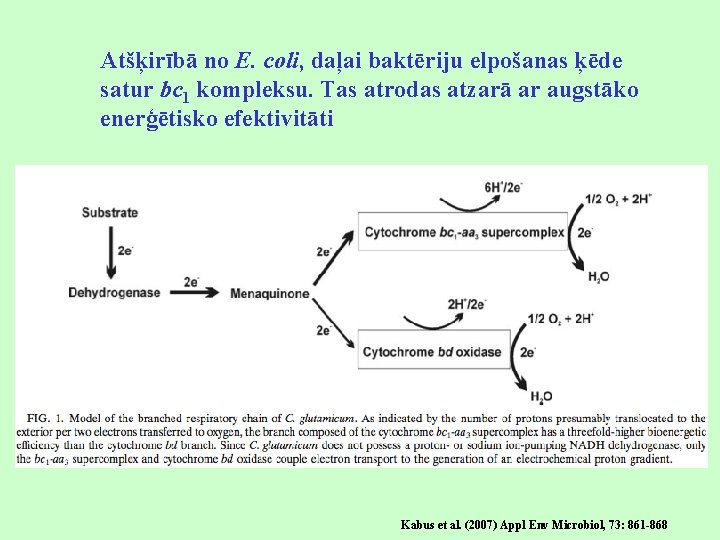
Atšķirībā no E. coli, daļai baktēriju elpošanas ķēde satur bc 1 kompleksu. Tas atrodas atzarā ar augstāko enerģētisko efektivitāti Kabus et al. (2007) Appl Env Microbiol, 73: 861 -868

Elpošanas ķēdes darbība izraisa baktēriju biomasas pastiprinātu augšanu, salīdzinot ar tīri fermentatīvu metabolismu! Pētot anaerobi augošas baktērijas Enterococcus faecalis un Zymomonas mobilis un raugus, kam precīzi zināms ATP iznākums uz molu katabolismā noārdītā substrāta, konstatēts, ka 1 mols katabolismā ģenerētā ATP nodrošina aptuveni 10 g sausnes biomasas veidošanos, jeb YATP ≈ 10 gsausnes/mole ATP Savukārt, elpošana nodrošina lielāku ATP iznākumu no mola katabolismā patērētā substrāta. Bauchop and Elsden (1960) J Gen Microbiol, 23: 457 -469
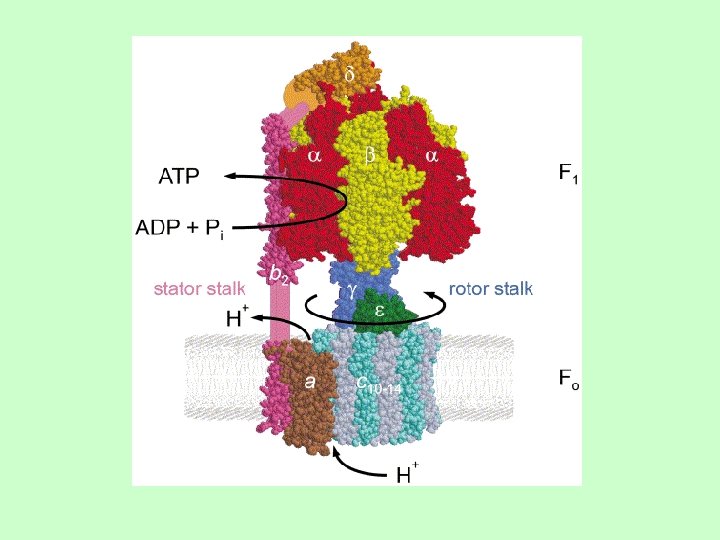

Protonatkarīgā ATP sintāze darbojas abos virzienos: • ja protondzinējspēks ir pietiekami liels, tā sintezē ATP, izmantojot protondzinējspēka enerģiju • ja H+ ir mazs – tā hidrolizē ATP, lai uzturētu protondzinējspēku – darbojas kā protonus pumpējoša ATPāze • ja elektronu transports neuztur H+ (piem. daudzās anaerobajās baktērijās) tad H+ATPāze ir galvenais protondzinējspēka uzturētājs
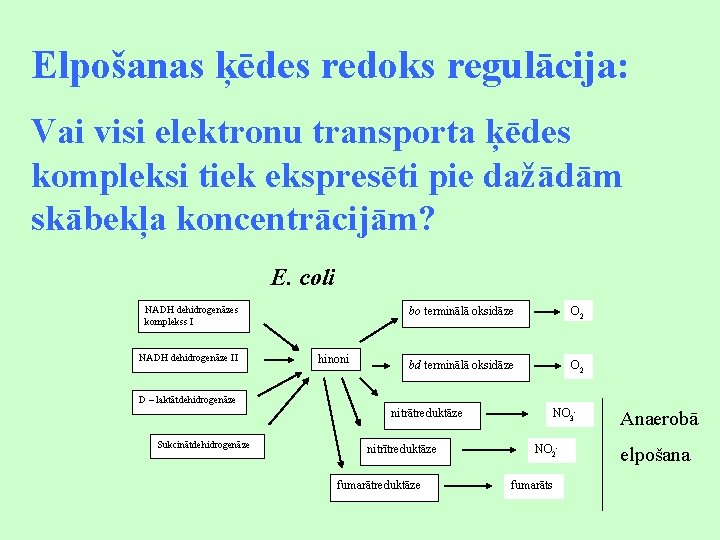
Elpošanas ķēdes redoks regulācija: Vai visi elektronu transporta ķēdes kompleksi tiek ekspresēti pie dažādām skābekļa koncentrācijām? E. coli NADH dehidrogenāzes komplekss I NADH dehidrogenāze II hinoni bo terminālā oksidāze O 2 bd terminālā oksidāze O 2 D – laktātdehidrogenāze nitrātreduktāze Sukcinātdehidrogenāze nitrītreduktāze fumarātreduktāze NO 3 NO 2 fumarāts Anaerobā elpošana
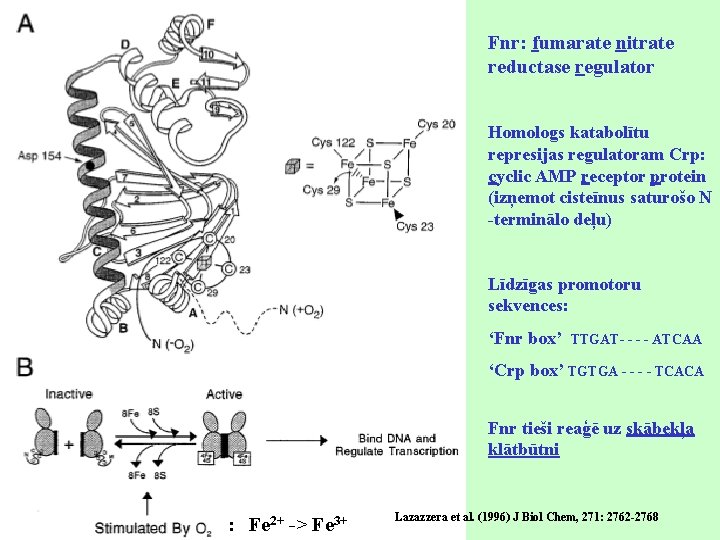
Fnr: fumarate nitrate reductase regulator Homologs katabolītu represijas regulatoram Crp: cyclic AMP receptor protein (izņemot cisteīnus saturošo N -terminālo deļu) Līdzīgas promotoru sekvences: ‘Fnr box’ TTGAT- - ATCAA ‘Crp box’ TGTGA - - TCACA Fnr tieši reaģē uz skābekļa klātbūtni : Fe 2+ -> Fe 3+ Lazazzera et al. (1996) J Biol Chem, 271: 2762 -2768
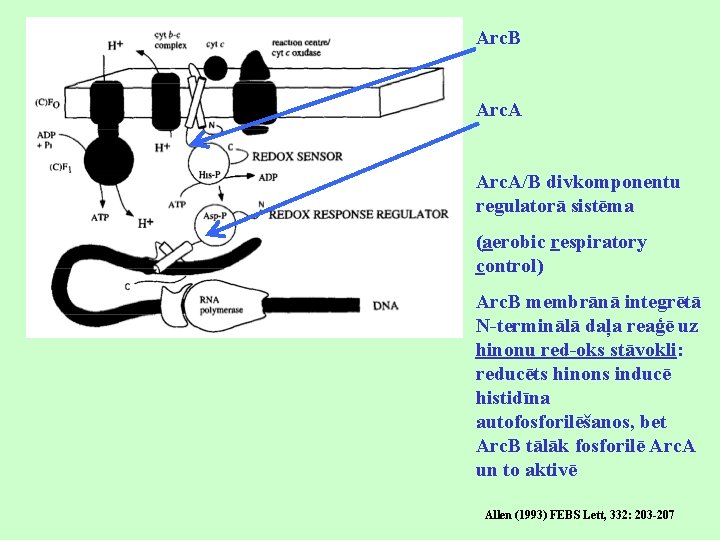
Arc. B Arc. A/B divkomponentu regulatorā sistēma (aerobic respiratory control) Arc. B membrānā integrētā N-terminālā daļa reaģē uz hinonu red-oks stāvokli: reducēts hinons inducē histidīna autofosforilēšanos, bet Arc. B tālāk fosforilē Arc. A un to aktivē Allen (1993) FEBS Lett, 332: 203 -207
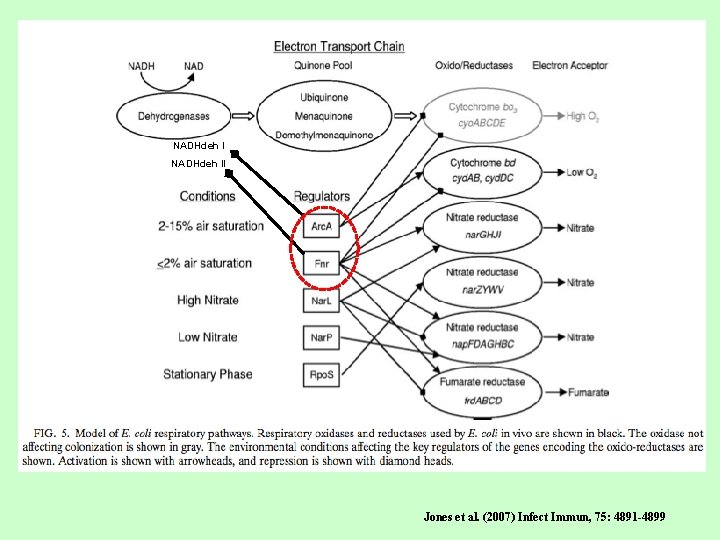
NADHdeh II Jones et al. (2007) Infect Immun, 75: 4891 -4899

Elpošanas ķēde N 2 fiksējošās baktērijās nevien ģenerē enerģiju, bet arī veic respiratorās aizsardzības (“Respiratory protection”) funkciju. Nitrogenāzes komplekss ir nestabils O 2 klātbūtnē A. vinelandii spēj saistīt N 2 tikai tad, ja šūnā tiek uzturēta ļoti zema skābekļa koncentrācija A. vinelandii aerobos apstākļos pastiprināti ekspresē citohromu bd, kuram, salīdzinot ar E. coli, ir zemāka skābekļa afinitāte un augstāks apgriezienu skaits. Cyd- mutanti skābekļa klātbūtnē nespēj saistīt N 2. Zemu skābekļa koncentrāciju šūnā nodrošina ļoti aktīva, bet enerģētiski mazefektīva elpošanas ķēde A. vinelandii Cyd. R ir Fnr homologs Cyd. R nodrošina cyt bd transkripcijas represiju, ja skābekļa iekššūnas koncentrācija ir zema, un zaudē savu represora funkciju pie augstas skābekļa koncentrācijas Poole and Cook (2000) Adv Microb Physiol, 43: 165 -224

Vairumam Gram-pozitīvo baktēriju sastop citu redoks regulatoro sistēmu, kuras nav Gram-negatīvajās baktērijās – Rex represoru Rex atklāts Streptomyces coelicolor; tas ir 258 aminoskābes saturošs proteīns, kurš disociē no savas saistīšanās vietas pie promotera tad, kad pie tā piesaistās NADH. Tas ir regulators, kurš tieši reaģē uz NADH/NAD attiecību (NADH un NAD konkurē par vienu saistīšanās vietu). NADH nesaistījis Rex kavē cyt d un hema biosintēzes komponentu ekspresiju NAD+ NADH Cyd. AB Brekasis et al. (2003) EMBO Journal, 22: 4856 -4865

Ekstremofīlā dzīvesveida bioenerģētikas problēmas: • Jānodrošina pietiekami zema membrānas H+ (Na+) caurlaidība • Jānodrošina makromolekulu stabilitāte • Jāuztur pietiekami augsts protondzinējspēks vai nātrijdzinējspēks ATP sintēzei un transportam • Jānodrošina iekššūnas p. H homeostāze

Termofīlajām baktērijām un arhejiem proteīnu termostabilitāti nodrošina: • izteikti nepolāra centrālā molekulas daļa • minimāla virsmas/tilpuma attiecība • maz glicīna (kas tādējādi palielina molekulas rigiditāti) • uz virsmas daudz jonu saišu • aktīvas chaperonu sistēmas, kas reparē denaturētās molekulas DNS termostabilitāti nodrošina: • reversā girāze, kas nodrošina pozitīvo superspiralizāciju • saistīšanās pie histoniem līdzīgiem proteīniem Acidofīliem un alkalofīliem primārais izdzīvošanas priekšnoteikums - nodrošināt iekššūnas p. H homeostāzi Picrophylus oshimae, kurš optimāli aug pie p. H 0. 7 un T 60 o. C, spēj uzturēt iekššūnas p. H ap 5 No šejienes – Svarīga membrānu stabilitāte un zema jonu caurlaidība!
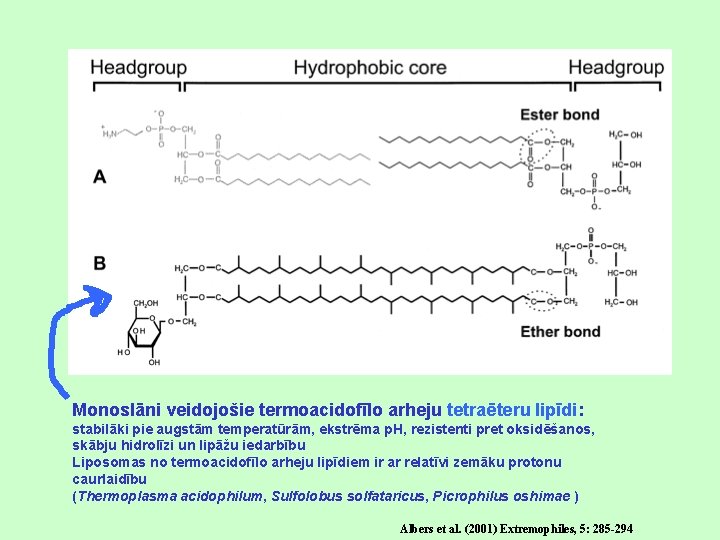
Monoslāni veidojošie termoacidofīlo arheju tetraēteru lipīdi: stabilāki pie augstām temperatūrām, ekstrēma p. H, rezistenti pret oksidēšanos, skābju hidrolīzi un lipāžu iedarbību Liposomas no termoacidofīlo arheju lipīdiem ir ar relatīvi zemāku protonu caurlaidību (Thermoplasma acidophilum, Sulfolobus solfataricus, Picrophilus oshimae ) Albers et al. (2001) Extremophiles, 5: 285 -294
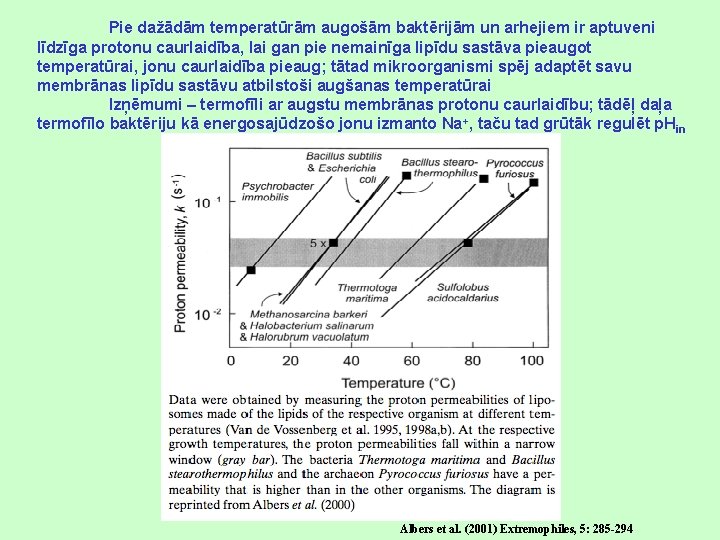
Pie dažādām temperatūrām augošām baktērijām un arhejiem ir aptuveni līdzīga protonu caurlaidība, lai gan pie nemainīga lipīdu sastāva pieaugot temperatūrai, jonu caurlaidība pieaug; tātad mikroorganismi spēj adaptēt savu membrānas lipīdu sastāvu atbilstoši augšanas temperatūrai Izņēmumi – termofīli ar augstu membrānas protonu caurlaidību; tādēļ daļa termofīlo baktēriju kā energosajūdzošo jonu izmanto Na+, taču tad grūtāk regulēt p. Hin Albers et al. (2001) Extremophiles, 5: 285 -294
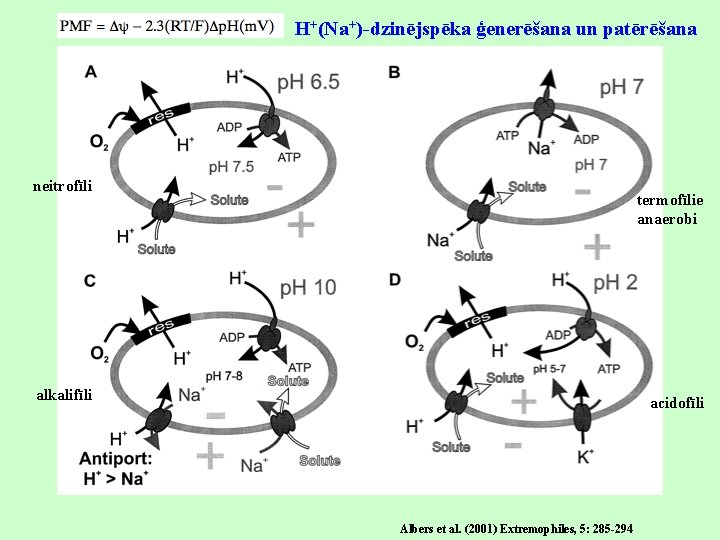
H+(Na+)-dzinējspēka ģenerēšana un patērēšana neitrofīli termofīlie anaerobi alkalifīli acidofīli Albers et al. (2001) Extremophiles, 5: 285 -294

Transporta sistēmas iedalās: • primārajās, kuras vienu enerģijas veidu pārvērš citā (piem. ķīmisko enerģiju – gradientu enerģijā) • sekundārajās, kuras viena gradienta enerģiju izmanto cita gradienta veidošanai protondzinējspēku tieši izmantojošās sistēmas pieder pie: sekundārajām
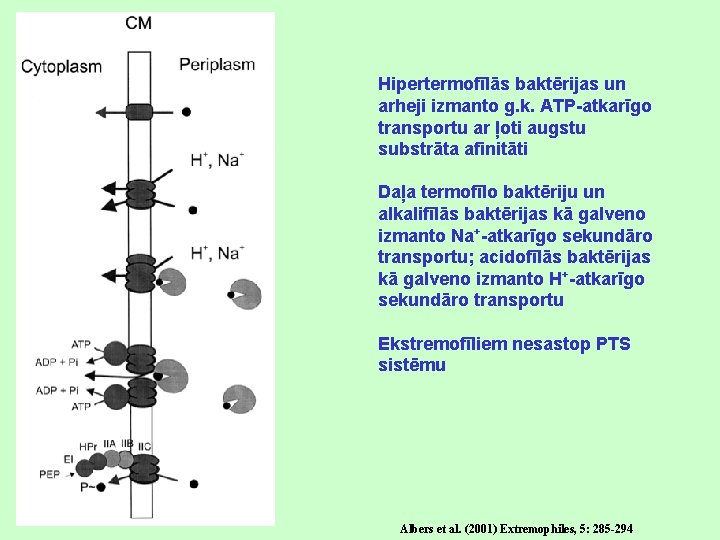
Hipertermofīlās baktērijas un arheji izmanto g. k. ATP-atkarīgo transportu ar ļoti augstu substrāta afinitāti Daļa termofīlo baktēriju un alkalifīlās baktērijas kā galveno izmanto Na+-atkarīgo sekundāro transportu; acidofīlās baktērijas kā galveno izmanto H+-atkarīgo sekundāro transportu Ekstremofīliem nesastop PTS sistēmu Albers et al. (2001) Extremophiles, 5: 285 -294
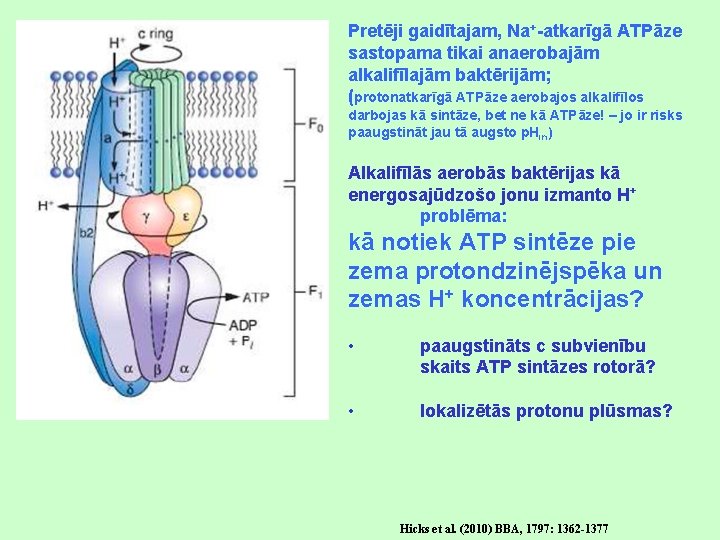
Pretēji gaidītajam, Na+-atkarīgā ATPāze sastopama tikai anaerobajām alkalifīlajām baktērijām; (protonatkarīgā ATPāze aerobajos alkalifīlos darbojas kā sintāze, bet ne kā ATPāze! – jo ir risks paaugstināt jau tā augsto p. Hin) Alkalifīlās aerobās baktērijas kā energosajūdzošo jonu izmanto H+ problēma: kā notiek ATP sintēze pie zema protondzinējspēka un zemas H+ koncentrācijas? • paaugstināts c subvienību skaits ATP sintāzes rotorā? • lokalizētās protonu plūsmas? Hicks et al. (2010) BBA, 1797: 1362 -1377
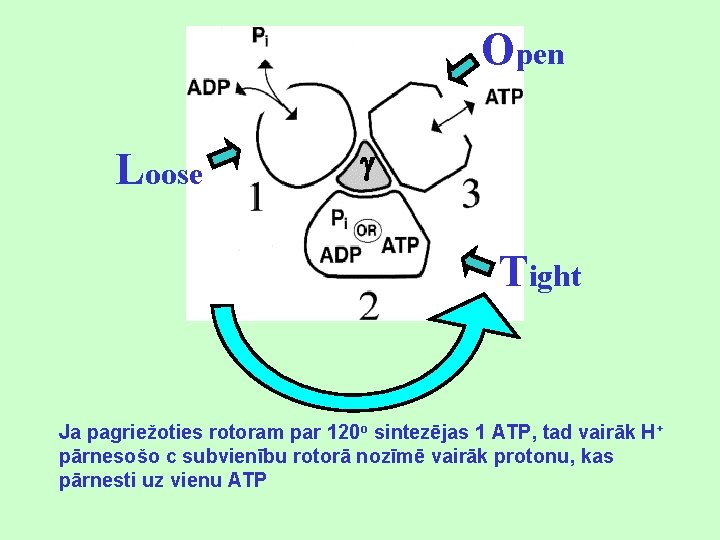
Open Loose Tight Ja pagriežoties rotoram par 120 o sintezējas 1 ATP, tad vairāk H+ pārnesošo c subvienību rotorā nozīmē vairāk protonu, kas pārnesti uz vienu ATP

E. coli ATPāzes rotors satur 10 c subvienības. Alkalifīliem c subvienību ir nedaudz vairāk: A tridecameric c ring of the adenosine triphosphate (ATP) synthase from thermoalkaliphilic Bacillus sp. strain TA 2. A 1 facilitates ATP synthesis at low electrochemical proton potential Meier et al. (2007) Mol Microbiol, 65: 1181 -1192 Ja H+= 136 m. V jeb 13. 1 k. J uz molu H+, un Gp= 45. 2 k. J uz molu ATP, tad H+/ATP = starp 3 un 4 Guffanti and Hicks (1991) J Gen Microbiol, 137: 2375 -2379 Ja H+= 50 m. V jeb 4. 8 k. J uz molu H+, un Gp= 46 k. J uz molu ATP, tad H+/ATP = starp 9 un 10 ! Alkalifīliem c subvienību skaits nav tik liels, un tas nevar būt mainīgs
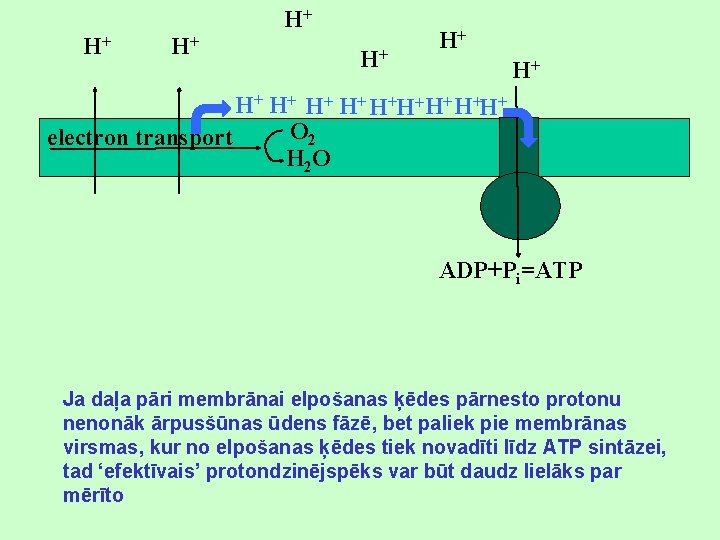
H+ H+ H+ H+H+H+ O 2 electron transport H 2 O ADP+Pi=ATP Ja daļa pāri membrānai elpošanas ķēdes pārnesto protonu nenonāk ārpusšūnas ūdens fāzē, bet paliek pie membrānas virsmas, kur no elpošanas ķēdes tiek novadīti līdz ATP sintāzei, tad ‘efektīvais’ protondzinējspēks var būt daudz lielāks par mērīto
- Slides: 28