Azot w zwizkach organicznych wizanie azotu wolnego przemiana






- Slides: 12

Azot w związkach organicznych Ø Ø wiązanie azotu wolnego, przemiana amoniaku w związki organiczne, redukcja azotanów(V) do amoniaku, biosynteza mocznika (ureogeneza)

Wiązanie azotu atmosferycznego v Wiązanie azotu – zmiana azotu atmosferycznego na związki organiczne przez organizmy żywe np. : Ø heterotroficzne bakterie anaerobowe (beztlenowe) z rodzaju Clostridium, Azotobacter, Ø autotroficzne bakterie aerobowe (tlenowe) z rodzaju Rhodospirillum, Ø bakterie symbiotyczne (brodawkowe) z rodzaju Rhizobium - aerobowe bakterie saprofityczne do momentu wniknięcia do włośników korzenia i utworzenia brodawek u roślin rodziny Leguminosae / Fabaceae oraz drzew i krzewów rodzaju Alnus, Myrica, Shepherdia, Coriaria, Hippophae, Ceanothus, Elaeagnus, Casuarina), Ø autotroficzne lub symbiotyczne sinice z rodzaju Anabaena, Nostoc, Oscillatoria,

Wiązanie azotu atmosferycznego Ø heterotrofy wykorzystują zewnętrze źródła węgla zredukowanego, Ø donorem elektronów redukujących azot może być proces utlenienia kwasu pirogronowego (lub anionu tego kwasu), które są przekazywane są na ferredoksynę i dalej na nitrogenazę, a następnie na azot, Ø autotrofy wykorzystują z reguły niezbędne elektrony do redukcji azotu dzięki procesowi fotosyntezy, Ø ogólne równanie wiązania wolnego azotu: ü N 2 + 8 H+ + 6 e- + 16 Mg. ATP 2 NH 4+ + 16 Mg. ADP + 16 ü kationy amonowe stanowią pierwszy i trwały produkt wiązania azotu, który podlega z reguły szybkiej przemianie w formy azotu organicznego,

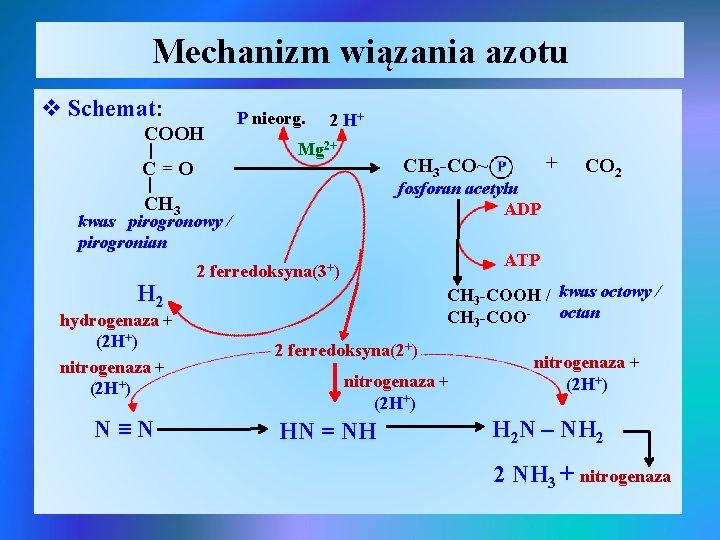
Mechanizm wiązania azotu v Schemat: COOH | C=O P nieorg. 2 H+ Mg 2+ | fosforan acetylu ADP CH 3 kwas pirogronowy / pirogronian H 2 hydrogenaza + (2 H+) nitrogenaza + (2 H+) N≡N + CH 3 -CO~ CO 2 ATP 2 ferredoksyna(3+) CH 3 -COOH / kwas octowy / octan CH 3 -COO- 2 ferredoksyna(2+) nitrogenaza + (2 H+) HN = NH nitrogenaza + (2 H+) H 2 N – NH 2 2 NH 3 + nitrogenaza

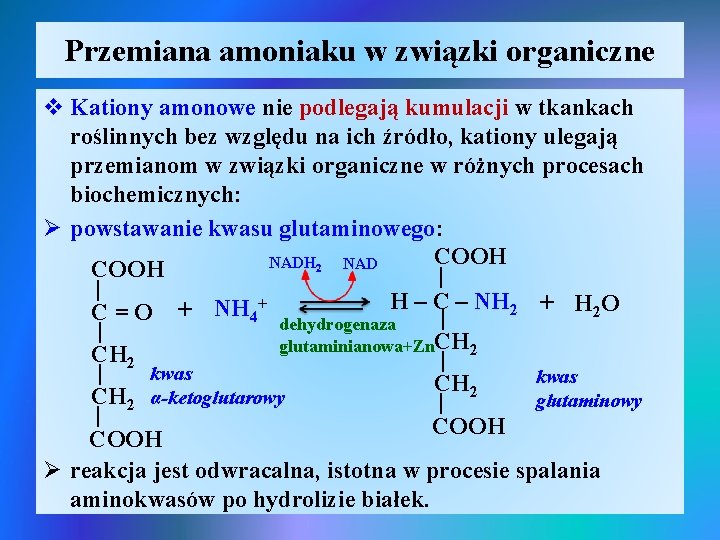
Przemiana amoniaku w związki organiczne v Kationy amonowe nie podlegają kumulacji w tkankach roślinnych bez względu na ich źródło, kationy ulegają przemianom w związki organiczne w różnych procesach biochemicznych: Ø powstawanie kwasu glutaminowego: COOH NADH 2 NAD COOH | | C = O + NH 4+ dehydrogenaza. H – C| – NH 2 + H 2 O | glutaminianowa+Zn. CH 2 | kwas CH 2 α-ketoglutarowy glutaminowy | | COOH Ø reakcja jest odwracalna, istotna w procesie spalania aminokwasów po hydrolizie białek.

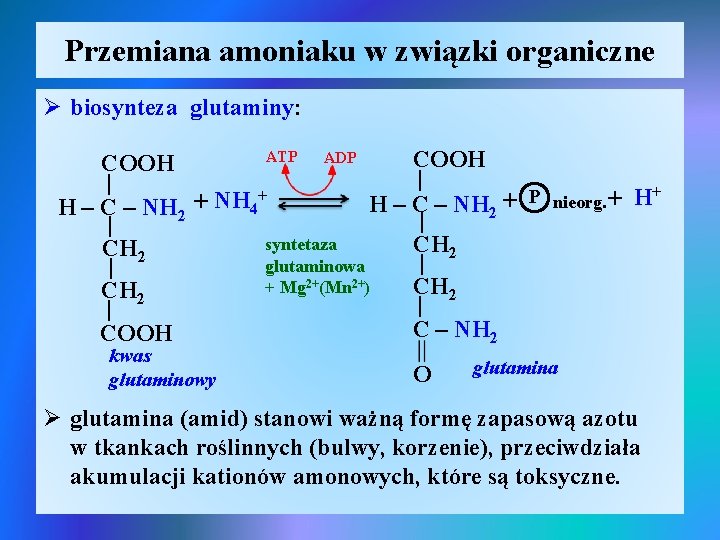
Przemiana amoniaku w związki organiczne Ø biosynteza glutaminy: ATP ADP COOH | | + H – C – NH 2 + P H – C – NH 2 + NH 4 | | syntetaza CH 2 | glutaminowa | + Mg 2+(Mn 2+) CH 2 | | C – NH 2 COOH kwas glutaminowy O nieorg. + H+ glutamina Ø glutamina (amid) stanowi ważną formę zapasową azotu w tkankach roślinnych (bulwy, korzenie), przeciwdziała akumulacji kationów amonowych, które są toksyczne.

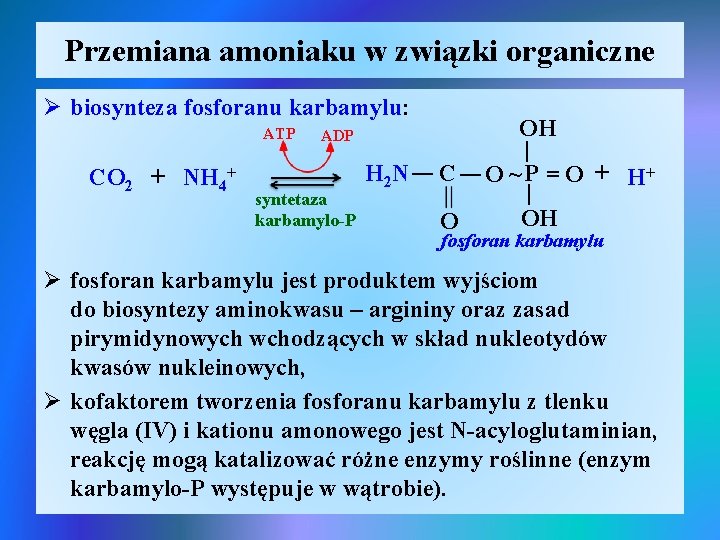
Przemiana amoniaku w związki organiczne Ø biosynteza fosforanu karbamylu: ATP C O OH | O ~ P = O + H+ | OH | syntetaza karbamylo-P H 2 N | CO 2 + NH 4+ ADP fosforan karbamylu Ø fosforan karbamylu jest produktem wyjściom do biosyntezy aminokwasu – argininy oraz zasad pirymidynowych wchodzących w skład nukleotydów kwasów nukleinowych, Ø kofaktorem tworzenia fosforanu karbamylu z tlenku węgla (IV) i kationu amonowego jest N-acyloglutaminian, reakcję mogą katalizować różne enzymy roślinne (enzym karbamylo-P występuje w wątrobie).

Redukcja azotanów(V) do amoniaku v Proces redukcji anionów NO 3 - do kationów NH 4+ przebiega wieloetapowo: Ø w obecności enzymu reduktazy azotanowej, która oprócz apoenzymu zawiera grupy prostetyczne FAD i Mo, anion NO 3 - jest redukowany do anionu NO 2 -, Ø donorem elektronów jest NAD Ø reduktaza azotanowa jest enzymem adaptacyjnym – indukowanym, jest nietrwała, wytwarzana w obecności anionów NO 3 -, Ø w kolejnym etapie przy udziale reduktazy azotynowej, której grupą prostetyczną jest ferredoksyna - Fd (donor elektronów) anion NO 2 - podlega dalszej redukcji do amoniaku (kationu amonowego)

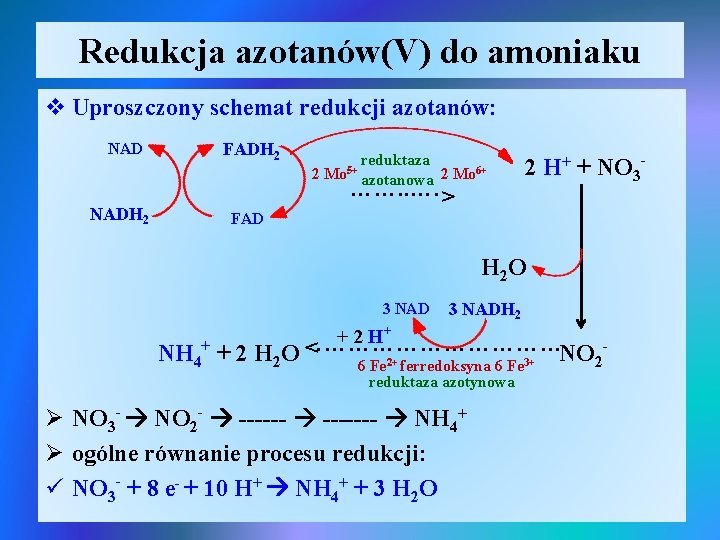
Redukcja azotanów(V) do amoniaku v Uproszczony schemat redukcji azotanów: NADH 2 FADH 2 reduktaza 2 Mo 5+ azotanowa 2 Mo 6+ ……. . …. > 2 H+ + NO 3 - FAD H 2 O 3 NAD + 2 H+ ……………. > NH 4+ + 2 H 2 O 3 NADH 2 6 Fe 2+ ferredoksyna 6 Fe 3+ reduktaza azotynowa Ø NO 3 - NO 2 - ------- NH 4+ Ø ogólne równanie procesu redukcji: ü NO 3 - + 8 e- + 10 H+ NH 4+ + 3 H 2 O NO 2 -

Biosynteza mocznika - ureogeneza v Amoniak i mocznik są produktami przemiany aminokwasów: Ø amoniak, produkt dezaminacji aminokwasów, jest związkiem toksycznym, Ø część amoniaku jest usuwana z moczem w formie kationu amonowego powstającego w reakcji amoniaku i nadmiaru kationów wodorowych we krwi (regulacja odczynu krwi), Ø większość grup aminowych usuwane jest w formie związku obojętnego i nietoksycznego – mocznika, Ø zespół enzymów i aktywatorów katalizuje reakcję ureogenezy – przekształcenia amoniaku w mocznik, Ø forma sumaryczna reakcji ureogenezy: ü HCO 3 - + NH 4+ + NH 3 CO(NH 2)2 + 2 H 2 O

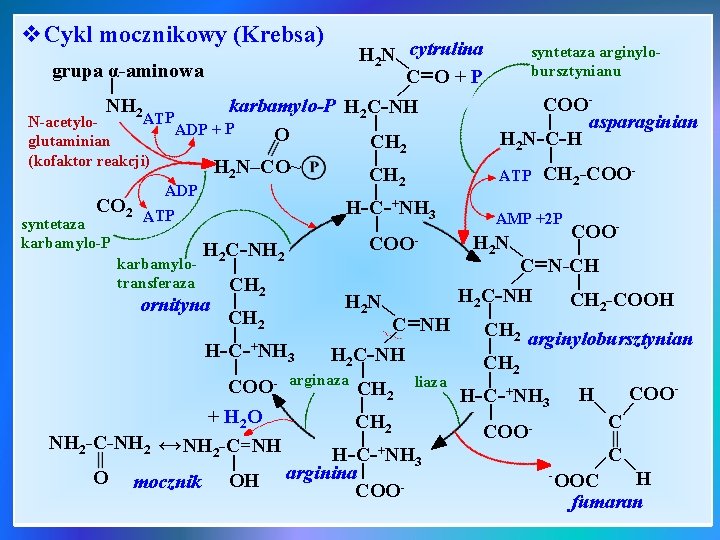
Cykl mocznikowy (Krebsa) Ø reakcja jest silnie endoenergetyczna, nie może przebiegać samorzutnie, jest sprzężona z reakcjami egzoenergetycznymi, Ø jest proces cykliczny, w którym występuje szereg związków pośrednich i bierze udział kilka enzymów, Ø proces tworzenia jest katalitycznie zwiększany przez dodatek niewielkiej ilości aminokwasów (ornityny, cytruliny, argininy), dodatek przyspiesza obrót cyklu metabolicznego, Ø u ssaków niezbędnym kofaktorem reakcji jest N-acetyloglutaminian - jest on efektorem allosterycznym (modyfikatorem) dla enzymu

v. Cykl mocznikowy (Krebsa) | syntetaza arginylo. H 2 N cytrulina bursztynianu grupa α-aminowa C= O + P | COOkarbamylo-P H 2 C-NH NH 2 ATP N-acetylo| asparaginian | ADP + P O H 2 N -C -H glutaminian CH 2 | | (kofaktor reakcji) H 2 N–CO~ CH ATP CH -COO- | | ADP H-C-+NH 3 H 2 C-NH 2 | CH 2 +NH COO+ H 2 O NH 2 -C-NH 2 ↔ NH 2 -C=NH | OH | C=N-CH | H 2 C-NH CH 2 -COOH 3 arginaza | CH 2 liaza | CH 2 arginylobursztynian | CH 2 | | H-C-+NH 3 | COO- CH 2 H-C-+NH 3 arginina | COO- H | - C | C COO | | | C=NH H 2 C-NH | H -C - mocznik H 2 N CH 2 | H 2 N COO- | | | ornityna O COO- AMP +2 P | karbamylotransferaza | | CO 2 ATP syntetaza karbamylo-P 2 2 H OOC fumaran
 Wizania
Wizania Reakcja bromowania etanu
Reakcja bromowania etanu Typy reakcji organicznych
Typy reakcji organicznych Postulat hammonda
Postulat hammonda Wzory empiryczne i rzeczywiste
Wzory empiryczne i rzeczywiste Termodynamika
Termodynamika Nauka o strukturze i funkcjonowaniu przyrody to
Nauka o strukturze i funkcjonowaniu przyrody to Negatif nitrojen dengesi nedir
Negatif nitrojen dengesi nedir Konfiguracja elektronowa cl
Konfiguracja elektronowa cl Krążenie azotu w przyrodzie
Krążenie azotu w przyrodzie Liczba masowa pewnego izotopu pierwiastka e jest równa 234
Liczba masowa pewnego izotopu pierwiastka e jest równa 234 Pedagogika czasu wolnego
Pedagogika czasu wolnego Unia celna a strefa wolnego handlu
Unia celna a strefa wolnego handlu