Powietrze jako mieszanina gazw Zadanie 1 Oblicz objto

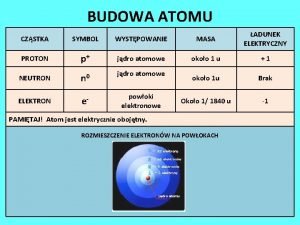
Powietrze jako mieszanina gazów

Zadanie 1 Oblicz objętość tlenu i objętość azotu w pokoju o wymiarach 3 m x 2 m x 4 m. Zadanie 2 Przyporządkuj nazwy składników powietrza do podanych grup. tlen, wodór, azot, ksenon, para wodna, hel, zanieczyszczenia, tlenki azotu, neon, tlenek węgla(IV), argon Zmienne składniki powietrza Stałe składniki powietrza

ZADANIE 3 Oblicz masę powierza potrzebną do spalenia 20 gram magnezu. Mg + O 2 → Mg. O ZADANIE 4 ZADANIE 5

ZADANIE 6

Tlen jako najważniejszy składnik powietrza

ZADANIE 1 Oblicz masę tlenu znajdującą się w pomieszczeniu o wymiarach 3 m 4 m 3 m. Przyjmij gęstość tlenu 1, 309 g/dm 3. Wynik wyraź w kilogramach ZADANIE 2 ZAPISZ ZA POMOCĄ SYMBOLI I UZGODNIJ REAKCJE : - POWSTANIA TLENKU AZOTU (V). - ANALIZY TLENKU ŻELAZA (III) - SYNTEZY TLENKU WAPNIA -ROZKŁADU WODY -POWSTANIA TLENKU SIARKI (IV) ZADANIE 3 Podanie niżej tlenki podziel na tlenki metali i niemetali. Podkreśl te które mają stały stan skupienia Mg. O, NO 2 , SO 3 , Cu. O, K 2 O, CO, P 2 O 5 , Ca. O,

ZADANIE 4 Zapisz obserwacje i sformułuj wniosek. Podaj zapis słowny przebiegu reakcji chemicznej z doświadczenia zatytułowanego “Spalanie siarki w tlenie". Obserwacje: Wniosek: Zapis słowny przebiegu reakcji chemicznej: Zapis symboliczny przebiegu reakcji chemicznej ZADANIE 5 ZADANIE 6

Praca domowa Korzystając z różnorodnych źródeł uzupełnij poniższą tabelkę

Tlenek węgla (IV)

ZADANIE 1 • ZADANIE 2. Oblicz, ile gramów tlenku wapnia można otrzymać w wyniku prażenia 200 g wapienia (m. Ca = 40 u, m. C = 12 u, m. O = 16 u). Zapisz równanie tej reakcji chemicznej. ZADANIE 3 ZADANIE 4
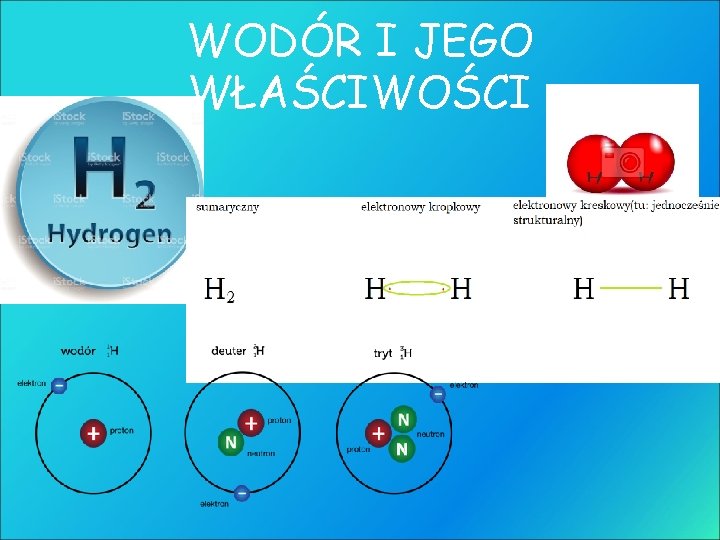
WODÓR I JEGO WŁAŚCIWOŚCI

Czego dowiesz się dziś z lekcji? • • Gdzie możemy spotkać czysty wodór? W jaki sposób go otrzymać? Jakie są jego właściwości ? W jaki sposób możemy wykorzystać wodór?

Występowanie wodoru W stanie wolnym • Pierwiastek , którego jest najwięcej we wszechświecie • W powietrzu występuje w górnych warstwach atmosfery powstały z wybuchów wulkanów W stanie związanym • Jako składnik wody • We wszystkich organizmach żywych • Składnik wielu skał i minerałów
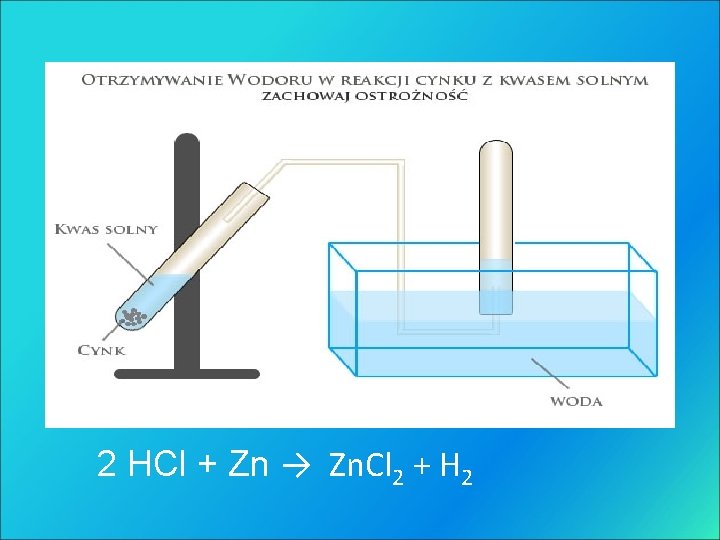
2 HCl + Zn → Zn. Cl 2 + H 2
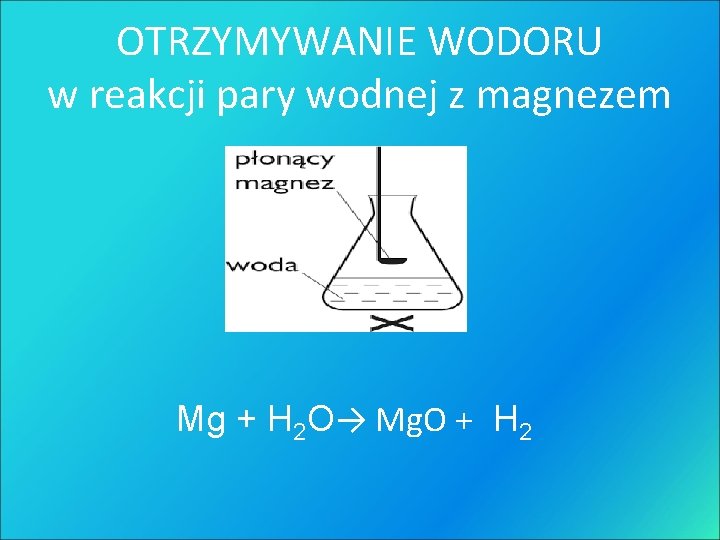
OTRZYMYWANIE WODORU w reakcji pary wodnej z magnezem Mg + H 2 O→ Mg. O + H 2

WŁAŚCIWOŚCI WODORU FIZYCZNE CHEMICZNE • BEZWONNY • NAJLŻEJSZY Z GAZÓW • PALNY – SPALA SIĘ Z • BEZBARWNY CHARAKTERYSTYCZNYM „SZCZEKNIĘCIEM” A • SŁABO ROZPUSZCZALNY W ZMIESZANY Z TLENEM W WODZIE STOSUNKU 2: 1 TWORZY MIESZNINĘ PIORUNUJĄCĄ • AKTYWNY – CHĘTMNIE ŁĄCZY SIĘ Z PIERWIASTKAMII

2 H 2 + O 2 → 2 H 2 O


ZWIĄZKI WODORU Z PIERWIASTKAMI TO WODORKI Ti H 2

Zastosowanie wodoru • Paliwo rakietowe • Przemysł spożywczyutwardzanie tłuszczy • Gaz przemysłowy • Paliwo przyszłości

Czas na Wasze ulubione zadanka; ))


4.

Zadania utrwalające:



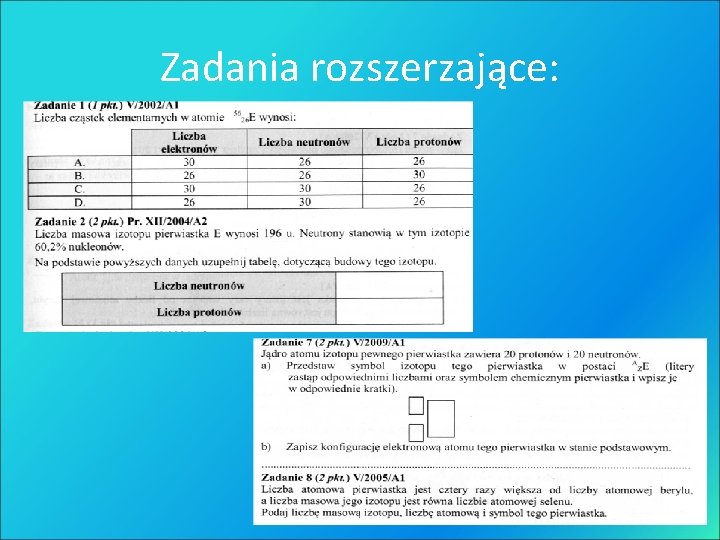
Zadania rozszerzające:

ZAD Liczba masowa (A) pewnego izotopu pierwiastka E jest równa 234. Neutrony stanowią 60, 68% liczby nukleonów. Oblicz wartość liczby atomowej (Z) tego pierwiastka. ZAD Liczba atomowa pewnego pierwiastka wynosi 53. W jednym z izotopów suma liczby protonów, neutronów i elektronów jest równa 180. Ustal symbol AZE.

Zad Krzem ma następującą konfigurację K 2 L 8 M 4. Zapisz konfigurację pierwiastka X , który ma o 10 protonów więcej w jądrze od krzemu i konfigurację pierwiastka Y , który ma o 10 protonów mniej niż krzem zad BOR NATURALNY ZAWIERA OKÓŁO 18. 8% BORU-10 I 81. 2% BORU -11. ILE NEUTRONÓW ZNAJDUJE SIĘ W 500 ATOMACH NATURALNEGO BORU. Zad. Obliczyć zawartość procentową dwóch izotopów boru, jeżeli masa atomowa boru wynosi 10. 81 u, jeden z izotopów ma w jądrze 5 neutronów, a drugi 6 Zad. Miedź jest mieszaniną dwóch izotopów, z których jeden zawiera 34 neutrony i stanowi 69. 1% mieszaniny. Obliczyć liczby masowe obu izotopów, jeżeli masa atomowa miedzi wynosi 63, 55 u Zad. Obliczyć masę atomową pierwiastka stanowiącego mieszaninę 3 izotopów o liczbach masowych 28 (92, 2%), 29 (4, 7%), 30 (3, 1%). odszukaj ten pierwiastek w układzie
- Slides: 30