BUDOWA ATOMU CZSTKA SYMBOL WYSTPOWANIE MASA ADUNEK ELEKTRYCZNY
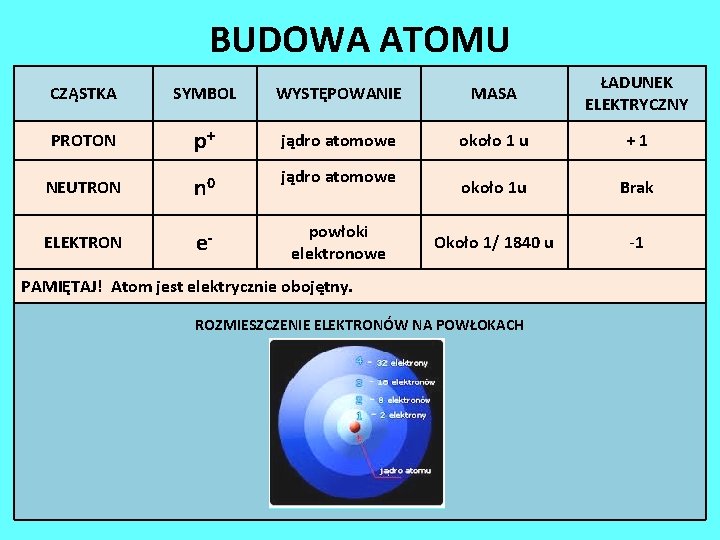
BUDOWA ATOMU CZĄSTKA SYMBOL WYSTĘPOWANIE MASA ŁADUNEK ELEKTRYCZNY PROTON p+ jądro atomowe około 1 u + 1 NEUTRON n 0 jądro atomowe około 1 u Brak ELEKTRON e- powłoki elektronowe Około 1/ 1840 u -1 PAMIĘTAJ! Atom jest elektrycznie obojętny. ROZMIESZCZENIE ELEKTRONÓW NA POWŁOKACH
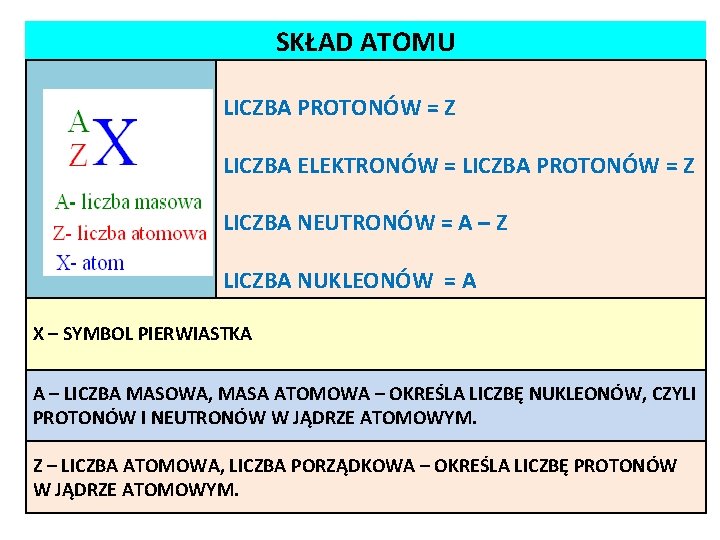
SKŁAD ATOMU LICZBA PROTONÓW = Z LICZBA ELEKTRONÓW = LICZBA PROTONÓW = Z LICZBA NEUTRONÓW = A – Z LICZBA NUKLEONÓW = A X – SYMBOL PIERWIASTKA A – LICZBA MASOWA, MASA ATOMOWA – OKREŚLA LICZBĘ NUKLEONÓW, CZYLI PROTONÓW I NEUTRONÓW W JĄDRZE ATOMOWYM. Z – LICZBA ATOMOWA, LICZBA PORZĄDKOWA – OKREŚLA LICZBĘ PROTONÓW W JĄDRZE ATOMOWYM.
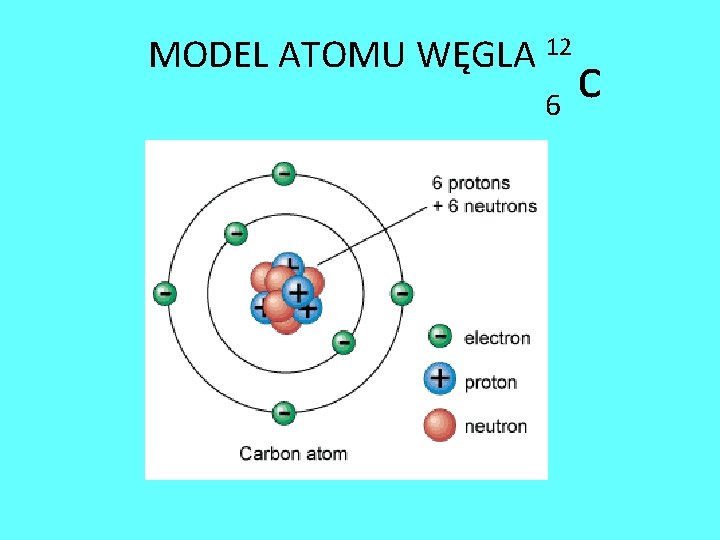
MODEL ATOMU WĘGLA 12 c 6
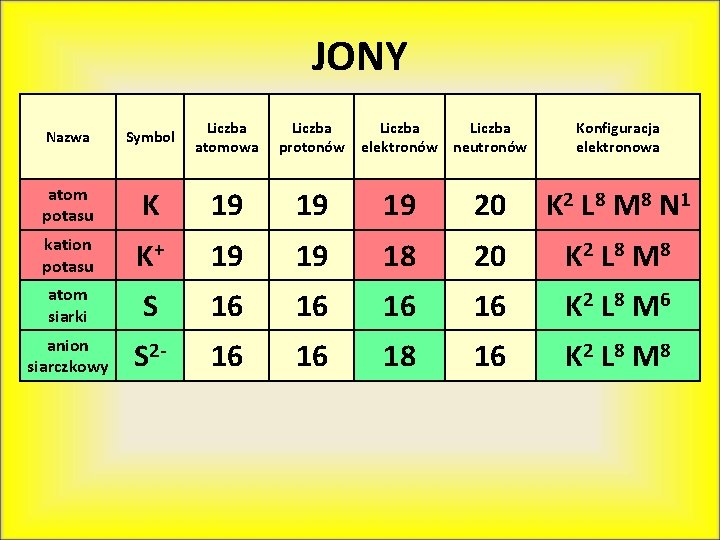
JONY Nazwa Symbol Liczba atomowa Liczba protonów Liczba elektronów neutronów Konfiguracja elektronowa atom potasu K 19 19 19 20 K 2 L 8 M 8 N 1 kation potasu K+ 19 19 18 20 K 2 L 8 M 8 atom siarki S 16 16 K 2 L 8 M 6 anion siarczkowy S 2 - 16 16 18 16 K 2 L 8 M 8

BUDOWA ATOMU, A POŁOŻENIE PIERWIASTKA W UKŁADZIE OKRESOWYM nr grupy 17 Liczba atomowa 35 nr okresu 4 Liczba powłok elektronowych 4 brom 35 Liczba elektronów walencyjnych 7 (17 – 10) Br 79, 904 Liczba protonów 35 Masa atomowa 80 u Liczba elektronów 35 Liczba nukleonów 80 Konfiguracja elektronowa: K 2 L 8 M 18 N 7 Liczba neutronów 80 -35 = 45

PRAWO OKRESOWOŚCI Prawo okresowości mówi, że właściwości pierwiastków uporządkowanych zgodnie ze wzrastającą liczbą atomową zmieniają się w sposób ciągły i okresowy. Układ okresowy składa się z rzędów poziomych zwanych okresami, jest ich 7. Kolumny pionowe zwane są grupami, jest ich 18. Nazwy grup tworzymy od nazwy pierwszego pierwiastka danej grupy (wyjątek grupa 1!) Grupa 1 – litowce Grupa 2 – berylowce Grupa 13 - borowce Grupa 14 – węglowce Grupa 15 – azotowce Grupa 16 – tlenowce Grupa 17 – fluorowce Grupa 18 – helowce, gazy szlachetne Grupy 1, 2 i od 13 do 18 zwane są grupami głównymi. Grupy od 3 do 12 zwane są grupami pobocznymi.
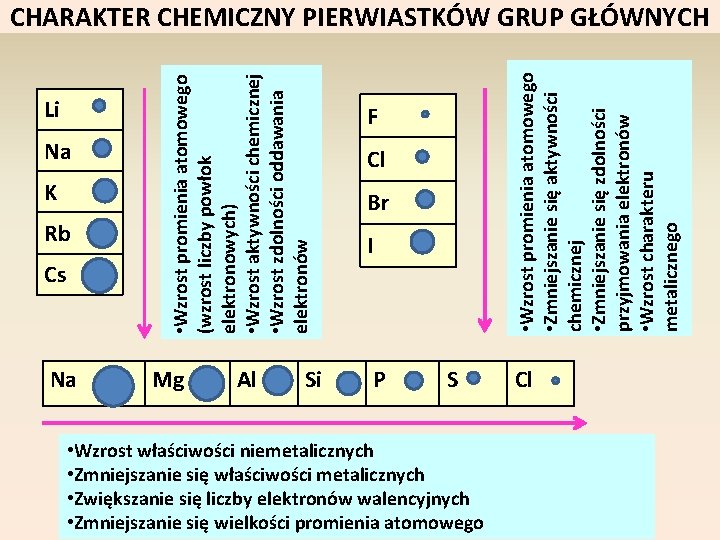
Li Na K Rb Cs Na • Wzrost promienia atomowego (wzrost liczby powłok elektronowych) • Wzrost aktywności chemicznej • Wzrost zdolności oddawania elektronów Mg Al Si F Cl Br I P • Wzrost promienia atomowego • Zmniejszanie się aktywności chemicznej • Zmniejszanie się zdolności przyjmowania elektronów • Wzrost charakteru metalicznego CHARAKTER CHEMICZNY PIERWIASTKÓW GRUP GŁÓWNYCH S • Wzrost właściwości niemetalicznych • Zmniejszanie się właściwości metalicznych • Zwiększanie się liczby elektronów walencyjnych • Zmniejszanie się wielkości promienia atomowego Cl
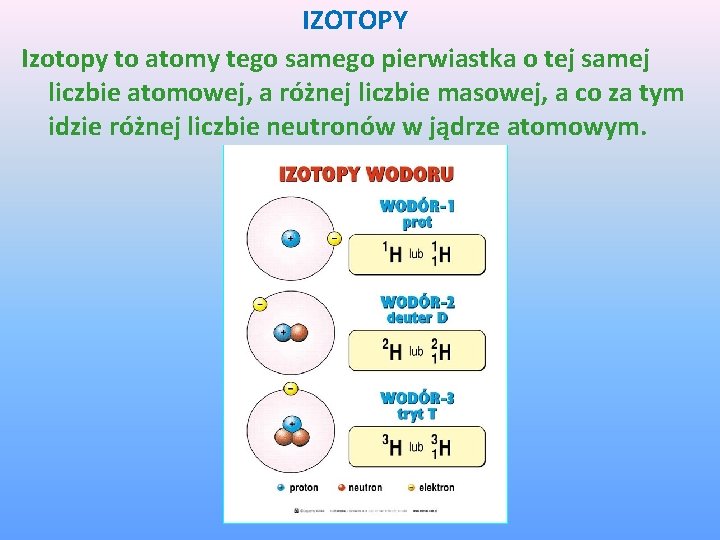
IZOTOPY Izotopy to atomy tego samego pierwiastka o tej samej liczbie atomowej, a różnej liczbie masowej, a co za tym idzie różnej liczbie neutronów w jądrze atomowym.
PODZIAŁ IZOTOPÓW ZE WZGLĘDU NA POCHODZENIE IZOTOPY NATURALNE występujące w przyrodzie SZTUCZNE otrzymane przez człowieka na drodze przemian promieniotwórczych
PODZIAŁ IZOTOPÓW ZE WZGLĘDU NA TRWAŁOŚĆ IZOTOPY TRWAŁE takie, których jądra nie ulegają samorzutnym przemianom w inne, jest ich 272 PROMIENIOTWÓRCZE (nietrwałe), czyli takie, których jądra ulegają samorzutnym przemianom, jest ich ponad 2000
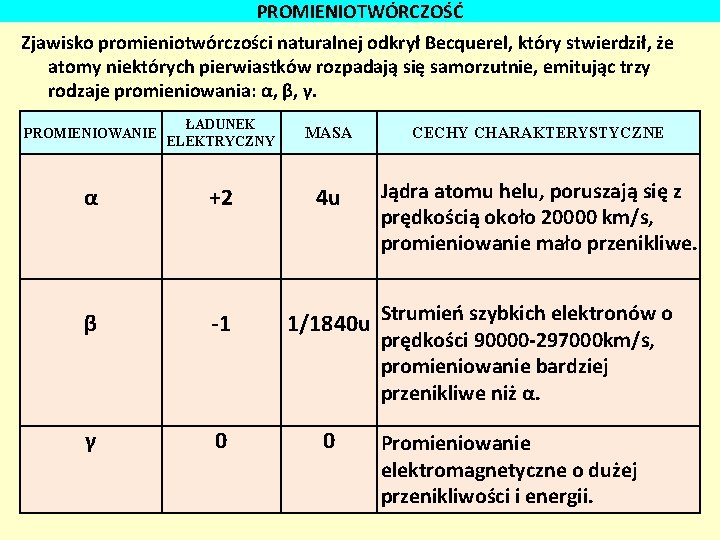
PROMIENIOTWÓRCZOŚĆ Zjawisko promieniotwórczości naturalnej odkrył Becquerel, który stwierdził, że atomy niektórych pierwiastków rozpadają się samorzutnie, emitując trzy rodzaje promieniowania: α, β, γ. PROMIENIOWANIE ŁADUNEK ELEKTRYCZNY MASA CECHY CHARAKTERYSTYCZNE α +2 4 u Jądra atomu helu, poruszają się z prędkością około 20000 km/s, promieniowanie mało przenikliwe. β -1 γ 0 1/1840 u Strumień szybkich elektronów o prędkości 90000 -297000 km/s, promieniowanie bardziej przenikliwe niż α. 0 Promieniowanie elektromagnetyczne o dużej przenikliwości i energii.

PROMIENIOTWÓRCZOŚĆ Promieniotwórczość polega na samorzutnym rozpadzie (rozszczepieniu) jąder atomów niektórych pierwiastków tzw. pierwiastków promieniotwórczych. Istnieją dwa rodzaje pierwiastków promieniotwórczych: • te, które rozszczepiając się tworzą nowy pierwiastek i wysyłają cząstki α • te, które rozszczepiając się tworzą nowy pierwiastek i wysyłają cząstki β Wyróżniamy dwa rodzaje promieniotwórczości: • NATURALNĄ (pierwiastki promieniotwórcze samoistnie ulegają rozpadowi) • SZTUCZNĄ (wywoływaną bombardowaniem danego jądra np. neutronami lub protonami). Izotopy promieniotwórcze różnych pierwiastków różnią się między sobą intensywnością i czasem promieniowania, czyli tzw. okresem połowicznego rozpadu (zaniku), zwanym też okresem półtrwania. Okres połowicznego rozpadu jest to czas, po którym połowa atomów w próbce pierwiastka ulega rozpadowi.
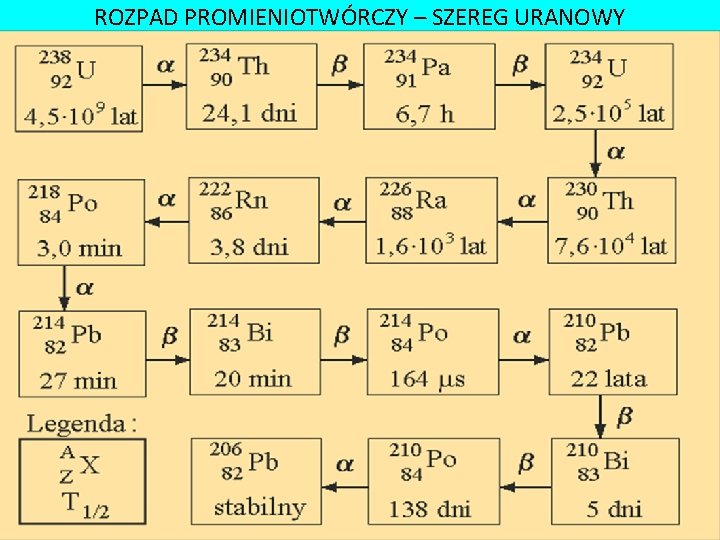
ROZPAD PROMIENIOTWÓRCZY – SZEREG URANOWY

ŚREDNIA MASA ATOMOWA Wiedząc, że gal występujący w przyrodzie jest mieszaniną dwóch izotopów o składzie 60, 2% izotopu o masie 69 u i 39, 8% izotopu o masie 71 u, oblicz średnią masę galu.

ZASTOSOWANIE IZOTOPÓW Kobalt 60 Co do sterylizacji żywności (niszczy pasożyty i pleśnie, dzięki czemu możliwe jest jej długie przechowywanie). Kobalt 60 Co i cez 137 Cs do diagnostyki stanu technicznego i wykrywania wad urządzeń przemysłowych. Do diagnostyki i terapii schorzeń nowotworowych, np. 60 Co – używany w bombie kobaltowej – urządzeniu stosowanym w medycynie do zdalnego napromieniowania chorych tkanek pacjenta, 131 I – do badań tarczycy. 14 C zastosowano jako zegar archeologiczny bo umożliwia datowanie znalezisk archeologicznych i paleontologicznych. Uran wzbogacony o izotop 235 znajduje zastosowanie w reaktorach jądrowych jako paliwo jądrowe. Rad wykorzystuje się do celów leczniczych i do celów naukowych. Pluton stosowany w głowicach bomb jądrowych
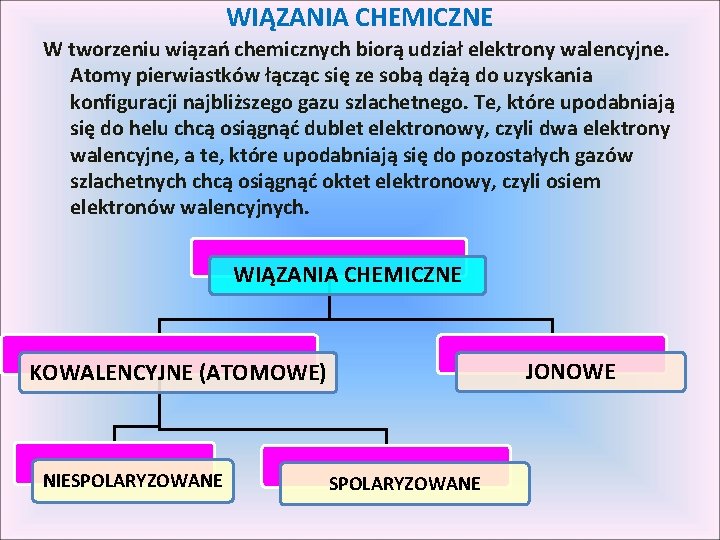
WIĄZANIA CHEMICZNE W tworzeniu wiązań chemicznych biorą udział elektrony walencyjne. Atomy pierwiastków łącząc się ze sobą dążą do uzyskania konfiguracji najbliższego gazu szlachetnego. Te, które upodabniają się do helu chcą osiągnąć dublet elektronowy, czyli dwa elektrony walencyjne, a te, które upodabniają się do pozostałych gazów szlachetnych chcą osiągnąć oktet elektronowy, czyli osiem elektronów walencyjnych. WIĄZANIA CHEMICZNE JONOWE KOWALENCYJNE (ATOMOWE) NIESPOLARYZOWANE
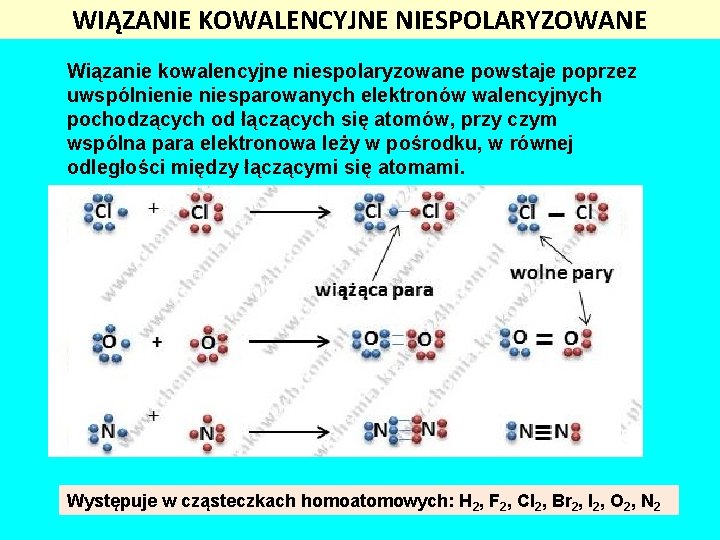
WIĄZANIE KOWALENCYJNE NIESPOLARYZOWANE Wiązanie kowalencyjne niespolaryzowane powstaje poprzez uwspólnienie niesparowanych elektronów walencyjnych pochodzących od łączących się atomów, przy czym wspólna para elektronowa leży w pośrodku, w równej odległości między łączącymi się atomami. Występuje w cząsteczkach homoatomowych: H 2, F 2, Cl 2, Br 2, I 2, O 2, N 2
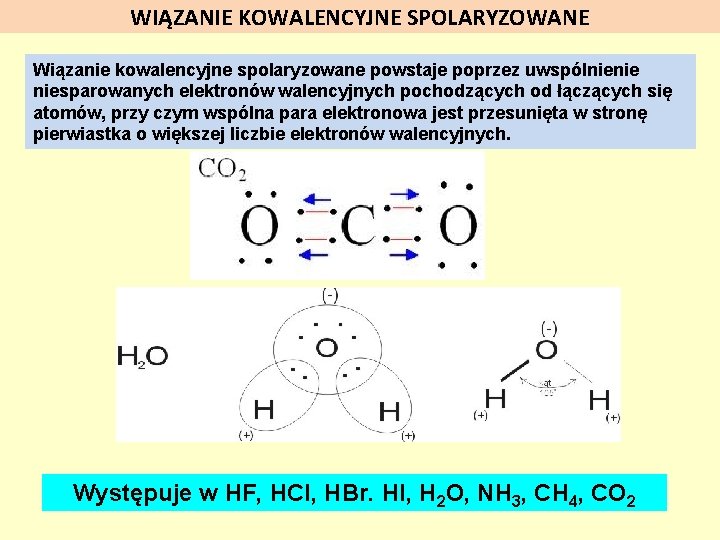
WIĄZANIE KOWALENCYJNE SPOLARYZOWANE Wiązanie kowalencyjne spolaryzowane powstaje poprzez uwspólnienie niesparowanych elektronów walencyjnych pochodzących od łączących się atomów, przy czym wspólna para elektronowa jest przesunięta w stronę pierwiastka o większej liczbie elektronów walencyjnych. Występuje w HF, HCl, HBr. HI, H 2 O, NH 3, CH 4, CO 2

WŁAŚCIWOŚCI ZWIĄZKÓW Z WIĄZANIEM KOWALENCYJNYM • występują we wszystkich trzech stanach skupienia (stałym, ciekłym i gazowym), • w stanie stałym tworzą sieć krystaliczną, • mają niskie temperatury wrzenia i topnienia, • w stanie ciekłym nie przewodzą prądu elektrycznego ponieważ ich cząsteczki są obojętne jako całość.

WIĄZANIE JONOWE Wiązanie jonowe polega na łączeniu (oddziaływaniu) kationów i anionów powstałych z łączących się atomów. Atom, który oddaje elektrony staje się jonem dodatnim - kationem, a atom, który przyjmuje elektrony staje się jonem ujemnym - anionem. Występuje najczęściej między atomami aktywnych metali (1 i 2 grupa układu okresowego) i aktywnych niemetali (grupa 17 i 16 układu okresowego) np. Na. Cl, KBr, Li. F, Ca. Cl 2, K 2 S, Na 2 O, Al. Cl 3 itp.

WŁAŚCIWOŚCI ZWIĄZKÓW Z WIĄZANIEM JONOWYM • występują w stałym stanie skupienia, tworząc sieć krystaliczną. • mają wysokie temperatury wrzenia i topnienia. • stopione lub rozpuszczone w wodzie przewodzą prąd elektryczny, gdyż zawierają zdolne do poruszania się kationy i aniony.
- Slides: 21