Wizania chemiczne 1 2 3 4 5 Wizanie

- Slides: 8

Wiązania chemiczne 1. 2. 3. 4. 5. Wiązanie jonowe Wiązanie kowalencyjne spolaryzowanie Wiązanie koordynacyjne Wiązanie wodorowe

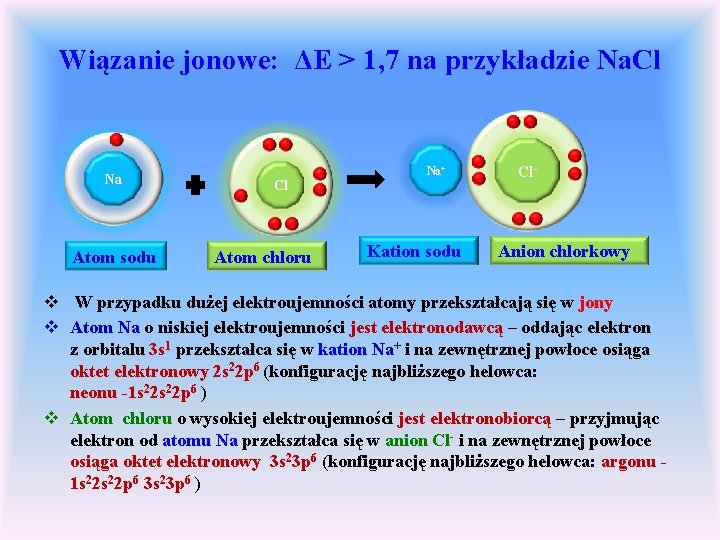
Wiązanie jonowe: ΔE > 1, 7 na przykładzie Na. Cl Na Atom sodu Na+ Cl Atom chloru Kation sodu Cl- Anion chlorkowy v W przypadku dużej elektroujemności atomy przekształcają się w jony v Atom Na o niskiej elektroujemności jest elektronodawcą – oddając elektron z orbitalu 3 s 1 przekształca się w kation Na+ i na zewnętrznej powłoce osiąga oktet elektronowy 2 s 22 p 6 (konfigurację najbliższego helowca: neonu -1 s 22 p 6 ) v Atom chloru o wysokiej elektroujemności jest elektronobiorcą – przyjmując elektron od atomu Na przekształca się w anion Cl- i na zewnętrznej powłoce osiąga oktet elektronowy 3 s 23 p 6 (konfigurację najbliższego helowca: argonu 1 s 22 p 6 3 s 23 p 6 )

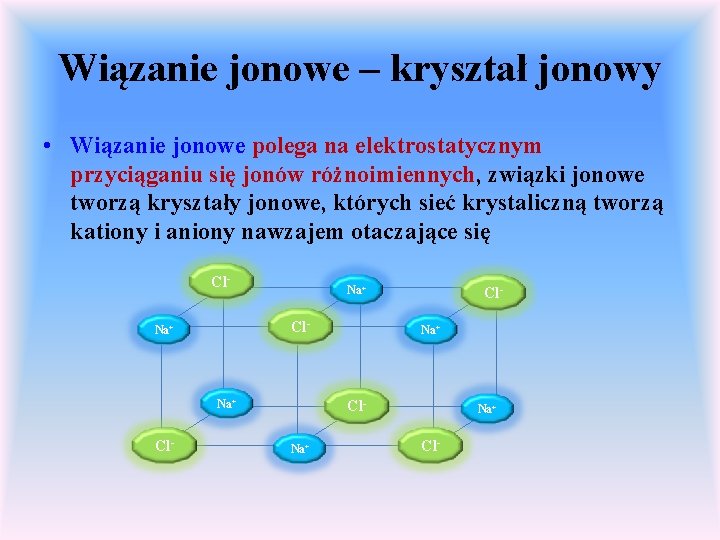
Wiązanie jonowe – kryształ jonowy • Wiązanie jonowe polega na elektrostatycznym przyciąganiu się jonów różnoimiennych, związki jonowe tworzą kryształy jonowe, których sieć krystaliczną tworzą kationy i aniony nawzajem otaczające się Cl- Na+ Na+ Cl- Cl. Na+ Na+ Cl-

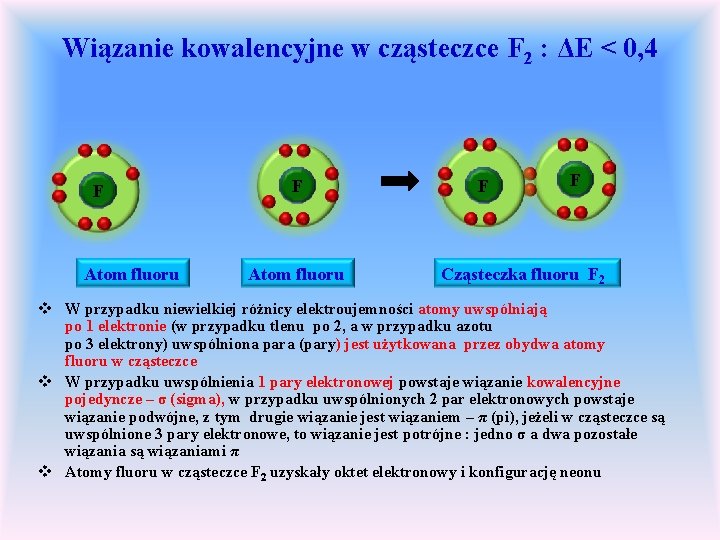
Wiązanie kowalencyjne w cząsteczce F 2 : ΔE < 0, 4 F Atom fluoru F F Cząsteczka fluoru F 2 v W przypadku niewielkiej różnicy elektroujemności atomy uwspólniają po 1 elektronie (w przypadku tlenu po 2, a w przypadku azotu po 3 elektrony) uwspólniona para (pary) jest użytkowana przez obydwa atomy fluoru w cząsteczce v W przypadku uwspólnienia 1 pary elektronowej powstaje wiązanie kowalencyjne pojedyncze – σ (sigma), w przypadku uwspólnionych 2 par elektronowych powstaje wiązanie podwójne, z tym drugie wiązanie jest wiązaniem – π (pi), jeżeli w cząsteczce są uwspólnione 3 pary elektronowe, to wiązanie jest potrójne : jedno σ a dwa pozostałe wiązania są wiązaniami π v Atomy fluoru w cząsteczce F 2 uzyskały oktet elektronowy i konfigurację neonu

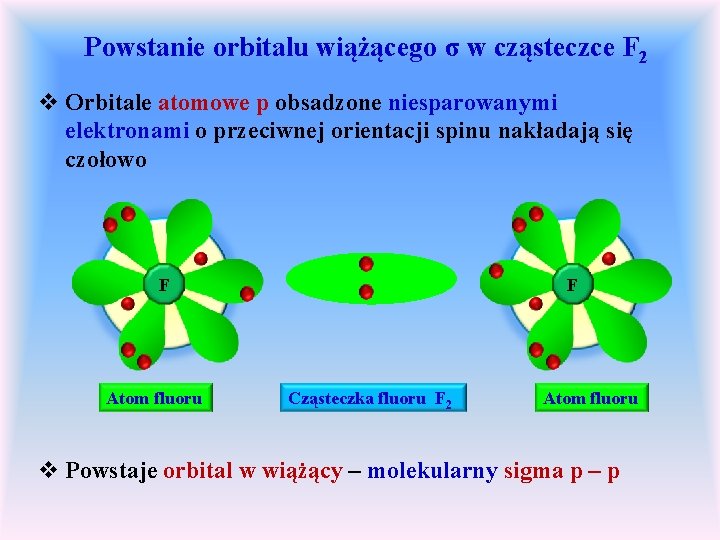
Powstanie orbitalu wiążącego σ w cząsteczce F 2 v Orbitale atomowe p obsadzone niesparowanymi elektronami o przeciwnej orientacji spinu nakładają się czołowo F Atom fluoru F Cząsteczka fluoru F 2 Atom fluoru v Powstaje orbital w wiążący – molekularny sigma p – p

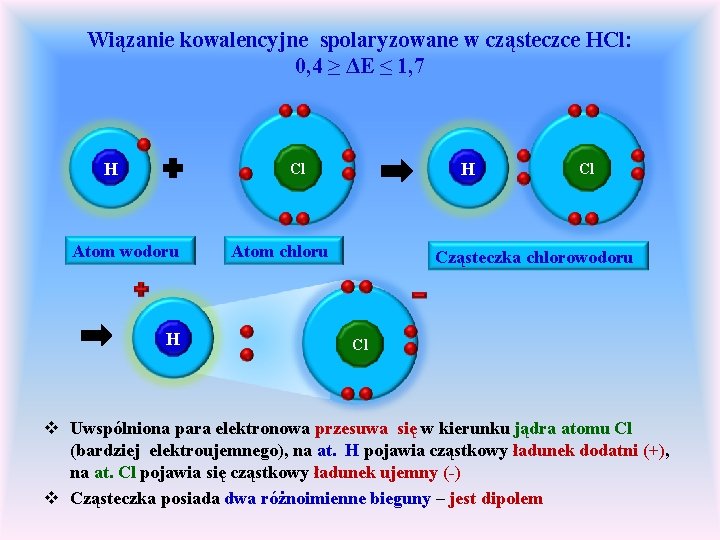
Wiązanie kowalencyjne spolaryzowane w cząsteczce HCl: 0, 4 ≥ ΔE ≤ 1, 7 H H Cl Atom wodoru H Atom chloru Cl Cząsteczka chlorowodoru Cl v Uwspólniona para elektronowa przesuwa się w kierunku jądra atomu Cl (bardziej elektroujemnego), na at. H pojawia cząstkowy ładunek dodatni (+), na at. Cl pojawia się cząstkowy ładunek ujemny (-) v Cząsteczka posiada dwa różnoimienne bieguny – jest dipolem

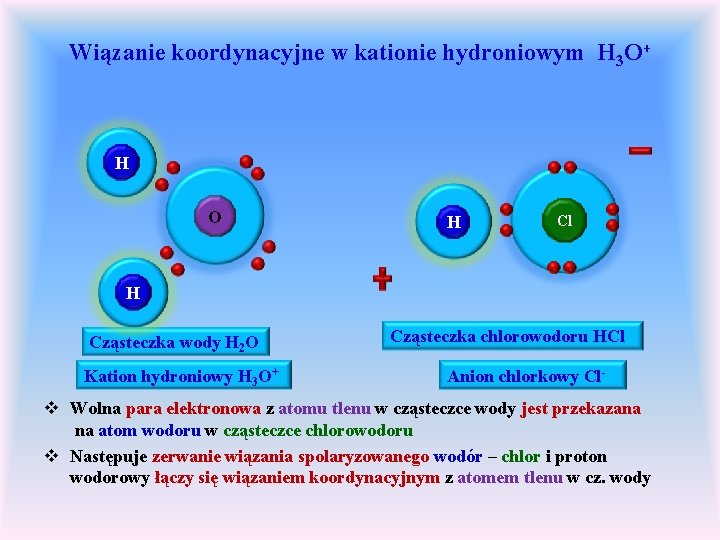
Wiązanie koordynacyjne w kationie hydroniowym H 3 O+ H O H Cl H Cząsteczka wody H 2 O Kation hydroniowy H 3 O+ Cząsteczka chlorowodoru HCl Anion chlorkowy Cl- v Wolna para elektronowa z atomu tlenu w cząsteczce wody jest przekazana na atom wodoru w cząsteczce chlorowodoru v Następuje zerwanie wiązania spolaryzowanego wodór – chlor i proton wodorowy łączy się wiązaniem koordynacyjnym z atomem tlenu w cz. wody

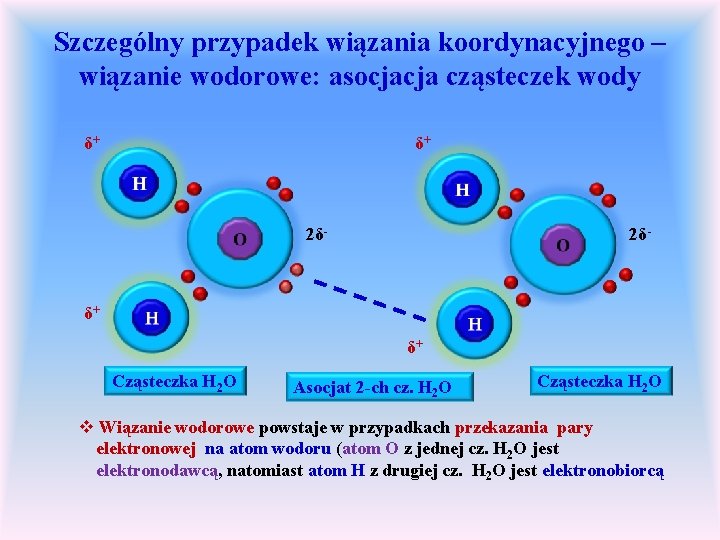
Szczególny przypadek wiązania koordynacyjnego – wiązanie wodorowe: asocjacja cząsteczek wody δ+ δ+ 2δ- δ+ δ+ Cząsteczka H 2 O Asocjat 2 -ch cz. H 2 O Cząsteczka H 2 O v Wiązanie wodorowe powstaje w przypadkach przekazania pary elektronowej na atom wodoru (atom O z jednej cz. H 2 O jest elektronodawcą, natomiast atom H z drugiej cz. H 2 O jest elektronobiorcą