A TERMODINAMIKA MSODIK FTTELE I A II fttel





































- Slides: 49

A TERMODINAMIKA MÁSODIK FŐTÉTELE I. A II. főtétel néhány megfogalmazása. II. Az entrópia termodinamikai és statisztikus definíciója. Entrópiatétel. III. A rendszer, a környezet és ezek együttes entrópiájának változása tökéletes gázok reverzíbilis és irreverzíbilis izoterm expanziója során. IV. Az adiabatikus folyamatok entrópiaváltozása. V. Az entrópia változása néhány fontos folyamatban VI. A hő átalakítása munkává: a Carnot-ciklus lényege és a hatásfok fogalma. VII. Hőerőgépek, hűtőgépek és hőszivattyúk működésének lényege. 1

I. A II. FŐTÉTEL NÉHÁNY MEGFOGALMAZÁSA • Előzmény: néhány általános tapasztalat • Adott körülmények között csak egyetlen önkéntes (spontán) folyamatirány létezik. ? 2

I. A II. FŐTÉTEL NÉHÁNY MEGFOGALMAZÁSA • Előzmény: néhány általános tapasztalat • Adott körülmények között csak egyetlen önkéntes (spontán) folyamatirány létezik. 3

I. A II. FŐTÉTEL NÉHÁNY MEGFOGALMAZÁSA • Előzmény: néhány általános tapasztalat • Adott körülmények között csak egyetlen önkéntes (spontán) folyamatirány létezik. 4

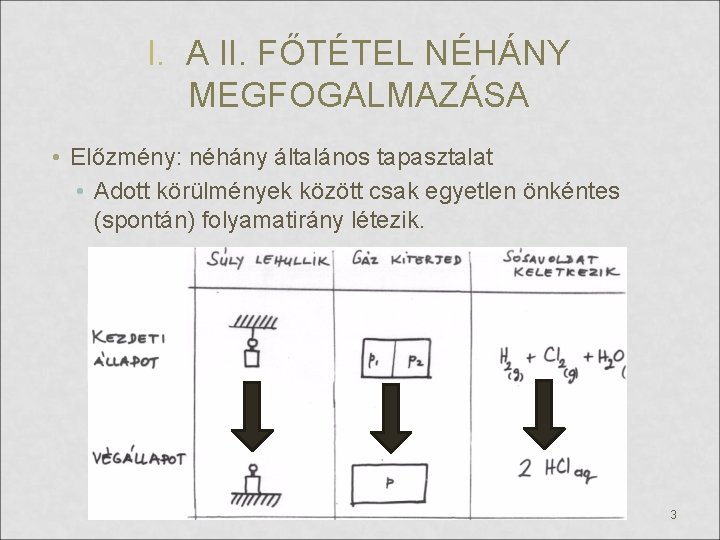
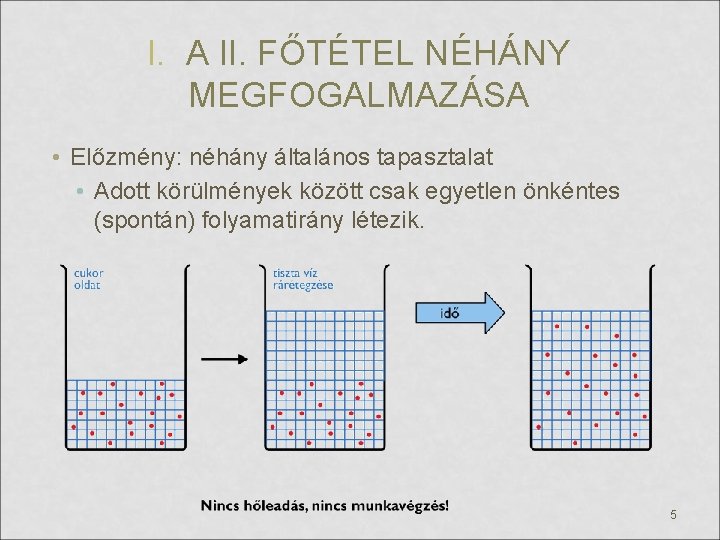
I. A II. FŐTÉTEL NÉHÁNY MEGFOGALMAZÁSA • Előzmény: néhány általános tapasztalat • Adott körülmények között csak egyetlen önkéntes (spontán) folyamatirány létezik. 5

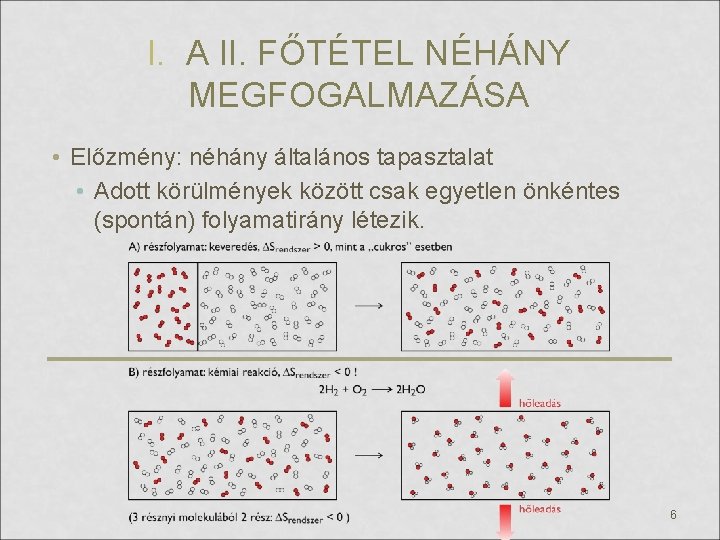
I. A II. FŐTÉTEL NÉHÁNY MEGFOGALMAZÁSA • Előzmény: néhány általános tapasztalat • Adott körülmények között csak egyetlen önkéntes (spontán) folyamatirány létezik. 6

I. A II. FŐTÉTEL NÉHÁNY MEGFOGALMAZÁSA • Előzmény: néhány általános tapasztalat • Adott körülmények között csak egyetlen önkéntes (spontán) folyamatirány létezik. • A hő csak magasabb hőmérsékletű testről megy át önként hidegebbre, fordítva nem. • Adott körülmények mellett létezik egy jól meghatározott végállapot: ez az egyensúlyi állapot. Ezen „túl” sohasem megy a rendszer. • Fordított irányú folyamat munkabefektetés és/vagy hőközlés árán valósíthatók meg. • Nincs olyan folyamat, melyben a hő teljes egészében munkává alakul, miközben más változás nem következik be. • Másképpen: másodfajú perpetuum mobile nem szerkeszthető. • Csak önként végbemenő folyamat végez munkát. 7

I. A II. FŐTÉTEL NÉHÁNY MEGFOGALMAZÁSA • Előzmény: néhány általános tapasztalat • Adott körülmények között csak egyetlen önkéntes (spontán) folyamatirány létezik. • A hő csak magasabb hőmérsékletű testről megy át önként hidegebbre, fordítva nem. Maurits Cornelis Escher • Adott körülmények mellett létezik egy jól meghatározott végállapot: ez az egyensúlyi állapot. Ezen „túl” sohasem megy a rendszer. (1898 -1972) • Fordított irányú folyamat munkabefektetés és/vagy hőközlés árán Waterfall valósíthatók meg. • Nincs olyan folyamat, melyben a hő teljes egészében munkává alakul, miközben más változás nem következik be. • Másképpen: másodfajú perpetuum mobile nem szerkeszthető. • Csak önként végbemenő folyamat végez munkát. 8

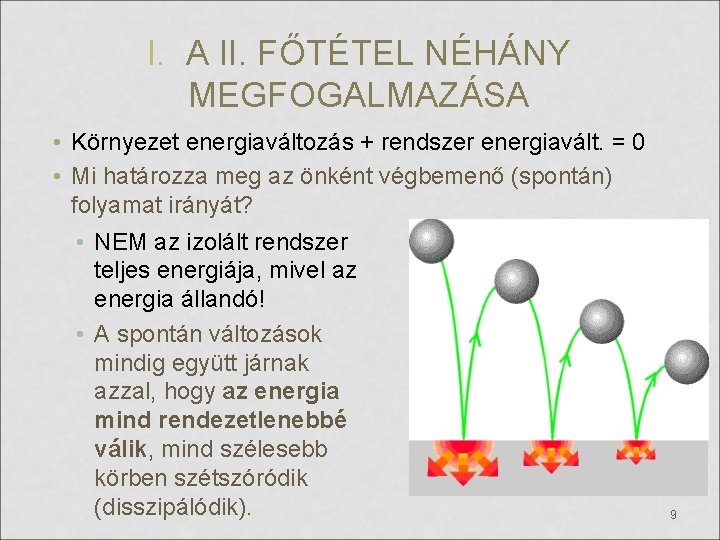
I. A II. FŐTÉTEL NÉHÁNY MEGFOGALMAZÁSA • Környezet energiaváltozás + rendszer energiavált. = 0 • Mi határozza meg az önként végbemenő (spontán) folyamat irányát? • NEM az izolált rendszer teljes energiája, mivel az energia állandó! • A spontán változások mindig együtt járnak azzal, hogy az energia mind rendezetlenebbé válik, mind szélesebb körben szétszóródik (disszipálódik). 9

I. A II. FŐTÉTEL NÉHÁNY MEGFOGALMAZÁSA • (itt most megelőlegezzük az entrópia fogalmát) • „anyagi rendszerek molekuláris rendezetlensége” (Rudolf Clausius) • Görög: τροπή = „változástartalom” 10

I. A II. FŐTÉTEL NÉHÁNY MEGFOGALMAZÁSA • Egy izolált rendszer entrópiája valamely önként lejátszódó folyamatban nő: ΔStot > 0. • Izolált rendszer entrópiája önmagában nem csökken. • Önként lezajló folyamatok esetén az izolált rendszer entrópiája nem csökkenhet. A valóságos folyamatok irreverzibilisek, ezekben az entrópia csak növekedhet. • Egyensúlyi állapotban a globálisan izolált rendszer entrópiája maximális. Ez az entrópiamaximum elve. 11

• A termodinamika I. főtétele izolált rendszerben a belső energia állandóságát mondja ki. • Az U belső energia állapotfüggvény alkalmazásával eldönthetjük, hogy egy adott változás megengedett-e. Csak azok a változások mehetnek végbe, amelyekben az izolált rendszer belső energiája állandó marad, azaz ΔU = 0. De ez nem mondja meg, hogy a folyamatok maguktól (spontán) milyen irányba mennek végbe. • Az I. főtétel megengedné, hogy pl. izolált rendszerben egy hideg test hőátadással tovább melegítsen egy melegebbet, hiszen eközben U nem változik. Ilyet mégsem tapasztalunk, csak olyat, hogy a hő melegebb testről megy át hidegebbre. Minden más esetben is csak egy spontán iránya van a változásoknak. 12

• A termodinamika II. főtétele az I. főtétel által megengedett folyamatok közül megadja az önként végbemenő (spontán) folyamatok irányát. • A klasszikus (fenomenológikus leírásmódú) termodinamika ezt egy újabb állapotfüggvény, az S entrópia segítségével teszi meg: Egy izolált rendszer entrópiája valamely spontán (önként lejátszódó) folyamatban nő: ΔStot > 0. • A statisztikus leírásmód szerint az önként végbe-menő változásokban mindig nő a rendezetlenség. Ennek egzakt fogalma a W termodinamikai való-színűség, aminek értéke (miként az entrópiáé) a spontán folyamatokban növekszik. [Ez a spontán energiaszétszóródás (disszipáció) elve. ] 13

• Rögzítsük ismét: Spontán folyamat: adott körülmények között magától, külső behatás nélkül végbemegy. Pl. : • meleg test lehűl (hőátmenet nagy T-ről kis T-re), • a réz(II)-szulfát oldatból a réz a cinkrúdra kiválik, • H 2 + Cl 2 → 2 HCl önként végbemegy. • Megfelelő körülmények (gőzgép, galvánelem stb. ) között a spontán folyamatok munkát végeznek! • Az ellenkező irányú – nem spontán – folyamat energiabefektetéssel (hőközléssel, munkavégzéssel) kikényszeríthető: • a test munkavégzéssel vagy hőközléssel ismét felmelegíthető, • a cinkrúdra kivált réz onnan „leeleketrolizálható”, • A HCl hő- vagy elektromos energiával felbontható. 14

• Később megtárgyaljuk: • nemcsak az irány (a „merre”), hanem a „meddig”, azaz a végállapot is egyértelmű, • ez a végállapot egyensúly jellegű, • az egyensúly mindkét irányból elérhető, • [az egyensúly dinamikus egyensúly (azaz az egyensúlyban – bár nem „látjuk” – az oda- és visszafolyamat egyaránt és azonos sebességgel lejátszódik). ] • Mindezt kvantitatívan további termodinamikai függvényekkel tudjuk és fogjuk leírni: • I. főtétel: U belső energia és H entalpia • II. főtétel: S entrópia 15

II. AZ ENTRÓPIA TERMODINAMIKAI ÉS STATISZTIKUS DEFINÍCIÓJA • A klasszikus (fenomenologikus) termodinamikában d. S a reverzíbilis hőcsere és hőmérsékletének hányadosa • infinitezimális: • ill. véges változásban: • A statisztikus termodinamikában: S = k ln. W ahol W a termodinamikai valószínűség. • [Az előző állítást, az utóbbi valószínűséget mond. A két megközelítés azonos értékű. Az utóbbi az S abszolút értéke szempontjából meghatározó. ] 16

II. AZ ENTRÓPIA TERMODINAMIKAI ÉS STATISZTIKUS DEFINÍCIÓJA • Az entrópiáról: • Állapotfüggvény: értéke csak a rendszer kezdeti és végállapotától függ, és független az úttól. • Extenzív mennyiség: értéke az anyagmennyiséggel arányos, mértékegysége: J K-1 (Clausius) • Az 1 mol anyagmennyiségre vonatkoztatott moláris entrópia már intenzív mennyiség, mértékegysége: J K-1 mol-1. • Látni fogjuk: 0 K-től számított abszolút értéke van és ezt meg tudjuk határozni. 17

II. AZ ENTRÓPIA TERMODINAMIKAI ÉS STATISZTIKUS DEFINÍCIÓJA • Mint a többi termodinamikai függvény (U, H) esetén, az entrópiára (S) is érvényes: • Entrópiája minden rendszernek van, és ez az S érték függ a rendszer állapotától (állapotjelzőitől), de nem függ attól, milyen úton jutott a rendszer ebbe az állapotba. • Entrópiaváltozás kísér minden folyamatot, fizikai-kémiai változást (pl. párolgási, reakcióentrópia). • A d. S vagy ΔS értékeket mindig reverzíbilis út/utak alapján számoljuk. • Az entrópia állapotfüggvény jellegéből következik, hogy reverzíbilis körfolyamatban az entrópiaváltozás értéke 0: 18

II. AZ ENTRÓPIA TERMODINAMIKAI ÉS STATISZTIKUS DEFINÍCIÓJA • Az entrópiatétel(ek): • [Az S fogalma és változásának számítása reverzíbilis folyamatokra épül. ] • Minden valóságos folyamat irreverzíbilis, ezért elszigetelt rendszerben csak olyan folyamatok mennek önként végbe, amelyek során az entrópia nő. [Megjegyzés: izolált rendszerben nincs entrópia-megmaradási tétel, szemben azzal, hogy a belső energiára van. ] • Izolált rendszer entrópiája egyensúlyban maximális. • Ezek tulajdonképpen a II. főtétel különböző megfogalmazásai az entrópia segítségével. 19

II. AZ ENTRÓPIA TERMODINAMIKAI ÉS STATISZTIKUS DEFINÍCIÓJA • Az entrópia statisztikus értelmezéséhez: (Ludwig Boltzmann (1844 -1906)) k: Boltzmann-állandó W: termodinamikai valószínűség (az adott makroállapothoz rendelhető mikroállaptok száma) 20

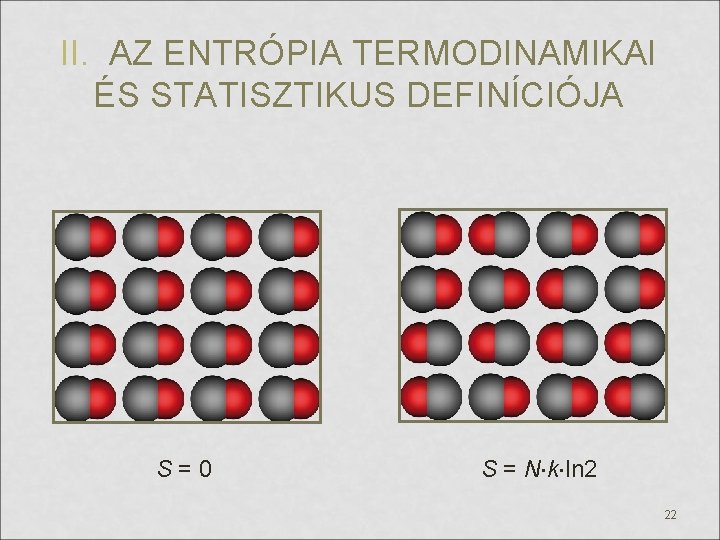
II. AZ ENTRÓPIA TERMODINAMIKAI ÉS STATISZTIKUS DEFINÍCIÓJA • Az entrópia statisztikus értelmezéséhez: (Ludwig Boltzmann (1877)) • Minden makroállapot (p, T, V, n) sok-sok mikroállapot révén valósul meg (mikroállapot: egyedi részecskék (atomok/molekulák) energiaállapotának koordinátái). • A különböző mikroállapotok betöltöttségét az abban lévő azonos koordinátájú molekulák száma adja. • Mindig a legvalószínűbb állapot valósul meg: ez a legtöbb változatban (sokféle betöltöttséggel) megvalósítható makroállapot. Ennek mértéke a W termodinamikai valószínűség. 21

II. AZ ENTRÓPIA TERMODINAMIKAI ÉS STATISZTIKUS DEFINÍCIÓJA S = 0 S = N k ln 2 22

II. AZ ENTRÓPIA TERMODINAMIKAI ÉS STATISZTIKUS DEFINÍCIÓJA Klasszikus termodinamika: az entrópia nő minden önként végbemenő, valóságos folyamatban. • Két független gáz entrópiája: S = S 1 + S 2 • Valószínűségszámításból: f(W 1, W 2) = f(W 1) f(W 2) • Ennek a feltételnek megfelelő S = f(W) függvény: S = k ln. W ahol k = 1, 38 10 -23 J/K (Boltzmann-állandó) S = S 1 + S 2 = k ln. W 1 + k ln. W 2 = k ln(W 1 W 2) • Az entrópia ez alapján a rendezetlenség mértéke. • A természetben önként végbemenő folyamatok az entrópia, azaz a rendezetlenség növekedése irányába mennek végbe. 23

II. AZ ENTRÓPIA TERMODINAMIKAI ÉS STATISZTIKUS DEFINÍCIÓJA • A klasszikus (formális) termodinamika szerint a spontán folyamatokban mindig nő az entrópia. Elvileg sincs kivétel, ez determináltságot jelent. • A statisztikus termodinamika elvileg megengedi az entrópia csökkenéssel járó folyamatokat is: ennek valószínűsége azonban valós (makroszkopikus) rendszerekben mérhetetlenül kicsi. [A labda eszerint magától is felpattanhatna a földről, de eddig ezt senki sem észlelte, és aligha fogjuk észlelni. ] 24

III. A RENDSZER, A KÖRNYEZET ÉS EZEK EGYÜTTES ENTRÓPIÁJÁNAK VÁLTOZÁSA • A II. főtétel izolált (elszigetelt) rendszerre vonatkozik. • A gyakorlatban a legtöbb vizsgált rendszer a környezetével termikusan és/vagy mechanikusan érintkezik. • Ilyenkor bármilyen változás mind a rendszerben (d. S), mind annak környezetében (d. Ssur vagy d. S’) entrópiaváltozást eredményez. • Ha a folyamat reverzíbilis, akkor a felvett, ill. leadott S nagysága azonos, ha irreverzíbilis (a valóságban mindig), akkor a rendszer és környezete együttes entrópiája megnő, entrópia „termelődik”. 25

III. A RENDSZER, A KÖRNYEZET ÉS EZEK EGYÜTTES ENTRÓPIÁJÁNAK VÁLTOZÁSA A Clausius-féle egyenlőtlenség: • A valóságos folyamatokban az entrópia jobban növekszik, mint a hőcseréből számított entrópia: d. S ≥ dq/T, azaz d. S – (dq/T) ≥ 0. • A > jel a valóságos, irreverzíbilis, • az = jel a reverzíbilis folyamatokra vonatkozik. 26

V. AZ ENTRÓPIA VÁLTOZÁSA NÉHÁNY FONTOS FOLYAMATBAN a) Entrópiaváltozás spontán hőcserében b) Entrópiaváltozás adiabatikus folyamatokban c) Az entrópia változása a térfogattal: a tökéletes gáz izoterm kiterjedése d) Entrópiaváltozás fázisátmenetben – az átmenet (pl. olvadás, forrás) hőmérsékletén e) Az entrópia változása a hőmérséklettel 27

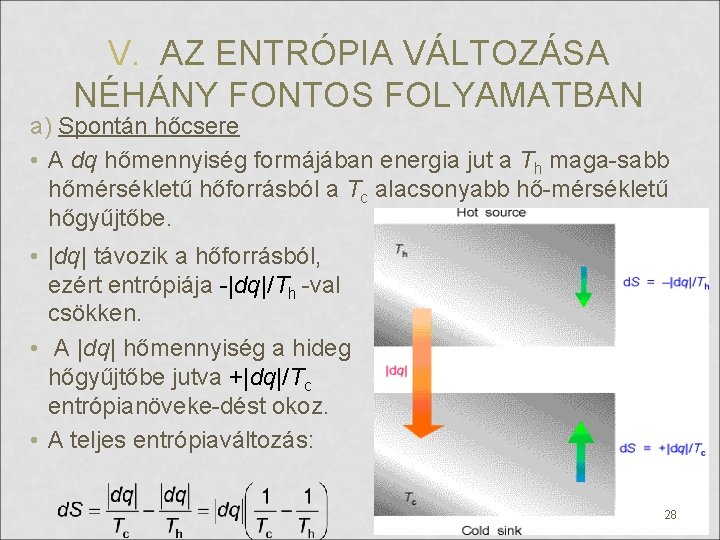
V. AZ ENTRÓPIA VÁLTOZÁSA NÉHÁNY FONTOS FOLYAMATBAN a) Spontán hőcsere • A dq hőmennyiség formájában energia jut a Th maga-sabb hőmérsékletű hőforrásból a Tc alacsonyabb hő-mérsékletű hőgyűjtőbe. • |dq| távozik a hőforrásból, ezért entrópiája -|dq|/Th -val csökken. • A |dq| hőmennyiség a hideg hőgyűjtőbe jutva +|dq|/Tc entrópianöveke-dést okoz. • A teljes entrópiaváltozás: 28

V. AZ ENTRÓPIA VÁLTOZÁSA NÉHÁNY FONTOS FOLYAMATBAN b) adiabatikus folyamatokban (itt nincs hőcsere) • Adiabatikus reverzíbilis folyamatokban az entrópia változatlan, ekkor ugyanis q = 0, így ΔS = qrev/T = 0. Ezek az izentrópikus folyamatok. • Ha a rendszerben irreverzíbilis adiabatikus változás megy végbe, akkor a rendszerben dqirrev = 0 és d. S ≥ 0. Az adiabatikus spontán változás során a rendszer entrópiája megnő. • Az adiabatikus spontán változás során nem jut hő a környezetbe, ezért a környezet entrópiája állandó marad, azaz d. Ssur = 0. • A rendszer és környezete együttes entrópiaváltozása teljesíti a d. Stot ≥ 0 feltételt. 29

V. AZ ENTRÓPIA VÁLTOZÁSA NÉHÁNY FONTOS FOLYAMATBAN c) Entrópiaváltozás izoterm folyamatokban: a tökéletes gáz kiterjedése (expanziója) • Ha a rendszerben a tökéletes gáz reverzíbilis izoterm kiterjedése megy végbe, akkor dq = -dw (mivel d. U = 0). [A munka fedezete a környezetből felvett hő. ] • Mi a helyzet az entrópiával? Konkrétabban: Hogyan változik az entrópia a térfogattal? 30

V. AZ ENTRÓPIA VÁLTOZÁSA NÉHÁNY FONTOS FOLYAMATBAN c) Entrópiaváltozás izoterm folyamatokban: a tökéletes gáz kiterjedése (expanziója) • Ha a rendszerben a tökéletes gáz reverzíbilis izoterm kiterjedése megy végbe, akkor dq = -dw (mivel d. U = 0). • A rendszer két állapota közötti entrópiakülönbség kiszámítása: • kell találnunk egy reverzíbilis utat (hőfelvétel és munkavégzés is van): • majd minden egyes lépésben integrálni kell a felvett hő és a hőfelvétel hőmérsékletének hányadosát. 31

V. AZ ENTRÓPIA VÁLTOZÁSA NÉHÁNY FONTOS FOLYAMATBAN c) Entrópiaváltozás izoterm folyamatokban: a tökéletes gáz kiterjedése (expanziója) • Ha a rendszerben a tökéletes gáz reverzíbilis izoterm kiterjedése megy végbe, akkor dq = -dw (mivel d. U = 0). • A rendszer két állapota közötti entrópiakülönbség kiszámítása: • A tökéletes gáz entrópiája a térfogattal növekszik. • Értelmezés: a nagyobb térfogat a molekulák számára nagyobb rendezetlenséget biztosít. 32

V. AZ ENTRÓPIA VÁLTOZÁSA NÉHÁNY FONTOS FOLYAMATBAN d) Fázisátalakulás entrópiája – a fázisátalakulás T-én • Olvadáskor/fagyáskor vagy forráskor/ lecsapódáskor a molekuláris rendezettségben jelentős változás következik be, így feltételezhető az entrópia jelentős megváltozása. • Olvadás: a rendezett állapotú szilárd szerkezet átalakul egy rendezetlenebb folyadékállapottá. S nő! • Párolgás: a kis térfogatot elfoglaló kondenzált fázis nagy térfogatot kitöltő gázzá alakul, így a rendszer entrópiája jelentős mértékben megnő. 33

V. AZ ENTRÓPIA VÁLTOZÁSA NÉHÁNY FONTOS FOLYAMATBAN d) Fázisátalakulás entrópiája – a fázisátalakulás T-én • Ttrs: normális fázisátmeneti hőmérséklet • A jég-víz fázisegyensúly: 1 atm nyomáson Ttrs = 273 K. • A víz-gőz fázisegyensúly: 1 atm nyomáson Ttrs = 373 K. • A fázisátalakulás hőmérsékletén a rendszer és környezete közötti bármilyen hőcsere reverzíbilis, mivel a rendszert alkotó két fázis egyensúlyban van. • Állandó nyomáson q = Δtrs. H, így a rendszer entrópiaváltozása: 34

V. AZ ENTRÓPIA VÁLTOZÁSA NÉHÁNY FONTOS FOLYAMATBAN d) Fázisátalakulás entrópiája – a fázisátalakulás T-én • A fagyás, kondenzálás exoterm (Δtrs. H < 0), így a fázisátmenet entrópiaváltozása negatív. Az entrópia-csökkenés összhangban van azzal, hogy a folyadék → szilárd alakulásakor a rendszer rendezettebbé válik. • Olvadás, párolgás endoterm (Δtrs. H > 0), így a fázisátalakulás entrópiaváltozása pozitív. A rendszer rendezetlenebb lesz. Az endoterm folyamatokban a rendszer entrópiája nő. • Trouton-szabály (tapasztalat): sok folyadék standard párolgási entrópiája közel azonos, kb. +85 J K-1. Az eltérések molekuláris szemléletben értelmezhetők. 35

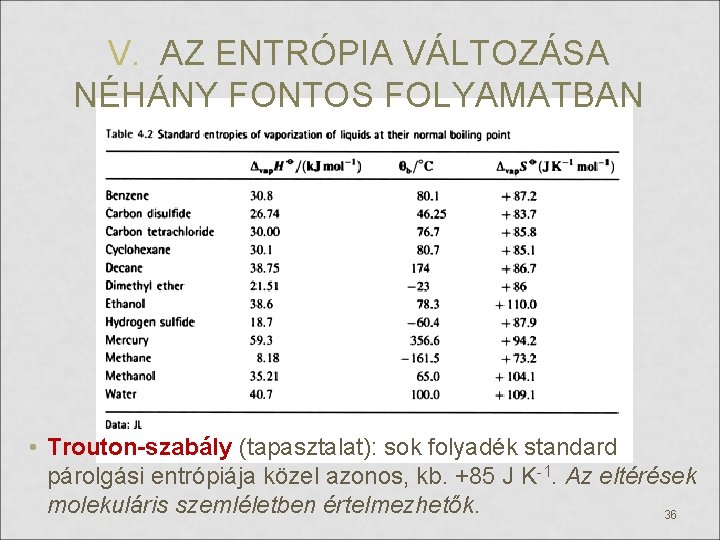
V. AZ ENTRÓPIA VÁLTOZÁSA NÉHÁNY FONTOS FOLYAMATBAN • Trouton-szabály (tapasztalat): sok folyadék standard párolgási entrópiája közel azonos, kb. +85 J K-1. Az eltérések molekuláris szemléletben értelmezhetők. 36

V. AZ ENTRÓPIA VÁLTOZÁSA NÉHÁNY FONTOS FOLYAMATBAN • Δfus. S < Δvap. S: párolgáskor nagyobb mértékben nő a rendezetlenség, mint olvadáskor • Trouton-szabály (tapasztalat): sok folyadék standard párolgási entrópiája közel azonos, kb. +85 J K-1. Az eltérések molekuláris szemléletben értelmezhetők. 37

V. AZ ENTRÓPIA VÁLTOZÁSA NÉHÁNY FONTOS FOLYAMATBAN e) Az entrópia változása a hőmérséklettel • A III. főtétel keretében fogjuk tárgyalni. – Nő! 38

VI. A HŐ ÁTALAKÍTÁSA MUNKÁVÁ. A CARNOT-CIKLUS ÉS A HATÁSFOK FOGALMA 39

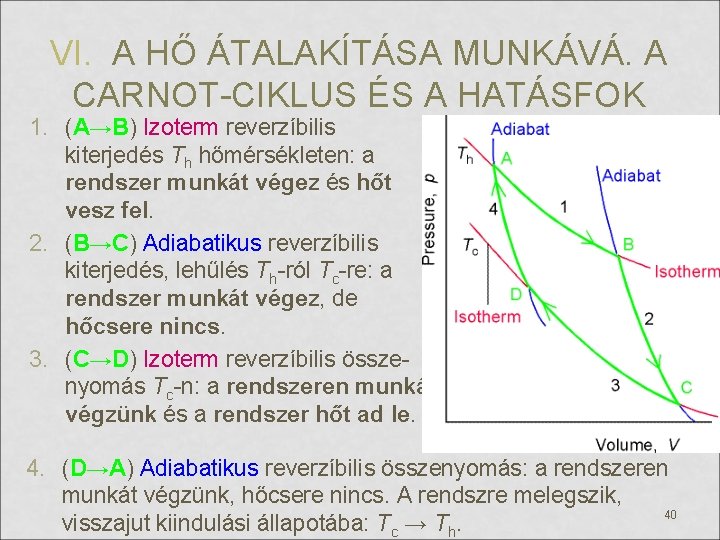
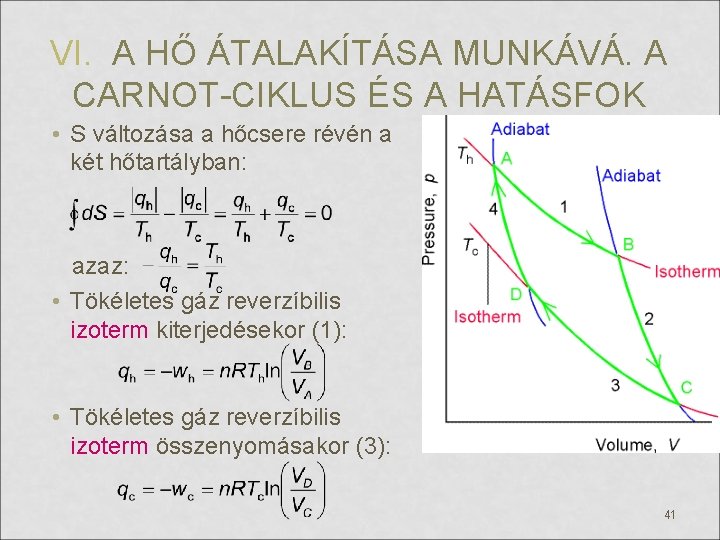
VI. A HŐ ÁTALAKÍTÁSA MUNKÁVÁ. A CARNOT-CIKLUS ÉS A HATÁSFOK 1. (A→B) Izoterm reverzíbilis kiterjedés Th hőmérsékleten: a rendszer munkát végez és hőt vesz fel. 2. (B→C) Adiabatikus reverzíbilis kiterjedés, lehűlés Th-ról Tc-re: a rendszer munkát végez, de hőcsere nincs. 3. (C→D) Izoterm reverzíbilis összenyomás Tc-n: a rendszeren munkát végzünk és a rendszer hőt ad le. 4. (D→A) Adiabatikus reverzíbilis összenyomás: a rendszeren munkát végzünk, hőcsere nincs. A rendszre melegszik, 40 visszajut kiindulási állapotába: Tc → Th.

VI. A HŐ ÁTALAKÍTÁSA MUNKÁVÁ. A CARNOT-CIKLUS ÉS A HATÁSFOK • S változása a hőcsere révén a két hőtartályban: azaz: • Tökéletes gáz reverzíbilis izoterm kiterjedésekor (1): • Tökéletes gáz reverzíbilis izoterm összenyomásakor (3): 41

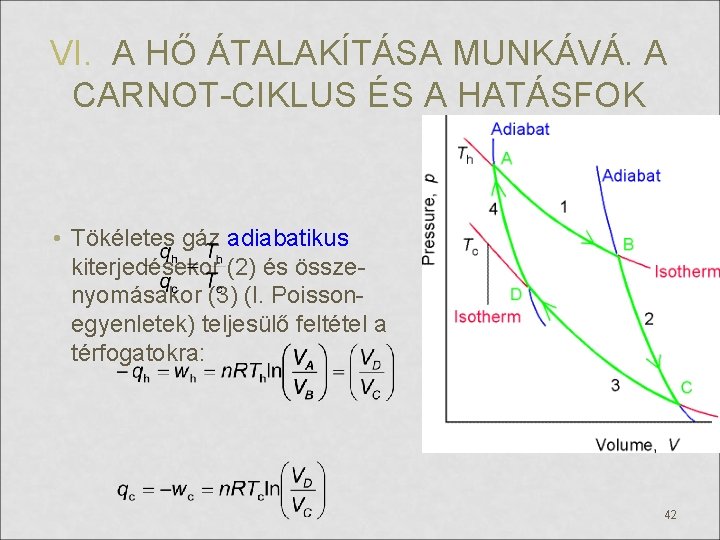
VI. A HŐ ÁTALAKÍTÁSA MUNKÁVÁ. A CARNOT-CIKLUS ÉS A HATÁSFOK • Tökéletes gáz adiabatikus kiterjedésekor (2) és összenyomásakor (3) (l. Poissonegyenletek) teljesülő feltétel a térfogatokra: 42

VI. A HŐ ÁTALAKÍTÁSA MUNKÁVÁ. A CARNOT-CIKLUS ÉS A HATÁSFOK Hatásfok a Carnot-körfolyamatban: • A hatásfok (ε): a termelt munka (azaz a qh – qc) és a felvett hő (qh) hányadosa: • ε annál nagyobb, minél kisebb Tc és minél nagyobb Th • ε maximumot (=1) ér el, ha Tc → 0, vagy Th → ∞. [Ez a valóságban sohasem következik be. ] • Valamennyi reverzíbilisen működő gépezet hatásfoka – függetlenül a konstrukciótól – azonos. 43

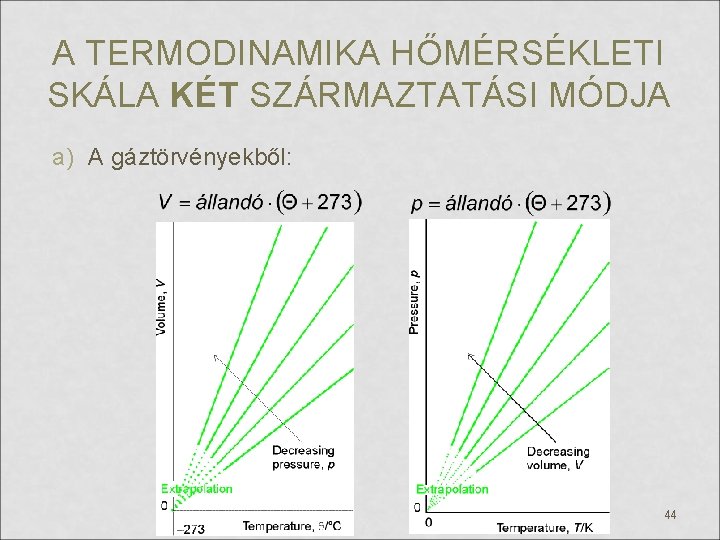
A TERMODINAMIKA HŐMÉRSÉKLETI SKÁLA KÉT SZÁRMAZTATÁSI MÓDJA a) A gáztörvényekből: 44

A TERMODINAMIKA HŐMÉRSÉKLETI SKÁLA KÉT SZÁRMAZTATÁSI MÓDJA b) A Carnot-ciklus, a hőerőgép hatásfoka alapján: azaz • A termodinamikai hőmérsékleti skála 0 pontja az a hőmérséklet, ahol a Carnot-hatásfok ε = 1 lenne. • Lehetne sokféle skála, [van is, ] de Celsius óta célszerűen T 3(víz) = 273, 16 K. 45

VII. HŐERŐGÉPEK, HŰTŐGÉPEK ÉS HŐSZIVATTYÚK MŰKÖDÉSÉNEK LÉNYEGE • Hőerőgép: termikus energiát (égéshőt) alakít át mechanikai munkává. Klasszikus esete a gőzgép (Watts gőzgépe az ipari forradalom kezdetét jelenti), majd a belső égésű motor, gőzturbina, gázturbina. • A gőzgépben munkát a magas hőmérsékleten kiterjedő gáz végzi egy dugattyúban, ciklusosan. • A hőerőgép elvi jelentőségű modellje a Carnot-ciklus. A gőzgép gyakorlata és elmélete, illetve a termodinamika kölcsönösen segítették egymás fejlődését. • Ebben az elrendezésben a tüzelőanyag (szén, olaj, gáz, fa, benzin stb. ) hőjéből munkát nyerünk. 46

VII. HŐERŐGÉPEK, HŰTŐGÉPEK ÉS HŐSZIVATTYÚK MŰKÖDÉSÉNEK LÉNYEGE • Hűtőgép: munka befektetésével hőt von ki a rendszerből (a hűtőtérből) és ad le magasabb hőmérsékletű helyen (a helyiségben), s ezzel hűti a rendszert (a hűtőteret). • Itt (elektromos) munka befektetése révén a kívánt helyen (a hűtőszekrény belsejében) hűtünk (és pl. a szobában egy kicsit fűtünk, de ez nem jelentős). • A teljesítménytényező számítása: 47

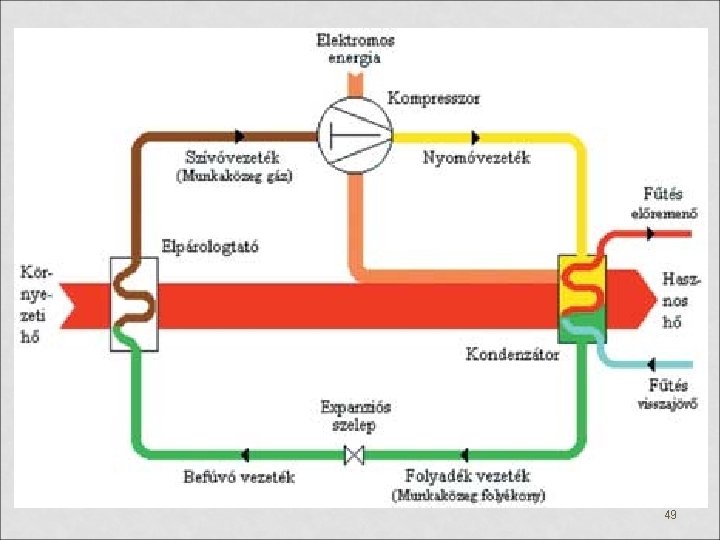
VII. HŐERŐGÉPEK, HŰTŐGÉPEK ÉS HŐSZIVATTYÚK MŰKÖDÉSÉNEK LÉNYEGE • Hőszivattyú: munka befektetésével hőt von ki egy nagy hőtartályból (pl. talaj, tó, levegő) és visz át egy másik helyre (lakás), amelyet ezzel fűt. • Itt (elektromos) munka befektetése révén fűtünk a kívánt helyen. • Az „ellenoldali” hűtés a nagy hőtartályban, (pl. a tóban, talajban) csak jelentéktelen hőmérséklet-csökkenést okoz. • A hőszivattyú jelentős beruházás, de középtávon jól megtérül. • A hűtőgép és a hőszivattyú is fordított Carnot-ciklus. 48

49