I zakon termodinamike CP m CV m R



















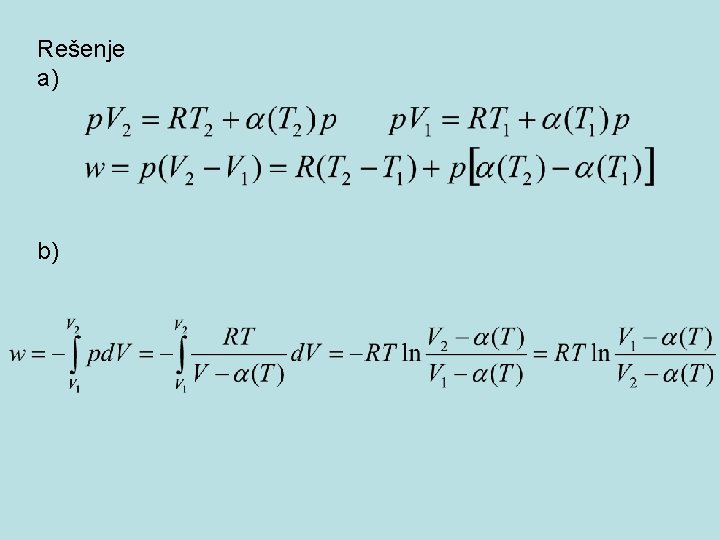













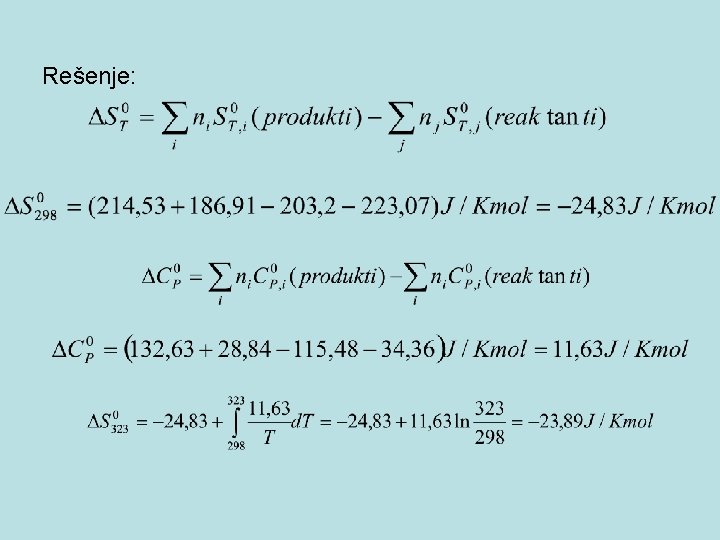















- Slides: 56

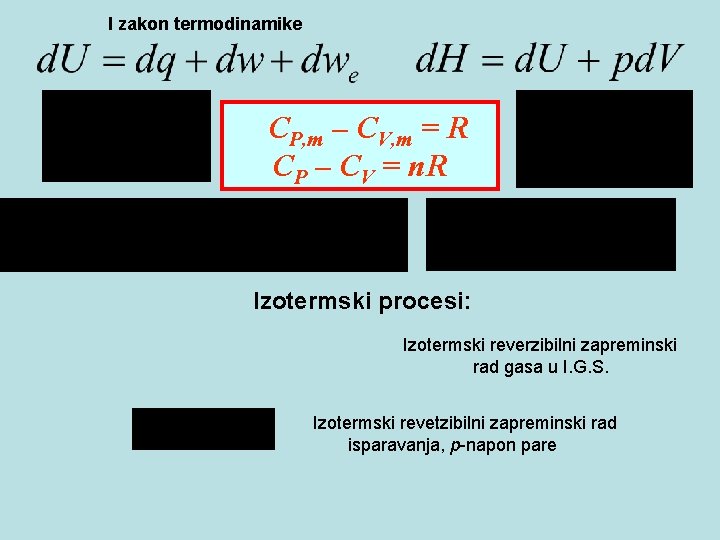
I zakon termodinamike CP, m – CV, m = R CP – CV = n. R Izotermski procesi: Izotermski reverzibilni zapreminski rad gasa u I. G. S. Izotermski revetzibilni zapreminski rad isparavanja, p-napon pare

Adijabatski procesi: Adijabatski zapreminski rad Jednačina adijabate

ZADATAK 1. Jedan mol gasa prelazi iz stanja sa pritiskom P 0 i zapreminom V 0 u stanje sa duplo većom zapreminom i pritiskom. Na p-V dijagramu taj proces je predstavljen pravom linijom. Koliki rad izvrši gas u tom procesu? a)Po. V 0 b) Po. V 0/2 c) 3 Po. V 0/2 d) 2 Po. V 0 e) 3 Po. V 0 f) ne znam P Rešenje: 2 2 Po Po 1 Vo 2 Vo V

ZADATAK 2. 7. U termodinamičkom procesu promena unutrašnje energije sistema je ∆U = -300 J, sistem prima toplotu od 100 J i širi se nasuprot pritiska od 1 bar. Kolika je promena zapremine (L)? a) 2 b) 3 c) 4 d) 5 e) 1 f) ne znam Rešenje:

Zadatak 3. • Električni grejač snage 15 W greje masu od 12 g vode tokom jednog minuta. Ako je početna temperatura vode 35 o. C, kolika će biti krajnja temperatura vode? Specifični toplotni kapacitet vode je 1 cal/g • Rešenje: Snaga grejača je: P=ΔU/t. Energija koju grejač oslobađa je: ΔU=P t=15 J/s 60 s=900 J

Zadatak 4. • 1 mol vode isparava. Kolika je promena entalpije ako je pritisak 1 bar? Promena unutrašnje energije pri isparavanju je 40. 7 k. J/mol. Rešenje:

Zadatak 5. Domaći • Koliko energije treba dovesti masi od 1, 35 kg vode da bi se zagrejala od 20 o. C do • temperature ključanja. Pretpostaviti da je Cvs=4, 18 J/g. K?

ZADATAK 6. : Izračunati U za reakciju sagorevanja 1, 0 mola propana na 25 o. C, ako je H=-2058 k. J. Rešenje: C 3 H 8(t)+5 O 2(g) 3 CO 2(g)+4 H 2 O(t) ng=3 -5=-2 U= H- ng. RT=-2058000 J+2 8, 3145 298=-2053 k. J

ZADATAK 7. Izračunati rad širenja pri elektrolizi 50 g vode pri konstantnom pritisku i temperaturi od 25 o. C. Rešenje: 2 H 2 O(t) 2 H 2(g)+O 2(g) w=-Psp V=-Psp(Vk-Vp) -Psp. Vk=

ZADATAK 8. Rad reverzibilnog izotermskog širenja jednog mola gasa u idealnom gasnom stanju od zapremine V 1 do zapremine V 2 je dat izrazom: a) –p(V 2 -V 1) b) –p(V 1 -V 2) c) d) CV(T 2 -T 1) f) ne znam e)

Zadatak 9. • Izračunati napon pare vode na 35 o. C ako se vodena para širi reverzibilno i izotermski od zapremine 5 cm 3 do zapremine 100 cm 3 ako se pri tome vrši rad od 534 m. J. Rešenje: w=-p(V 2 -V 1) w=-0, 534 J p=0, 534 Nm/95 10 -6 m 3=5621 Pa

Zadatak 10. Dva mola idealnog gasa podleže izotermalnoj reverzibilnoj ekspanziji od početne zapremine V 1 do krajnje zapremine 10 V 1 i vrši rad od 41860 J. Ako je početni pritisak 100 bar kolika je početna zapremina (u L) i temperatura (u K)? Rešenje w=n. RTln. V 2/V 1=n. RT· 2, 3 P 1 V 1=n. RT=w/2, 3=41860/2, 3=18200 J V 1=18200/100· 105=1, 82· 10 -3 m 3=1, 82 L n. RT=18200 J, T= 18200/2· 8, 314=1093 K

ZADATAK 11. Rad reverzibilnog adijabatskog širenja jednog mola gasa u idealnom gasnom stanju od zapremine V 1 pri temperaturi T 1 do zapremine V 2 pri temperaturi T 2, je dat izrazom: a) –p(V 2 -V 1) b) –p(V 1 -V 2) c) d) CV(T 1 -T 2) f) e)

ZADATAK 12. Jedan mol idealnog gasa na 300 K se širi adijabatski i reverzibilno od 20 bar do 1 bar. Koja je temperatura u krajnjem stanju gasa pretpostavljajući da je CV=(3/2) R? a) 105, 5 b) 90, 5 c) 205, 6 d)99, 6 Rešenje: e) 111, 0 f) ne znam

ZADATAK 13. : Izračunati krajnji pritisak argona (bar) posle reverzibilnog i adijabatskog širenja pri kome se zapremina poveća dva puta. Početni pritisak je iznosio 100 k. Pa a γAr=5/3. Rešenje: Iz jednačine adijabate se dobija:

ZADATAK 14. Izračunati rad i promenu unutrašnje energije pri adijabatskom širenju 0, 2 mol Ar od 0, 5 do 1, 0 L. Početna temperatura je izosila 25 o. C, a molarni toplotni kapacitet Ar na konstantnoj zapremini iznosi 12, 48 JK-1 mol-1. Rešenje:

ZADATAK 15: Domaći! Dva mola idealnog gasa za koji je Cv, m=5 R/2 je reverzibilno zagrevan do 356 K na konstantnoj zapremini. Početni pritisak i temperatura su bili P 1=111 k. Pa i T 1=277 K. Izračunati krajnji pritisak, U, q i w. Rešenje:

Zadatak 16. Jedan mol idealnog monoatomskog gasa u početku na 10 atm pritisku i temperaturi od 0 o. C širi se izotermski nasuprot pritiska od 1 atm. Uslovi su takvi da je konačna zapremina 10 puta veća od početne, krajnji pritisak je jednak spoljašnjem pritisku. (a) Izračunati početnu i krajnju zapreminu (b) Izračunati q, w, Uza proces. Kako je V 1=2, 24 L to je V 2=22, 4 L Ukupni proces je izotermski pa je U=0. Izvršeni rad je -P V=-1, 013·105 N/m 2 x(0, 0224 -0, 00224)m 3= w=-2042, 2 J, q=2042, 2 J

ZADATAK 17. Na vrlo niskoj temperaturi toplotni kapacitet čvrstih supstancija se može uzeti da je proporcionalan sa T 3, pa se može pisati da je C=a. T 3. Kolika je promena entalpije takve supstancije pri zagrevanju od 0 do temperature T (koja je bliska 0)? Rešenje:

Zadatak 18. • Gas se pokorava jednačini stanja: a) Odrediti reverzibilni rad koji se vrši pri zagrevanju gasa od T 1 do T 2 pri konstantnom pritisku. b) Odrediti reverzibilni izotermski rad pri širenju od V 1 do V 2.
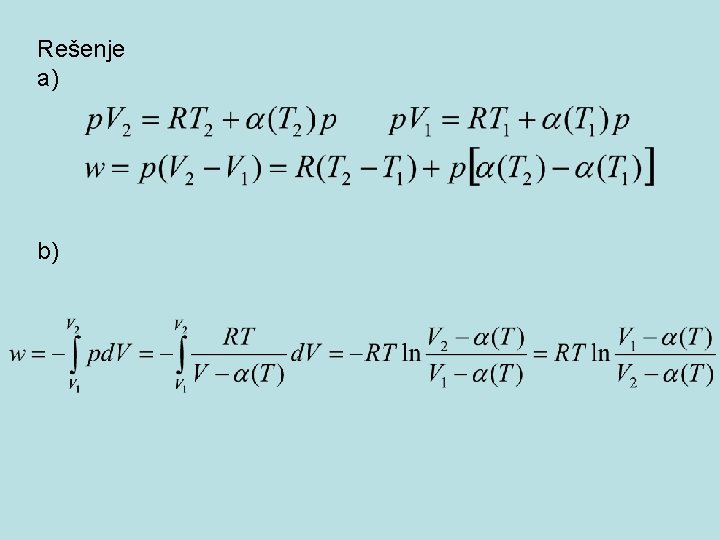
Rešenje a) b)

Zadatak 19. Jedan mol idealnog monoatomskog gasa na početnim P 1=2 atm i T 1=273 K je preveden na pritisak P 2=4 atm reverzibilnim putem definisanim sa P/V=const. Izračunati V 1, V 2 i T 2, U, H, q i w. Rešenje: Iz jedn. id. g. stanja je V 1=11, 2 L. Pošto je P/V=const. to je V 2=22, 4 L. Kombinovanjem P/V=const. sa PV=RT dobija se T/V 2=const. pa je T 2=4 T 1=1092 K U=CV T=(3 R/2)819=10, 21 k. J, H=CP T=17, 022 k. J. Da bi se dobilo w treba odrediti w=∫Pd. V. Iz početnih uslova, P/V=const=2/11, 2=0, 178 atm/L pa je w=0, 178∫Vd. V=0, 089(V 22 -V 12) =0, 089∙ 375=33, 3 Latm ili w=823 cal, q= U+w=3230 cal.

Zadatak 20 Jedan mol idealnog gasa sa CV=20, 93 J/mol step. u početku pri standardnim uslovima prolazi kroz sledeći reverzibilni ciklus: A: izohorsko zagrevanje do dvostruke vrednosti početne temperature od stanja 1 do 2, B: adijabatsko širenje od 2 do 3 do početne temperature C: izotermalnu kompresiju od 3 do 1. Izračunati q, w, ΔU i ΔH za korake A, B i C i za ciklus. Rešenje Korak A: V=const. T=273, 15 K, P=1 bar, w=0, ΔU=qv =CV ΔT= 20, 93·(2 T 1 -T 1)=20, 93· 273, 15=5717 J ii) Korak B: q=0, ΔU=w=CV ΔT=20, 93(T 1 -2 T 1)=-5717 J/mol, ΔH=-7988 J/mol, iii) Korak C: ΔU=0, T 2/T 3=2, V 3/V 2=(T 2/T 3)CV/R , V 2=V 1 w=RT 1 ln. V 3/V 1=RT 1 ln(T 2/T 3) CV/R=CVT 1 2, 303 log 2= 20, 93· 273, 15· 2, 303·log 2=3963, 46 J/mol, q=-3963, 46 J/mol

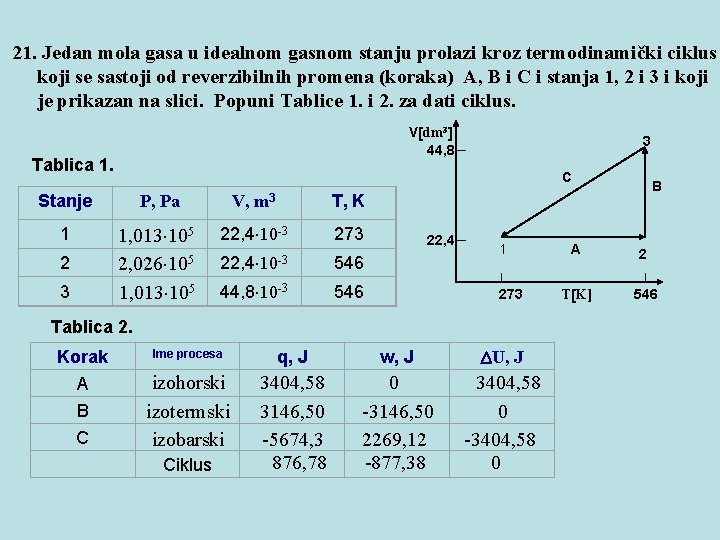
21. Jedan mola gasa u idealnom gasnom stanju prolazi kroz termodinamički ciklus koji se sastoji od reverzibilnih promena (koraka) A, B i C i stanja 1, 2 i 3 i koji je prikazan na slici. Popuni Tablice 1. i 2. za dati ciklus. V dm 3 Tablica 1. C Stanje P, Pa V, m 3 1 5 1, 013 10 5 2, 026 10 5 1, 013 10 22, 4 10 -3 273 22, 4 10 -3 546 44, 8 10 -3 546 2 3 3 44, 8 T, K 22, 4 1 273 Tablica 2. Korak Ime procesa q, J w, J U, J A izohorski izotermski izobarski 3404, 58 3146, 50 -5674, 3 876, 78 0 -3146, 50 2269, 12 -877, 38 3404, 58 0 -3404, 58 0 B C Ciklus B A 2 T K] 546

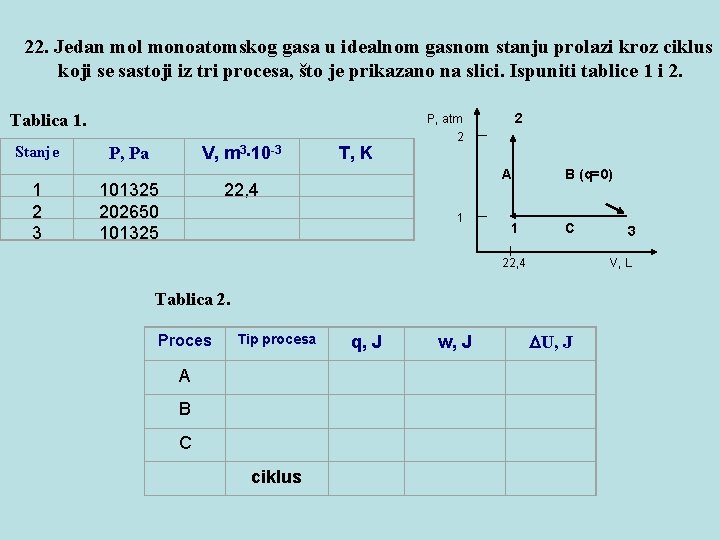
22. Jedan mol monoatomskog gasa u idealnom gasnom stanju prolazi kroz ciklus koji se sastoji iz tri procesa, što je prikazano na slici. Ispuniti tablice 1 i 2. Tablica 1. Stanje 1 2 3 2 P, atm P, Pa V, m 3 10 -3 T, K 22, 4 101325 202650 101325 2 A 1 B (q=0) 1 C 22, 4 3 V, L Tablica 2. Proces Tip procesa q, J w, J U, J A B C ciklus

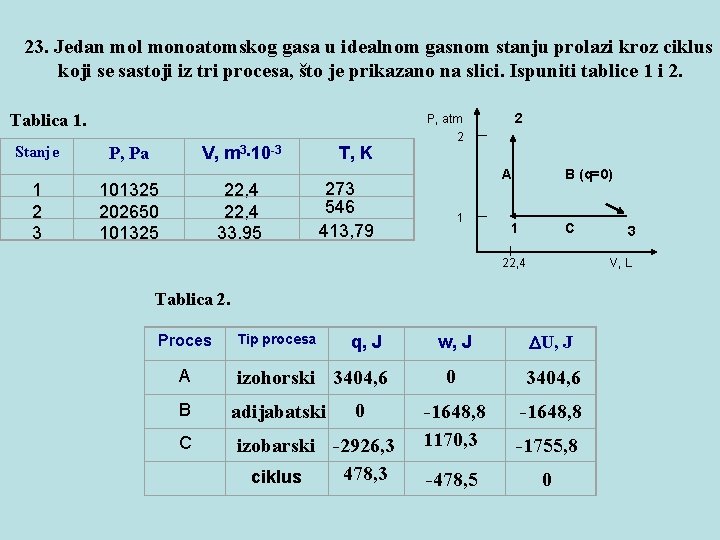
23. Jedan mol monoatomskog gasa u idealnom gasnom stanju prolazi kroz ciklus koji se sastoji iz tri procesa, što je prikazano na slici. Ispuniti tablice 1 i 2. Tablica 1. Stanje 1 2 3 V, m 3 10 -3 P, Pa 101325 202650 101325 22, 4 33, 95 2 T, K A 273 546 413, 79 1 B (q=0) 1 C 22, 4 Proces B C Tip procesa q, J izohorski 3404, 6 adijabatski 0 izobarski -2926, 3 478, 3 ciklus w, J 3 V, L Tablica 2. A 2 P, atm U, J 0 3404, 6 -1648, 8 1170, 3 -1648, 8 -1755, 8 -478, 5 0

24. Domaći: Jedan mola gasa u idealnom gasnom stanju prolazi kroz termodinamički ciklus koji se sastoji od : a) izotermske kompresije od 2 atm i 10 L do 20 atm i 1 L, b) izobarske ekspanzije kojom se gas vraća do zapremine od 10 L a temperatura menja od T 1 do T 2, c) izohorskog hlađenja do početnog stanja. Nacrtati grafik i popuniti tablicu vrednostima q, w i U za procese i ciklus.

25. Benzen (C 6 H 6) gori u vazduhu gradeći ugljendioksid i tečnu vodu. Koliko toplote po molu benzena se oslobodi pri sagorevanju? Standardna entalpija formiranja benzena je 49. 04 k. J/mol, CO 2(g) je -393, 5 k. J/mol i tečne vode je 285, 8 k. J/mol. 2 C 6 H 6 (l) + 15 O 2 (g) 12 CO 2 (g) + 6 H 2 O (l) H 0 rxn = S n H 0 f (produkti) - S m Hf 0 (reaktanti) H 0 rxn = [ 12 H 0 f (CO 2) + 6 H 0 f (H 2 O)] - [ 2 H 0 f (C 6 H 6)] H 0 rxn = [ 12 x(– 393. 5) + 6 x(– 285. 8) ] – [ 2 x 49. 04 ] = -6534. 88 k. J -6535 k. J = - 3267 k. J/mol C 6 H 6 2 mol

26. Izračunati standardnu entalpiju formiranja CS 2 (t): C(grafit) + O 2 (g) CO 2 (g) H 0 = -393. 5 k. J rxn 0 = -296. 1 k. J S(rombični) + O 2 (g) SO 2 (g) Hrxn 0 = -1072 k. J CS 2(t) + 3 O 2 (g) CO 2 (g) + 2 SO 2 (g) Hrxn 1. Napisaćemo entalpiju reakcije nastajanja CS 2 C(grafit) + 2 S(rombični) CS 2 (t) 2. Kombinovati date reakcije tako da se dobije željena reakcija: C(grafit) + O 2 (g) CO 2 (g) H 0 rxn = -393. 5 k. J 2 S(rombični) + 2 O 2 (g) 2 SO 2 (g) H 0 rxn = -296. 1 x 2 k. J + CO 2(g) + 2 SO 2 (g) CS 2 (t) + 3 O 2 (g) H 0 = +1072 k. J rxn C(grafit) + 2 S(rombični) CS 2 (t) H 0 rxn = -393. 5 + (2 x-296. 1) + 1072 = 86. 3 k. J

Zadatak 27. Zadatak: Izračunati standardnu entalpiju formiranja Δf. H za CH 4. Entalpija sagorevanja H 2, C(grafit) i CH 4 su - 285. 8, - 393. 5, i - 890. 4 k. J/mol respektivno. Rešenje: C (graphite) + 2 H 2 CH 4 Hf° = __? ____ 2 H 2(g) + O 2(g) 2 H 2 O(t) H = - 571. 6 k. J C(grafit) + O 2(g) CO 2(g) H = - 393. 5 k. J CO 2(g) + 2 H 2 O(t) CH 4(g) + 2 O 2(g) H= 890. 4 k. J (1) + (2) + (3) C (grafit) + 2 H 2 CH 4 Hf° = - 74. 7 k. J Nacrtati dijagram energetskih nivoa iz ovih podataka

Efikasnost toplotne mašine II zakon termodinamike. Reverzibilni i ireverzibilni Ireverzibilni Fazni prelazi

Maksvelove relacije

Entropija mešanja Termodinamičke jednačine stanja k-Bolcmanova konstanta, k=R/NA=1, 38· 10 -23 J/K

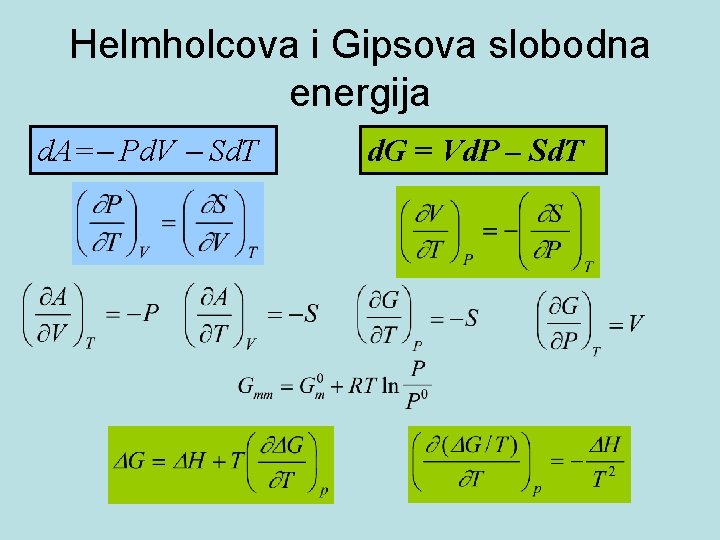
Helmholcova i Gipsova slobodna energija d. A= Pd. V Sd. T d. G = Vd. P – Sd. T

Zadatak 28. Stepen korisnog dejstva mašine koja hladnjaku preda jednu trećinu količine toplote uzete od grejača je: a) 0, 25 b) 0, 35 c) 0, 67 d) 0, 5 e) ne znam Zadatak 25. Izračunati entropiju topljenja (S) u J/mol K za KCl čija je tačka topljenja 7700 C. Promena entalpije topljenja 26, 8 k. J/mol. a) 34, 8 b) 0, 035 c)25, 7 d) 0, 026 e)487, 9 f) ne znam

Zadatak 29 Za sledeću reakciju na 250 C: Cu. O(č)+H 2(g) Cu(č)+H 2 O(g) vrednosti standardnih entropija su: S 0 Cu. Oč=42, 63 J/Kmol, S 0 H 2 g=130, 68 J/Kmol, S 0 Cuč=33, 15 J/Kmol i S 0 H 2 Og=188, 83 J/Kmol. Odrediti da li će se reakcija odigravati spontano sa aspekta sistema. Rešenje: Standardna promena entropije u reakciji je: Za gornju reakciju promena standardne entropije je: Pošto je promena entropije za sistem pozitivna to je reakcija spontana sa aspekta sistema.

30. Grafit i dijamant su dve alotropske modifikacije ugljenika. Izračunati ∆Ssis, ∆Sok i ∆Stot za hemijsku reakciju u kojoj grafit i gasoviti vodonik grade metan: C(graf. )+2 H 2(g) CH 4(g) ∆Ho 298, m=-74, 81 k. J/mol 5, 74 130, 684 186, 26 Somf (J/Kmol) Rešenje: ∆Ssis=186, 26 -2 x 130, 684 -5, 74=-80, 848 J/Kmol ∆Sok=74810/298=251 J/Kmol ∆Stot=-80, 848+251=170, 15 J/Kmol

Zadatak 31. Koja od sledećih reakcija je praćena najpozitivnijom promenom entropije? a) 2 CO(g) + O 2(g)→ 2 CO 2(g) b) N 2(g) + O 2(g) → 2 NO(g) c) 2 CH 4(g) + O 2(g) → 2 CH 3 OH(t) d) 2 H 2 O 2(t) + N 2 H 4(t) → N 2(g) + 4 H 2 O(g) e) C(č, grafit) + H 2 O(g) → CO(g) + H 2(g)

Zadatak 32: Za reakciju : CHCl 3(t)+Cl 2(g) CCl 4(t)+HCl(g) na 250 C standardne entropije su: S 0298(CHCl 3(t))=203, 02 J/Kmol S 0298(Cl 2(g))=223, 07 J/Kmol S 0298(CCl 4(t))=214, 53 J/Kmol S 0298(HCl(g))=186, 91 J/Kmol a toplotni kapaciteti su: C 0 p(CHCl 3(t))=115, 48 J/Kmol C 0 p(Cl 2(g))=34, 36 J/Kmol C 0 p(CCl 4(t))=132, 63 J/Kmol C 0 p(HCl(g))=28, 84 J/Kmol Odrediti standardnu promenu entropije reakcije na 50 o. C.
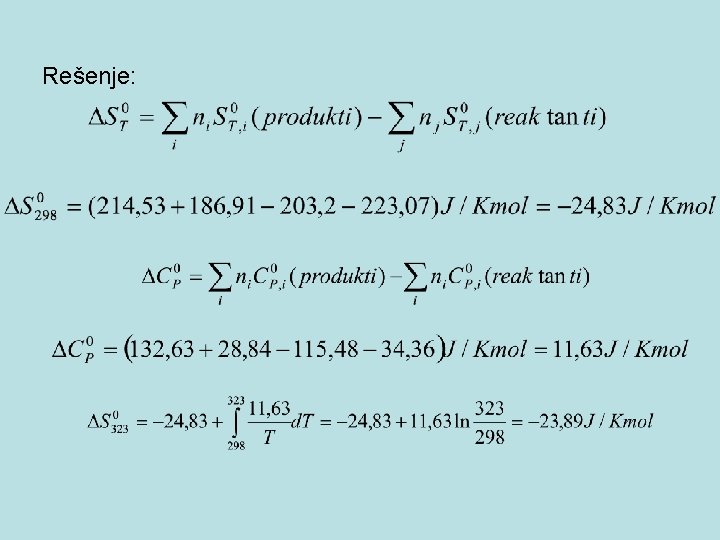
Rešenje:

Zadatak 33: Koliki je porast entropije kada zagrevamo 1 mol hloroforma, CHCl 3 od 240 do 330 K, ako je Cp=(91, 47+7, 5 10 -2 T) J/mol. K ? Rešenje:

Zadatak 34. Izračunati promenu entropije kada se idealan gas čiji je CV, m=5 R/2 komprimuje do jedne trećine svoje početne zapremine i istovremeno zagreje do tri puta veće temperature od početne. Rešenje:

Zadatak 35: U sistemu se odigrava proces u kome se entropija menja za 5, 51 J/K. Za vreme procesa 1, 5 k. J toplote dodato je sistemu na 350 K. Da li je proces termodinamićki reverzibilan? Rešenje: Proces nije termodinamički reverzibilan-ireverzibilan je

Zadatak 36: Uzorak bakra (M=63, 546 g/mol), mase 2, 75 kg i toplotnog kapaciteta 24, 44 J/Kmol, se hladi na konstantnom pritisku od 330 K do 275 K. Izračunati a) energiju koja se mora razmeniti u vidu toplote i b) promenu entropije sistema. Rešenje: a) b)

Zadatak 37: Uzorak azota mase 35 g na 230 K i 21, 1 atm širi se izotermalno do pritiska od 4, 3 atm. Izračunati promenu entropije gasa. Rešenje:

Zadatak 38: Uzorak idealnog gasa u početku na 270 K, 1, 20 atm i 11, 0 L komprimuje se izotermalno. Do koje zapremine treba da se komprimuje da bi se entropija smanjila za 3, 0 J/K Rešenje:

Zadatak 39: Jedan mol čvrstog bakra se širi izotermski od 200 bar do 1 bar. Izračunati promenu entropije sistema za proces u kome je , a gustina =8, 96 103 kgm-3. Rešenje:

Zadatak 40: Jedan mol CO 2(g) na 273 K se hladi do CO 2(t) na 194, 4 K. Hlađenje se vrši reverzibilno i ireverzibilno stavljanjem uzorka u tečni vodonik na 13, 96 K. Izračunati promenu entropije za proces ako je standardna entalpija isparavanja 23, 1752 k. Jmol-1 na 194, 4 K i ako je Cp=32, 22+(22, 18 10 -3)T+(-23, 47 10 -6)T 2. Rešenje: Može se razmatrati proces u dva koraka. Prvi je hlađenje gasa na konstantnom pritisku do tačke ključanja i drugi prevođenje u tečno stanje. Za reverzibilni proces je promena entropije sistema:

Reverzibilan proces: Stoga je ukupna promena entropije za reverzibilan proces:

Ako se promena vrši na irevrzibilan način toplota preneta u okolini je:

Zadatak 41. Promena Gipsove energije za neki izobarski proces može da se prikaže izrazom: Izračuneti promenu entropije i entalpije za taj proces. Rešenje Poznato je da je:

Zadatak 42. Kada se dva mola gasa na 330 K i 3, 5 atm izotermski komprimuje, entropija opadne za 25, 0 J/K. Izračunati krajnji pritisak gasa i promenu Gipsove energije za kompresiju. Rešenje:

Zadatak 43. Kada pritisak 35 g uzorka tečnosti raste izotermalno od 1 atm do 3000 atm, Gibsova energija raste za 12 k. J. Izračunati gustinu tečnosti (u g/cm 3).

Zadatak 44. Jedan mola idealnog monoatomskog gasa se prevodi iz početnog stanja (22, 4 L, 273 K, 1 atm, S=20 cal/K) u krajnje stanje ( 12, 4 L, 2 atm, 303 K). Izračunati U, H, S i G za ovu termodinamičku promenu.

Rešenje: • Označićemo stanja gasa: • Početno: Krajnje: V=22, 4 L=22, 4∙ 10 -3 m 3 V=12, 4 L=12, 4∙ 10 -3 m T=273 K T=303 K P= 1 atm=1, 013∙ 105 Pa P=2 atm=2, 026∙ 105 Pa S= 20 cal/Kmol=83, 72 J/Kmol Pošto je gas u idealnom gasnom stanju to je: U=Cv T=(3 R/2)x 30=374, 13 J H=Cp T=(5 R/2)x 30=623, 55 J

• Promena entropije Gipsove funkcije će se odrediti razmatrajući promenu kroz dva stupnja: • 1. 0, 0224 m 3 , 273 K, 1, 013∙ 105 Pa 0, 02486 m 3, 303 K, 1, 013∙ 105 Pa S 1=Cpln. T 2/T 1=(5 R/2)ln 1, 11=2, 167 J/K (Skrajnje=2, 169 J/K) G 1= H 1 -(T 2 S 2 -T 1 S 1)=623, 55 -(303 x 85, 887 -273 x 83, 72)= -2544, 651 J • 2. 0, 02486 m 3, 303 K, 1, 013∙ 105 Pa 0, 0124 m 3, 303 K; 2, 026∙ 105 Pa S 2=Rln. P 1/P 2=8, 314 x 2, 3 log 0, 5=-5, 763 J/K G 2=RTln. P 2/P 1=1746, 14 J Ukupne promene su: S=2, 167 -5, 763=-3, 596 J/K; G=-2544, 651+1746, 14=-798, 511 J