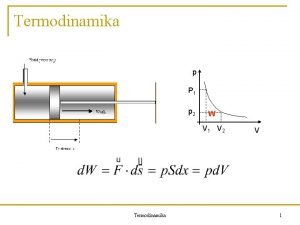
Mszaki htan Termodinamika s hkzls Energiatermels szakirny tovbbkpzs

Műszaki hőtan (Termodinamika és hőközlés) Energiatermelés szakirányú továbbképzés

Célkitűzések, alapfogalmak, módszerek BEVEZETÉS

Mérnöki tevékenység Tervezés és üzemeltetés Biztonság Gazdaságosság Megbízhatóság Funkció Ergonómia Termék, folyamat Környezetvédelem
Célkitűzések Termodinamik a Hőtan Hőközlés
Kapcsolódások Fizika Matematika Kémia Termodinamik a
Kapcsolódások Matematika Áramlástan Hőközlé s

Termodinamika • Elnevezés eredete: – θερμη (therme) + δυναμις (dinamisz) = hő+erő – Valójában: termosztatika – Az „igazi” termodinamika: nemegyensúlyi termodinamika • Vizsgálati terület: energiaátalakulások • Módszer: – modellek (rendszer, közeg, folyamat) – axiómák (főtételek)

A termodinamika területei NEM EGYENSÚLYI FOLYAMATOK REVERZIBILIS KEVERÉKEK KÖZEGEK IDEÁLIS GÁZ TISZTA ANYAGOK KVÁZISTATIKUS MÁSODIK FŐTÉTEL ELVEK EGYENSÚLY MEGMARADÁSI TÉTELEK
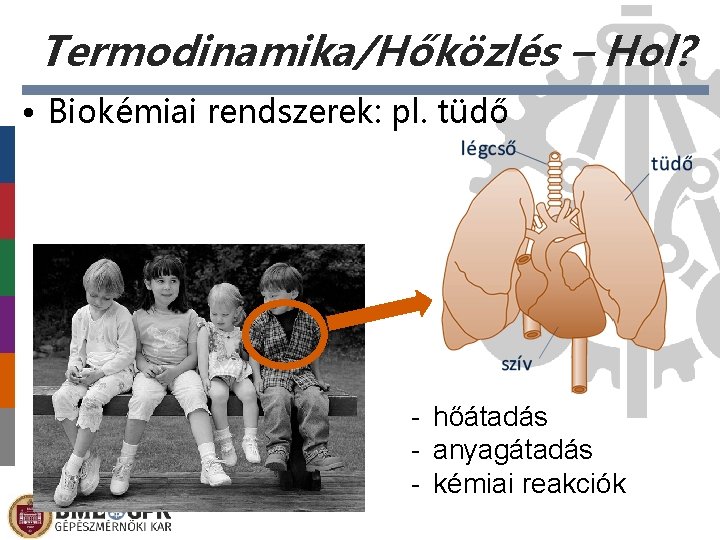
Termodinamika/Hőközlés – Hol? • Biokémiai rendszerek: pl. tüdő - hőátadás - anyagátadás - kémiai reakciók
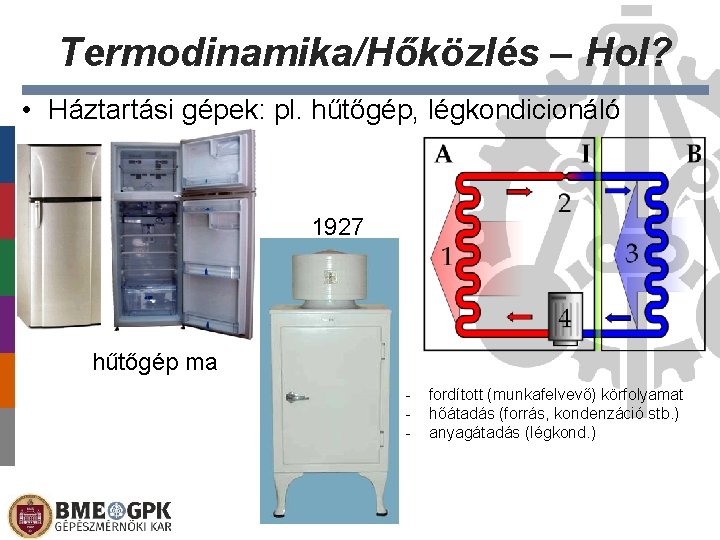
Termodinamika/Hőközlés – Hol? • Háztartási gépek: pl. hűtőgép, légkondicionáló 1927 hűtőgép ma - fordított (munkafelvevő) körfolyamat hőátadás (forrás, kondenzáció stb. ) anyagátadás (légkond. )
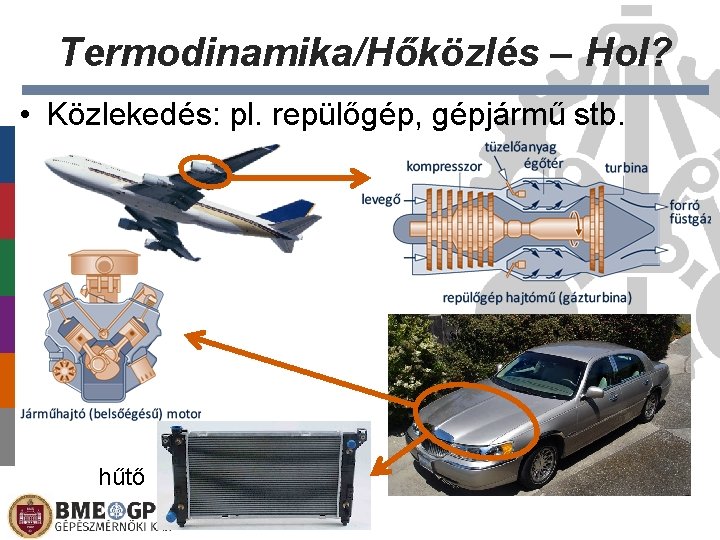
Termodinamika/Hőközlés – Hol? • Közlekedés: pl. repülőgép, gépjármű stb. hűtő
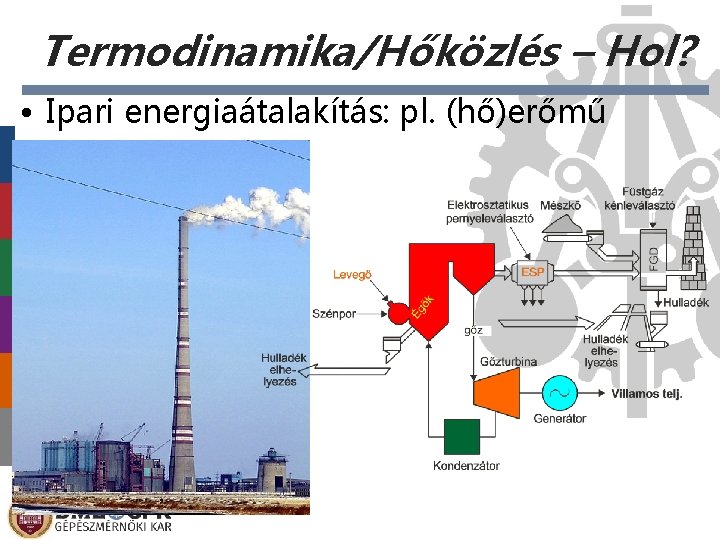
Termodinamika/Hőközlés – Hol? • Ipari energiaátalakítás: pl. (hő)erőmű

Termodinamika/Hőközlés – Hol? • Elektronikai eszközök: pl. számítógép hagyományos hőcsöves

TERMODINAMIKA Előláb-szöveg

Alapfogalmak, rendszer-, folyamat - és közegmodellek TERMODINAMIK A

Fogalmak A termodinamika nyelvezete • görög és latin eredetű kifejezések – izotermikus = állandó hőmérsékletű – adiatermikus = hőszigetelt • mennyiségek rövidítése (jelölése) angol elnevezés alapján; minden SI szerint – – – p (pressure): nyomás V (volume): térfogat T, t (temperature): hőmérséklet τ (time): idő W (work): munka E (energy): energia
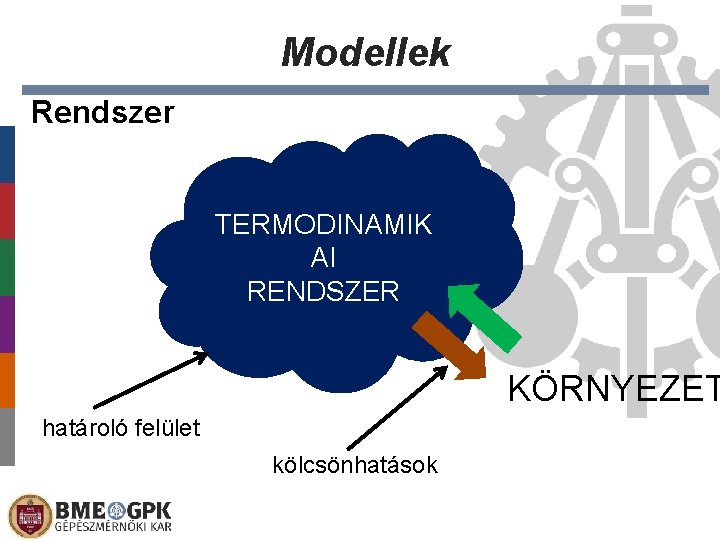
Modellek Rendszer TERMODINAMIK AI RENDSZER KÖRNYEZET határoló felület kölcsönhatások

Kölcsönhatások • Jelleg – anyagi jellegű – energia jellegű • Típusok – határoló felület függvénye – – – merev/deformálódó: mechanikai diatermikus/adiatermikus: termikus áteresztő/féligáteresztő/nem áteresztő: kémiai szigetelő/vezető: villamos árnyékoló/nem árnyékoló: mező jellegű kivétel: gravitációs
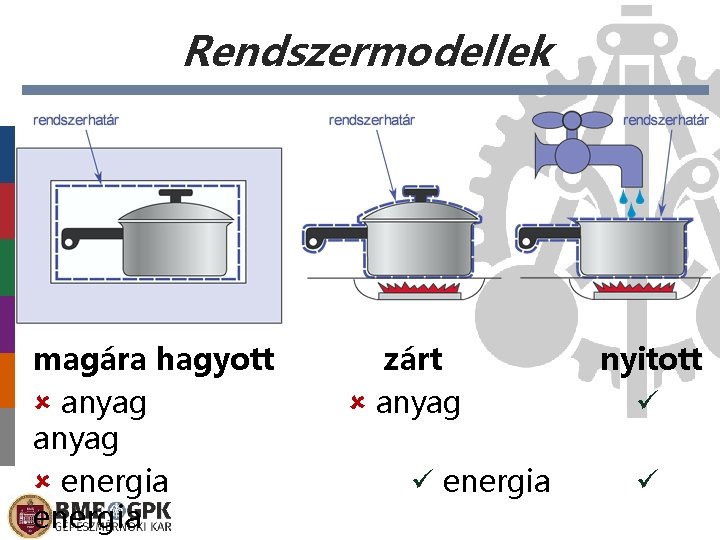
Rendszermodellek magára hagyott anyag energia zárt anyag energia nyitott

Modellezés filozófiája • Ockham (Occam) borotvája – lex parsimoniae = takarékosság (tömörség) elve – „Pluralitas non est ponenda sine necessitate” – A sokaság szükségtelenül nem tételezendő – általában az egyszerűbb megoldás a helyes William Ockham (kb. 1285– 1348) angol nemzetiségű ferences rendi szerzetes

Modellezés filozófiája • Neumann János a modellekről: „… a tudomány nem magyarázni próbál, alig próbál interpretálni – a tudomány főként modelleket állít fel. A modellen olyan matematikai konstrukciót értünk, amely – bizonyos szóbeli értelmezést hozzáadva – leírja a megfigyelt jelenségeket. Az ilyen matematikai konstrukciókat kizárólag és pontosan az igazolja, hogy működnek. ” Budapest, 1903. december 28. – Washington, 1957. február 8. , magyar származású matematikus
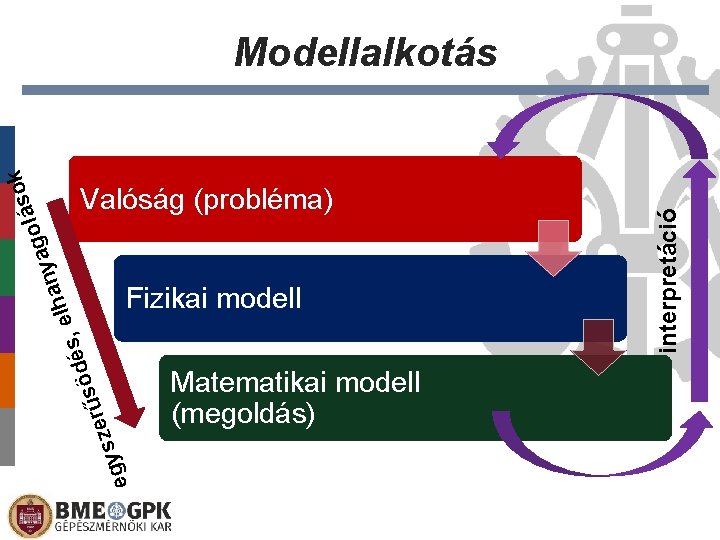
y n a h , el z s y eg er és d ö űs Fizikai modell Matematikai modell (megoldás) interpretáció Valóság (probléma) a k o s á gol Modellalkotás
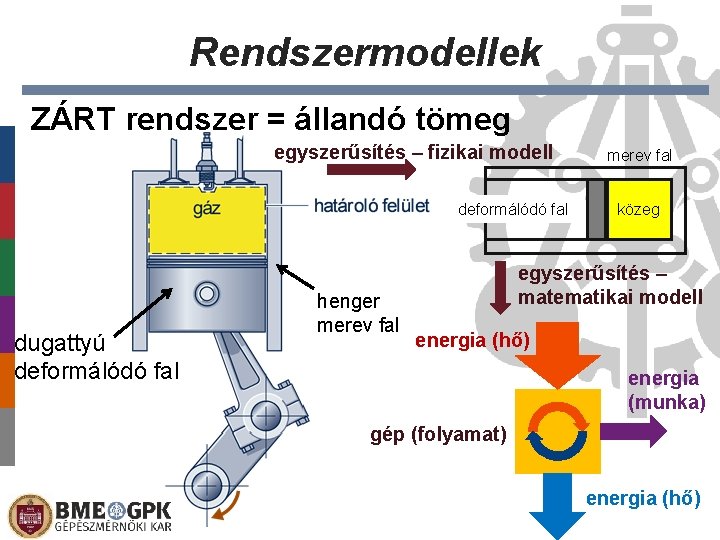
Rendszermodellek ZÁRT rendszer = állandó tömeg egyszerűsítés – fizikai modell deformálódó fal dugattyú deformálódó fal henger merev fal közeg egyszerűsítés – matematikai modell energia (hő) energia (munka) gép (folyamat) energia (hő)
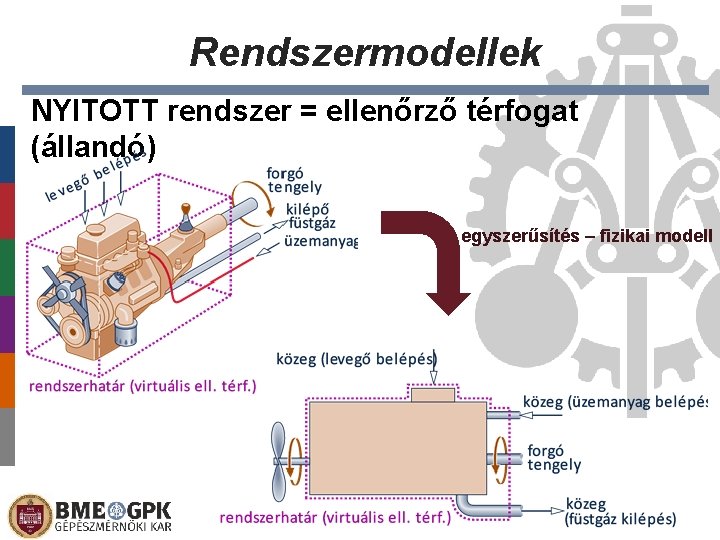
Rendszermodellek NYITOTT rendszer = ellenőrző térfogat (állandó) egyszerűsítés – fizikai modell
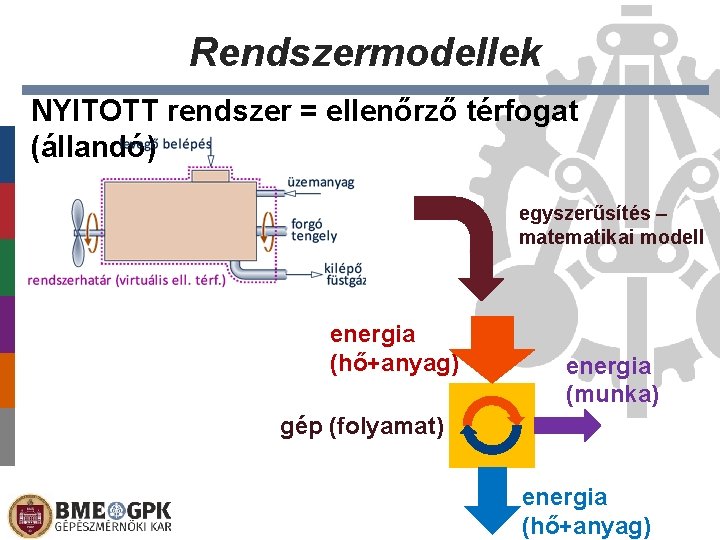
Rendszermodellek NYITOTT rendszer = ellenőrző térfogat (állandó) egyszerűsítés – matematikai modell energia (hő+anyag) energia (munka) gép (folyamat) energia (hő+anyag)

A rendszer leírása Leíró jellemzők • mikroszkopikus (belső felépítés, részecskék) statisztikus fizika [belső energia, entrópia] • makroszkopikus (megfigyelhető, mérhető) műszaki termodinamika [nyomás, hőmérséklet] Fogalmak • • • állapotjelző állapotváltozás egyensúly, egyensúlyi állapotváltozás, kvázistatikus állapotváltozás

A rendszer leírása • Állapotjelzők – extenzív – intenzív – fajlagos extenzív • Anyag- vagy fázisjellemzők

Közegmodellek • Az anyag viselkedését írják le • Fizikai modell matematikai modell – állapotjelzők közötti függvénykapcsolat – f (p, V, T, …)=0 • egyszerű modellek – tiszta anyagok – komponens, fázis, szabadságfok – Gibbs-fázisszabály • Ideális gáz – fizikai modell – matematikai modell: p. V-m. RT=0
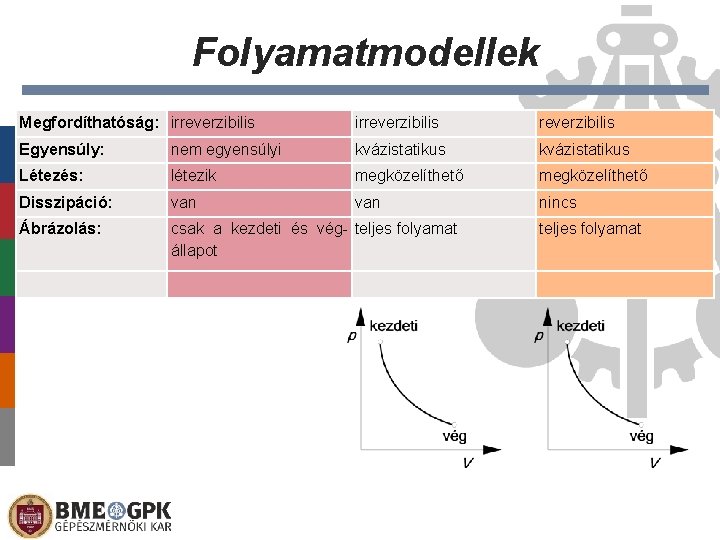
Folyamatmodellek Megfordíthatóság: irreverzibilis Egyensúly: nem egyensúlyi kvázistatikus Létezés: létezik megközelíthető Disszipáció: van nincs Ábrázolás: csak a kezdeti és vég- teljes folyamat állapot teljes folyamat

Folyamatmodellek Egyszerű állapotváltozások • egy állapothatározó rögzített – izobár = állandó nyomás – izochor = állandó térfogat – izotermikus = állandó hőmérséklet – izentalpikus = állandó entalpia • kölcsönhatások korlátozottak – adiabatikus: csak mechanikai engedett – izentrópikus: adiabatikus és reverzibilis

Főtételek és kapcsolódó fogalmak FŐTÉTELEK

Főtételek Közös jellemzők • Eredetük: megfigyelés, mérés, következetés • Matematikai úton nem bizonyíthatók • Egymásból nem levezethetők • Érvényességük térben és időben nem korlátlan

Főtételek A termodinamika főtételei: • 0. főtétel: egyensúly • I. főtétel: energiamegmaradás • II. főtétel: megfordíthatóság/átalakíthatóság • III. főtétel: elérhetetlenség

I. főtétel: az energia megmaradása A felfedezés útja 1. , az „angol út” JAMES PRESCOTT JOULE (1818 -1889) mérések munka-hő egyenérték „Abban a hitben, hogy a pusztítás ereje egyedül a Teremtő birtoka, teljességgel egyetértek Roget-val és Faraday-jel azon véleményüket illetően, hogy bármely elmélet, amely a gyakorlatba ültetve az erő megsemmisítését kívánja meg, szükségszerűen téves. ”

I. főtétel: az energia megmaradása 2. a „francia út” (racionális mérnöki iskola) a legjobb gép (hőerőgép) keresése NICOLAS CARNOT és fia NICOLAS LÉONARD SADI CARNOT (1796 -1832) a hő-munka átalakítást vizsgálták második főtétel GUSTAVE CORIOLIS munka fogalom, munka és mozgási energia kapcs.

I. főtétel: az energia megmaradása 3. , a „német út”, a „metafizikai út” élő szervezetek vizsgálata JULIUS ROBERT VON MAYER (18141878) (eredetileg orvos, az is maradt) HERMANN L. F. HELMHOLTZ (1821 -

I. főtétel: az energia megmaradása Robert Mayer: „ 1840 nyarán a Jáva szigetére újonnan megérkezett európaiakon végrehajtott érvágásoknál azt tapasztaltam, hogy a kar vénájából eresztett vérnek majdnem kivétel nélkül föltünően vörös színe volt. Ez a jelenség magára vonta teljes figyelmemet. Kiindulván a Lavoisier égés-elméletéből, mely az állati hőt égésfolyamatnak tulajdonítja, azt a kettős színváltozást, melyet a vér a kicsiny és a nagy körfutás hajszáledényeiben szenved, úgy tekintettem, mint a vérrel végbemenő oxidácziónak érzékileg észrevehető jelét, látható reflexusát. Az emberi test állandó mérsékletének megtartására kell, hogy annak hőfejlesztése a hő veszteségével, tehát a környező médium mérsékletével is szükségképen bizonyos értékviszonyban álljon s ennélfogva kell, hogy mind a hőtermelés és az oxidáczió- folyamat, mind pedig mind a két vérnemnek színkülönbsége a forró égöv alatt egészben véve kisebb legyen mint a hidegebb vidékeken. ”

I. főtétel: az energia megmaradása Robert Mayer, 1842: „Az erők okok, és így azokra teljes mértékben alkalmazható az alaptétel: causa aequat effectum. Ha a c ok okozata e, akkor c = e; ha e ismét az oka egy másik f okozatnak, akkor e = f stb. c = e = f. . . = c. Az okok és okozatok egy láncolatában, mint ahogy az egyenlet természetéből következik, sohasem válhat egy tag vagy egy tag egy része nullává. Minden ok első tulajdonsága tehát az elpusztíthatatlansága. Ha az adott c ok létrehozta a vele egyenlő e hatást, ezzel c egyúttal megszűnt létezni; c tehát e-vé vált. Ha e létrehozása után c egészen vagy részben még megmaradt volna, úgy ezen visszamaradó oknak további okozat kellene hogy megfeleljen; c okozata tehát e kellene hogy legyen ellentétben c = e feltevésünkkel. Így, minthogy c e-be, e f-be stb. megy át, ezeket a mennyiségeket egy és ugyanazon objektum különböző megjelenési formáinak kell tekintenünk. Az a képesség, hogy különböző formákat tud felvenni, a másik lényeges tulajdonsága minden oknak. A két tulajdonságot összefoglalva mondhatjuk: az okok kvantitatíve elpusztíthatatlanok és kvalitatíve változékony objektumok. ” Az erő (energia): elpusztíthatalan és változékony (átalakítható).

I. főtétel: az energia megmaradása • Energia fogalma (E, energy) – belső energia (ἐνέργεια=aktivitás), U – entalpia (ἔνθαλπος=hőtartalom), H • Munka fogalma (W, work) – transzportmennyiség, útfüggő – nem állapotjelző, hanem folyamatjellemző – rendszerfüggő: nyitott technikai, zárt fizikai • Hő fogalma (Q, caloricum) – transzportmennyiség, útfüggő – nem állapotjelző, hanem folyamatjellemző – termikus kölcsönhatás

I. főtétel: az energia megmaradása • Az I. főtétel zárt, nyugvó rendszerre: ΔU =Q +Wfiz • Az I. főtétel nyitott, nyugvó rendszerre: ΔH =Q +Wtech • Mozgó rendszer, teljes energia zárt: Etot=U +Ekin+Epot nyitott: Etot=H +Ekin+Epot

I. főtétel: az energia megmaradása • Fizikai és technikai munka figyeljük a táblát!

II. főtétel • Tapasztalati megfigyelés: a magától hő csak a melegebb helyről a hidegebb hely felé áramlik • N. S. CARNOT: hőáramlás és gőzgépek (idézet) • kiterjesztés: megfordíthatóság, reverzibilitás • jellemző mennyiség: entrópia (εντροπία=belső változás), S • következmény: munka és hő NEM

II. főtétel • Az entrópia definíciója: a termikus kölcsönhatás extenzív paramétere • Az entrópia forrásegyenlete:

II. főtétel Folyamatok az entrópiaváltozás tükrében Vizsgálandó: • transzportált entrópia: rendszer, környezet • produkált: rendszer ΔSössz= ΔSR+ΔSkörny Rendszer és környezet együttes entrópiaváltozása: • >0: valós, irreverzibilis folyamat • =0: reverzibilis (valóságban nem létező) folyamat

0. főtétel A termodinamikai egyensúly: – makroszkopikusan változatlan (nyugvó) rendszer – intenzív állapotjelzők homogén eloszlásúak Kölcsönható rendszerek egyensúlya – intenzív állapotjelzők azonossága és – falak átjárhatósága ARNOLD SOMMERFELD (1868– 1951) 1951: „A hőmérséklet egyenlősége feltétele két rendszer vagy egy rendszer két része közötti termikus egyensúlynak”
0. főtétel • Az egyensúly tulajdonsága – szimmetrikus – tranzitív • Az egyensúly stabilitása – semleges (neutrális) – stabil – metastabil – labilis

III. főtétel • Az „elérhetetlenség” • Walther Nernst (1864 -1941), kémiai Nobel-díj: 1920 • Nem lehetséges egy rendszer hőmérsékletét véges sok lépésben 0 K-re csökkenteni. (1912) • A rendszer entrópiája konstans értékhez tart, ha a hőmérséklete a 0 K-hez közelít. • maradvány vagy konfigurációs entrópia

A főtételek és a hőmérséklet • 0. főtétel: bevezeti a hőmérséklete • II. főtétel: skálát (abszolút) rendel hozzá • III. főtétel: megadja az absz. skála 0 pontját

Az ideális gáz modellje és állapotegyenlete Az ideális gáz állapotváltozásai AZ IDEÁLIS GÁZ ÉS ÁLLAPOTVÁLTOZÁSAI

Az ideális gáz • Fizikai modell – kiterjedés nélküli tömegpontok – tömegpontok között nincs kölcsönhatás – fal és tömegpont között rugalmas ütközés ( nyomás) • Matematikai modell: állapotegyenlet f (p, V, T, m) = 0 p. V-m. RT =0 p. V = m. RT pv = RT

Az ideális gáz • Matematikai modell: kalorikus állapotfüggvény H = f (T, N ) és U = f (T, N ) • Az ideális gáz anyagjellemzői: • R : specifikus gázállandó • • M : moláris tömeg • κ: adiabatikus kitevő (fajhőviszony) • fajhő (fajlagos hőkapacitás): • izobár: cp és izochor c. V

Az ideális gáz • Egyszerű állapotváltozások munka és hőforgalma figyeljük a táblát!

GÁZKÖRFOLYAMATOK

Körfolyamatok • Folyamatos energiaátalakítás – Inhomogenitás létrehozása, és fenntartása – Korlátok: • I. főtétel: mennyiségi • II. főtétel: minőségi: a hő csak egy része alakítható munkává • Munkaszolgáltató (hőerőgép) – Carnot, Joule, Otto, Diesel • Munkát igénylő (munkagép) – Hűtőgép, hőszivattyú

Körfolyamatok • Hőerőgép: – Termikus hatásfok • Munkagép: – Fajlagos hűtő teljesítmény – Fajlagos fűtő teljesítmény • Carnot-körfolyamat • Egyenértékű Carnot körfolyamat Figyeljük a táblát!
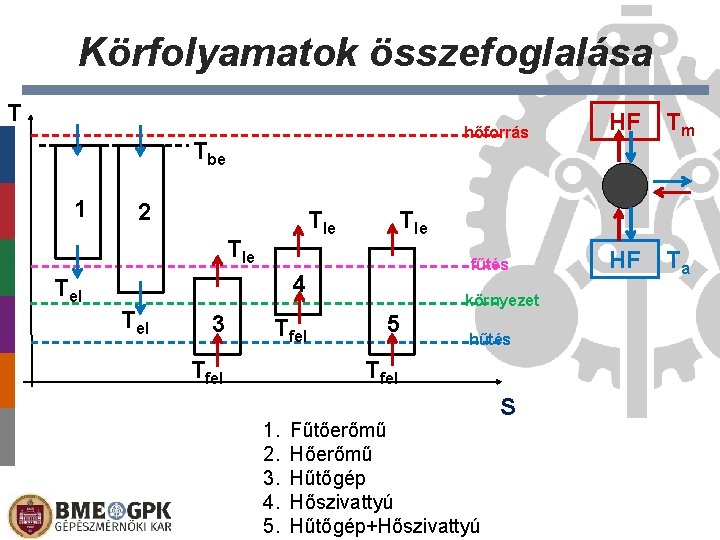
Körfolyamatok összefoglalása T hőforrás Tbe 1 2 Tle Tel 3 Tfel fűtés környezet 5 hűtés Tfel 1. 2. 3. 4. 5. Tm HF Ta Tle 4 Tel HF Fűtőerőmű Hűtőgép Hőszivattyú Hűtőgép+Hőszivattyú S
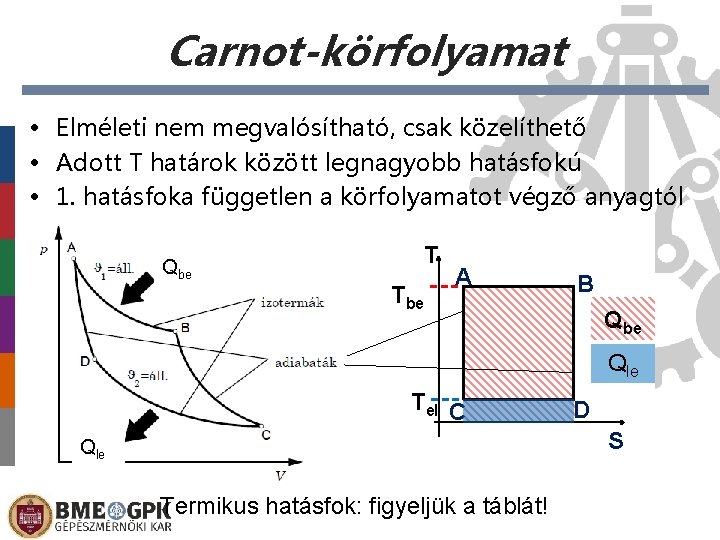
Carnot-körfolyamat • Elméleti nem megvalósítható, csak közelíthető • Adott T határok között legnagyobb hatásfokú • 1. hatásfoka független a körfolyamatot végző anyagtól Qbe T Tbe A B Qbe Qle Tel C D S Qle Termikus hatásfok: figyeljük a táblát!
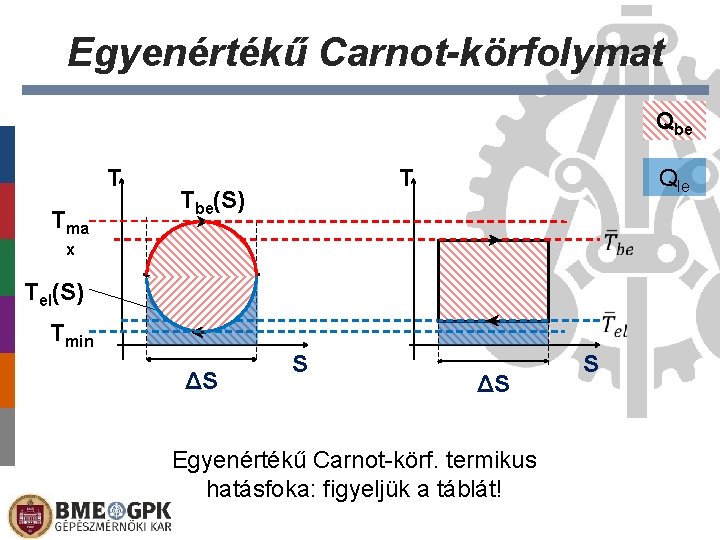
Egyenértékű Carnot-körfolymat Qbe T Tma Qle T Tbe(S) x Tel(S) Tmin ΔS S ΔS Egyenértékű Carnot-körf. termikus hatásfoka: figyeljük a táblát! S
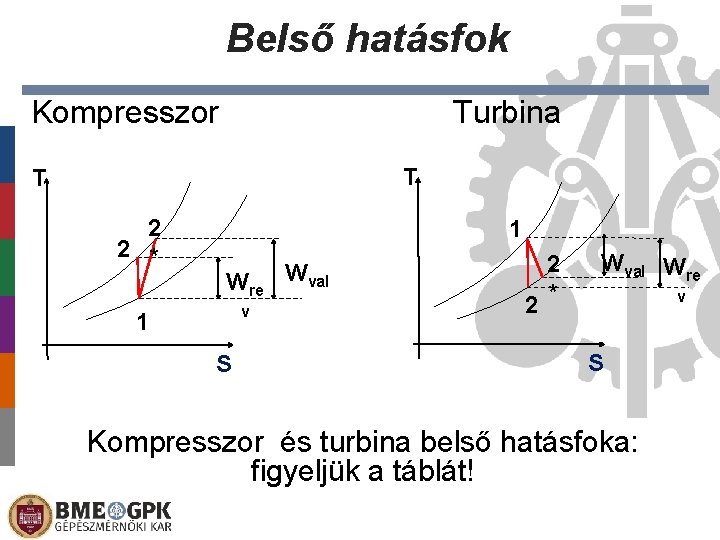
Belső hatásfok Kompresszor Turbina T T 2 2 * 1 Wre v 1 S Wval 2 2 * Wval Wre v S Kompresszor és turbina belső hatásfoka: figyeljük a táblát!

Többgépes körfolyamat BRAYTON-körfolyamat (1872) George Brayton (1830 -189 amerikai gépészmérnök Eredeti ötlet: John Barber, 1

Gázturbina BRAYTON-körfolyamatot megvalósító gép

Gázturbina
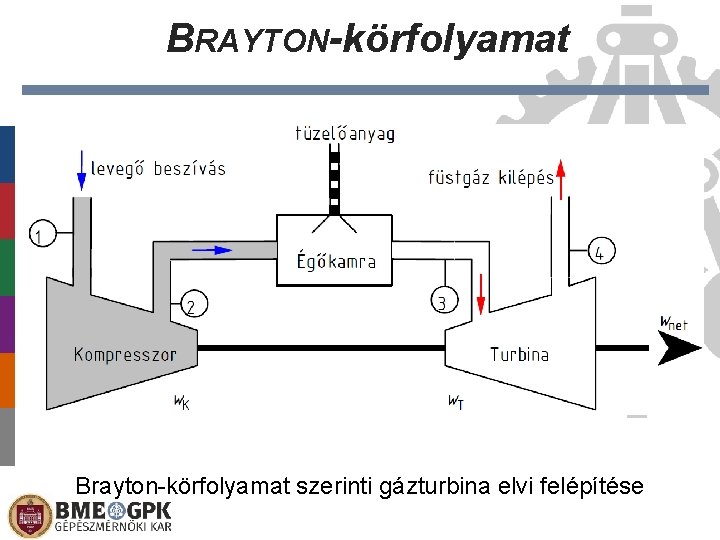
BRAYTON-körfolyamat Brayton-körfolyamat szerinti gázturbina elvi felépítése
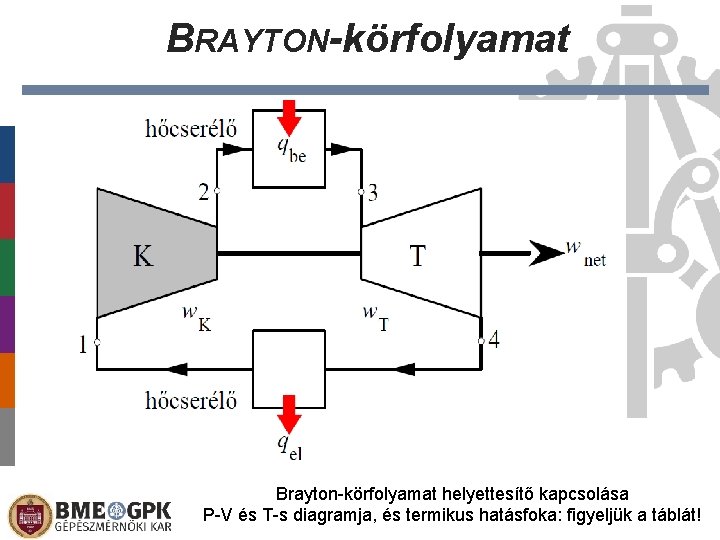
BRAYTON-körfolyamat Brayton-körfolyamat helyettesítő kapcsolása P-V és T-s diagramja, és termikus hatásfoka: figyeljük a táblát!
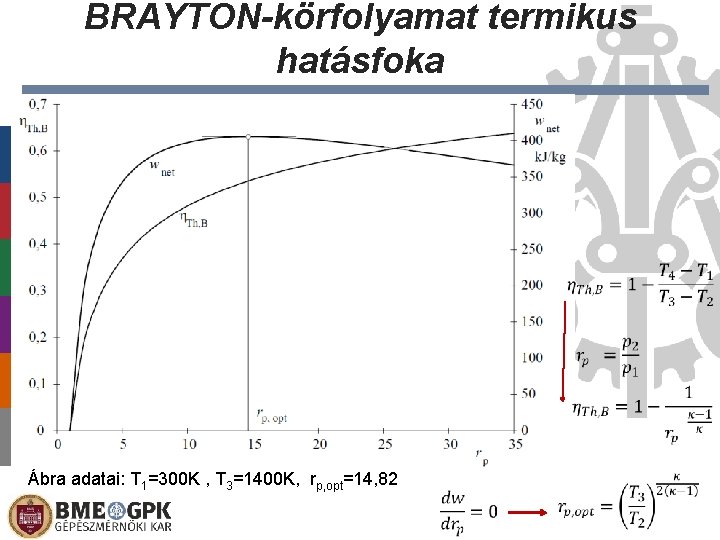
BRAYTON-körfolyamat termikus hatásfoka Ábra adatai: T 1=300 K , T 3=1400 K, rp, opt=14, 82
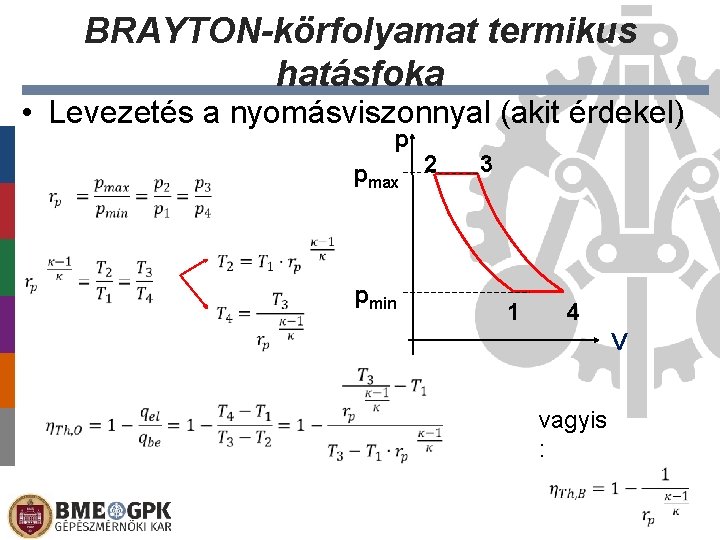
BRAYTON-körfolyamat termikus hatásfoka • Levezetés a nyomásviszonnyal (akit érdekel) p pmax 2 3 pmin 1 4 V vagyis :
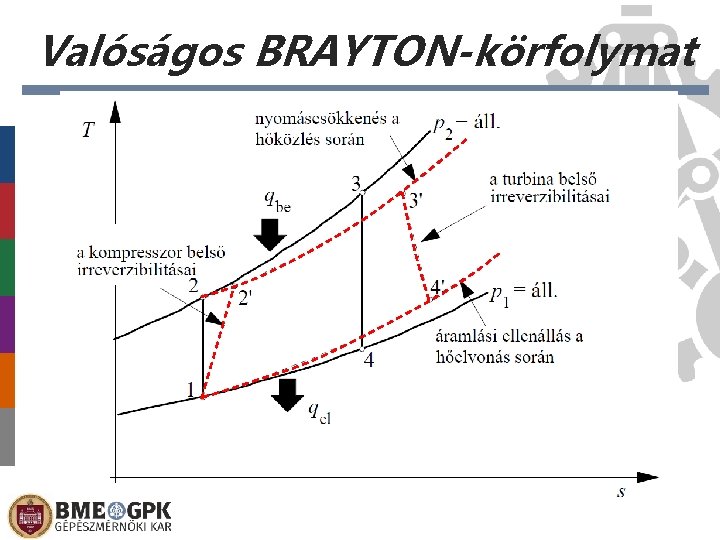
Valóságos BRAYTON-körfolymat
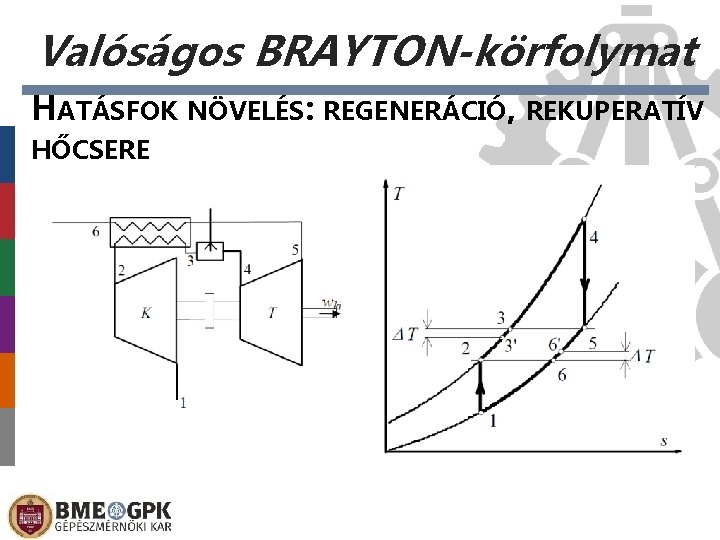
Valóságos BRAYTON-körfolymat HATÁSFOK HŐCSERE NÖVELÉS: REGENERÁCIÓ, REKUPERATÍV

Valóságos BRAYTON-körfolymat HATÁSFOK EXPANZIÓ NÖVELÉS: TÖBBLÉPCSŐS KOMPRESSZIÓ ÉS

fázisegyensúlyi- és állapotdiagramok, gőz/folyadék körfolyamatok TÖBBFÁZISÚ RENDSZEREK

Fázisátalakulások, fázisegyensúly • Elsőrendű (hőhatással járnak) – – Olvadás / fagyás: szilárd ↔ folyadék Párolgás / kondenzáció: folyadék ↔ gőz Szublimáció / deszublimáció: szilárd ↔ gőz Átkristályosodás szilárd ↔ szilárd • Másodrendű (nincs hőhatás) – He szuperfolyékonnyá válik (http: //www. youtube. com/watch? v=2 Z 6 UJbwx. BZI ) – Mágnesesség ferromágneses →paramágneses – Szupravezetés alacsony T-n • Egyensúly dinamikus, feltétele: p, T, µ

Fázisegyensúlyi diagram µ 1 (p, T) = µ 2 (p, T) → p = f (T) és T = f (p) Gibbs-féle fázisszabály: Komp + 2 = Fázis + Szab. fok
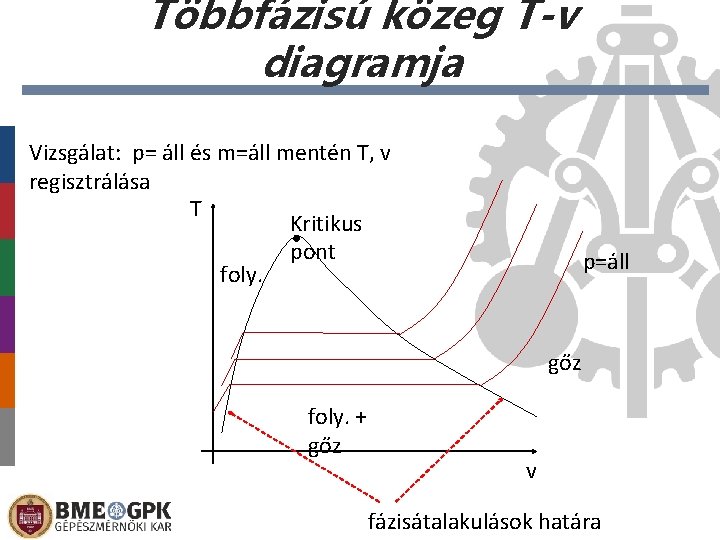
Többfázisú közeg T-v diagramja Vizsgálat: p= áll és m=áll mentén T, v regisztrálása T Kritikus pont foly. p=áll gőz foly. + gőz v fázisátalakulások határa
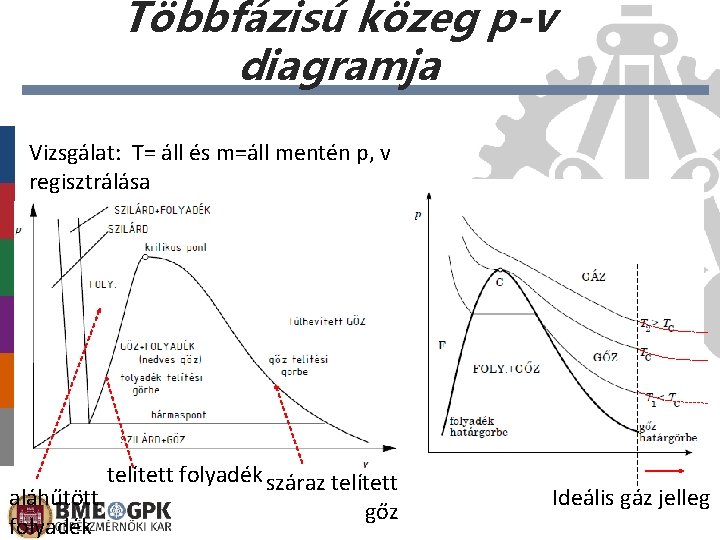
Többfázisú közeg p-v diagramja Vizsgálat: T= áll és m=áll mentén p, v regisztrálása aláhűtött folyadék telített folyadék száraz telített gőz Ideális gáz jelleg

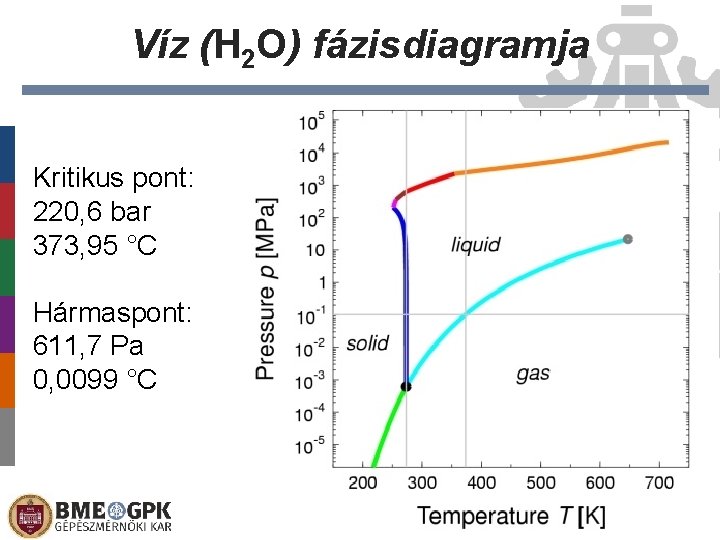
Víz (H 2 O) fázisdiagramja Kritikus pont: 220, 6 bar 373, 95 °C Hármaspont: 611, 7 Pa 0, 0099 °C
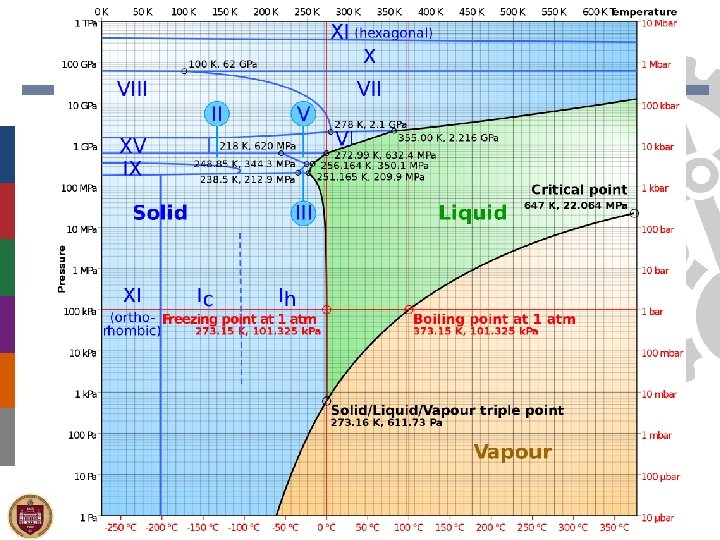

Szuperkritikus állapot http: //www. youtube. com/watch? v=GEr 3 Nxs. PTO A
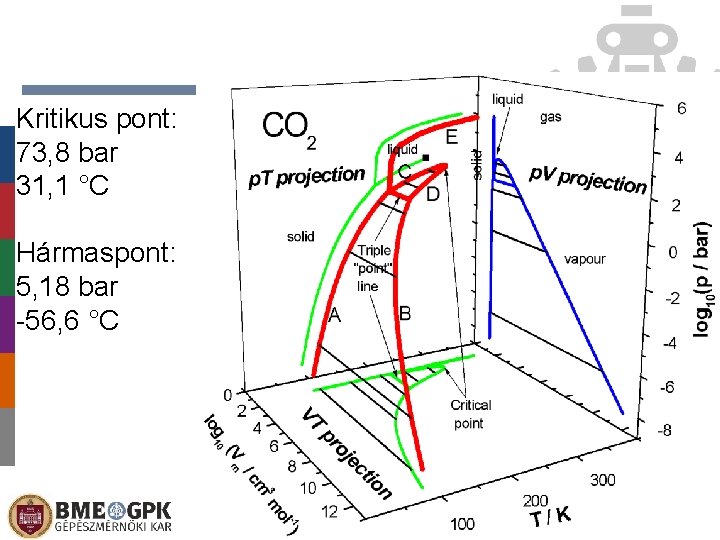
Kritikus pont: 73, 8 bar 31, 1 °C Hármaspont: 5, 18 bar -56, 6 °C
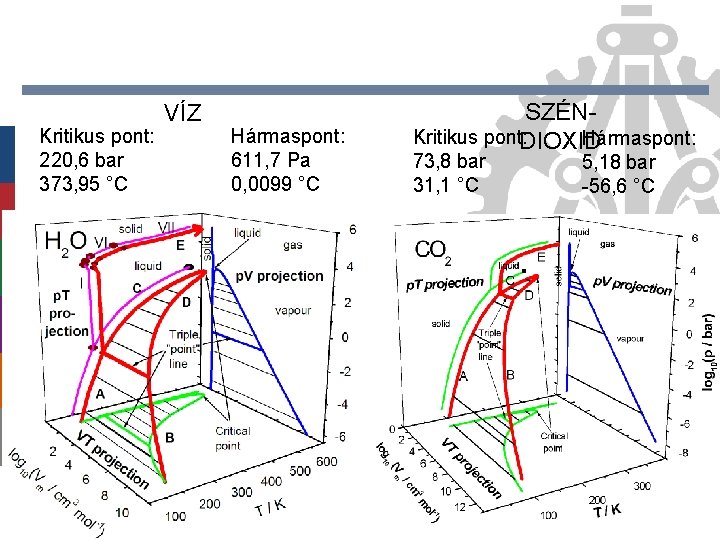
Kritikus pont: 220, 6 bar 373, 95 °C VÍZ Hármaspont: 611, 7 Pa 0, 0099 °C SZÉNKritikus pont: DIOXID Hármaspont: 73, 8 bar 31, 1 °C 5, 18 bar -56, 6 °C
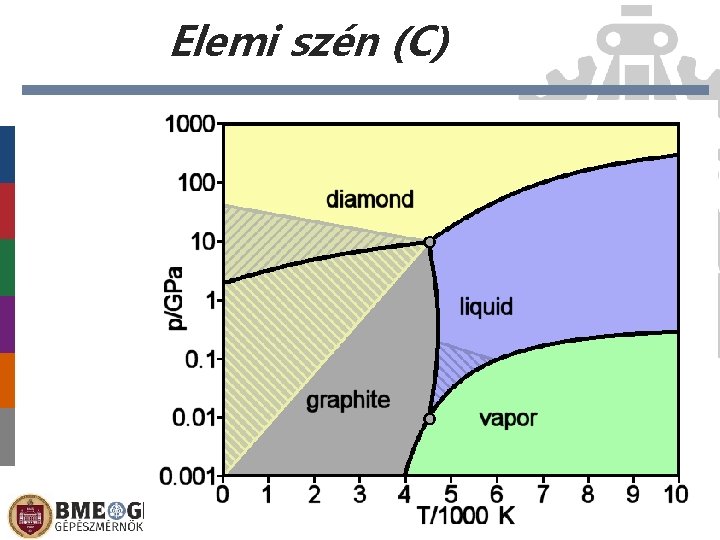
Elemi szén (C)
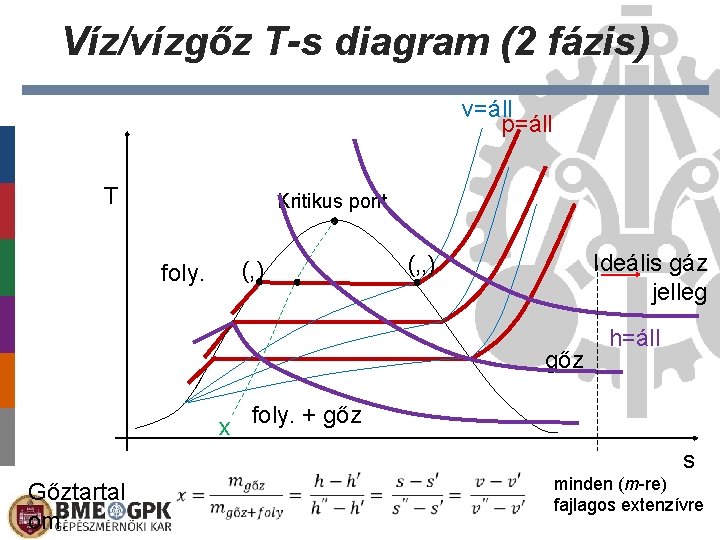
Víz/vízgőz T-s diagram (2 fázis) v=áll p=áll T Kritikus pont foly. (‚) Ideális gáz jelleg (‚‚) gőz h=áll x foly. + gőz Gőztartal om: s minden (m-re) fajlagos extenzívre
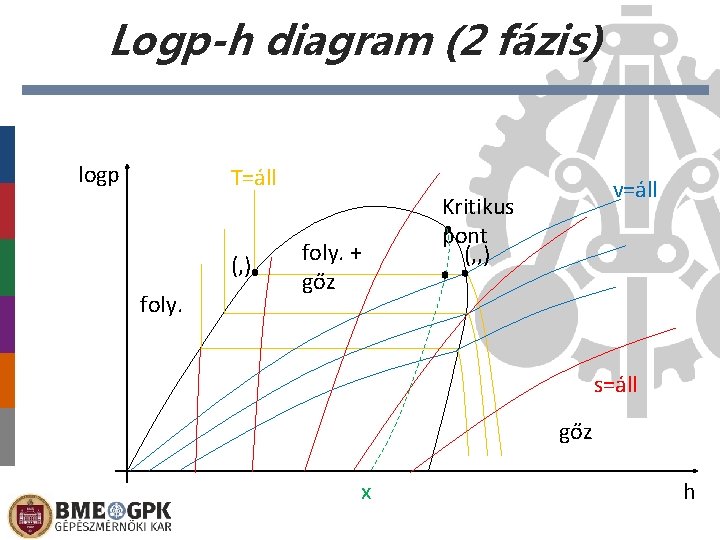
Logp-h diagram (2 fázis) logp T=áll (‚) foly. + gőz v=áll Kritikus pont (‚‚) s=áll gőz x h

Rankine – Clausius körfolyamat

Rankine – Clausius körfolyamat • • Mérlegek és folyamatok, Termikus hatásfok, Egyenértékű Carnot-körfolyamat, Hatásfokjavítás Figyeljük a táblát!

Munkagépek (fordított körfolyamatok) • Hűtőgép • Hőszivattyú • Megvalósításuk: – Fordított Carnot-körfolyamat kétfázisú rendszerben – (Fordított Brayton-körfolyamat) – Kompresszoros hűtőkörfolyamat • Elméleti • Valós (csak a veszteségek bemutatása)
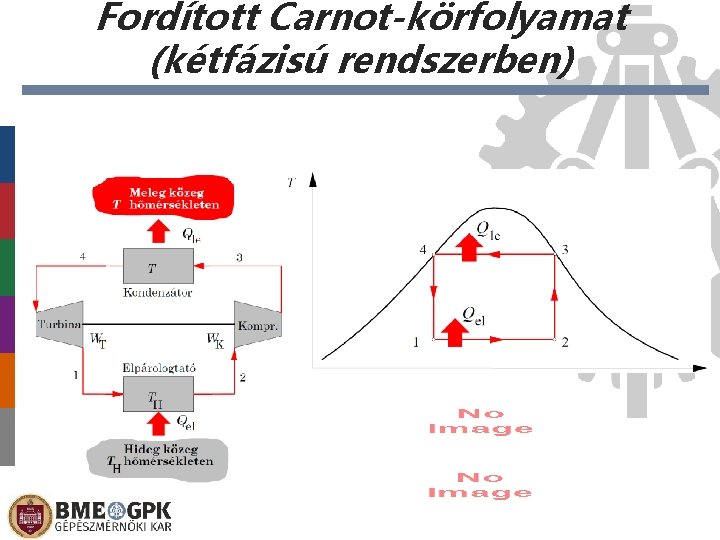
Fordított Carnot-körfolyamat (kétfázisú rendszerben)
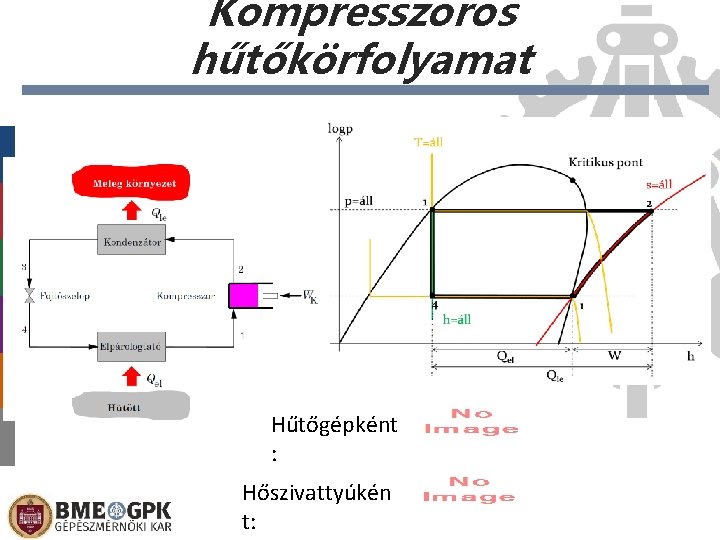
Kompresszoros hűtőkörfolyamat Hűtőgépként : Hőszivattyúkén t:

log(p)-h diagram (2 fázis) logp p=áll T=áll Kritikus pont 1 4 s=áll 2 1 h=áll Qel Qle W h
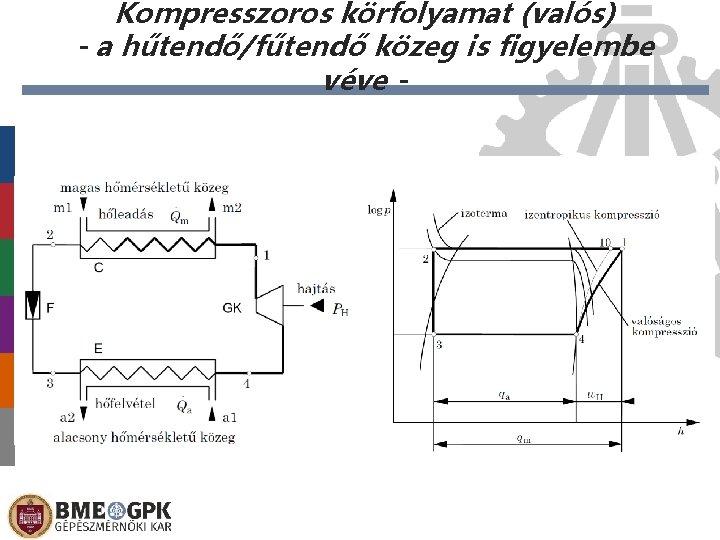
Kompresszoros körfolyamat (valós) - a hűtendő/fűtendő közeg is figyelembe véve -
- Slides: 90