1 3 Teilchenmodell der Stoffe ChemieUnterricht von Michael




























- Slides: 33

1. 3 Teilchenmodell der Stoffe Chemie-Unterricht von Michael Olah

Was bisher behandelt wurde: • 1. 1 Reine Stoff • 1. 2 Die drei Aggregatszustände

1. 3 Teilchenmodell der Stoffe In der Chemie dienen Modellvorstellungen (gedankliche Modelle) zur Veranschaulichung bestimmter Vorgänge und Sachverhalte. Modelle geben die Realität vereinfacht wieder.

1. 3 Teilchenmodell der Stoffe Mit Hilfe des Teilchenmodells kann man folgendes erklären: - Der Aufbau eines reinen Stoffes - Die drei Aggregatzustände - Das Lösen eines Feststoffes - Diffusion (selbständige Durchmischung)

Beobachtung 1: Brownsche Bewegung • Beobachtung von Robert Brown in den 1820 er Jahren: Pollen in Wasser bewegen sich unter dem Mikroskop betrachtet zitterförmig. Dieses Phänomen wurde als Brownsche Bewegung bezeichnet.

Brownsche Bewegung • Unter dem Mikroskop betrachtet bewegen sich die Fetttröpfchen in der Milch ebenfalls zitterförmig. • Milch = Fetttröpfchen in Wasser

Beobachtung 2: Mischen von Wasser und Alkohol • Mischen von 50 ml Wasser und 50 ml Wasser • Mischen von 50 ml Alkohol und 50 ml Alkohol • Mischen von 50 ml Wasser und 50 ml Alkohol • Was erwartet ihr?

Beobachtung 2: Mischen von Wasser und Alkohol Beim Mischen von 50 ml Wasser und 50 ml Alkohol entsteht ein Gemisch mit einem Volumen von nur 97 ml!

Das Teilchenmodell 1) Ein reiner Stoff besteht aus sehr vielen sehr kleinen Teilchen. Alle Teilchen eines reinen Stoffes haben die gleiche Form (gleiches Volumen) und Masse. Zwischen den Teilchen ist leerer Raum. 2) Die Teilchen verschiedener reiner Stoffe sind unterschiedlich. Reiner Stoff A Reiner Stoff B

Das Teilchenmodell 3) Die Teilchen sind in ständiger Bewegung. Diese ist umso stärker je höher die Temperatur ist.

Erklärung der Brownschen Bewegung • Die Teilchen des Wassers und die viel grösseren Fettteilchen stossen zusammen. Wir sehen nur die Zitterbewegung der Fettteilchen, die Wasser-Teilchen sind zu klein und daher unsichtbar für uns. http: //www. agwiss. de/Animationen/demos/brown. htm

Erklärung: Mischen von Wasser und Alkohol Die Volumenverringerung kommt dadurch zustande, dass einige der kleineren Teilchen in die Lücken zwischen den grösseren Teilchen schlüpfen. Das Experiment sagt nichts darüber aus, welche Teilchensorte (Wasser-Teilchen oder Alkohol-Teilchen) grösser ist.

Modell: Erbsen und Senfkörner 50 ml Bohnen und 50 ml Gerste werden vermischt. Auch hier kommt es zu einer Volumenverringerung.

Erklärung der Aggregatszustände mit dem Teilchenmodell

Anziehungskräfte 4) Zwischen den Teilchen bestehen Anziehungskräfte. Je näher zwei Teilchen beieinander sind, desto stärker sind die Anziehungskräfte. Die Anziehungskräfte haben nur eine geringe Reichweite. Diese Anziehungskräfte kann man sich wie die magnetische Kraft bei einem Magnet vorstellen.

Der feste AZ (s) Die Anziehungskräfte zwischen den Teilchen halten die Teilchen in einer regelmässigen Anordnung zusammen. Man spricht auch von einer Gitteranordnung oder kurz Gitter. Der Abstand zwischen den Teilchen ist sehr klein.

Schmelzen Wird ein fester Stoff erwärmt, bewegen sich die Teilchen am Gitterplatz immer stärker. Sobald der Schmelzpunkt erreicht wird, brechen die Teilchen aus dem Gitter aus.

Der flüssige AZ (l) Der Abstand zwischen den Teilchen ist im flüssigen AZ grösser als im festen AZ, die Anziehungskräfte sind deshalb schwächer als im festen AZ: Die Teilchen können zwar zusammengehalten werden, jedoch nicht in einer regelmässigen Anordnung.

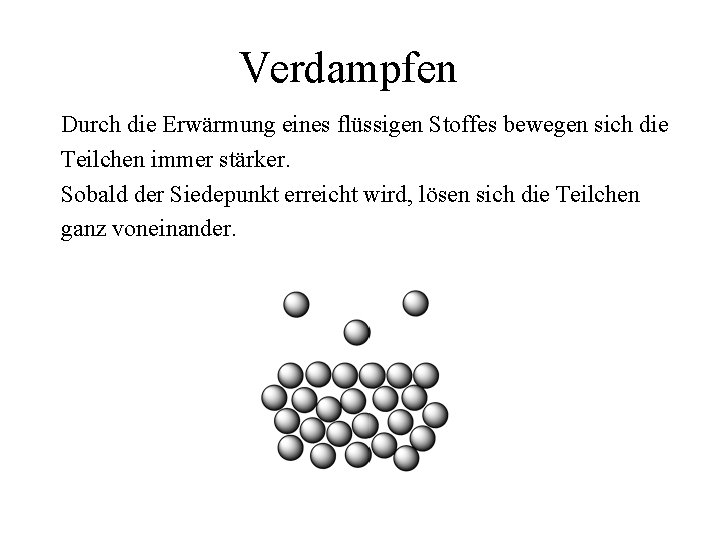
Verdampfen Durch die Erwärmung eines flüssigen Stoffes bewegen sich die Teilchen immer stärker. Sobald der Siedepunkt erreicht wird, lösen sich die Teilchen ganz voneinander.

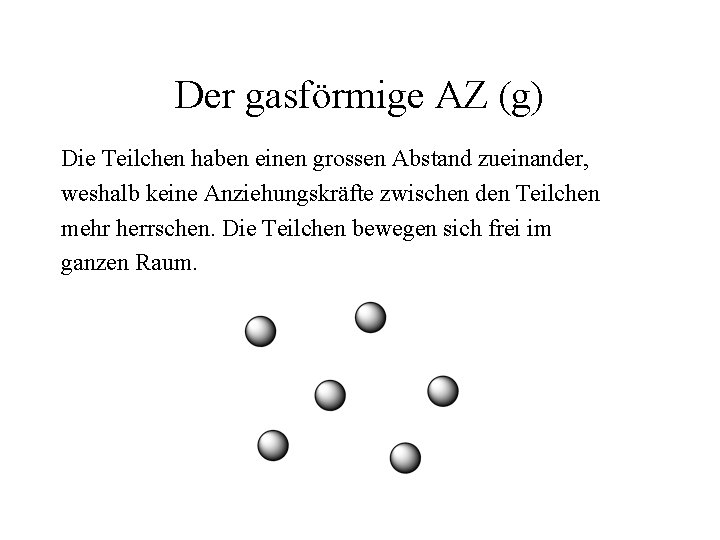
Der gasförmige AZ (g) Die Teilchen haben einen grossen Abstand zueinander, weshalb keine Anziehungskräfte zwischen den Teilchen mehr herrschen. Die Teilchen bewegen sich frei im ganzen Raum.

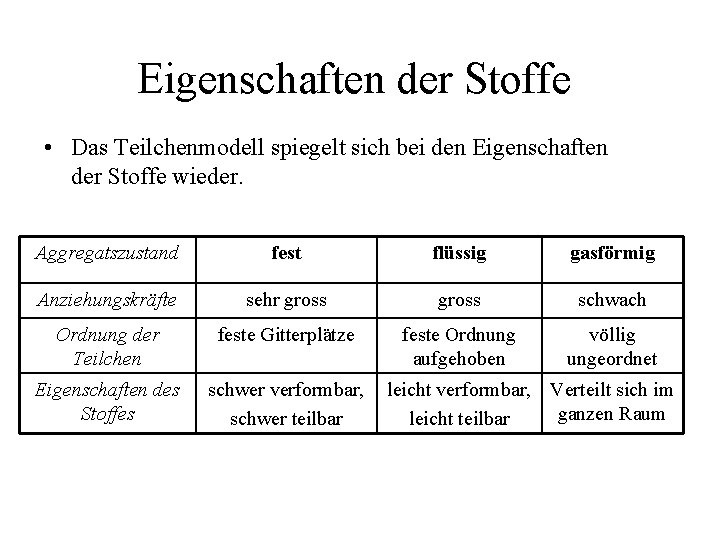
Eigenschaften der Stoffe • Das Teilchenmodell spiegelt sich bei den Eigenschaften der Stoffe wieder. Aggregatszustand fest flüssig gasförmig Anziehungskräfte sehr gross schwach Ordnung der Teilchen feste Gitterplätze feste Ordnung aufgehoben völlig ungeordnet Eigenschaften des Stoffes schwer verformbar, schwer teilbar leicht verformbar, Verteilt sich im ganzen Raum leicht teilbar

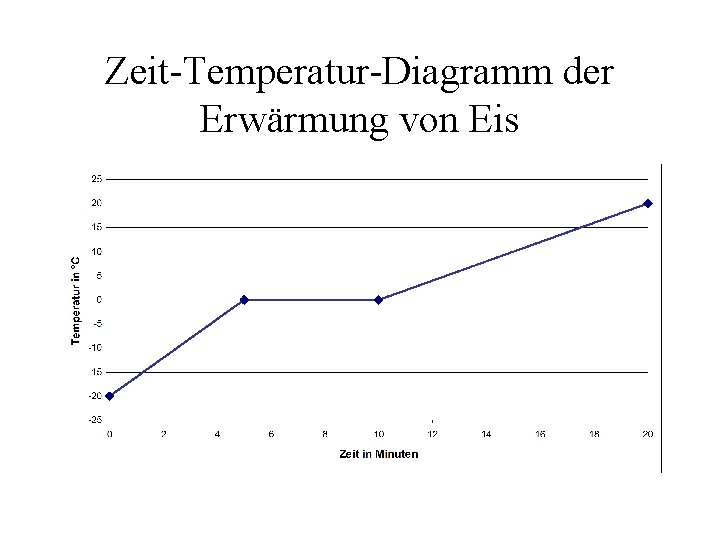
Energie bei Aggregatzustandsänderungen Tiefgekühltes Eis hat eine Temperatur von ca. - 20 °C. Nimmt man das Eis aus dem Tiefkühler steigt die Temperatur langsam an, bis es bei 0 °C zu schmelzen beginnt. Die Temperatur beträgt nun konstant 0 °C bis das Eis vollständig geschmolzen ist. Erst wenn das ganze Eis geschmolzen ist steigt die Temperatur weiter an.

Zeit-Temperatur-Diagramm der Erwärmung von Eis

Schmelz- und Erstarrungswärme Für das Schmelzen wird Energie benötigt. Sie wird von den Teilchen gebraucht um die Anziehungskräfte teilweise zu überwinden und sich aus dem Gitter zu lösen. Diese Energie heisst Schmelzwärme. Die gleiche Wärmemenge wird beim Erstarren frei. Diese Energie nennt man Erstarrungswärme.

Beispiel Erstarrungswärme Bei Handwärmern nützt man die Erstarrungswärme um gezielt Wärme freizusetzen. Die Erstarrung braucht eine Initialisierung (Starter), bei Handwärmern ist dies oft ein Stück Metall, welches geknickt werden muss.

Verdampfen Erwärmt man Wasser in einem Topf bis 100 °C beginnt das Wasser zu sieden. Die Temperatur des Wassers bleibt dabei konstant bei 100 °C bis alles Wasser verdampft ist.

Verdampfungs- und Kondensationswärme Beim Verdampfen wird Energie benötigt um die Anziehungskräfte vollständig zu überwinden. Diese Energie nennt man Verdampfungswärme. Die gleiche Wärmemenge wird beim Kondensieren frei. Diese Energie nennt man Kondensationswärme.

Verdunstung Flüssiges Wasser wechselt teilweise bereits bei Zimmertemperatur in den gasförmigen AZ über. Dieser Vorgang nennt man Verdunstung. Der Grund dafür ist, dass einige Teilchen an der Oberfläche einer Flüssigkeit sich zu heftig bewegen und nicht durch die Anziehungskräfte festgehalten werden können. Auch für die Verdunstung wird Energie benötigt. Man nennt sie Verdunstungswärme.

Erklärung weiterer Phänomene mit dem Teilchenmodell

Lösen eines Feststoffes Mit dem Teilchenmodell lässt sich auch das Lösen eines Feststoffes erklären: Die Teilchen einer Flüssigkeit (z. B. Wasser) schieben sich zwischen die Teilchen des Feststoffes im Gitter (z. B. Kochsalz). Die Feststoff-Teilchen lösen sich vom Gitter und werden gleichmässig verteilt.

Lösen eines Feststoffes

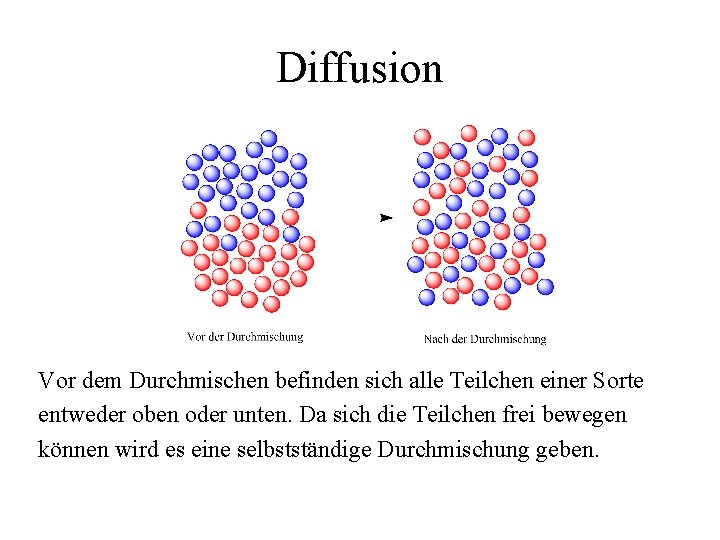
Diffusion Die selbstständige Durchmischung zweier Stoffe nennt man Diffusion. Sie beruht auf der freien Beweglichkeit der Teilchen im flüssigen oder gasförmigen Zustand.

Diffusion Vor dem Durchmischen befinden sich alle Teilchen einer Sorte entweder oben oder unten. Da sich die Teilchen frei bewegen können wird es eine selbstständige Durchmischung geben.