Berechnung molarer Reaktionsenthalpien Der Satz von Hess RH
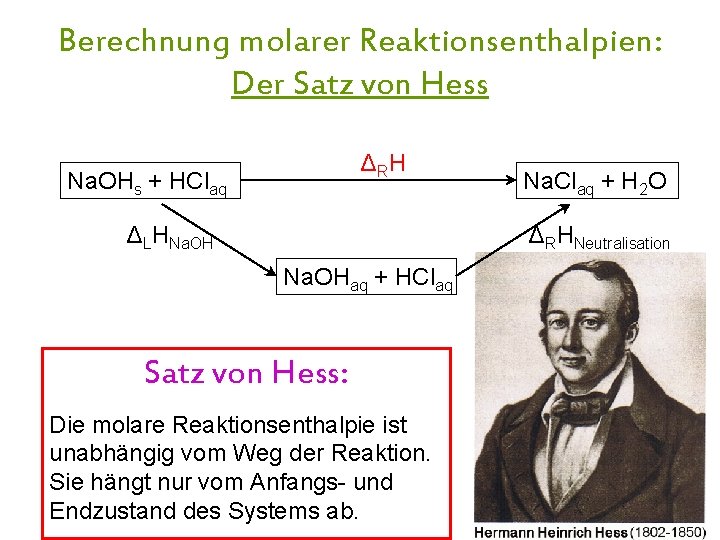
Berechnung molarer Reaktionsenthalpien: Der Satz von Hess Δ RH Na. OHs + HClaq ΔLHNa. OH Na. Claq + H 2 O ΔRHNeutralisation Na. OHaq + HClaq ΔRH = ΔLHNa. OH + ΔRHNeutralisation Satz von Hess: = -43 Reaktionsenthalpie + (-55 ) Die molare ist unabhängig vom Weg der Reaktion. = -98 nur vom Anfangs- und Sie hängt Endzustand des Systems ab.
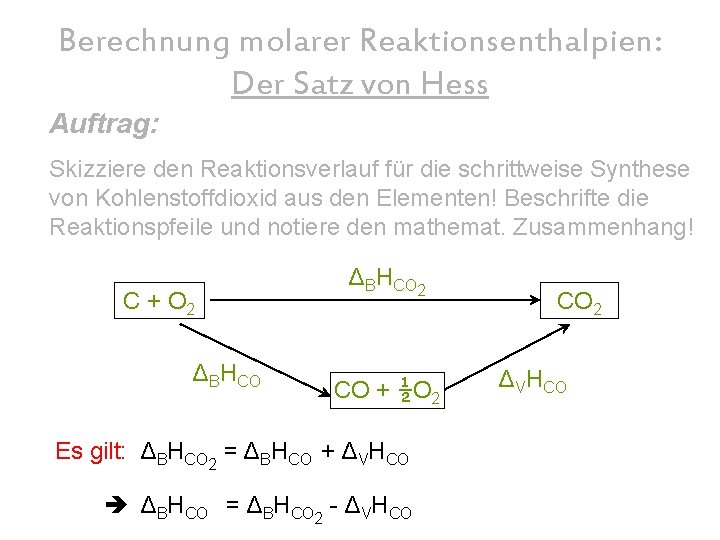
Berechnung molarer Reaktionsenthalpien: Der Satz von Hess Auftrag: Skizziere den Reaktionsverlauf für die schrittweise Synthese von Kohlenstoffdioxid aus den Elementen! Beschrifte die Reaktionspfeile und notiere den mathemat. Zusammenhang! C + O 2 ΔBHCO 2 CO + ½O 2 Es gilt: ΔBHCO 2 = ΔBHCO + ΔVHCO ΔBHCO = ΔBHCO 2 - ΔVHCO CO 2 ΔVHCO
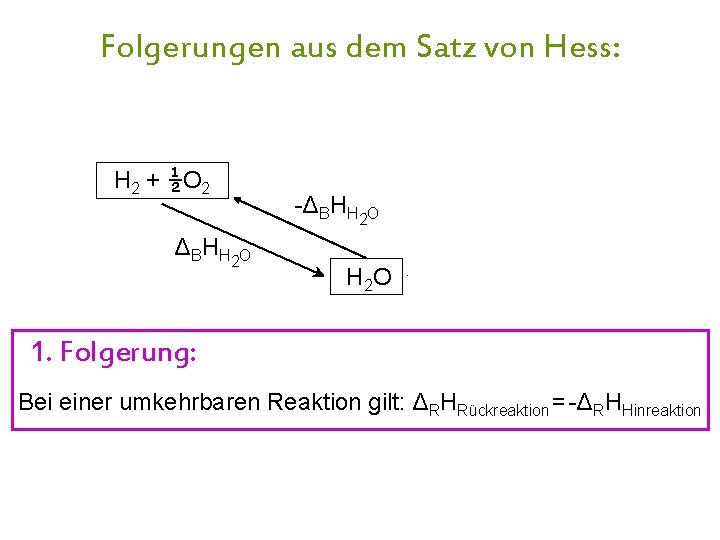
Folgerungen aus dem Satz von Hess: H 2 + ½O 2 Δ B H H 2 O -ΔBHH 2 O H 2 + ½O 2 -ΔBHH 2 O 1. Folgerung: Bei einer umkehrbaren Reaktion gilt: ΔRHRückreaktion = -ΔRHHinreaktion
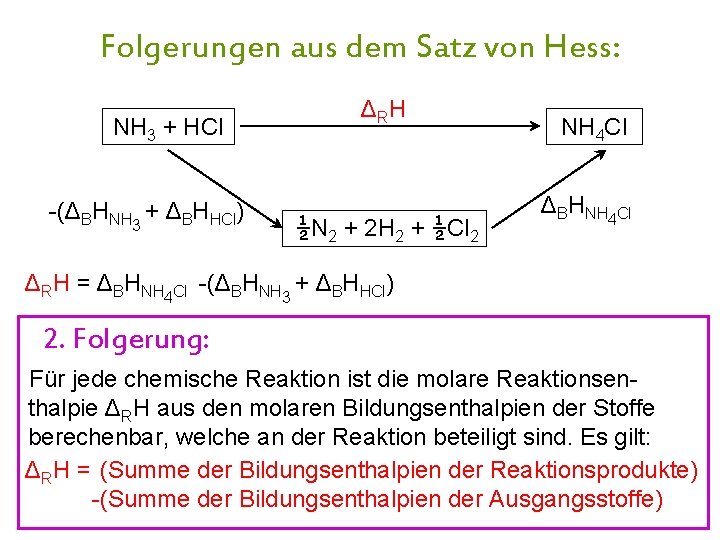
Folgerungen aus dem Satz von Hess: NH 3 + HCl -(ΔBHNH 3 + ΔBHHCl) Δ RH ½N 2 + 2 H 2 + ½Cl 2 NH 4 Cl ΔBHNH 4 Cl ΔRH = ΔBHNH 4 Cl -(ΔBHNH 3 + ΔBHHCl) Nebenrechnung: -1 – ( -46 k. J·mol-1 - 92 k. J·mol-1) 2. =2 +-704 k. J·mol ½NFolgerung: 1½ H NH 3 ΔRH = ΔBHNH 3 2 Für jede chemische Reaktion ist die Δ molare Reaktionsen½H + ½Cl HCl H = Δ HHCl -1 2 2 R B Δ H = -566 k. J·mol R thalpie ΔRH aus den molaren Bildungsenthalpien der Stoffe berechenbar, an. NH der +Reaktion Es gilt: ½N 2 + 2 H 2 welche + ½Cl 2 HCl ΔRbeteiligt H = ΔBHsind. 3 NH 3 + ΔBHHCl ΔRH = (Summe der Bildungsenthalpien der Reaktionsprodukte) -(Summe der Bildungsenthalpien der Ausgangsstoffe)

Übungen 1. SO 3 + H 2 O H 2 SO 4 ΔRH = ΔBHH 2 SO 4 - (ΔBHSO 3 + ΔBHH 2 O) = -814 - ( -396 – 242 ) im Tafelwerk nachschlagen! = -176 2. CO + 2 H 2 CH 3 OH ΔRH = -128 3. ΔRH = ΔBHCH 3 OH - (ΔBHCO + 2 ΔBHH 2) 2 Na + H 2 O 2 Na. OH + H 2 ΔRH = -569 = -238, 5 - ( -110, 5 - 2 0 ) 4. CH 3 OH + O 2 = -128 HCOOH + H 2 O ΔRH = -532, 7
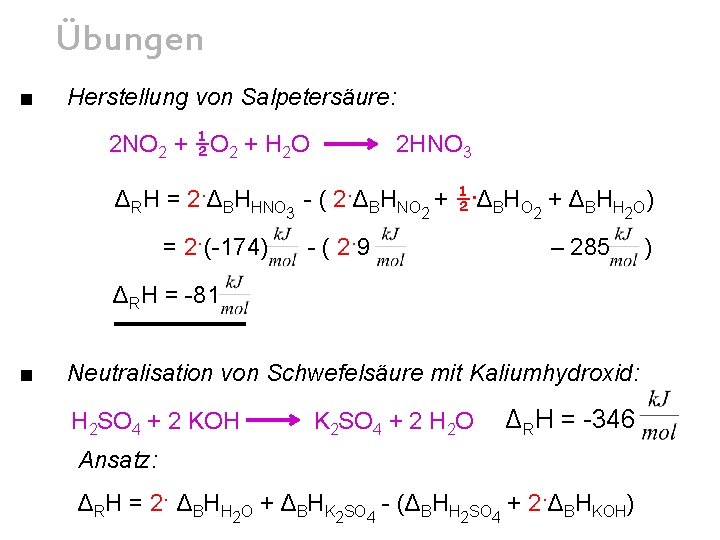
Übungen ■ Herstellung von Salpetersäure: 2 NO 2 + ½O 2 + H 2 O 2 HNO 3 ΔRH = 2·ΔBHHNO 3 - ( 2·ΔBHNO 2 + ½·ΔBHO 2 + ΔBHH 2 O) = 2·(-174) - ( 2·9 – 285 ΔRH = -81 ■ Neutralisation von Schwefelsäure mit Kaliumhydroxid: H 2 SO 4 + 2 KOH K 2 SO 4 + 2 H 2 O ΔRH = -346 Ansatz: ΔRH = 2· ΔBHH 2 O + ΔBHK 2 SO 4 - (ΔBHH 2 SO 4 + 2·ΔBHKOH) )
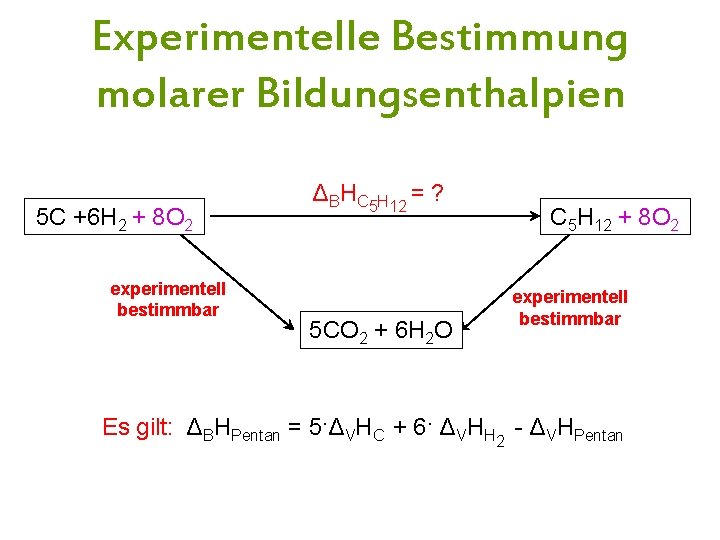
Experimentelle Bestimmung molarer Bildungsenthalpien 5 C +6 H 2 + 8 O 2 experimentell bestimmbar ΔBHC 5 H 12 = ? 5 CO 2 + 6 H 2 O C 5 H 12 + 8 O 2 experimentell bestimmbar Es gilt: ΔBHPentan = 5·ΔVHC + 6· ΔVHH 2 - ΔVHPentan
- Slides: 7