UNIDAD REACCIONES QUMICAS OBJETIVO Conocer las diferencias entre

UNIDAD: REACCIONES QUÍMICAS OBJETIVO: • Conocer las diferencias entre cambio físico y cambios químicos. • Identificar • Balancear las partes de una ecuación química. reacciones químicas. Fuente: archivos de departamento. / QUI-256 PUCV / Imágenes Educar. ar

¿EN QUÉ SE DIFERENCIAN LOS CAMBIOS FÍSICOS DE LOS CAMBIOS QUÍMICOS? Cambio físico Es una transformación en la que no varía la naturaleza de sus compuestos. Es reversible ya que una vez sucedida la transformación, pueden volver a su estado inicial. Se trata principalmente de un cambio de estado (ejemplo, de sólido a gas) Cambio químico Es una transformación en la que cambia la naturaleza de sus compuestos. Es irreversible ya que una vez sucedida la transformación no se puede volver a su estado inicial. Se expresa en reacciones químicas

¿CÓMO RECONOCER UNA REACCIÓN QUÍMICA? Emisión de luz Liberación de gases Liberación de energía química (calor) Formación de un sólido (precipitado) Cambio de color

REACCIONES Y ECUACIONES QUÍMICAS En una reacción química sucede un cambio químico, por lo cual las sustancias obtenidas (productos) son de distinta naturaleza que sus reactantes. Toda reacción química se expresa utilizando ecuaciones químicas: 4 Fe(s) + 3 O 2 (g) reactantes 2 Fe 2 O 3 (s) productos
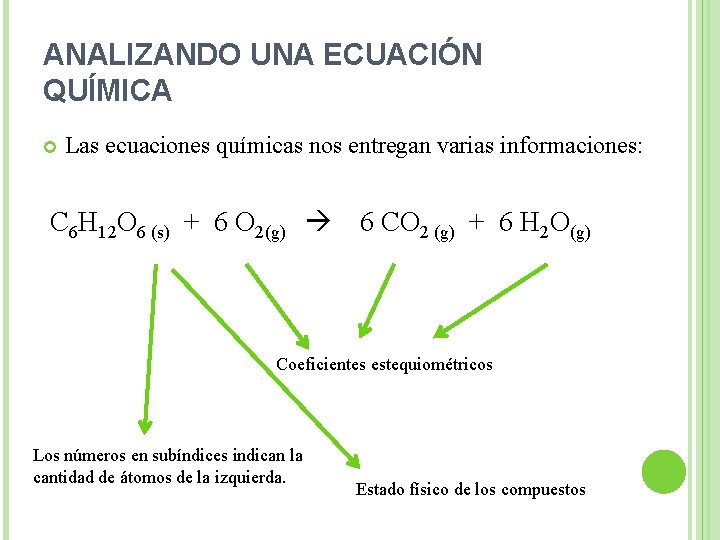
ANALIZANDO UNA ECUACIÓN QUÍMICA Las ecuaciones químicas nos entregan varias informaciones: C 6 H 12 O 6 (s) + 6 O 2(g) 6 CO 2 (g) + 6 H 2 O(g) Coeficientes estequiométricos Los números en subíndices indican la cantidad de átomos de la izquierda. Estado físico de los compuestos

¿CÓMO OCURRE UNA REACCIÓN QUÍMICA? Para explicar cómo sucede una reacción química, existe una serie de postulados conocidos como: Teoría de las colisiones. Esta teoría consiste en considerar la materia como partículas esféricas y del mismo tamaño. Señala que las reacciones suceden cuando las partículas de los reactantes sufren choques efectivos entre sí.

¿CUÁNDO UN CHOQUE ES EFECTIVO? Para que un choque sea efectivo, debe cumplir con las siguientes características: 1) Cuando tienen la orientación adecuada, si la orientación no es adecuada, las partículas chocarán y rebotarán. 2) Que el choque sea lo suficientemente fuerte para romper los enlaces de los reactantes. 3) Si a partir del choque, se libera suficiente energía como para romper los enlaces, entonces tiene la energía de activación para realizarse.
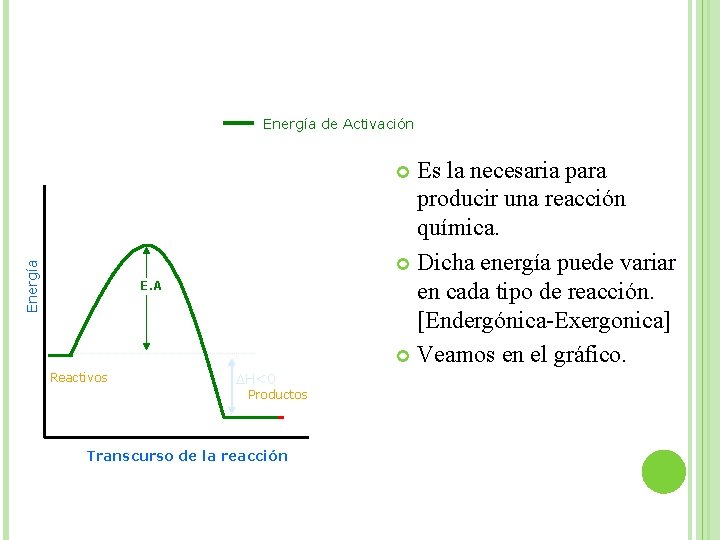
Energía de Activación Es la necesaria para producir una reacción química. Dicha energía puede variar en cada tipo de reacción. [Endergónica-Exergonica] Veamos en el gráfico. Energía E. A Reactivos H<0 Productos Transcurso de la reacción

LEY DE CONSERVACIÓN DE LA MASA En el s. XVIII Antonie Lavoiser elaboró una de las leyes fundamentales de la naturaleza. Al experimentar con reacción de combustión y medir las masas, planteó una explicación: «La masa de las sustancias que se queman es la misma que las sustancias que se producen durante la combustión, solo hay transformación de unas en otras» Esta ley se puede enunciar como: «La materia no se crea ni se destruye, solo se transforma»

BALANCE DE REACCIONES QUÍMICAS La ley de conservación de la masa implica algunas consecuencias en la representación de las reacciones químicas. Los átomos de los elementos y compuestos se reordenan durante la reacción química, para formar determinados productos. En dicho proceso, la cantidad de átomos presentes en reactantes y productos debe ser la misma, de tal manera que se establece un balance químico.

MÉTODOS PARA BALANCEAR REACCIONES QUÍMICAS Método de tanteo: se basa en utilizar múltiplos de número enteros para igualar las cantidades de átomos en reactivos y productos. Método algebraico: utiliza expresiones algebraicas y ecuaciones para calcular el valor de los coeficientes estequiometricos. Método ión-electrón: es un tipo de balance químico para reacciones redox o de intercambio de electrones (este tipo se verá en 3° medio)

BALANCE DE ECUACIONES QUÍMICAS POR TANTEO Al balancear una ecuación química, debemos contabilizar la cantidad de átomos que tenemos en los reactantes y productos. Si las cantidades son diferentes, entonces debemos balancear agregando un coeficiente estequiometrico. Veamos como:
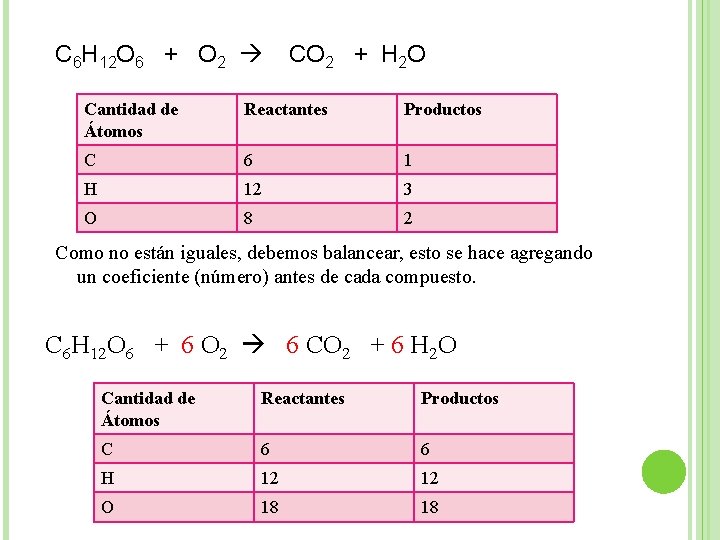
C 6 H 12 O 6 + O 2 CO 2 + H 2 O Cantidad de Átomos Reactantes Productos C 6 1 H 12 3 O 8 2 Como no están iguales, debemos balancear, esto se hace agregando un coeficiente (número) antes de cada compuesto. C 6 H 12 O 6 + 6 O 2 6 CO 2 + 6 H 2 O Cantidad de Átomos Reactantes Productos C 6 6 H 12 12 O 18 18

BALANCE DE REACCIONES QUÍMICAS POR MÉTODO ALGEBRAICO 1) 2) 3) 4) 5) Asignar una letra a cada coeficiente estequiometrico. Escribir hacia abajo los átomos que forman la reacción. Expresar para cada átomo una ecuación algebraica correspondiente. Designar el valor 1 a una de las letras (normalmente la más repetida). Calcular los valores de cada expresión y reemplazar en los coeficientes.
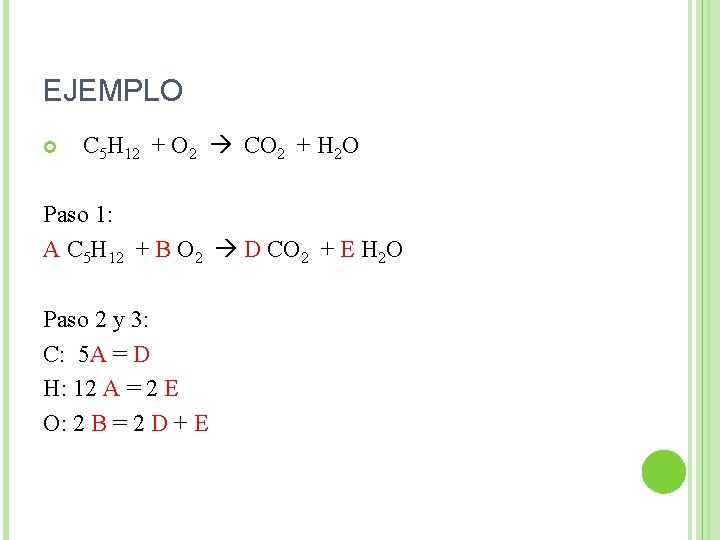
EJEMPLO C 5 H 12 + O 2 CO 2 + H 2 O Paso 1: A C 5 H 12 + B O 2 D CO 2 + E H 2 O Paso 2 y 3: C: 5 A = D H: 12 A = 2 E O: 2 B = 2 D + E
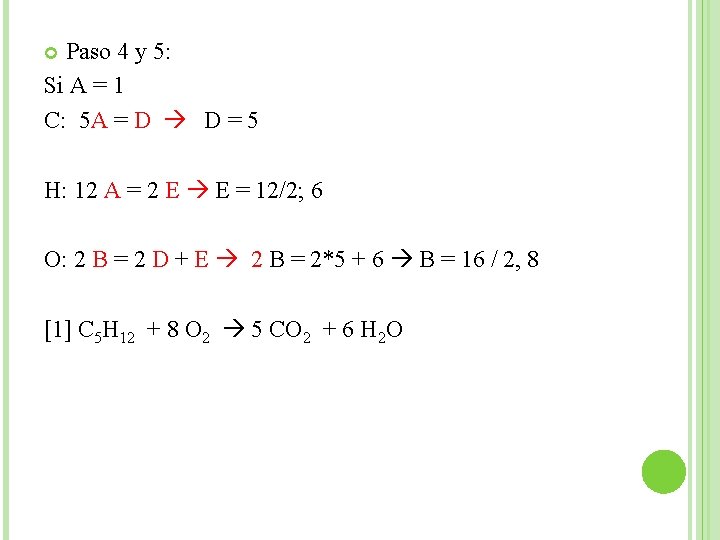
Paso 4 y 5: Si A = 1 C: 5 A = D D = 5 H: 12 A = 2 E E = 12/2; 6 O: 2 B = 2 D + E 2 B = 2*5 + 6 B = 16 / 2, 8 [1] C 5 H 12 + 8 O 2 5 CO 2 + 6 H 2 O
- Slides: 16