Termodinamika kimikoa ERREAKZIO ENDOTERMIKOAK beroa zurgatzen denean ERREAKZIO
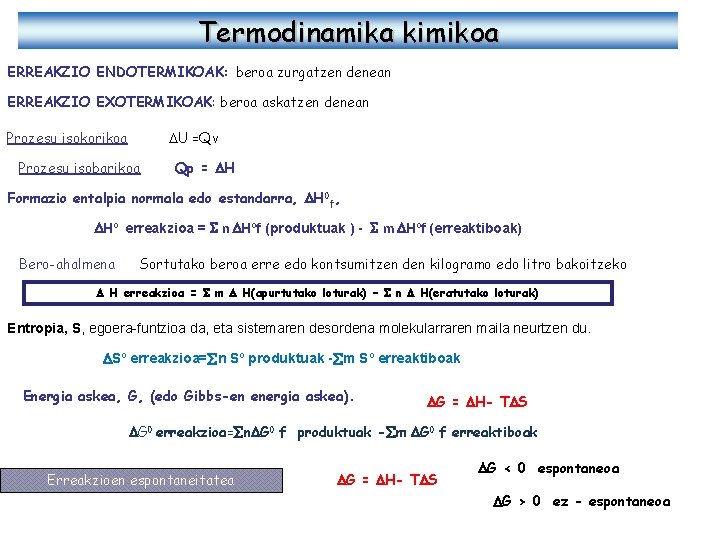
Termodinamika kimikoa ERREAKZIO ENDOTERMIKOAK: beroa zurgatzen denean ERREAKZIO EXOTERMIKOAK: beroa askatzen denean Prozesu isokorikoa DU =Qv Prozesu isobarikoa Qp = H Formazio entalpia normala edo estandarra, H 0 f, Hº erreakzioa = S n Hºf (produktuak ) - S m Hºf (erreaktiboak) Bero-ahalmena Sortutako beroa erre edo kontsumitzen den kilogramo edo litro bakoitzeko H erreakzioa = S m H(apurtutako loturak) – S n H(eratutako loturak) Entropia, S, egoera-funtzioa da, eta sistemaren desordena molekularraren maila neurtzen du. Sº erreakzioa= n Sº produktuak - m Sº erreaktiboak Energia askea, G, (edo Gibbs-en energia askea). G = H- T S G 0 erreakzioa= n G 0 f produktuak - m G 0 f erreaktiboak Erreakzioen espontaneitatea G = H- T S G < 0 espontaneoa G > 0 ez - espontaneoa

Zinetika kimikoa Erreakzio kimikoen teoria Aktibazio energia Talka eraginkorra Partikulen orientazioa edo Talka ez-eraginkorra Konplexu aktibatua, energia handikoa eta egoera ezegonkorra duena (trantsizio egoera). Trantsizio egoera eta erreaktiboen arteko energia diferentzia aktibazio energia Ea da. Katalizatzaileak Katalizatzailea erreakzio abiadura asko aldatzen duen substantzia bat da Erreakzioaren bidea aldatzen dute, aktibazio energia aldatuz baina aldagai termodinamikoa (entalpia, entropia eta Gibbs energia askea) berdinak mantentzen dira Oreka homogeneoak: masa ekintzaren legea [C]c[D]d a. A + b. B c. C + d. D Kc = [A]a[B]b Kc–ren eta doitutako ekuazioaren arteko erlazioa H 2(g) + I 2(g) 2 HI(g) Erreakzio-zatidura Qc Disoziazio-gradua a 2 HI(g) H 2(g) + I 2(g) Kc’’ = 1/ Kc a<1 K’’c = [H 2][I 2] [HI]2

Oreka heterogeneoak: Haupeatze erreakzioak Disoluzio batek solutu-kantitate gehiagorik disolba ezin dezakeenean asea edo saturatua da Disolbagarritasuna (s) Solutuaren kantitate maximo bat disolbatuta eta beste kantitate bat disolbatu gabe oreka heterogeneo Oreka konstante: disolbagarritasun-biderkaduraren konstantea edo disolbagarritasun konstantea Ks edo Kps Biderkadura ionikoa Qs Qs <Ks edo Qs =Ks edo Qs > K s Le Chatelier-en printzipioa Oreka batean eragina duten faktoreen (T, P edo kontzentrazioak) kanpo-aldakuntzak sistemaren birdoiketa dakar, aldakuntza horren efektua moteltzeko eta, horrela, oreka-egoera berria lortu ahal izateko. Kontzentrazioa Presioa Aldaketa Tenperatura Orekaren desplazamendua Substantzia baten kontzentrazioa handitzea Substantzia hori kontsumitzeko noranzkora Substantzia baten kontzentrazioa gutxitzea Substantzia hori ekoizteko noranzkora Presioa handitu Presioa gutxitu Tenperatura igo Tenperatura jaitsi Gasen molen kopurua gutxitzeko noranzkoa Gasen molen kopurua handitzeko noranzkoa Erreakzio endotermikoaren noranzkoa Erreakzio exotermikoaren noranzkoa
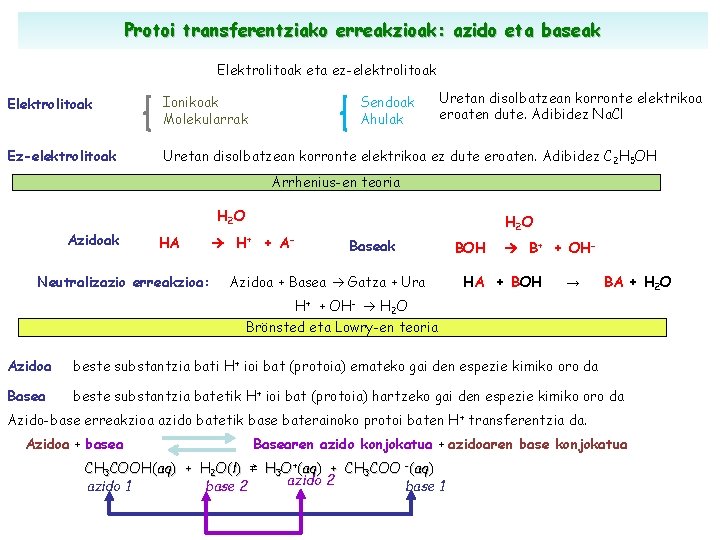
Protoi transferentziako erreakzioak: azido eta baseak Elektrolitoak eta ez-elektrolitoak Sendoak Ahulak Uretan disolbatzean korronte elektrikoa eroaten dute. Adibidez Na. Cl Elektrolitoak Ionikoak Molekularrak Ez-elektrolitoak Uretan disolbatzean korronte elektrikoa ez dute eroaten. Adibidez C 2 H 5 OH Arrhenius-en teoria H 2 O Azidoak HA Neutralizazio erreakzioa: H+ + A - H 2 O Baseak Azidoa + Basea Gatza + Ura BOH B+ + OH- HA + BOH → BA + H 2 O H+ + OH- H 2 O Brönsted eta Lowry-en teoria Azidoa beste substantzia bati H+ ioi bat (protoia) emateko gai den espezie kimiko oro da Basea beste substantzia batetik H+ ioi bat (protoia) hartzeko gai den espezie kimiko oro da Azido-base erreakzioa azido batetik base baterainoko protoi baten H + transferentzia da. Azidoa + basea Basearen azido konjokatua + azidoaren base konjokatua CH 3 COOH(aq) + H 2 O(l) ⇄ H 3 O+(aq) + CH 3 COO -(aq) azido 2 base 1 base 2 azido 1
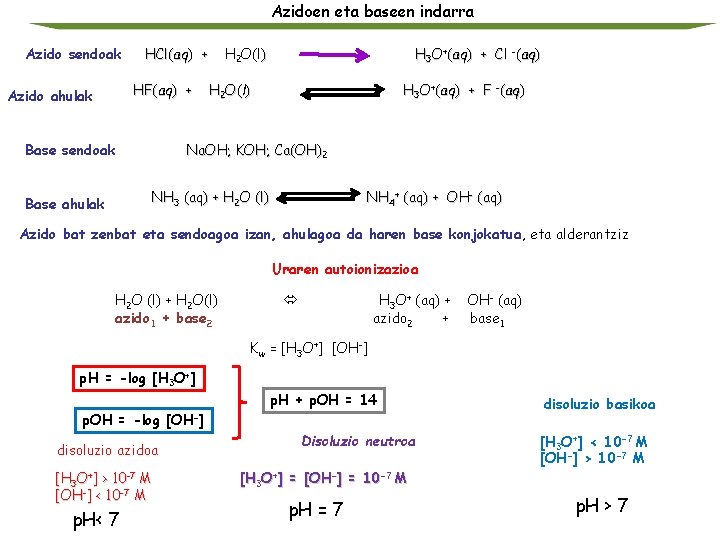
Azidoen eta baseen indarra Azido sendoak HCl(aq) + HF(aq) + Azido ahulak Base sendoak H 2 O(l) H 3 O+(aq) + Cl -(aq) H 2 O(l) H 3 O+(aq) + F -(aq) Na. OH; KOH; Ca(OH)2 NH 3 (aq) + H 2 O (l) Base ahulak NH 4+ (aq) + OH- (aq) Azido bat zenbat eta sendoagoa izan, ahulagoa da haren base konjokatua, eta alderantziz Uraren autoionizazioa H 2 O (l) + H 2 O(l) azido 1 + base 2 H 3 O+ (aq) + azido 2 + OH- (aq) base 1 Kw = [H 3 O+] [OH-] p. H = -log [H 3 O+] p. H + p. OH = 14 p. OH = -log disoluzio azidoa [H 3 O+] > 10 -7 M [OH-] < 10 -7 M p. H< 7 [OH-] Disoluzio neutroa disoluzio basikoa [H 3 O+] < 10 -7 M [OH-] > 10 -7 M [H 3 O+] = [OH-] = 10 -7 M p. H = 7 p. H > 7
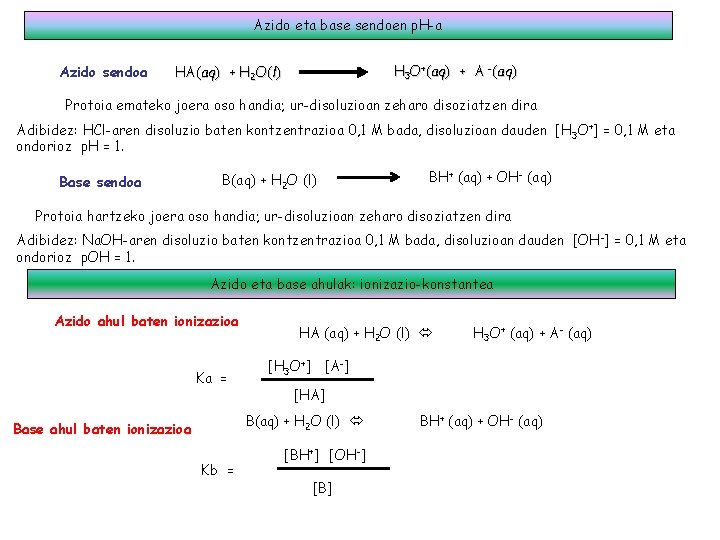
Azido eta base sendoen p. H-a Azido sendoa H 3 O+(aq) + A -(aq) HA(aq) + H 2 O(l) Protoia emateko joera oso handia; ur-disoluzioan zeharo disoziatzen dira Adibidez: HCl-aren disoluzio baten kontzentrazioa 0, 1 M bada, disoluzioan dauden [H 3 O+] = 0, 1 M eta ondorioz p. H = 1. Base sendoa B(aq) + H 2 O (l) BH+ (aq) + OH- (aq) Protoia hartzeko joera oso handia; ur-disoluzioan zeharo disoziatzen dira Adibidez: Na. OH-aren disoluzio baten kontzentrazioa 0, 1 M bada, disoluzioan dauden [OH -] = 0, 1 M eta ondorioz p. OH = 1. Azido eta base ahulak: ionizazio-konstantea Azido ahul baten ionizazioa Ka = HA (aq) + H 2 O (l) [H 3 O+] [A-] [HA] B(aq) + H 2 O (l) Base ahul baten ionizazioa Kb = H 3 O+ (aq) + A- (aq) [BH+] [OH-] [B] BH+ (aq) + OH- (aq)

Azido-base adierazleak izaera azidoak edo basikoa ahula duen substantzia da eta kolore desberdinak aurkezten ditu p. H-aren arabera HIn + H O+ + In 2 3 Forma azidoa Forma basikoa Forma azidoak , HIn, eta forma basikoak, In- , kolore ezberdinak dituzte Gatzen hidrolisia (laborategia) Gatz baten hidrolisia gatzaren ioiek urarekin egin dezaketen azido-base erreakzioa da. Azido sendotik eta base sendotik datozen gatzak adibidez: Na. Cl, Na. NO 3 , KI Ez da hidrolisi-erreakziorik sortzen p. H = 7 adibidez: Na 2 CO 3 ; Na. HCO 3 Base sendotik eta azido ahuletik datozen gatzak ; CH 3 COONa Azido ahularen base konjokatua hidrolizatzen da; p. H>7. Base ahuletik eta azido sendotik datozen gatzak adibidez: NH 4 Cl; NH 4 NO 3 Base ahularen azido konjokatua hidrolizatzen da; p. H <7. Base ahul batetik eta azido ahuletik datozen gatzak Base ahularen azido konjokatua hidrolizatzen da, eta adibidez: NH 4 CN ; (NH 4)2 CO 3 azido ahularen base konjokatua hidrolizatzen da Disoluzioaren p. H-a jatorrizko azidoaren eta basearen indar erlatiboaren araberakoa da. Azido-base balorazioak (laborategia)

Elektroi-transferentziako erreakzioak Oxidazioa: oxigenoarekin konbinatzea edo hidrogenoa galtzea CH 3 OH HCHO HCOOH H 2 S (g) + ½ O 2 (g) S (s) + H 2 O (l) Erredukzioa: oxigenoa galtzea, edo hidrogenoarekin erreakzionatzea CH 3 COCH 3 CHOHCH 3 Oxidazio-erredukzioko erreakzioa elektroi-transferentziaren bidez gertatzen den erreakzioa da. Oxidazioa: elektroien galera-prozesua da, erreduktore batek jasaten duena. Erredukzioa: elektroien irabazte-prozesua da, oxidatzaile batek jasaten duena. Oxidazio zenbakia Oxidazio-zenbakia elementuaren sinboloaren gainean +n, edo, -n, moduan idazten da. Esleipen-arauak: …………… Oxidazio-erredukzioko erreakzioak parte hartzen duten elementuen oxidazio-zenbakietan aldakuntzaren bat gertatzen da. Oxidazio-erdierreakzioa prozesu bat da, non elementu batek bere oxidazio-zenbakia handitzen duen. Erredukzio-erdierreakzioa prozesu bat da, non elementu batek bere oxidazio-zenbakia gutxitzen duen. Oxidatzaileak eta haren forma erreduzituak erredox bikote konjokatua osatzen dute eta alderantziz.
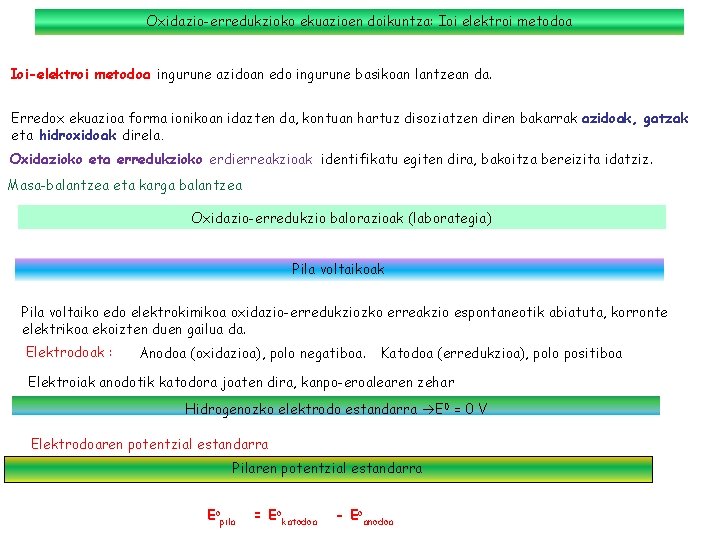
Oxidazio-erredukzioko ekuazioen doikuntza: Ioi elektroi metodoa Ioi-elektroi metodoa ingurune azidoan edo ingurune basikoan lantzean da. Erredox ekuazioa forma ionikoan idazten da, kontuan hartuz disoziatzen diren bakarrak azidoak, gatzak eta hidroxidoak direla. Oxidazioko eta erredukzioko erdierreakzioak identifikatu egiten dira, bakoitza bereizita idatziz. Masa-balantzea eta karga balantzea Oxidazio-erredukzio balorazioak (laborategia) Pila voltaikoak Pila voltaiko edo elektrokimikoa oxidazio-erredukziozko erreakzio espontaneotik abiatuta, korronte elektrikoa ekoizten duen gailua da. Elektrodoak : Anodoa (oxidazioa), polo negatiboa. Katodoa (erredukzioa), polo positiboa Elektroiak anodotik katodora joaten dira, kanpo-eroalearen zehar Hidrogenozko elektrodo estandarra E 0 = 0 V Elektrodoaren potentzial estandarra Pilaren potentzial estandarra Eopila = Eokatodoa - Eoanodoa
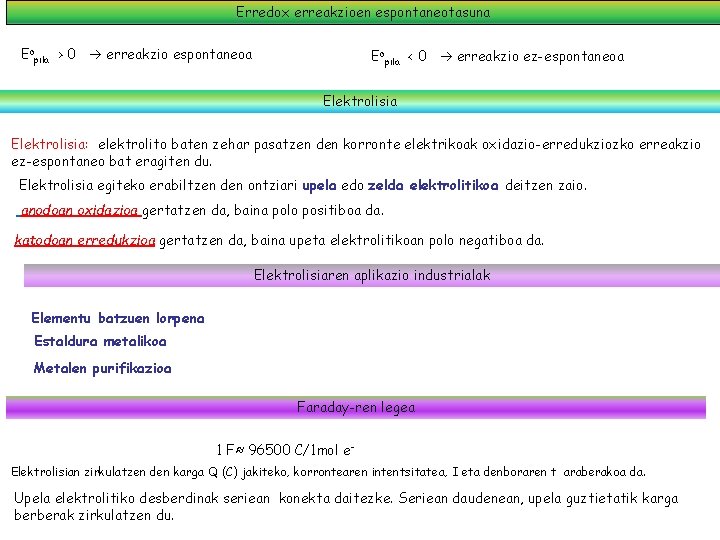
Erredox erreakzioen espontaneotasuna Eopila > 0 erreakzio espontaneoa Eopila < 0 erreakzio ez-espontaneoa Elektrolisia: elektrolito baten zehar pasatzen den korronte elektrikoak oxidazio-erredukziozko erreakzio ez-espontaneo bat eragiten du. Elektrolisia egiteko erabiltzen den ontziari upela edo zelda elektrolitikoa deitzen zaio. anodoan oxidazioa gertatzen da, baina polo positiboa da. katodoan erredukzioa gertatzen da, baina upeta elektrolitikoan polo negatiboa da. Elektrolisiaren aplikazio industrialak Elementu batzuen lorpena Estaldura metalikoa Metalen purifikazioa Faraday-ren legea 1 F≈ 96500 C/1 mol e. Elektrolisian zirkulatzen den karga Q (C) jakiteko, korrontearen intentsitatea, I eta denboraren t araberakoa da. Upela elektrolitiko desberdinak seriean konekta daitezke. Seriean daudenean, upela guztietatik karga berberak zirkulatzen du.
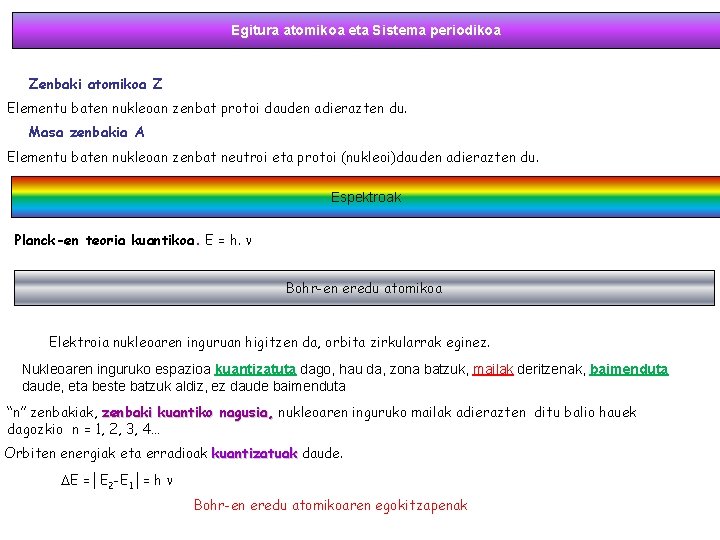
Egitura atomikoa eta Sistema periodikoa Zenbaki atomikoa Z Elementu baten nukleoan zenbat protoi dauden adierazten du. Masa zenbakia A Elementu baten nukleoan zenbat neutroi eta protoi (nukleoi)dauden adierazten du. Espektroak Planck-en teoria kuantikoa. E = h. n Bohr-en eredu atomikoa Elektroia nukleoaren inguruan higitzen da, orbita zirkularrak eginez. Nukleoaren inguruko espazioa kuantizatuta dago, hau da, zona batzuk, mailak deritzenak, baimenduta daude, eta beste batzuk aldiz, ez daude baimenduta “n” zenbakiak, zenbaki kuantiko nagusia, nukleoaren inguruko mailak adierazten ditu balio hauek dagozkio n = 1, 2, 3, 4… Orbiten energiak eta erradioak kuantizatuak daude. DE =│E 2 -E 1│= h n Bohr-en eredu atomikoaren egokitzapenak

Eredu mekaniko kuantikoa Uhina - korpuskulua bitasun edo dualitatea Nukleoaren inguruko espazioaren eskualde bat da non energia-kantitate jakineko elektroi bat aurkitzeko probabilitatea handia da. Orbital atomikoa Ziurgabetasun-printzipioa Zenbaki kuantikoak n : zenbaki kuantiko nagusia n= 1, 2, 3, 4…. Zenbaki osoak dira. Maila energetikoa adierazten du. Orbitalaren tamainarekin erlazionatuta dago. l : zenbaki kuantiko orbitala edo momentu angeluarra l = 0… …. . … n-1 Zenbaki osoak dira, balio bakoitzak azpi-maila energetikoa adierazten du. Orbitalaren formarekin erlazionatuta dago. l=0 (s); l = 1 (p); l = 2 (d); l = 3 (f) ml : zenbaki kuantiko magnetikoa ml : -l… … 0 …. . . +l ml –k erlazionatuta dago orbitak espazioan duen orientazioarekin ms : spinaren zenbaki kuantiko Elektroiaren spina: elektroiak bere ardatzaren inguruan egiten duen errotazio-higidura. + 1 2 Atomoen konfigurazio elektronikoak Eraikuntza araua Orbitalen energiaren orden hazkorra n+l araua eta : - 1 2
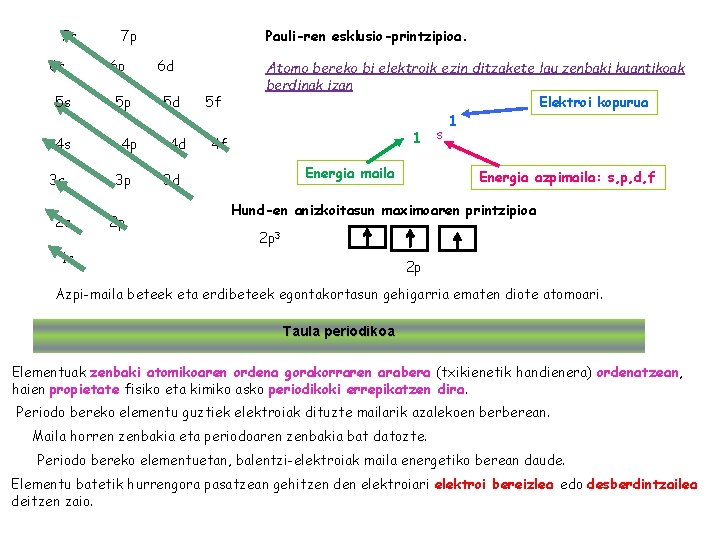
7 s 6 s 5 s 4 s 3 s 2 s Pauli-ren esklusio-printzipioa. 7 p 6 p 5 p 4 p 3 p 2 p 6 d 5 d 4 d 5 f 4 f Atomo bereko bi elektroik ezin ditzakete lau zenbaki kuantikoak berdinak izan Elektroi kopurua 1 s 1 Energia maila 3 d Energia azpimaila: s, p, d, f Hund-en anizkoitasun maximoaren printzipioa 2 p 3 1 s 2 p Azpi-maila beteek eta erdibeteek egontakortasun gehigarria ematen diote atomoari. Taula periodikoa Elementuak zenbaki atomikoaren ordena gorakorraren arabera (txikienetik handienera) ordenatzean, haien propietate fisiko eta kimiko asko periodikoki errepikatzen dira. Periodo bereko elementu guztiek elektroiak dituzte mailarik azalekoen berberean. Maila horren zenbakia eta periodoaren zenbakia bat datozte. Periodo bereko elementuetan, balentzi-elektroiak maila energetiko berean daude. Elementu batetik hurrengora pasatzean gehitzen den elektroiari elektroi bereizlea edo desberdintzailea deitzen zaio.
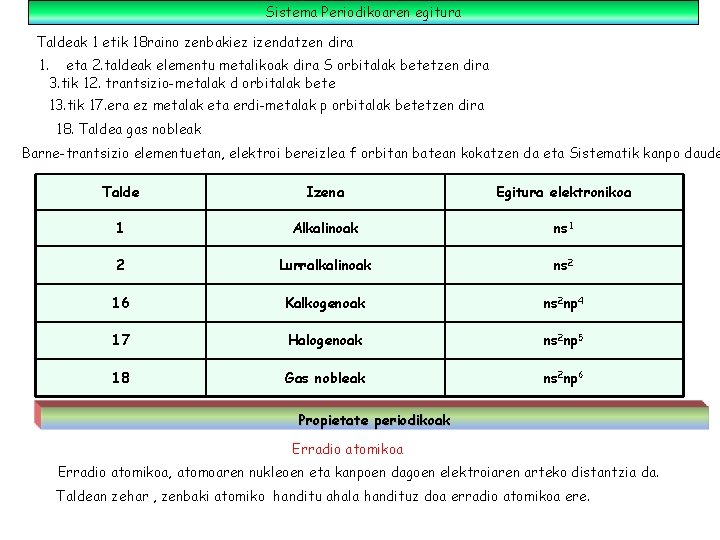
Sistema Periodikoaren egitura Taldeak 1 etik 18 raino zenbakiez izendatzen dira 1. eta 2. taldeak elementu metalikoak dira S orbitalak betetzen dira 3. tik 12. trantsizio-metalak d orbitalak bete 13. tik 17. era ez metalak eta erdi-metalak p orbitalak betetzen dira 18. Taldea gas nobleak Barne-trantsizio elementuetan, elektroi bereizlea f orbitan batean kokatzen da eta Sistematik kanpo daude Talde Izena Egitura elektronikoa 1 Alkalinoak ns 1 2 Lurralkalinoak ns 2 16 Kalkogenoak ns 2 np 4 17 Halogenoak ns 2 np 5 18 Gas nobleak ns 2 np 6 Propietate periodikoak Erradio atomikoa, atomoaren nukleoen eta kanpoen dagoen elektroiaren arteko distantzia da. Taldean zehar , zenbaki atomiko handitu ahala handituz doa erradio atomikoa ere.

Periodoan zehar , zenbaki atomiko handitu ahala gutxituz doa erradio atomikoa. Katioiak jatorrizko atomoak baino txikiagoak dira. Anioiaren erradioa atomo neutroarena baino handiagoa da. Ionizazio energia (I) : oinarrizko egoeran dagoen X atomo isolatuari elektroi bat kentzeko behar den gutxieneko energia da. X (g) + I X+ (g) + 1 e. Taldean zenbaki atomikoa handitu ahala txikiagoa da ionizazio energia. Periodoan zenbaki atomikoarekin batera handitzen da. Atomoak 2. , 3. , … elektroia emateko behar dituen ionizazio-energiak gero eta handiagoak dira. Afinitate elektronikoa (A): atomoak elektroi bat harrapatzen duenean askatzen den energia. X (g) + 1 e- X- (g) + A Periodoan zenbaki atomikoarekin batera handitzen da Taldean zenbaki atomikoarekin batera txikitzen da. Elektronegatibotasuna Molekula bateko atomo batek loturako elektroiak erakartzeko duen ahalmena neurtzen du. Periodoetan handitu egiten da zenbaki atomikoa handitu ahala. Taldeetan handitu egiten da zenbaki atomikoa txikiagotu ahala. Izaera metalikoa Periodo batean izaera metalikoa zenbaki atomikoarekin batera txikitzen da. Talde batean izaera metalikoa zenbaki atomikoarekin batera handitzen da. Propietateen aldaketa graduala dela medio, elementu batzuk ez dira ez erabat metalak, eta horregatik, erdimetalak deitu zaie.

Lotura kimikoa Substantziak eratzen dituzten ioien, atomoen eta molekulen arteko elkarketa da. Oro har, atomoek elkarri lotzen zaizkionean zortzikote arau betetzen dute. Gas nobleak bereziki egonkorrak dira 8 elektroi dituztelako (ns 2 np 6 He ezik). Lotura ionikoa elektronegatibibotasuna oso ezberdina duten elementuen artean ematen da, hau da metal eta ez-metal artean. Atomoek sistema periodikoan gertuen duten gas noblearen egitura elektronikoa lortzeko elektroiak ematen edo hartzen dituzte (ioi bihurtuz). Elementu baten balentzia ionikoa da elementuaren atomoek ioi positibo edo negatibo bilakatzen lortzen duten karga. Lotura ionikoa ioi positiboen eta ioi negatiboen arteko indar elektrostatikoek sorrarazten duten elkarketa da. Elkarketa horren ondorioz, sare kristalino ionikoak eratzen dira. Koordinazio-zenbakiak (koordinazio indizea) sare kristalinoan ioi batek kontrako zeinuko zenbat ioi dituen inguruan, denak harengandik distantzia berera. Konposatu ioniko baten sare-energia, U, da egoera gaseosoan dauden ioietatik, eta haien artean batere elkarrekintzarik ez dagoela, mol bat kristal ioniko solido eratzeko behar den energia. Lotura kobalentea Bi atomok elektroi bikote bat edo gehiago partekatzen dutenean gertatzen den elkarketa da. Bi atomo elektroi bikote bat konpartitzen dutenean lotura kobalente bakuna da. Bi elektroi bikote elkarbanatzean lotura kobalente bikoitza da eta hiru elektroi bikote konpartitzean sortzen den lotura hirukoitza da.

Lotura Kobalente Lewis-en arabera Lotura kobalenteak irudikatzeko, puntuen ordez marrak ager daitezke elkartutako bi atomoen artean. Partekatutako elektroiak, elektroi lotzaileak, dira. Loturan parte hartzen ez duten elektroiak, elektroi ez-lotzaileak, dira. Bikote ez-lotzaileak marra batez ere ager daitezke. Elektroi partekatuak bi atomoetako batek bakarrik eman baditu, lotura kobalente koordinatua edo datiboa dela diogu. Elementu baten kobalentzia elementuak lotura kobalenteak eratzeko duen ahalmena da. Molekulen geometria balentzi mailako elektroi bikoteen aldarapen metodoa BMEBA Atomo zentrala inguratzen duten elektroi lotzaileak eta askeak orientatzen direnean, ahalik eta gehien hurbiltzen dira nukleoraeta aldi berean, urrunduz doaz elkarrengandik, beren arteko aldarapena txikiagoa izateko. Lotura kobalente apolarrean, elektroiak berdin banatzen dira bi atomoen artean eta dentsitatea elektronikoa, simetrikoa da bi nukleoekiko. Lotura kobalente polarrean loturako atomoetako bat bestea baino elektronegatiboagoa da, eta beregana erakartzen du partekatzen duten karga elektrikoa. Lotura kobalenteetan polaritatea neurtzeko erabiltzen den magnitudea momentu dipolarra µ da. Molekula polarra: lotura polarizatua eta lotura polarizatuaren orientazioa egokia izango da. Molekulen arteko indarrak mr ≠ 0 Van der Waals-en indarrak: dipolo-dipolo indarrak; dipolo-dipolo induzitua indarrak; sakabanaketa indarrak Hidrogeno zubiak: Hidrogeno-lotura eratzeko hidrogeno atomo batek lotura kobalente oso polarizatua eratu behar du oso txikia eta askoz elektronegatiboagoa den beste atomoarekin (F, O edo N) Lotura metalikoa Metalen atomoen artean diharduen elkarketa indarra da. Indar horrek sare kristalino metalikoaren egonkortasuna sortzen du.
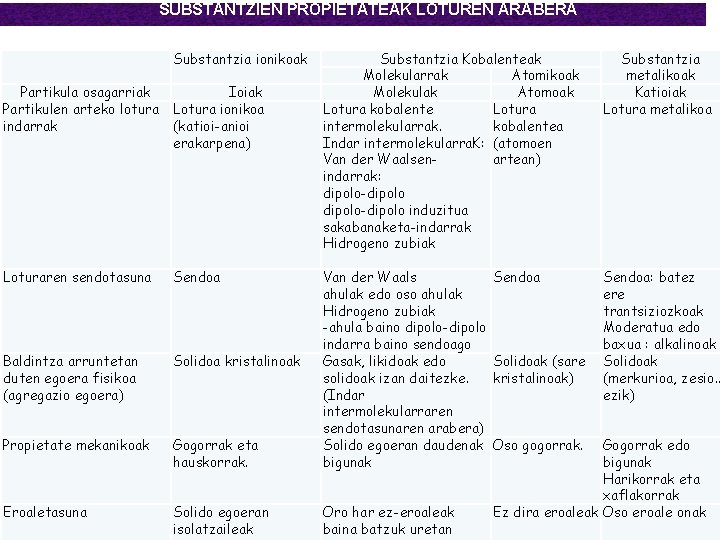
SUBSTANTZIEN PROPIETATEAK LOTUREN ARABERA Substantzia ionikoak Partikula osagarriak Partikulen arteko lotura indarrak Ioiak Lotura ionikoa (katioi-anioi erakarpena) Loturaren sendotasuna Sendoa Baldintza arruntetan duten egoera fisikoa (agregazio egoera) Solidoa kristalinoak Propietate mekanikoak Gogorrak eta hauskorrak. Substantzia Kobalenteak Molekularrak Atomikoak Molekulak Atomoak Lotura kobalente Lotura intermolekularrak. kobalentea Indar intermolekularra. K: (atomoen Van der Waalsenartean) indarrak: dipolo-dipolo induzitua sakabanaketa-indarrak Hidrogeno zubiak Van der Waals Sendoa ahulak edo oso ahulak Hidrogeno zubiak -ahula baino dipolo-dipolo indarra baino sendoago Gasak, likidoak edo Solidoak (sare solidoak izan daitezke. kristalinoak) (Indar intermolekularraren sendotasunaren arabera) Solido egoeran daudenak Oso gogorrak. bigunak Eroaletasuna Solido egoeran isolatzaileak Oro har ez-eroaleak baina batzuk uretan Substantzia metalikoak Katioiak Lotura metalikoa Sendoa: batez ere trantsiziozkoak Moderatua edo baxua : alkalinoak Solidoak (merkurioa, zesio. . ezik) Gogorrak edo bigunak Harikorrak eta xaflakorrak Ez dira eroaleak Oso eroale onak
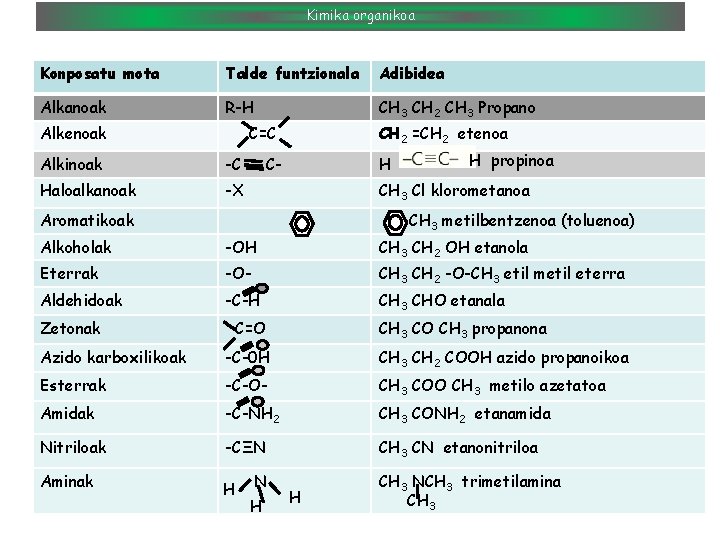
Kimika organikoa Konposatu mota Talde funtzionala Adibidea Alkanoak R-H CH 3 CH 2 CH 3 Propano Alkenoak C=C Alkinoak -C Haloalkanoak -X CH 2 =CH 2 etenoa C- H H propinoa CH 3 Cl klorometanoa Aromatikoak -CH 3 metilbentzenoa (toluenoa) Alkoholak -OH CH 3 CH 2 OH etanola Eterrak -O- CH 3 CH 2 -O-CH 3 etil metil eterra Aldehidoak -C-H CH 3 CHO etanala Zetonak C=O CH 3 CO CH 3 propanona Azido karboxilikoak -C-0 H CH 3 CH 2 COOH azido propanoikoa Esterrak -C-O- CH 3 COO CH 3 metilo azetatoa Amidak -C-NH 2 CH 3 CONH 2 etanamida Nitriloak -CΞN CH 3 CN etanonitriloa Aminak H N H H CH 3 NCH 3 trimetilamina CH 3

Isomeria Formula molekular berbera izanda, egitura edo konfigurazio espazial desberdinak dute. Kate-isomeria Atomo batzuek edo atomo talde batzuek karbonodun katean duten kokapenagatik bakarrik desberdintzen diren konposatuena da. Funtzio-isomeria Karbonodun katean talde funtzionalaren posizioan desberdintzen diren isomeroetan agertzen da. Posizio-isomeria Isomeroak talde funtzionalean desberdintzen direnean agertzen dira. Erreakzio organikoak Ordezkapen-erreakzioak A-B + C-D A-C + B-D A+B C Adizio-erreakzioak Eliminazio (ezbaketa)-erreakzioak Errekuntza Oxidazio-erredukzioa A B+C Exotermikoa Konposatu baten hidrogenoaren edukiera handitzen denean edo oxigenoaren edukiera gutxitzen denean, konposatu hori erreduzitu dela esaten da, eta, kontrakoa gertatzen denean, konposatu hori oxidatu dela esaten da.
- Slides: 20