Teoria cinetica dei Gas Ideali Velocit quadratica media












- Slides: 13

Teoria cinetica dei Gas Ideali Velocità quadratica media Termodinamica dei gas ideali

Dalla meccanica alla termodinamica • In Meccanica: lo stato di una particella è definito quando siano note, posizione (x, y, z) e velocità (vx, vy, vz), quindi 6 diverse variabili per ogni punto in moto. • In termodinamica: il concetto di stato deve essere ridefinito. I sistemi termodinamici, generalmente costituiti da un gran numero di particelle, tipicamente N (numero di Avogadro, ~1023), non sarebbe possibile conoscere 6 N variabili. • In Termodinamica non si può parlare più di determinismo della fisica Lo studio delle proprietà collettive di un “grand ensemble” richiede qualche riflessione. • Le proprietà di un insieme numeroso di particelle non sono la semplice somma delle proprietà delle singole particelle. • Per comprendere le relazioni fra la fisica di una singola particella e la fisica dei sistemi collettivi dovremo conoscere un po’ di statistica

Definizione di Gas Perfetto Per avere un gas perfetto si devono soddisfare le seguenti condizioni: 1. Disporre di un gran numero di particelle (Grand Ensemble) 2. Le molecole del gas devono essere puntiformi ed identiche tra loro (non devono avere un volume proprio); 3. Le molecole si devono muovere in modo totalente caotico (tutte le direzioni devono essere equiprobabili); 4. Le molecole devono interagire tra loro e con le pareti del recipiente mediante urti perfettamente elastici (non vi deve essere dispersione di energia durante gli urti); 5. Le molecole di un gas perfetto devono obedire solo alle leggi di Newton (le traiettorie dopo ogni urto devono essere rettiline).

Gas Ideali • Si può osservare che qualunque tipo di gas, confinato in un recipiente a bassa densità, segue la legge dei gas perfetti: p. V = n. RT. n è il numero di moli R = 8, 31 [J/mol K] costante dei gas • L’equazione di stato dei gas si può esprimere anche in funzione del numero di molecole N e diventa: p. V = Nk. T • con k = R/NA ed NA= 6, 02 x 1023 (Numero di Avogadro) e T temperatura assoluta (T sempre positiva) • L’importanza dell’equazione dei gas ideali è legata alla sua semplicità e al fatto che per basse densità è valida per tutti i tipi di gas (indipendente dalla specie atomica). • Anche l’aria che respiriamo soddisfa le condizioni dei gas perfetti.

Pressione di un gas perfetto • La variazione della quantità di moto lungo l’asse x è: Dpx = (-mvx) – (mvx) = -2 mvx • il tempo necessario per andare e tornare fra due pareti opposte, è 2 L = D tvx quindi Dt = 2 L/vx • la forza trasferita sulla parete è: • Questa è la forza impressa da una particella su una parete di lato L. (ATTENZIONE: P rappresenta la pressione e la lettera px la quantità di moto). • n numero di particelle, vx 2 velocità quadratica media nella direzione x. • A causa del moto caotico, la velocità quadratica media è 1/3 di vx P = 1/3 (n. M/V) v 2 qm

Velocità quadratica media • dalla formula p = (n. Mv 2 qm)/3 V p. V = n. Mv 2 qm/3 si vede che il prodotto p. V, dipende dalla velocità v delle singole particelle • e ricordando l’equazione di stato dei gas perfetti si avrà: • La velocità quadratica media è molto alta e dipende: dalla radice della temperatura, espressa in Kelvin, e dall’inverso della massa molare. • Domanda: Perché, se la velocità molecolare a temperatura ambiente è così alta, il tempo necessario a sentire l’odore di un fiala di profumo è di qualche minuto?

Cammino libero medio • Il camino fra due urti successivi è il cammino libero. La somma dei cammini divisa per il numero delle collisioni da il cammino libero medio che risulta essere: d = diametro della particella V = volume del contenitore N = numero di Avogadro • Al livello del mare l’aria ha un cammino libero medio di 0, 1 mm. A 100 km l = 16 cm. A 300 km l = 20 km. Come si ricava questa formula?

Spiegazione cammino libero medio • Nel tempo Dt una particella percorrerà una distanza pari v. Dt (dove v è la velocità presunta, velocità di Maxwell) in un cilindro di sezione pd 2. Il volume del cilindro è (pd 2)(v. Dt) • Il numero delle collisioni sarà uguale al numero delle particelle nel cilindro. Infatti possiamo supporre che la particella che si muove ha diametro 2 d mentre le altre, ipotizzate ferme, siano senza diametro. Distanza percorsa Volume del cilindro A cui va aggiunto un fattore 1/√ 2 per tener conto della differenza fra la velocità vm media su tutto il contenitore e la velocità relativa alle altre particelle vrel = √ 2 vm

Energia cinetica • Con il solito modello, l’energia cinetica traslazionale media sarà uguale all’energia cinetica di una particella con velocità vqm • Sostituendo a vqm il valore funzione della temperatura e della massa: Dove k. B costante di Boltzmann (vale 1. 38 x 10 -23). Questa formula ci dice che l’Energia cinetica media di un gas non dipende dal tipo di gas esaminato, ma solo dalla sua temperatura.

Significato di energia interna • L’energia interna Eint di un gas è la somma delle energie cinetiche delle singole particelle e siccome ogni particella ha una Energia cinetica E =(3/2)k. BT l’energia totale di un gas dipenderà solo dalla temperatura. Supponendo un gas formato da n. NA molecole avremo che L’Energia interna media sarà: n = numero di moli NA = numero di Avogadro Nello stato di gas perfetto, l’Energia interna di un gas Eint dipende solo dalla sua temperatura. Quindi misurare la temperatura è come sapere quanto vale la sua Eint

Esperimento di Stern • Nel 1926 il fisico tedesco Otto Stern ebbe l'idea di verificare la teoria di Maxwell. • Riscaldando del mercurio in un forno ad alta temperatura, ottenne un fascio di molecole che veniva iniettato in una camera in alto vuoto. • Nella camera ruotavano due dischi D 1 e D 2 dotati di due fenditure e sfasate l'una rispetto all'altra di un angolo noto. • Misurando la velocità dei dischi che permettevano ad una molecola di attraversare entrambe le due fenditure si poteva risalire alla velocità delle molecole di mercurio. • Quindi, graficando il numero di particelle che raggiungono il rivelatore P in funzione delle velocità dei dischi si ottiene la distribuzione delle velocità delle molecole a temperature diverse, cioè la distribuzione di Maxwell

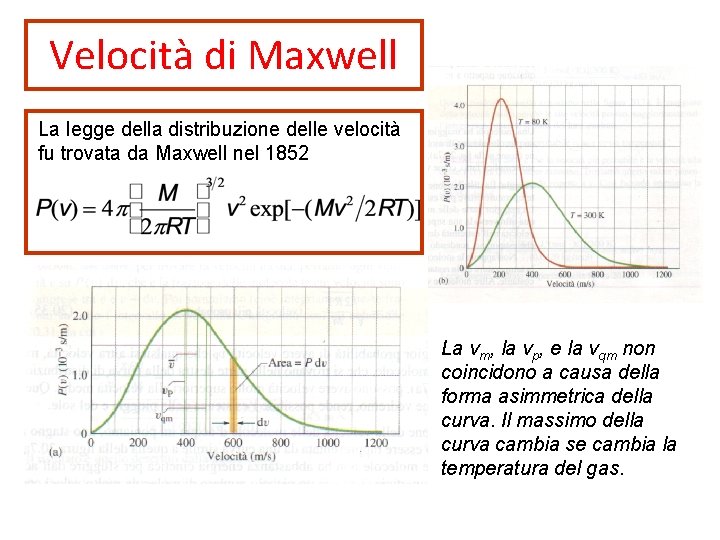
Velocità di Maxwell La legge della distribuzione delle velocità fu trovata da Maxwell nel 1852 La vm, la vp, e la vqm non coincidono a causa della forma asimmetrica della curva. Il massimo della curva cambia se cambia la temperatura del gas.

Distribuzione delle velocità • La curva ci da la probabilità di trovare un certo numero di particelle, P(v) dv, nell’intorno di una definita velocità. L’area sottesa dalla curva è il numero delle particelle costituenti il gas. Pertanto: • La velocità media sarà data dalla soluzione: • Allo stesso modo si può trovare la media della velocità quadratica • La velocità più probabile si trova ponendo uguale a zero la derivata di P(v)