Tema 9 Reaccions electroqumiques Electroqumica Part de la















- Slides: 16

Tema 9 Reaccions electroquímiques

Electroquímica Part de la química que estudia la interconversió entre l’energia elèctrica i l’energia química. Tracta de l’ús De les reaccions químiques per a produir electricitat (pila) De l’electricitat per a produir reaccions químiques (electròlisi)

CONTINGUT 1. - Reaccions redox. 2. - Termodinàmica de sistemes electroquímics. Piles galvàniques. 3. - Força electromotriu de les piles. Potencials d’elèctrode. 4. - Dependència de la fem amb les concentracions. Equació de Nernst. 5. - Corrosió.

1 REACCIONS REDOX. Reacció d’oxidació-reducció: Aquella reacció en què ocorre una transferència d’electrons. Zn + Cu 2+ « Zn 2+ + Cu Zn « Zn 2+ + 2 e- Semireacció d’oxidació Zn perd electrons: s’oxida; és l’agent reductor Cu 2+ + 2 e- « Cu Semireacció de reducció Cu 2+ guanya electrons: es redueix; és l’agent oxidant Intervenen dos parells redox conjugats Zn 2+/Zn Cu 2+/Cu

CO + ½ O 2 « CO 2 Com posar de manifest la transferència electrònica? Mitjançant els estats d’oxidació A cada element li assignem un estat d’oxidació: +2 -2 0 +4 -2 CO + ½ O 2 « CO 2 Una reacció serà redox si hi ha canvis en eixos estats. Avantatges Proporciona un mecanisme per reconéixer reaccions redox Ajuda a ajustar reaccions redox [Batxiller]

2 TERMODINÀMICA DE SISTEMES ELECTROQUÍMICS. PILES GALVÀNIQUES. Sistemes electroquímics: Aquells on ocorren reaccions de transferència d’electrons. Zn Cu Cu 2+ SO 42 - Zn 2+ Zn + Cu 2+ ® Zn 2+ + Cu Reacció per contacte directe. Així no és un dispositiu útil per generar corrent elèctric. Pila electroquímica: Dispositiu en el qual es produeix un corrent elèctric (flux d’e- a través d’un circuit) gràcies a una reacció espontània (pila galvànica o voltaica) o en el qual s’utilitza corrent elèctric per dur a terme una reacció química no espontània (cèl×lula electrolítica).

Luigi Galvani (1737 -1798) Alessandro Giuseppe Antonio Anastasio Volta (1745 -1827)

Pila Daniell (-) Zn ® Zn 2+ + 2 e. Oxidació (+) Cu 2+ + 2 e- ® Cu Reducció Zn (s) | Zn 2+ (1 M) || Cu 2+ (1 M) | Cu(s) John Frederic Daniell (1790 -1845)

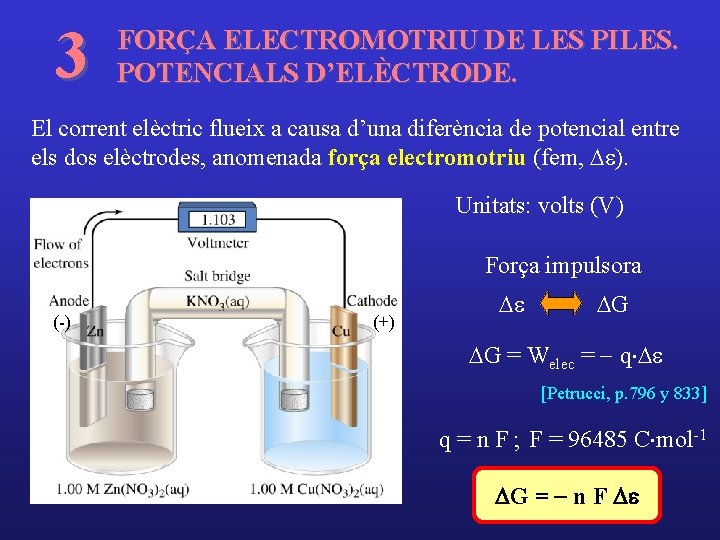
3 FORÇA ELECTROMOTRIU DE LES PILES. POTENCIALS D’ELÈCTRODE. El corrent elèctric flueix a causa d’una diferència de potencial entre els dos elèctrodes, anomenada força electromotriu (fem, De). Unitats: volts (V) Força impulsora (-) (+) De DG DG = Welec = - q×De [Petrucci, p. 796 y 833] q = n F ; F = 96485 C×mol-1 DG = - n F De

DG = - n F De • Reacció espontània: DG < 0 Þ De > 0 • Reacció no espontània: DG > 0 Þ De < 0 (la reacció espontània serà l’inversa) • Equilibri: DG = 0 Þ De = 0 (no es produeix energia elèctrica; la pila s’ha esgotat) Michael Faraday (1791 -1867) En condicions estàndard: DGº = - n F Deº (Concentracions dels ions = 1 M) Deº és una propietat intensiva

En lloc de tabular valors de Deº de totes les piles, tabulem potencials d’elèctrode • S’escull un elèctrode de referència al qual per conveni se li assigna el valor de potencial zero: Elèctrode estàndard d’hidrogen. 2 H+ (aq) + 2 e- « H 2 (g) • Es construeixen piles amb un elèctrode d’hidrogen i amb un altre, el potencial del qual volem esbrinar, i es mesura la fem de la pila. • Eixa fem serà el potencial estàndard de l’altre elèctrode. eº = 0. 00 V

Es tabulen potencials estàndard (eº) de reducció ß Sèrie electroquímica A major eº, major tendència a reduir-se té l’espècie oxidada del parell redox (més oxidant és). p. ex. : Zn 2+ + 2 e- « Zn Cu 2+ + 2 e- « Cu eº = -0. 76 V eº = +0. 34 V Més tendència a reduir-se; més oxidant La fem d’una pila es calcula com: Deº = eº(càtode) - eº(ànode) p. ex. : 0. 34 – (-0. 76) = 1. 10 V [reducció] [oxidació] Perquè funcione la pila (reacció espontània): Deº > 0

4 DEPENDÈNCIA DE LA FEM AMB LES CONCENTRACIONS. EQUACIÓ DE NERNST. Si les condicions no són estàndard, quant val la fem? DG = DGº + RT ln Q DG = - n F De DGº = - n F Deº [Tema 4] - n F De = - n F Deº + RT ln Q Equació de Nernst A 25ºC :

1920 Premi Nobel de Química “En reconeixement al seu treball en termoquímica”. Walther Hermann Nernst (1864 -1941) [http: //nobelprize. org/chemistry/laureates/1920/index. html]

Altres aplicacions de l’equació de Nernst a) Obtenció de constants d’equilibri de reaccions redox En l’equilibri: De = 0 i Q = Keq b) Obtenció d’eº en condicions no estàndard

5 CORROSIÓ. En qué consisteix? Quines són les semireaccions implicades? Quines reaccions posteriors originen el rovell? Com afecta el p. H? Com es pot previndre? - Recobriments - Galvanizat - Protecció catòdica [Petrucci, tema 21, p. 849 -850]