Tema 4 Lequilibri en les reaccions qumiques Tema

Tema 4 L’equilibri en les reaccions químiques
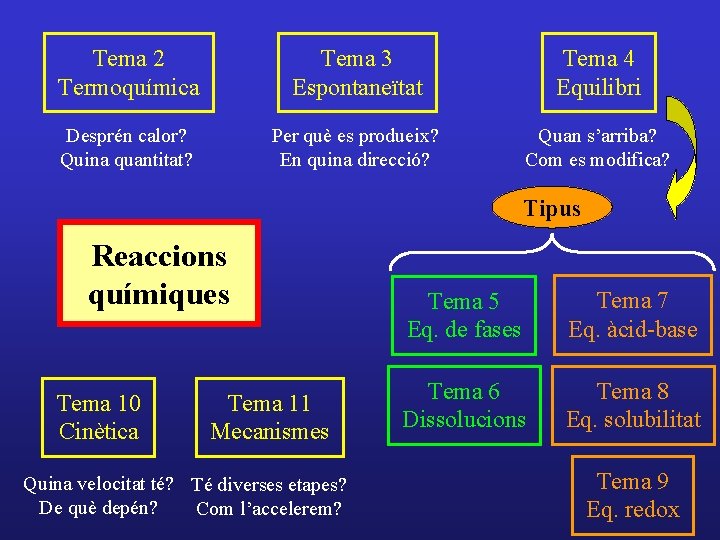
Tema 2 Termoquímica Tema 3 Espontaneïtat Tema 4 Equilibri Desprén calor? Quina quantitat? Per què es produeix? En quina direcció? Quan s’arriba? Com es modifica? Tipus Reaccions químiques Tema 10 Cinètica Tema 11 Mecanismes Quina velocitat té? Té diverses etapes? De què depén? Com l’accelerem? Tema 5 Eq. de fases Tema 7 Eq. àcid-base Tema 6 Dissolucions Tema 8 Eq. solubilitat Tema 9 Eq. redox
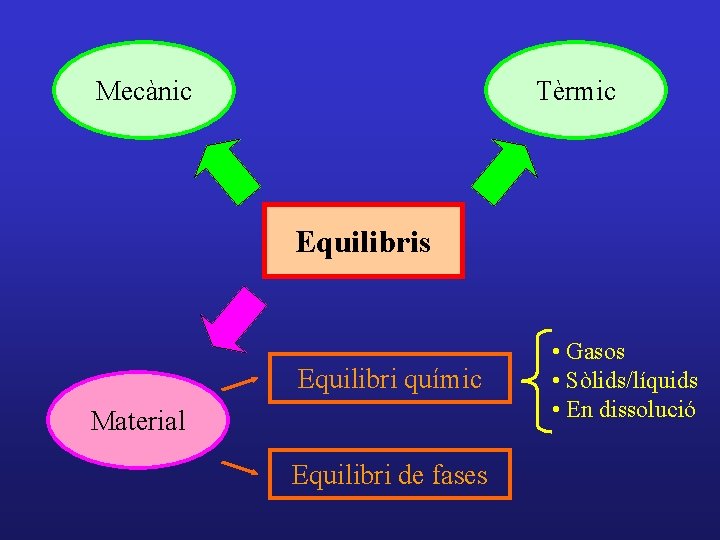
Mecànic Tèrmic Equilibris Equilibri químic Material Equilibri de fases • Gasos • Sòlids/líquids • En dissolució

CONTINGUT 1. - Aspectes bàsics de l’equilibri químic. 2. - Condició general de l’equilibri químic. 3. - Equilibri químic en sistemes gasosos ideals. 4. - Equilibris heterogenis. 5. - Variació de la constant d’equilibri amb la temperatura. 6. - Principi de Le Châtelier.

1 ASPECTES BÀSICS DE L’EQUILIBRI QUÍMIC. Estat d’equilibri: estat en què la composició del sistema es manté fixa. 1. 1. Perspectiva cualitativa. • Equilibri dinàmic. • Els sistemes evolucionen espontàniament cap a un estat d’equilibri. • Les propietats de l’estat d’equilibri són les mateixes, independentement de la direcció des de la qual s’arriba. 1. 2. Perspectiva cuantitativa. Llei d’acció de masses a. A + b. B « c. C + d. D
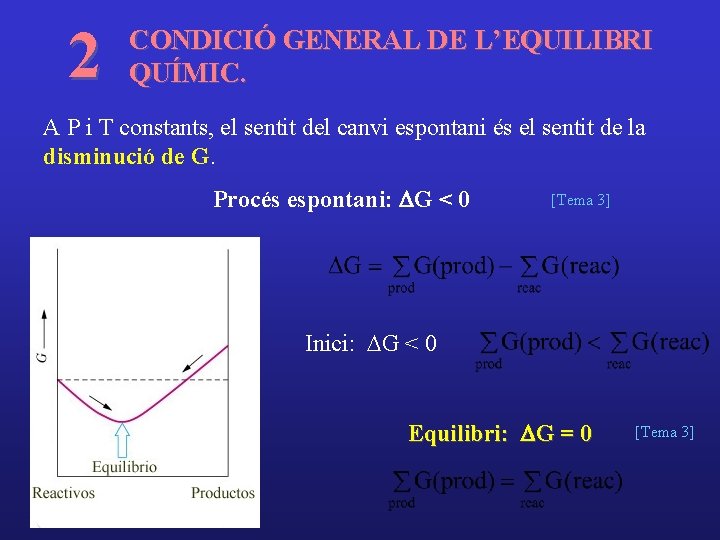
2 CONDICIÓ GENERAL DE L’EQUILIBRI QUÍMIC. A P i T constants, el sentit del canvi espontani és el sentit de la disminució de G. Procés espontani: DG < 0 [Tema 3] Inici: DG < 0 Equilibri: DG = 0 [Tema 3]

3 EQUILIBRI QUÍMIC EN SISTEMES GASOSOS IDEALS. EQUILIBRI HOMOGENI Per a una mescla de gasos ideals: [Levine, pg 175 -177] Q : Quocient de reacció Isoterma de reacció
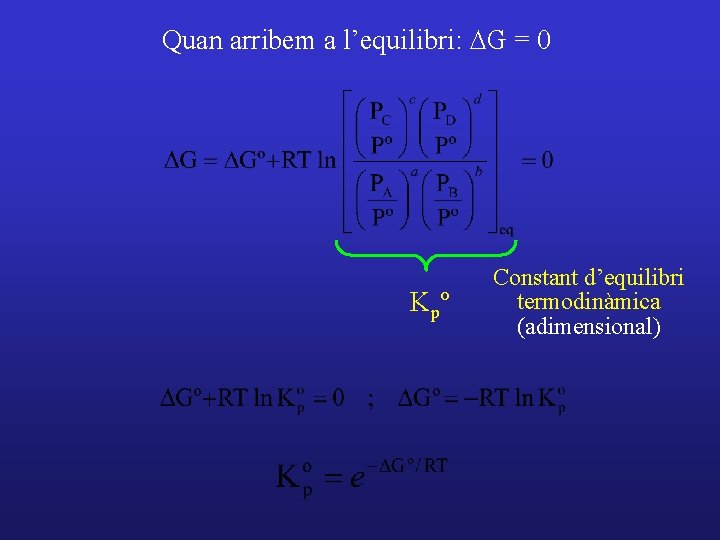
Quan arribem a l’equilibri: DG = 0 Kpº Constant d’equilibri termodinàmica (adimensional)

Conseqüències: • Si DGº >> 0 ; Kpº << 1 : poca tendència r ® p • Si DGº << 0 ; Kpº >> 1 : molta tendència r ® p • Kpº > 0 i depén de DGº • DGº només depén de T; Kpº també. • Disposem de 2 formes de determinar Kpº

Cap a on evoluciona la reacció? • Si Q < Kpº DG < 0 r ® p espontània • Si Q > Kpº DG > 0 r ® p no espontània (p ® r espontània) • Si Q = Kpº DG = 0 Equilibri

Altres expressions de la constant d’equilibri Kp (dimensional) En funció de les concentracions: (Pº)-Dn [Petrucci, pg 635] Kp = Kc (RT)Dn Si Dn = 0 K pº = K p = K c

4 EQUILIBRIS HETEROGENIS. Aquells en què les substàncies es troben en fases diferents p. ex. : Ca. CO 3 (s) « Ca. O (s) + CO 2 (g) La situació d’equilibri no es veu afectada per la quantitat de sòlid o líquid, sempre i quan aquestes substàncies estiguen presents. La constant d’equilibri és independent de les quantitats de sòlids i líquids en l’equilibri. Ca. CO 3 (s) « Ca. O (s) + CO 2 (g) Kc = [CO 2]

5 VARIACIÓ DE LA CONSTANT D’EQUILIBRI AMB LA TEMPERATURA. Com podem modificar la situació d’equilibri? Q = Kpº 1 Canviant la constant d’equilibri 2 Canviant Q

1 Canviant la constant d’equilibri Canviant la temperatura Ecuació de van’t Hoff

1901 Primer premi Nobel de Química “En reconeixement als extraodinaris serveis que ha prestat amb el descobriment de les lleis de la dinàmica química i la pressió osmòtica en dissolucions”. Jacobus Henricus van’t Hoff [http: //nobelprize. org/chemistry/laureates/1901/index. html] Ecuació integrada de van’t Hoff (1852 -1911) Si DHº és constant

Conseqüències: T 2 > T 1 a) Si DHº > 0 (endotèrmica) T Kpº Quan augmenta T s’afavoreix la formació de productes. Es desplaça cap a la dreta.

Conseqüències: T 2 > T 1 b) Si DHº < 0 (exotèrmica) T Kpº ¯ Quan augmenta T s’afavoreix la formació de reactius. Es desplaça cap a l’esquerra.

Conseqüències: T 2 > T 1 c) Si DHº = 0 La constant d’equilibri no canvia amb T

6 PRINCIPI DE LE CH TELIER. Com podem modificar la situació d’equilibri? 2 Canviant Q Canviant la resta de factors (mols de reactius, productes, P, V, . . . )

Principi de Le Châtelier “Si un sistema químic que està en equilibri se sotmet a una pertorbació que canvie qualsevol de les variables que determina l’estat d’equilibri, el sistema evolucionarà per tal de contrarestar l’efecte de la pertorbació”. Henri Louis Le Châtelier (1850 -1936)

6. 1. Efecte d’un canvi de temperatura (a P constant) • Si DHº > 0 (endotèrmica): T Þ es desplaçarà a la dreta • Si DHº < 0 (exotèrmica): T Þ es desplaçarà a l’esquerra 6. 2. Efecte de l’addició/sustracció de mols de reactius o productes gasosos (a T i V constants) • Si afegesc productes: Q > Kc Þ es desplaçarà a l’esquerra • Si afegesc reactius: Q < Kc Þ es desplaçarà a la dreta

6. 3. Efecte d’un canvi de volum (a T constant) La disminució de V fa que la concentració total de molècules augmente. El sistema tendirà a reduir-la. ß Es desplaça cap a on hi haja un menor nombre de mols gasosos 6. 4. Efecte de la pressió total (a T constant) Un augment de P té el mateix efect que una disminució de V ß Es desplaça cap a on hi haja un menor nombre de mols gasosos

6. 5. Addició d’un gas inert (a T i V constants) No altera l’equilibri 6. 6. Addició d’un catalitzador No afecta a l’equilibri 6. 7. Addició d’un reactiu/producte sòlid o líquid No altera l’equilibri
- Slides: 23