Szjregi daganatok molekulris patolgija Tmr Jzsef SE Klinikai












- Slides: 41

Szájüregi daganatok molekuláris patológiája Tímár József SE Klinikai Központ, 2. sz. Patológiai Intézet

FFI • • Rosszindulatú daganatok előfordulása hazánkban Tüdő Kolorektális Fejnyaki lhcc Prosztata Húgyhólyag Vérképző-nyirok Gyomor Vese 6800 4900 3800 3700 2000 1700 1300 1200 • 34000 • • • Emlő Kolorektális Tüdő Vérképző Méhtest Petefészek Méhnyak Gyomor Vese • 32000 Fejnyaki: orális, faringeális Laringeális, glottikus 2006 Nő 7400 4000 3700 1800 1300 1100 1000 900

ffi • • • Rosszindulatú daganatok miatti halálozás hazánkban nő Tüdő Kolorektális Fejnyaki lc Prosztata Gyomor Vérképző Hasnyálmirigy Húgyhólyag Nyelőcső Máj 17000 5300 2400 1300 1000 980 840 800 560 500 2005 • • • Tüdő Emlő Kolorektális Vérképző Hasnyálmirigy Gyomor Petefészek Epehólyag Méhnyak Méhtest 13400 2200 2100 860 800 740 600 460 400 380

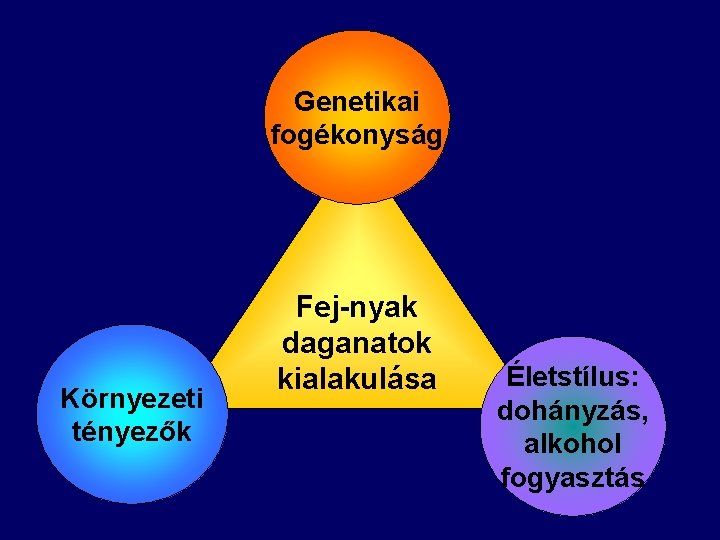
Genetikai fogékonyság Környezeti tényezők Fej-nyak daganatok kialakulása Életstílus: dohányzás, alkohol fogyasztás

Fejnyaki rákok etiológiája • • Kémiai karcinogenezis: Alkoholizmus Dohányzás Szájhigiéne

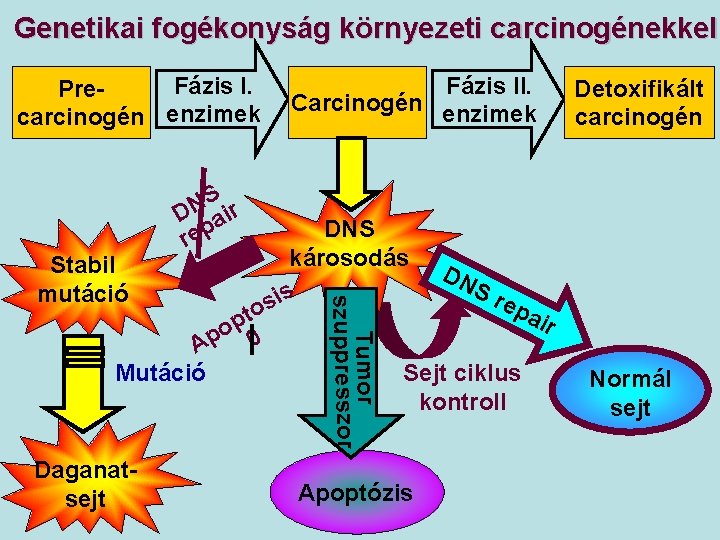
Genetikai fogékonyság környezeti carcinogénekkel Fázis I. Precarcinogén enzimek to p o 0 p A Mutáció DNS károsodás sis Daganatsejt Tumor szuppresszor Stabil mutáció S N D air rep Fázis II. Carcinogén enzimek DN Sr ep air Sejt ciklus kontroll Apoptózis Detoxifikált carcinogén Normál sejt

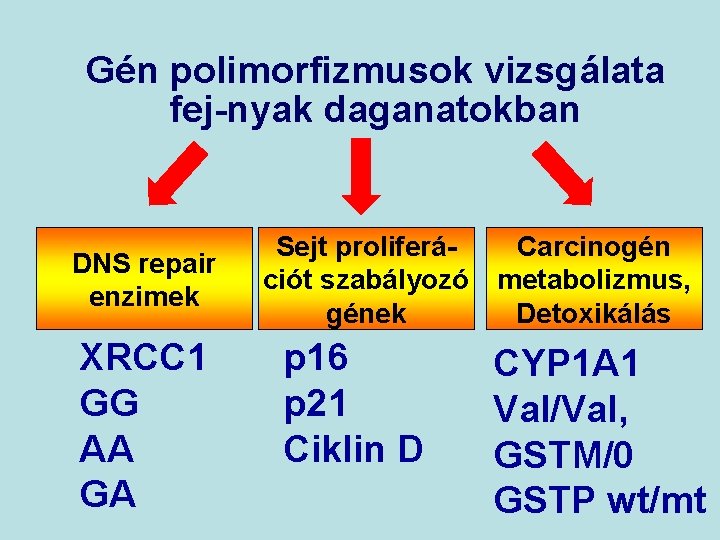
Gén polimorfizmusok vizsgálata fej-nyak daganatokban DNS repair enzimek XRCC 1 GG AA GA Sejt proliferáCarcinogén ciót szabályozó metabolizmus, gének Detoxikálás p 16 p 21 Ciklin D CYP 1 A 1 Val/Val, GSTM/0 GSTP wt/mt

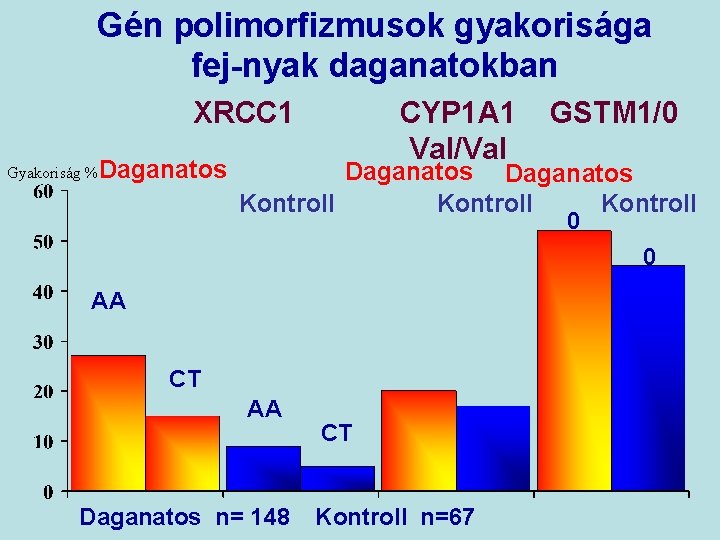
Gén polimorfizmusok gyakorisága fej-nyak daganatokban XRCC 1 Gyakoriság % Daganatos CYP 1 A 1 Val/Val GSTM 1/0 Daganatos Kontroll 0 0 AA CT AA Daganatos n= 148 CT Kontroll n=67

Gén polimorfizmusok vizsgálata fej-nyak daganatokban 1. DNS repair enzimek XRCC 1 AA genotípus tumor mintákban szignifikánsan (400%) magasabb a kontroll populációhoz viszonyítva. 2. GSTM 0 fenotípus daganatos és kontroll csoportban közel azonos (52%, 48%) 3. Dohányzó csoportban az AA homozigóta és GA heterozigóták aránya megnövekszik.

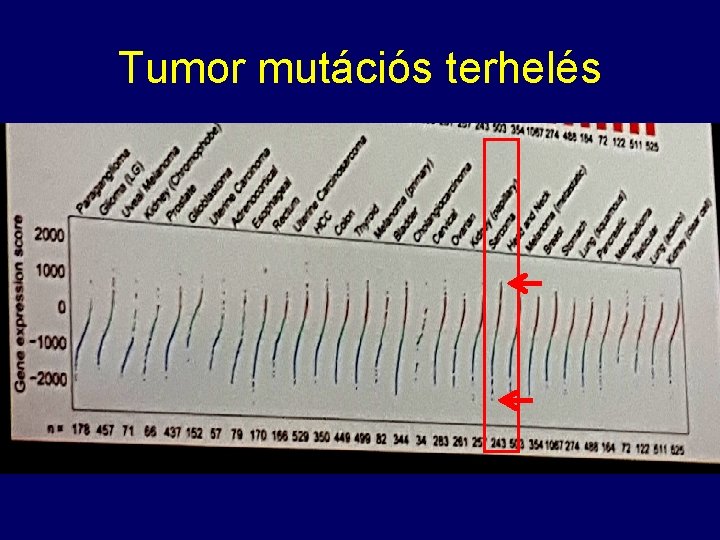
Tumor mutációs terhelés

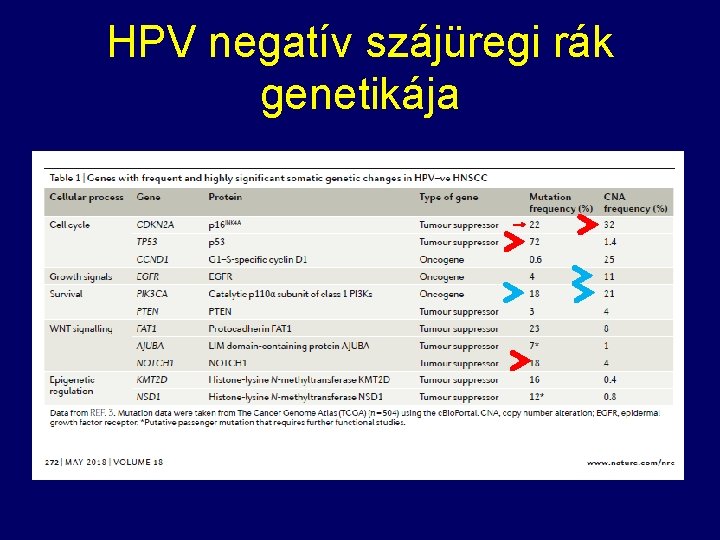
HPV negatív szájüregi rák genetikája

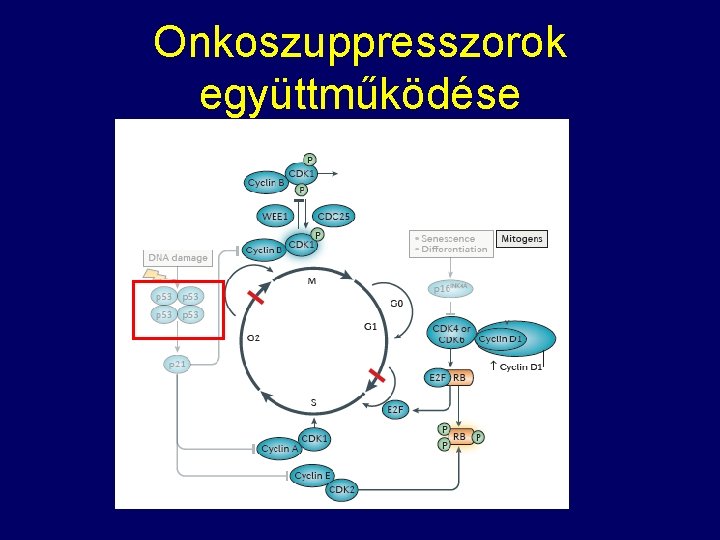
Onkoszuppresszorok együttműködése

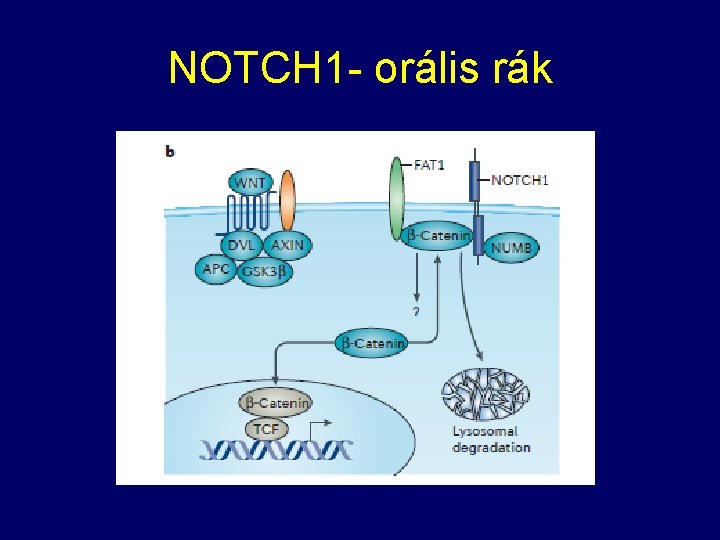
NOTCH 1 - orális rák

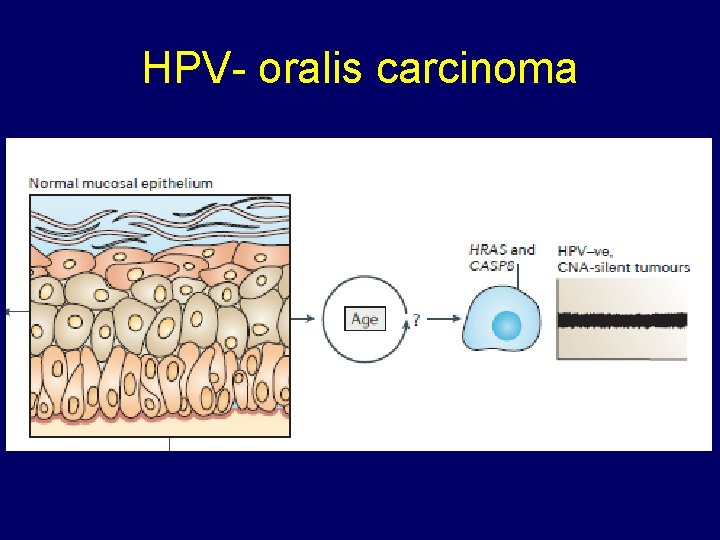
HPV- oralis carcinoma

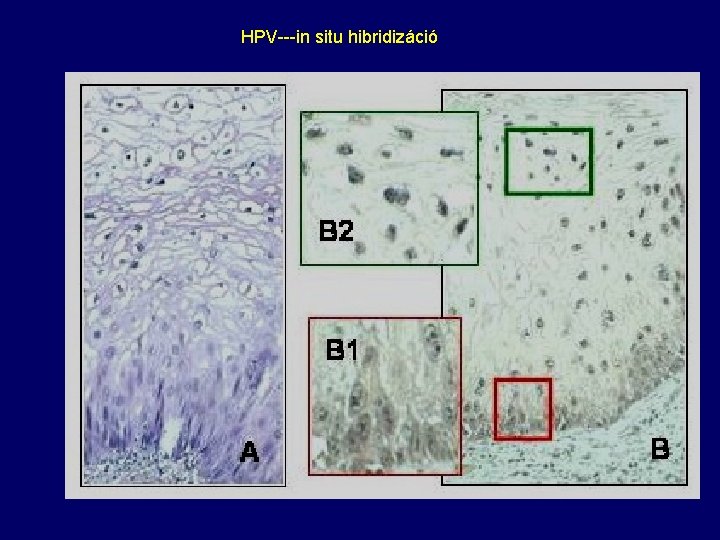
HPV---in situ hibridizáció

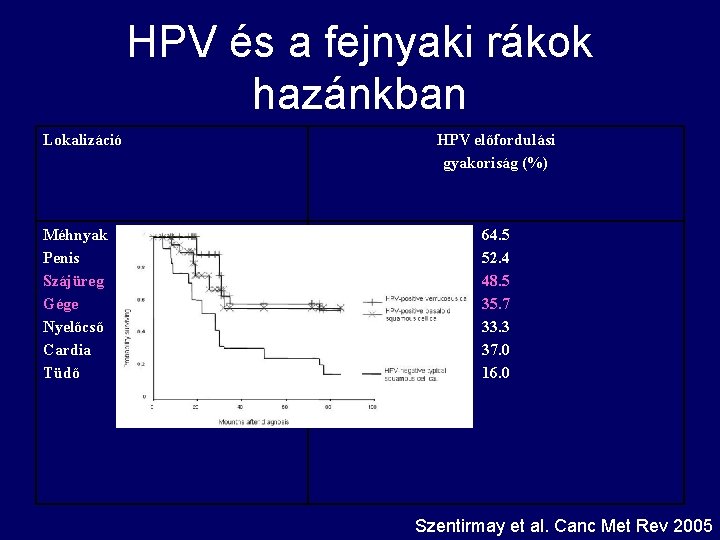
HPV és a fejnyaki rákok hazánkban Lokalizáció Méhnyak Penis Szájüreg Gége Nyelőcső Cardia Tüdő HPV előfordulási gyakoriság (%) 64. 5 52. 4 48. 5 35. 7 33. 3 37. 0 16. 0 Szentirmay et al. Canc Met Rev 2005

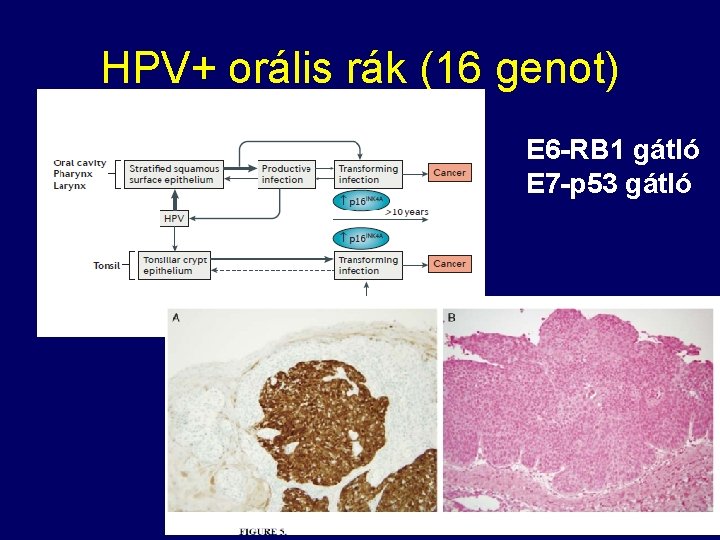
HPV+ orális rák (16 genot) E 6 -RB 1 gátló E 7 -p 53 gátló

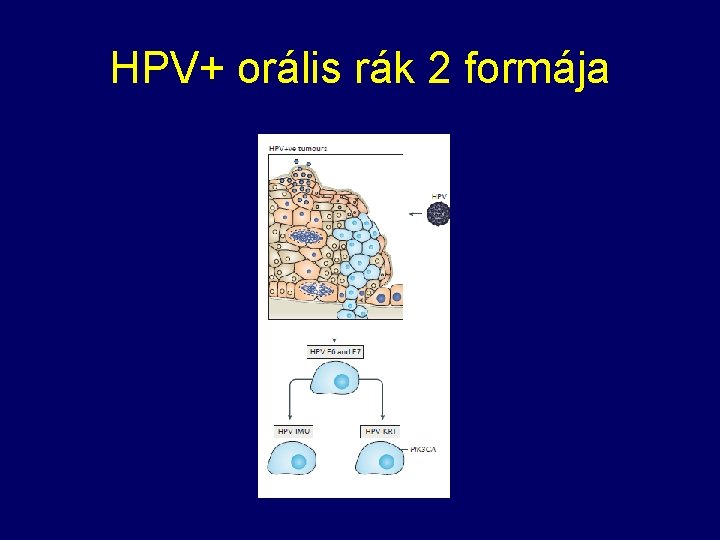
HPV+ orális rák 2 formája


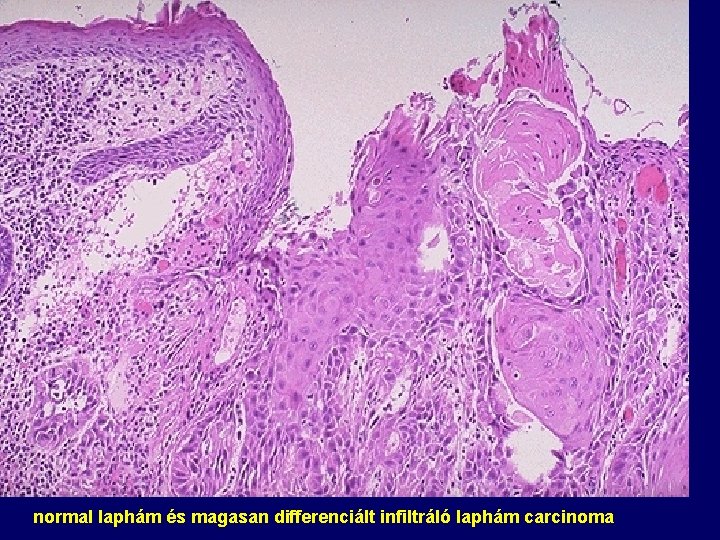
normal laphám és magasan differenciált infiltráló laphám carcinoma

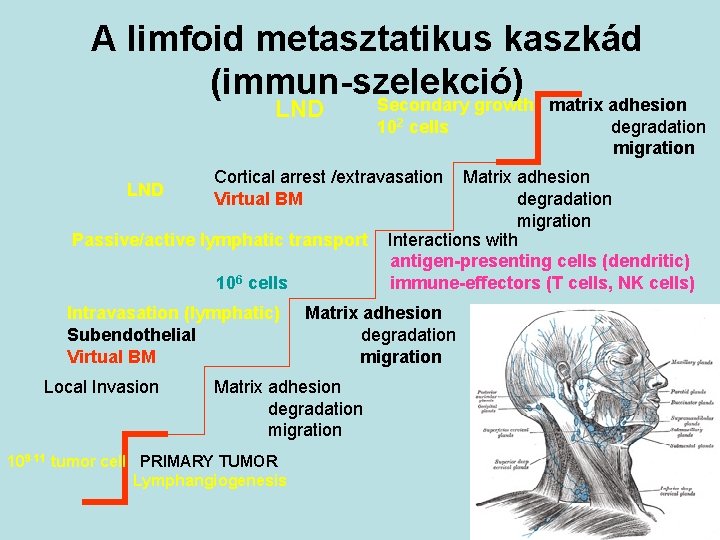
A limfoid metasztatikus kaszkád (immun-szelekció) Secondary growth matrix adhesion LND Cortical arrest /extravasation Virtual BM Passive/active lymphatic transport 106 cells Intravasation (lymphatic) Subendothelial Virtual BM Local Invasion 102 cells 109 -11 tumor cell PRIMARY TUMOR Lymphangiogenesis Matrix adhesion degradation migration Interactions with antigen-presenting cells (dendritic) immune-effectors (T cells, NK cells) Matrix adhesion degradation migration

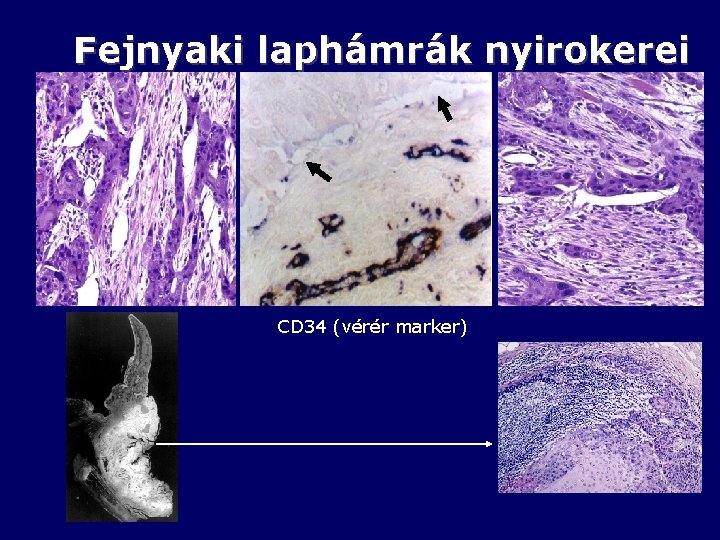
Fejnyaki laphámrák nyirokerei CD 34 (vérér marker)

Angiogenezis prognosztikai jelentősége • Angiogenezis • Lymphangiogenezis MVD nem prognosztikus • L-MVD prognosztikus VEGF A/B nem • VEGFC/D prognosztikus • VEGFR 2/3 prognosztikus

Angiogenezis-gátló terápiák gyógyszer Bevacizumab fázis II Daganat-stádium kezelés Első, másodvonal, R/M HNC Bevacizumab 15 mg/kg q 3 w + erlotinib 150 mg per nap betegszám CR % PR % SD % Co. R% TTP (h) PFS (h) OS (h) 51 4 10 56 70 70 4 7 Anti-VEGF Bevacizumab II Első, másodvonal, R/M HNC Bevacizumab 15 mg/kg q 3 w + pemetrexed 14 18 27 54 99 99 6 - Sorafenib II Első, másodvonal, R/M HNC Sorafenib 800 mg per nap 44 0 3 45 48 4, 2 - 8 Sorafenib II másodvonal R/M HNC Sorafenib 800 mg per nap 28 0 4 37 41 1, 8 - 4 VEGFR-TKI

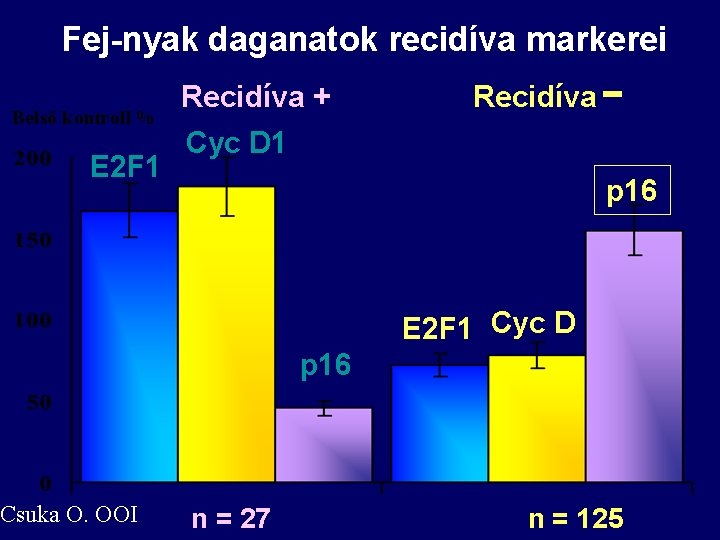
Fej-nyak daganatok recidíva markerei Belső kontroll % E 2 F 1 Csuka O. OOI Recidíva + Recidíva Cyc D 1 p 16 E 2 F 1 Cyc D p 16 n = 27 n = 125

A HNSC metasztázis markerei • E-CDH 1 és CD 44 H/s vesztés • • Fokozott a 6 b 4 integrin Fokozott/mutált C-met Fokozott AMFR (foszfohexoz izomeráz) Fokozott COX-2

Génexpressziós profilváltás az anatómia függvényében pozitív negatív fokozott csökkent fokozott Negatív pozitív Metastasis-Super. Array: változás >2 x

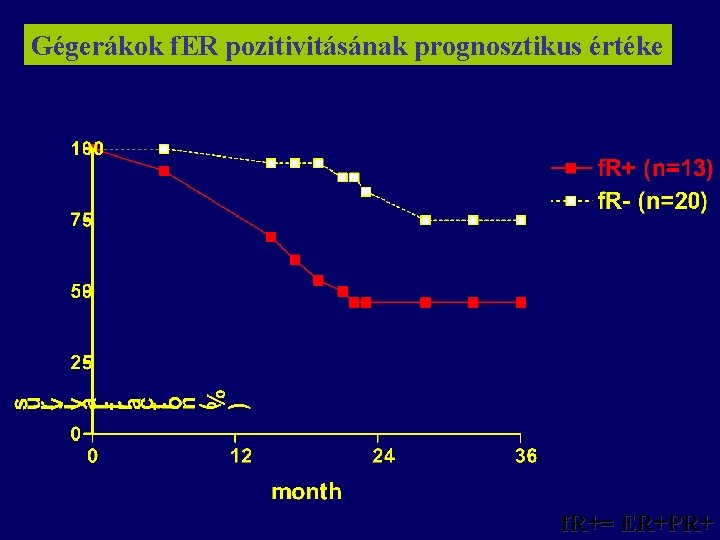
Gégerákok f. ER pozitivitásának prognosztikus értéke f. R+= ER+PR+

HNSC prediktív patológia • • CPD+5 FU indukció======Ch. RT HPV 16: titer= ffi / nemdohányzó / fiatal HPV 16 titer: IC resp /CTR resp / 4 year OS Worden et al. JCO 26: 3138, 2008 • IC /Ch. RT szervmegtartás és túlélés • Alacsony EGFR, HPV+/magas p 16: RRjó, OS magas • Magas EGFR, alacsonyp 53/magas BCLx. L, nő, dohányzó: kedvezőtlen terápiás válasz, alacsony túlélés…. . • Kumar et al. JCO 26. 3128, 2008

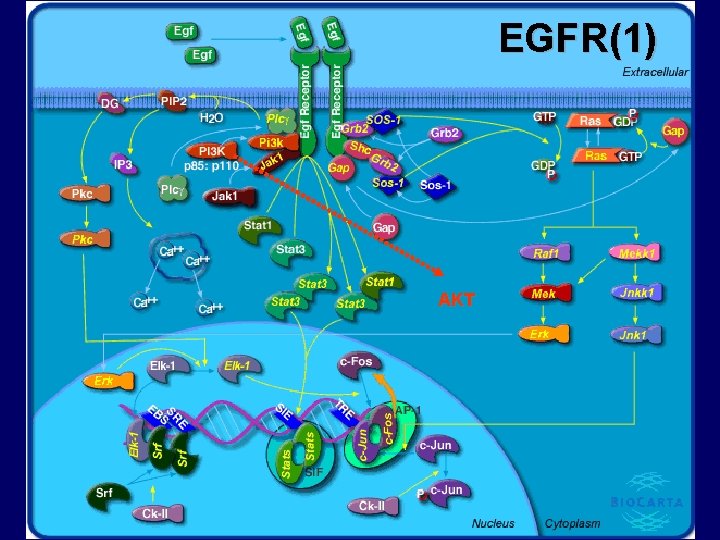
EGFR(1) AKT

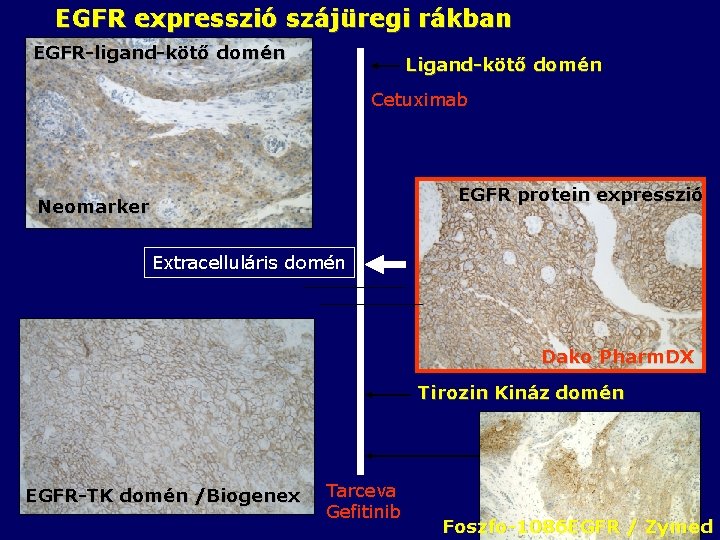
EGFR expresszió szájüregi rákban EGFR-ligand-kötő domén Ligand-kötő domén Cetuximab EGFR protein expresszió Neomarker Extracelluláris domén Dako Pharm. DX Tirozin Kináz domén EGFR-TK domén /Biogenex Tarceva Gefitinib Foszfo-1086 EGFR / Zymed

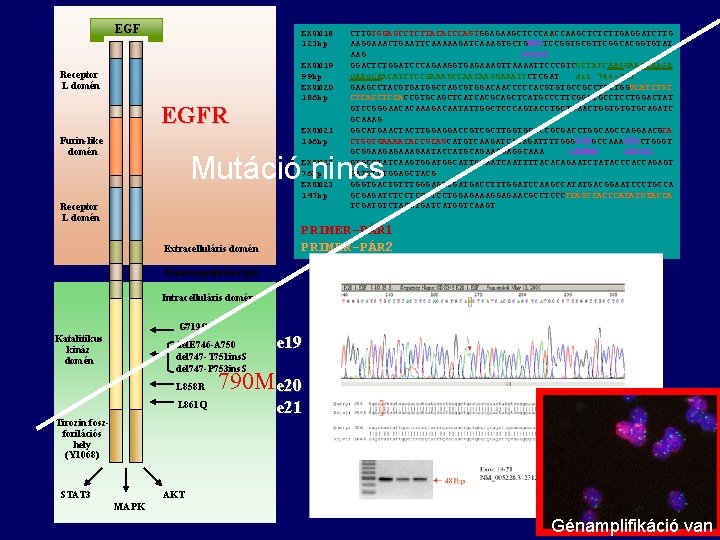
EGF Receptor L domén EGFR Furin-like domén EXON 18 CTTGTGGAGCCTCTTACACCCAGTGGAGAAGCTCCCAAGCTCTCTTGAGGATCTTG 123 bp AAGGAAACTGAATTCAAAAAGATCAAAGTGCTGGGCTCCGGTGCGTTCGGCACGGTGTAT AAG G 719 C EXON 19 GGACTCTGGATCCCAGAAGGTGAGAAAGTTAAAATTCCCGTCGCTATCAAGGAATTAAGA 99 bp GAAGCAACATCTCCGAAAGCCAACAAGGAAATCCTCGAT del 746 -753 EXON 20 GAAGCCTACGTGATGGCCAGCGTGGACAACCCCCACGTGTGCCGCCTGCTGGGCATCTGC 186 bp CTCACCTCCACCGTGCAGCTCATCACGCAGCTCATGCCCTTCGGCTGCCTCCTGGACTAT GTCCGGGAACACAAAGACAATATTGGCTCCCAGTACCTGCTCAACTGGTGTGTGCAGATC GCAAAG EXON 21 GGCATGAACTACTTGGAGGACCGTCGCTTGGTGCACCGCGACCTGGCAGCCAGGAACGTA 156 bp CTGGTGAAAACACCGCAGCATGTCAAGATCACAGATTTTGGGCTGGCCAAACTGCTGGGT GCGGAAGAGAATACCATGCAGAAGGAGGCAAA L 858 R L 861 Q EXON 22 GTGCCTATCAAGTGGATGGCATTGGAATCAATTTTACACAGAATCTATACCCACCAGAGT 76 bp GATGTCTGGAGCTACG EXON 23 GGGTGACTGTTTGGGAGTTGATGACCTTTGGATCCAAGCCATATGACGGAATCCCTGCCA 147 bp GCGAGATCTCCTCCATCCTGGAGAAAGGAGAACGCCTCAGCCACCCATATGTACCA TCGATGTCTACATGATCATGGTCAAGT Mutáció nincs Receptor L domén Extracelluláris domén PRIMER-PÁR 1 PRIMER-PÁR 2 Transzmembrán régió Intracelluláris domén G 719 C Katalitikus kináz domén del. E 746 -A 750 del 747 -T 751 ins. S del 747 -P 753 ins. S L 858 R 790 M e 20 L 861 Q e 21 Tirozin foszforilációs hely (Y 1068) STAT 3 e 19 AKT MAPK Génamplifikáció van

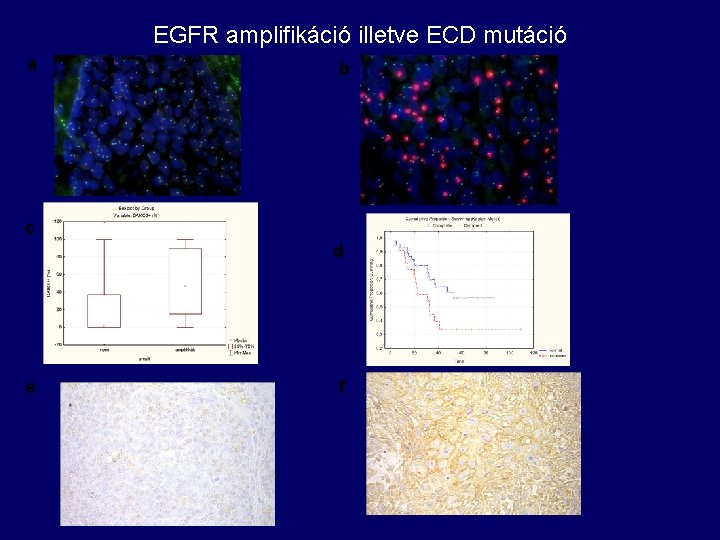
EGFR amplifikáció illetve ECD mutáció a b c d e f

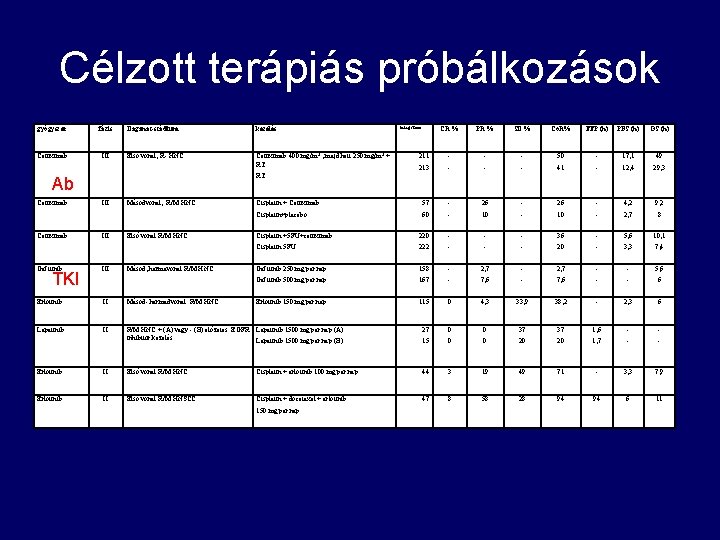
Célzott terápiás próbálkozások gyógyszer fázis Cetuximab III Daganat-stádium kezelés Első vonal, R- HNC Cetuximab 400 mg/m 2 , majd heti 250 mg/m 2 + RT Cetuximab Gefitinib TKI CR % PR % SD % Co. R% TTP (h) PFS (h) OS (h) 211 - - - 50 - 17, 1 49 213 - - - 41 - 12, 4 29, 3 Cisplatin + Cetuximab 57 - 26 - 4, 2 9, 2 Cisplatin+placebo 60 - 10 - 2, 7 8 Cisplatin +5 FU+cetuximab 220 - - - 36 - 5, 6 10, 1 Cisplatin 5 FU 222 - - - 20 - 3, 3 7, 4 Gefitinib 250 mg per nap 158 - 2, 7 - - 5, 6 Gefitinib 500 mg per nap 167 - 7, 6 - - 6 Erlotinib 150 mg per nap 115 0 4, 3 33, 9 38, 2 - 2, 3 6 RT Ab Cetuximab betegszám III III Másodvonal, R/M HNC Első vonal R/M HNC Másod, harmavonal R/M HNC Erlotinib II Másod- harmadvonal R/M HNC Lapatinib II R/M HNC + (A) vagy - (B) előzetes EGFR Lapatinib 1500 mg per nap (A) inhibitor kezelés Lapatinib 1500 mg per nap (B) 27 0 0 37 37 1, 6 - - 15 0 0 20 20 1, 7 - - Erlotinib II Első vonal R/M HNC Cisplatin + erlotinib 100 mg per nap 44 3 19 49 71 - 3, 3 7, 9 Erlotinib II Első vonal R/M HNSCC Cisplatin + docetaxel + erlotinib 47 8 58 28 94 94 6 11 150 mg per nap

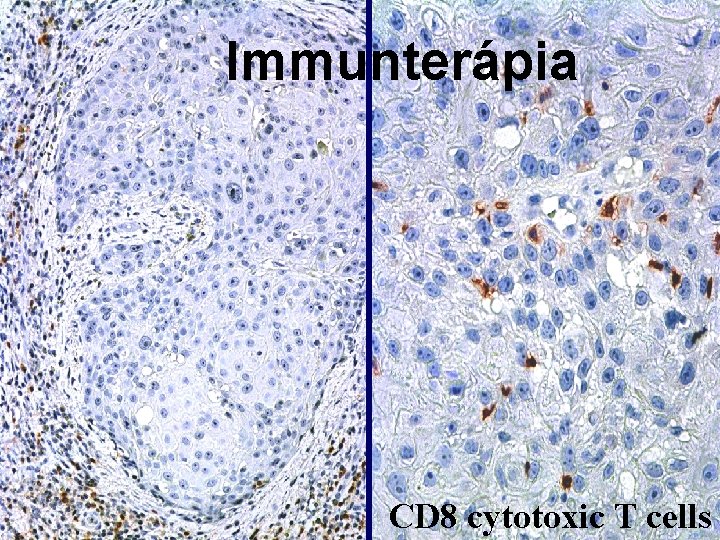
Immunterápia CD 8 cytotoxic T cells


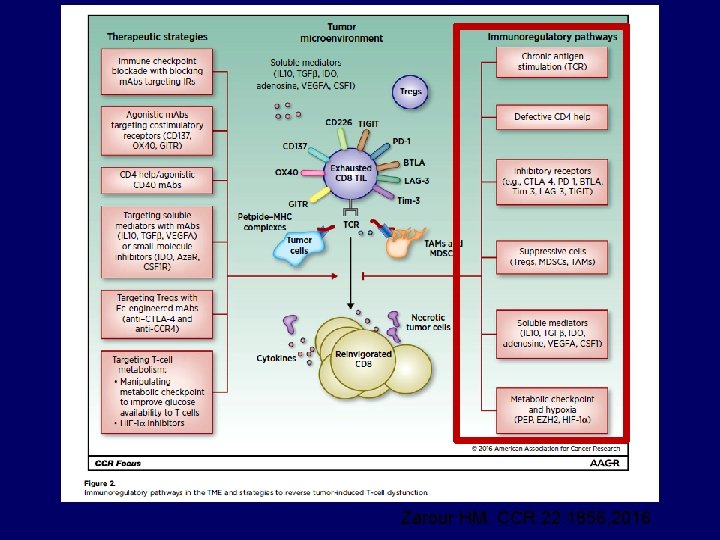
Zarour HM. CCR 22: 1856, 2016

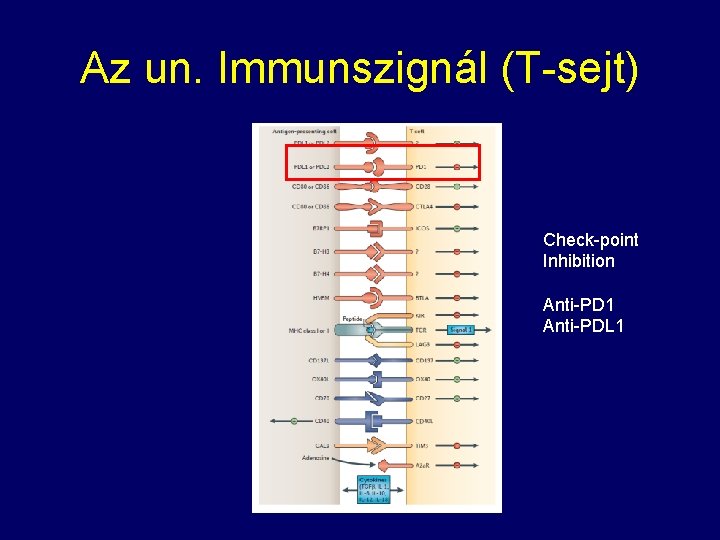
Az un. Immunszignál (T-sejt) Check-point Inhibition Anti-PD 1 Anti-PDL 1

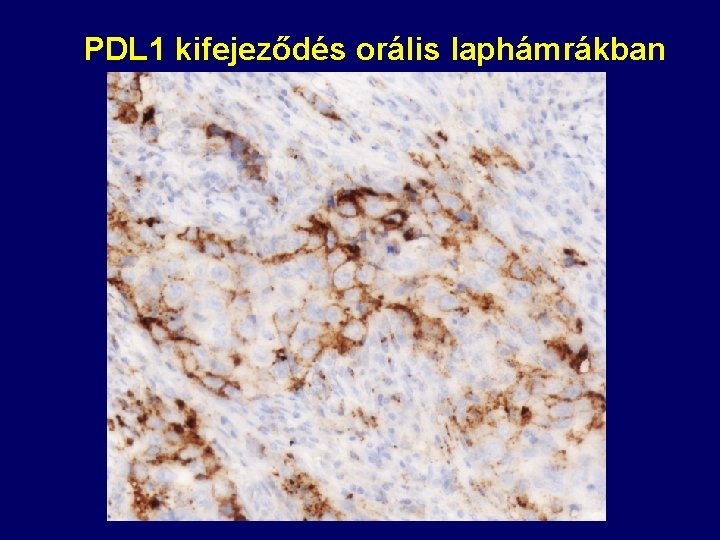
PDL 1 kifejeződés orális laphámrákban

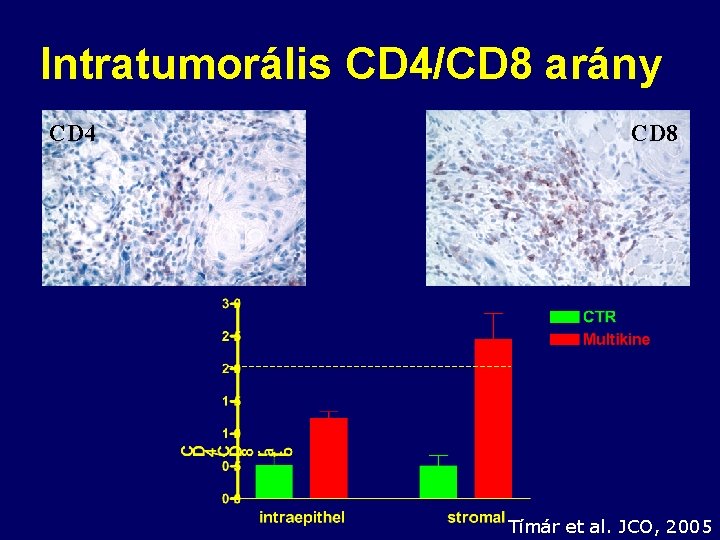
Intratumorális CD 4/CD 8 arány CD 4 CD 8 Tímár et al. JCO, 2005

Immunterápia • PDL 1+ orális rákok esetében anti-PD 1 vagy anti-PDL 1 antitest terápia • Magas TMB esetén un. Check point inhibitor terápia