Solubilidad y sus factores Ciencias Naturales Qumica Solubilidad

Solubilidad y sus factores Ciencias Naturales: Química

Solubilidad es una medida de la capacidad que tiene el soluto, de disolverse en un determinado disolvente. Implícitamente se corresponde con la máxima cantidad de soluto que se puede disolver en una cantidad determinada de solvente a una temperatura fija. Puede expresarse en unidades de concentración como por ejemplo %m/m, %m/v, %v/v.
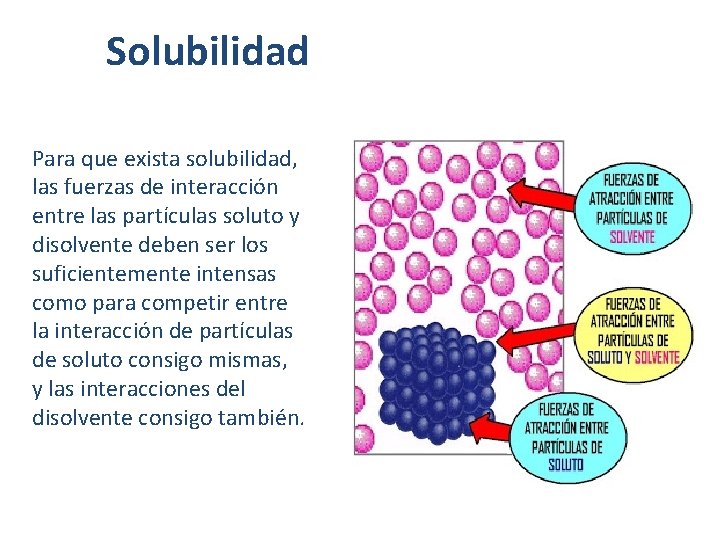
Solubilidad Para que exista solubilidad, las fuerzas de interacción entre las partículas soluto y disolvente deben ser los suficientemente intensas como para competir entre la interacción de partículas de soluto consigo mismas, y las interacciones del disolvente consigo también.
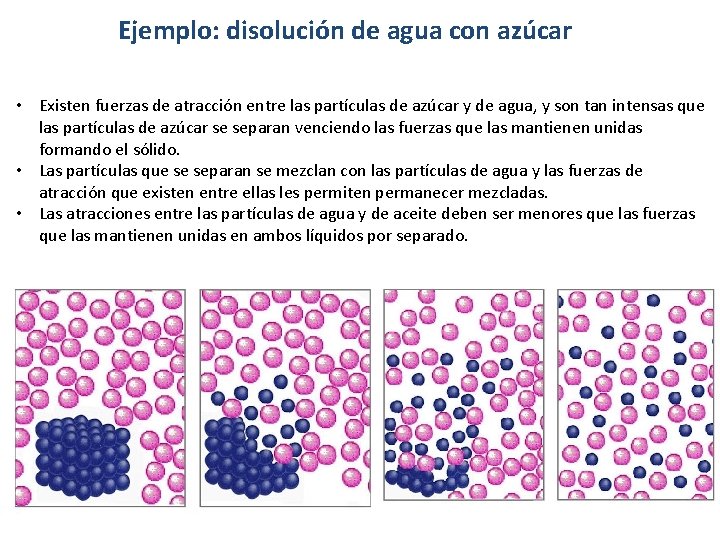
Ejemplo: disolución de agua con azúcar • Existen fuerzas de atracción entre las partículas de azúcar y de agua, y son tan intensas que las partículas de azúcar se separan venciendo las fuerzas que las mantienen unidas formando el sólido. • Las partículas que se separan se mezclan con las partículas de agua y las fuerzas de atracción que existen entre ellas les permiten permanecer mezcladas. • Las atracciones entre las partículas de agua y de aceite deben ser menores que las fuerzas que las mantienen unidas en ambos líquidos por separado.
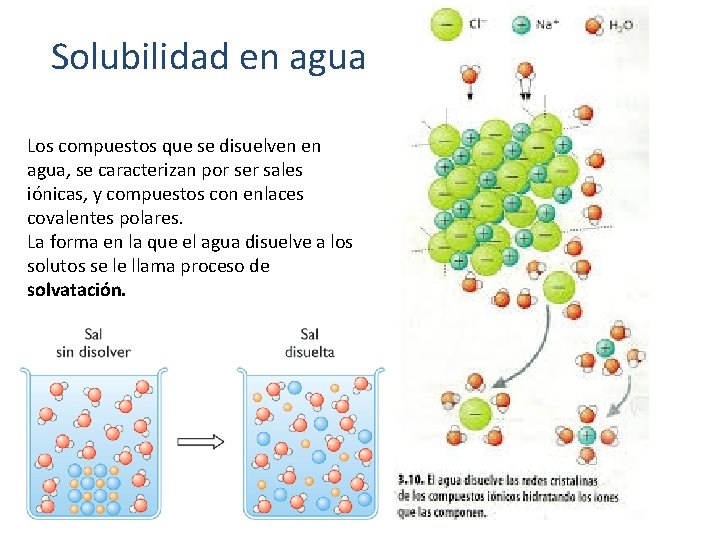
Solubilidad en agua Los compuestos que se disuelven en agua, se caracterizan por ser sales iónicas, y compuestos con enlaces covalentes polares. La forma en la que el agua disuelve a los solutos se le llama proceso de solvatación.

© 2009 Prentice-Hall Inc.

© 2009 Prentice-Hall Inc.

© 2009 Prentice-Hall Inc.

Factores que afectan la solubilidad de una disolución
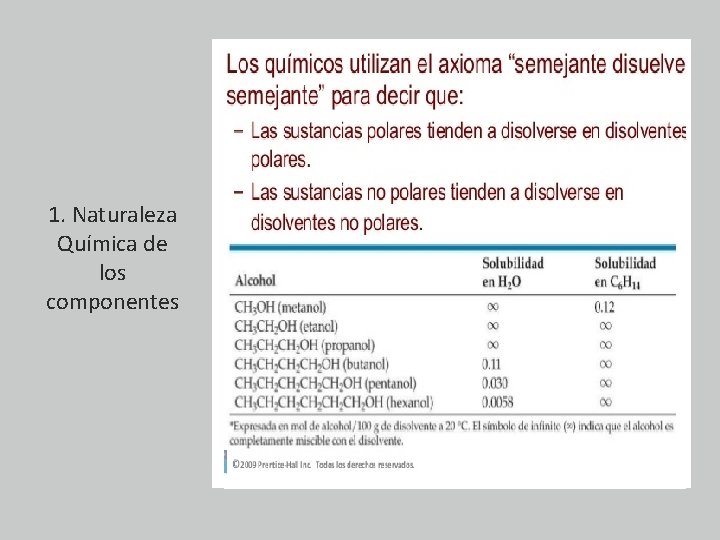
1. Naturaleza Química de los componentes
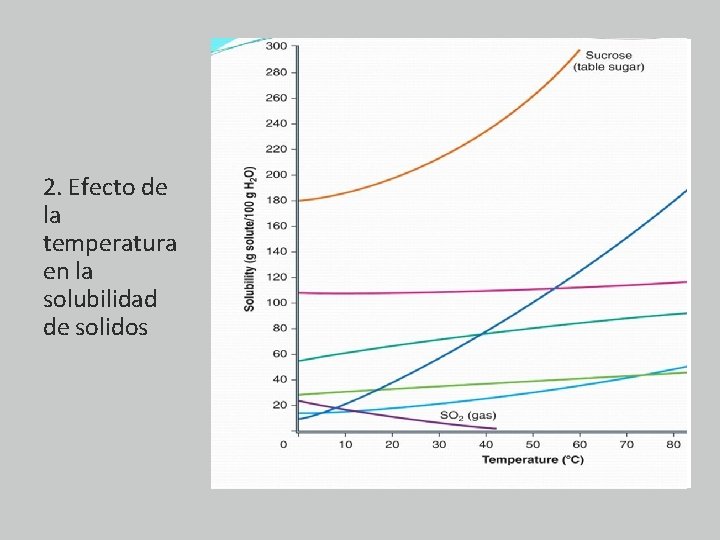
2. Efecto de la temperatura en la solubilidad de solidos
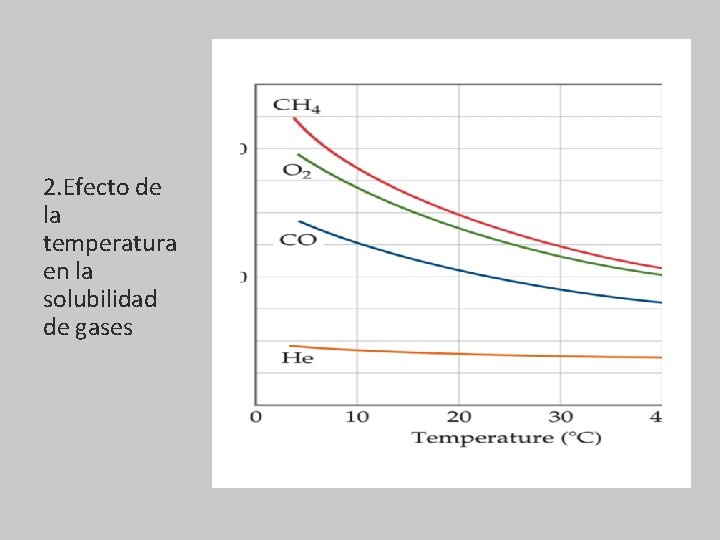
2. Efecto de la temperatura en la solubilidad de gases

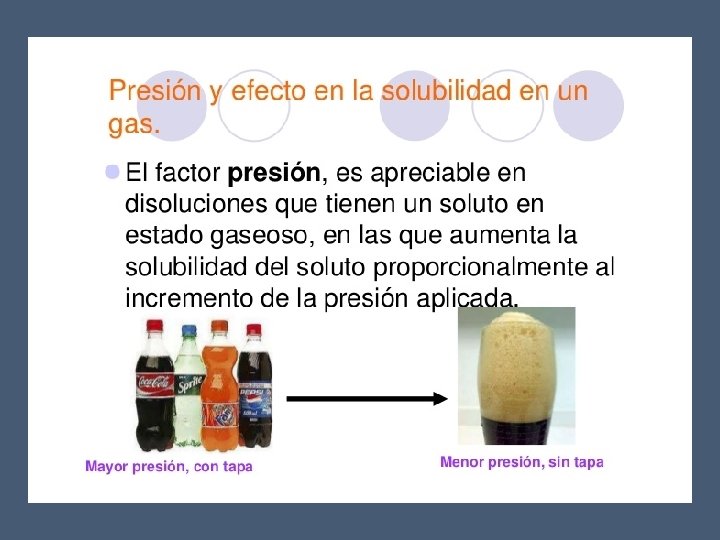
3. La presión (solo en gases)

Factores Mecánicos • En contraste con la velocidad de disolución, la cual depende principalmente de la temperatura, la velocidad de recristalización depende de la concentración de soluto en la superficie de la red cristalina, caso que se favorece cuando una solución está inmóvil. • Por lo tanto, la agitación de la solución evita esta acumulación, maximizando la disolución.

• • Preguntas…. . • • 1. ¿Por qué la sal se disuelve en agua y no en aceite? 2. ¿Cuál es la diferencia entre enlazar e interaccionar? 3. ¿Que tipos de interacciones existen? . Explique cada una de ellas 4. Si se que 100 ml de agua disuelven 10 gramos de sal. Y tengo 200 ml de agua y le agrego 30 gramos de sal. ¿ que tipo de solución tengo? Explique 5. ¿Porque se dice que u compuesto es apolar o polar? . Investigue. 6. ¿Cuales son los factores de los que dependen que una sustancia se disuelva en otra? 7. ¿Porque al dejar una bebida sobre la mesa destapada durante un día perdería el gas, y si esta quedara en el refrigerador no se vería tanto efecto? 8. si se que en 100 ml de agua se pueden disolver 50 gramos de bicarbonato. De un ejemplo de una solución Insaturada, Sobresaturada.

FIN Próxima Clase: Unidades de concentración
- Slides: 17