RULLY SUSILOWATI DEPT KIMIA FARMASI FFUA Copyright 1996





















- Slides: 26

RULLY SUSILOWATI DEPT. KIMIA FARMASI FFUA Copyright 1996 -2001 © Dale Carnegie & Associates, Inc.

ELEKTROKIMIA • merupakan cabang ilmu kimia yang mempelajari perubahan energi listrik dan energi kimia • prosesnya : redoks ( reduksi dan oksidasi ) • dari reaksi kimia spontan dapat dihasilkan energi yang dirubah menjadi energi listrik • Energi listrik digunakan untuk menghasilkan suatu reaksi kimia tidak spontan

Reaksi reduksi § R. pelepasan oksigen § R. pengikatan hidrogen § R. pengikatan elektron § R. penurunan bilangan oksidasi Contoh : C 6 H 5 NO 2 + 3 H 2 C 6 H 5 NH 2 + 2 H 2 O Fe(CN)63 - + e Fe(CN)64 - Ag+ + e Ag Pb 4+ + 2 e Pb 2+

Reaksi Oksidasi § R. pengikatan oksigen § R. pelepasan hidrogen § R. pelepasan elektron § R. peningkatan bilangan oksidasi Contoh : C 2 H 5 OH + O 2 C 6 H 18 O 6 Zn Mn. O 422 Cl- CH 3 COOH + H 2 O C 6 H 16 O 6 + H 2 Zn 2+ +2 e Mn. O 41 - + e Cl 2 + 2 e

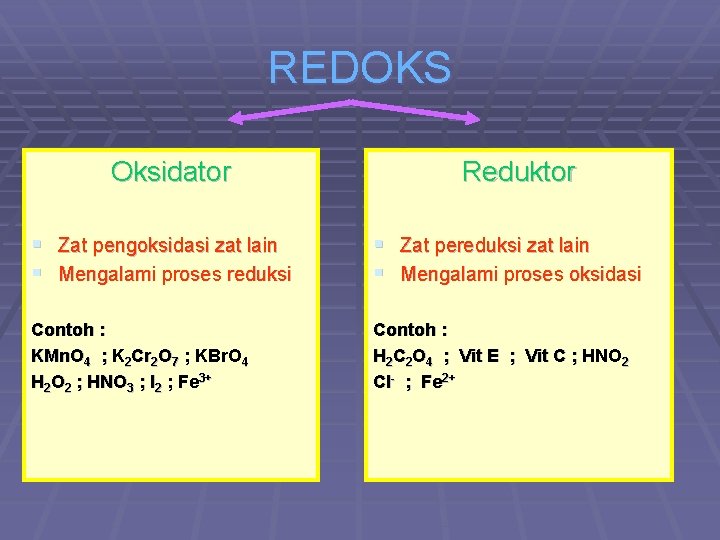
REDOKS Oksidator Reduktor § Zat pengoksidasi zat lain § Mengalami proses reduksi § Zat pereduksi zat lain § Mengalami proses oksidasi Contoh : KMn. O 4 ; K 2 Cr 2 O 7 ; KBr. O 4 H 2 O 2 ; HNO 3 ; I 2 ; Fe 3+ Contoh : H 2 C 2 O 4 ; Vit E ; Vit C ; HNO 2 Cl- ; Fe 2+

Redoks ( Reduksi – Oksidasi ) § Reaksi transfer elektron § Tidak dapat berlangsung sendiri-2 § Berjalan serempak / bersamaan Contoh : § 2 Fe 3+ + Sn 2+ § 5 H 2 O 2 + Mn. O 41 - + H+ § Br. O 3 - + 6 I- + 6 H+ 2 Fe 2+ + Sn 4+ 2 Mn 2+ + 5 O 2 + 8 H 2 O Br- + 3 I 2 + 3 H 2 O

Reaksi redoks tidak melibatkan elektron bebas 2 Fe 3+ + Sn 2+ 2 Fe 2+ + Sn 4+ 2 Fe 3+ + 2 e Sn 2+ 2 Fe 3+ + Sn 2+ 2 Fe 2+ ( reduksi ) Sn 4+ + 2 e ( oksidasi ) 2 Fe 2+ + Sn 4+ ( redoks ) Reaksi reduksi dan oksidasi masing-masing disebut : • Reaksi paruh • Setengah reaksi Reaksi redoks disebut : • Reaksi total

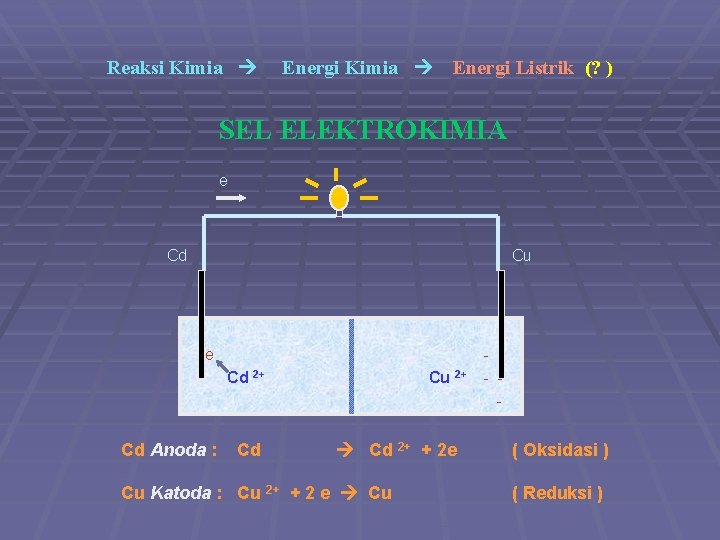
Reaksi Kimia Energi Listrik (? ) SEL ELEKTROKIMIA e Cd Cu e Cd 2+ Cd Anoda : Cd Cu 2+ Cd 2+ + 2 e Cu Katoda : Cu 2+ + 2 e Cu - - - ( Oksidasi ) ( Reduksi )

SEL ELEKTROKIMIA Terdiri dari : § Elektrolit § Elektroda : ● Anoda : Reaksi Oksidasi ● Katoda : Reaksi Reduksi

SEL ELEKTROKIMIA Sel Volta / Sel Galvani § Menghasilkan energi listrik § § § dari reaksi kimia/ energi kimia Anoda : kutub negatip Katoda : kutub positip Contoh : aki, baterai Sel Elektrolisis § Menghasilkan energi kimia § § § dari reaksi energi istrik Anoda : kutub positip Katoda : kutub negatip Contoh : alat penyepuh ( electroplating )

EMF ( Electromotive Force ) GGL ( Gaya Gerak Listrik ) adalah : Perbedaan potensial elektroda yang menyebabkan terjadinya arus listrik mengalir dari elektroda potensial tinggi ke elektroda potensial yang lebih rendah pada suatu sel elektrokimia. Satuan : Volt Alat untuk mengukur : Potensiometer Simbol : [ E ; ε ]

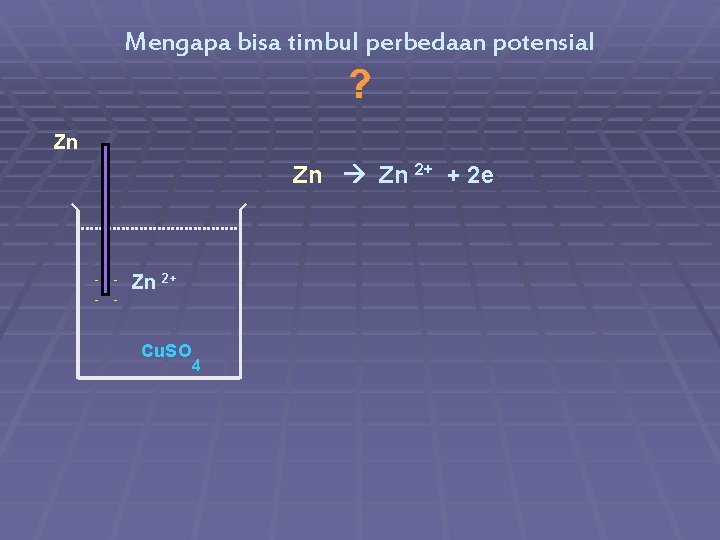
Mengapa bisa timbul perbedaan potensial ? Zn Zn 2+ + 2 e - - Zn 2+ Cu. SO 4

Penulisan Sel 1. Sel Galvani ditulis dengan setengah sel anoda (elektroda negatif) di sebelah kiri dan setengah sel katoda (elektroda positif ) di sebelah kanan. 2. Satu garis tegak/miring. Zn 2+ menunjukkan batas fasa, sedangkan 2 garis menunjukkan adanya jembartan garam. 3. Dua zat yang ada dalam fasa yang sama dipisahkan dengan tanda koma 4. Konsentrasi larutan dinyatakan dalam tanda kurung setelah rumus kimianya Contoh : Zn(s)/Zn 2+(1, 00 m) // Cu 2+(1, 00 m) /Cu (s) Zn(s)/ Zn 2+ (1, 00 m) / Cu 2+ (1, 00 m) /Cu (s) Pt/ Fe 2+, Fe 3+// H+/ H 2/ Pt

GGL & Reaksi Sel 1. GGL sel adalah jumlah potensial elektroda tunggal sesuai dengan reaksi yang terjadi di dalam sel/elektroda tersebut. 2. Apabila sel ditulis dengan elektroda negatif di sebelah kiri, maka elektron akan mengalir melalui rangkaian di luar sel dari KIRI ke KANAN , maka reaksi sel yang terjadi adalah SPONTAN dan GGL sel akan bertanda + 3. Reaksi yang terjadi pada elektroda sebelah kiri adalah oksidasi dan elektroda sebelah kana adalah reduksi Contoh : Zn(s)/Zn 2+ (1, 00 m)//Cu 2+ (1, 00 m)/Cu(s) Zn 2+(aq) + 2 e Cu 2+(aq) + 2 e Zn(s) + Cu 2+(aq) Cu(s) ( reaksi oksidasi ) + Zn 2+(aq) + Cu(s) ( reaksi reduksi ) ( reaksi sel )

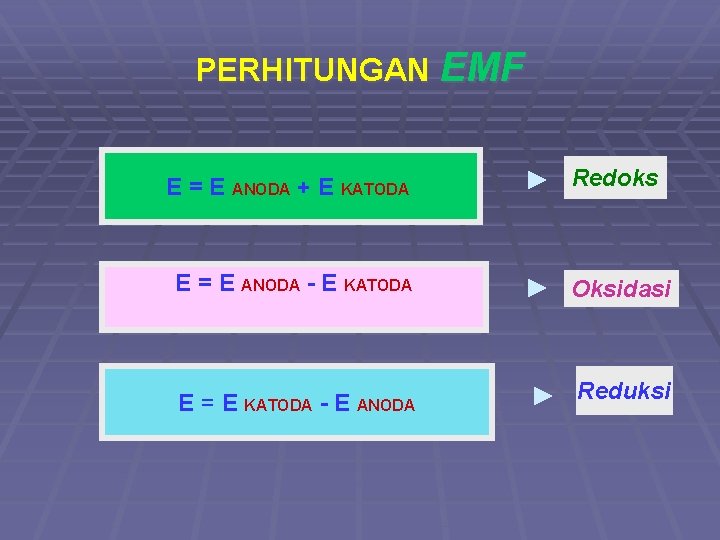
PERHITUNGAN EMF E = E ANODA + E KATODA Redoks E = E ANODA - E KATODA Oksidasi E = E KATODA - E ANODA Reduksi

ELEKTRODA § Elektroda Standar : ● Elektroda Hidrogen Standar ( SHE ) § Elektroda Pembanding : ● Elektroda Kalomel ● Elektroda Ag/Ag. Cl § Elektroda p. H : • Elektroda Hidrogen • Elektroda Gelas

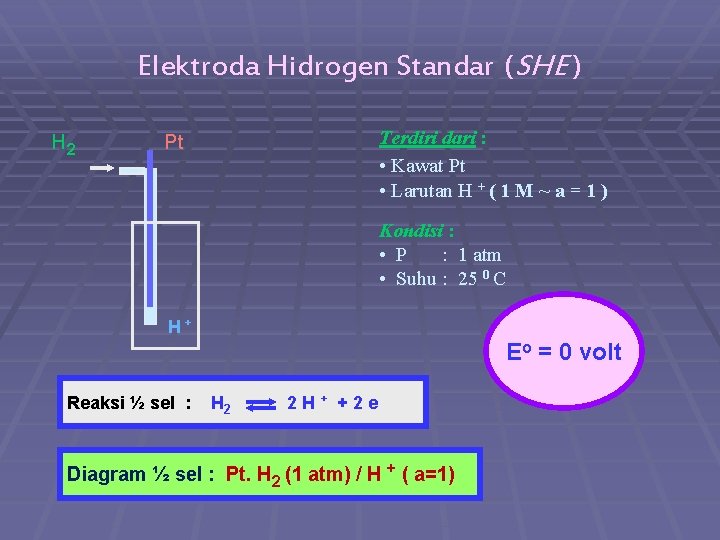
Elektroda Hidrogen Standar (SHE ) H 2 Terdiri dari : • Kawat Pt • Larutan H + ( 1 M ~ a = 1 ) Pt Kondisi : • P : 1 atm • Suhu : 25 0 C H+ Eo = 0 volt Reaksi ½ sel : H 2 2 H+ +2 e Diagram ½ sel : Pt. H 2 (1 atm) / H + ( a=1)

ELEKTRODA KALOMEL Reaksi : Hg 2 Cl 2(p) + 2 e 2 Hg (p) + 2 Cl. A. Kalomel 0, 1 N ( Kalomel desinormal ) Diagram : Hg/Hg 2 Cl 2(p), KCl (0, 1 N) Eo = 0, 3338 volt B. Kalomel 1 N ( Kalomel normal ) Diagram : Hg/Hg 2 Cl 2(p), KCl (1 N) Eo = 0, 2800 volt C. Kalomel JENUH ( saturated ) Diagram : Hg/Hg 2 Cl 2(p), KCl (Jenuh) Eo = 0, 2415 volt

HUKUM FARADAY • Jumlah zat yang dihasilkan pada reaksi elektroda adalah setara dengan jumlah listrik yang mengalir pada reaksi elektrolisis Dari percobaan : 1 Coulomb [ C ] ~ 0, 00111797 gram Ag BA Ag = 107, 870 gram 1 BE Ag membutuhkan = 107, 870/ 0, 00111797 C = 96. 487 C ~ 96. 500 C 1 F = 96. 500 C 1 e ~ 1, 602. 10 -19 C 1 F ~ 96. 500/1, 602. 10 -19 e ~ 6, 023. 10 23 e

COULOMETER § Alat / sel elektrolisis yang digunakan untuk mengukur jumlah listrik yang melewati suatu sirkuit / rangkaian dengan mengamati perubahan kimia yang terjadi § Rumus : Berat Zat = BA x i x t 96. 500 BA : berat atom zat i : arus listrik t : waktu Gram

Contoh Perhitungan potensial Elektroda 1. Sel Galvani dengan diagram sel : Cd/Cd 2+ ( a=1) // KCl (1 N), Hg 2 Cl 2(p)/Hg Eo sel = 0, 6830 volt ( 25 o. C, 1 atm ) Hitung Eo elektroda Cd, bila berfungsi sebagai kutub negatip. Jawab : Kutub neg ( anoda ~ oksidasi ) : Cd 2+ + 2 e Kutub pos ( katoda ~ reduksi ) : Hg 2 Cl 2(p) + 2 e 2 Hg (p) + 2 Cl Eo = + 0, 2800 volt Eo sel = Eo anoda + Eo katoda 0, 6830 = + 0, 2800 Eo Cd = 0, 4030 volt 2. Hg/ Hg 2 Cl 2(p), KCl (0, 1 N) / Cu 2+ ( a=1 ) / Cu Eo sel = 0, 0570 volt ( 25 o. C, 1 atm ) Elektroda kalomel kutub negatip Hitung Eo Cu

Contoh Perhitungan potensial sel 1. Cd/Cd 2+ ( a=1) // Cu 2+ ( a=1 ) / Cu ( 25 o. C, 1 atm ) Hitung Eo sel, bila sel berfungsi sebagai penghasil listrik Jawab : Asumsi : Kutub neg (anoda) adalah elektroda Cd Anoda : Cd 2+ + 2 e Eo Cd = 0, 4030 volt Katoda : Cu 2+ + 2 e Cu Eo Cu = 0, 3370 volt + Cd + Cu 2+ Cd 2+ + Cu Eo sel = 0, 7400 volt Eo sel > 0 Reaksi spontan Elektroda Cd anoda ( oksidasi ), kutub negatip Elektroda Cu katoda ( reduksi ), kutub posititip 2. Bagaimana bila elektroda Cu sebagai kutub negatip ?

Rumus a. A + b. B Nernst c. C + d. D ΔG = ΔG o + RT ln ac. C. ad. D a a A. ab B ΔG = – n F Eo + RT ln ac. C. ad. D a a A. ab B E = Eo – RT ln ac. C. ad. D n. F a a A. ab B E = Eo – 2, 3026 RT log ac. C. ad. D n. F a a A. ab B n = elektron yang terlibat dalam reaksi F = 96. 500 C R = konstanta gas Pada t = 25 o. C E = Eo – 0, 059 log ac. C. ad. D n aa A. ab B T = suhu

Contoh Berapa potensial elektroda Zn : Zn / Zn 2+ ( a = 0, 1 ) pada 25 o. C, 1 atm Oksidasi : Zn 2+ + 2 e E = Eo – 0, 059 log a Zn 2+ n a Zn = 0, 7618 – 0, 059 log 0, 1 2 1 = 0, 7914 volt Reduksi : Zn 2+ + 2 e Zn E = Eo – 0, 059 log a Zn 2+ n a Zn = – 0, 7618 – 0, 059 log 1 2 0, 1 = – 0, 7914 volt

Contoh Zn / Zn 2+ (0, 1) // Cl- (1 N), Hg 2 Cl 2/Hg Berapa E sel ? Jawab : Elektroda Zn : anoda ( oksidasi ) E Zn = 0, 7914 volt Elektroda kalomel normal : katoda ( reduksi ) E Kal = 0, 2800 volt E sel = E anoda + E katoda = 0, 7914 + 0, 2800 = 1, 0714 volt Berapa E sel bila pada elektroda kalomel a KCl = 0, 2 ?

EMF (E) dan Konstante kesetimbangan (K) a. A + b. B c. C + d. D K = a c. C. a d. D a a. A. a b. B Keadaan setimbang : ΔG = 0 ΔG = - n F E Pada 25 o. C : 0 = Eo – 0, 059 log ac. C. ad. D n a a A. ab B Eo = 0, 059 log K n E=0