MANAJEMEN FARMASI INDUSTRI Silabus Manajemen Farmasi Industri 1

MANAJEMEN FARMASI INDUSTRI

Silabus Manajemen Farmasi Industri 1. Pengantar 2. c-GMP (CPOB Terkini) 3. Validasi di Industri Farmasi 4. Registrasi dan Pendaftaran Obat Jadi 5. Manajemen Produksi dan Operasi Industri Farmasi 6. Pengelolaan Limbah Industri Farmasi (c) bambang. priyambodo@yahoo. co. id 2

Bahan Bacaan 1. Anonim, 2006, Pedoman Cara Pembuatan Obat yang Baik, edisi 2006. 2. Anonim, 2001, Petunjuk Operasional Cara Pembuatan Obat yang Baik. 3. Priyambodo, B. , 2007, Manajemen Farmasi Industri, Global Pustaka Utama, Yogyakarta 4. Nash, R. A. and Wacher A. , H. , 2003, Pharmaceutical Process Validation.

Pengantar Persyaratan/Jaminan : INDUSTRI FARMASI • Khasiat (efficacy) • Keamanan (safety) • Mutu (quality) (c) bambang. priyambodo@yahoo. co. id 5

Persyaratan Kualitas Obat Persyaratan Kualias Obat, menurut Academy of Pharmaceutical Science, USA : n Mengandung kuantitas masing-masing bahan aktif sesuai dengan persyaratan pada etiket, yang masih dalam nilai batas sesuai dengan spesifikasinya n Mengandung kuantitas bahan aktif yang sama, dalam setiap satuan takaran obat. Tidak boleh mengandung bahan lain, yang tidak dinyatakan secara jelas n Sampai saat digunakan oleh penderita, tetap terjaga potensi, penampilan dan ketersediaan terapeutikanya untuk tujuan pengobatan n Pada saat digunakan, melepaskan bahan aktif agar supaya tercapai secara penuh ketersediaan biologisnya PRODUK INDUSTRI FARMASI DIATUR SECARA KETAT, BAIK OLEH INDUSTRI FARMASI MAUPUN OLEH PEMERINTAH (c) bambang. priyambodo@yahoo. co. id 6

Kapitalisasi Pasar Farmasi Dunia $643 billion (c) bambang. priyambodo@yahoo. co. id 7
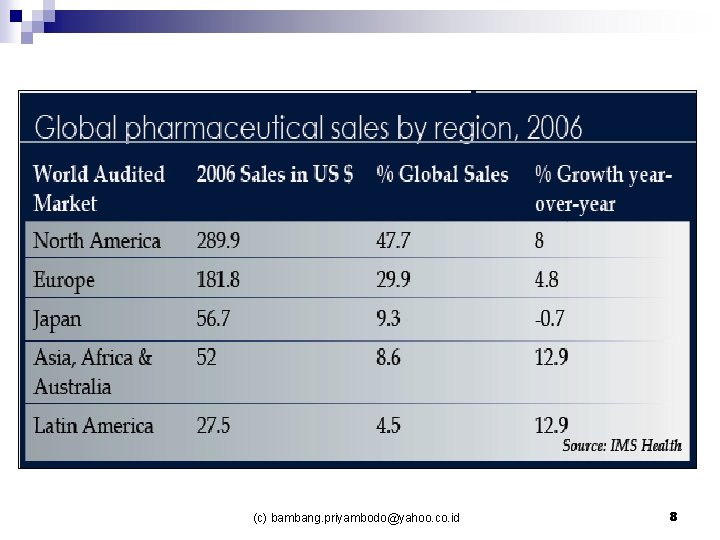
(c) bambang. priyambodo@yahoo. co. id 8
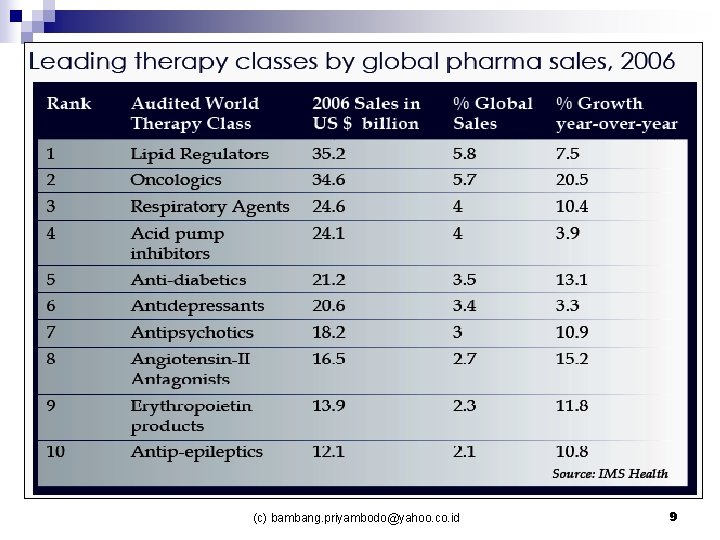
(c) bambang. priyambodo@yahoo. co. id 9
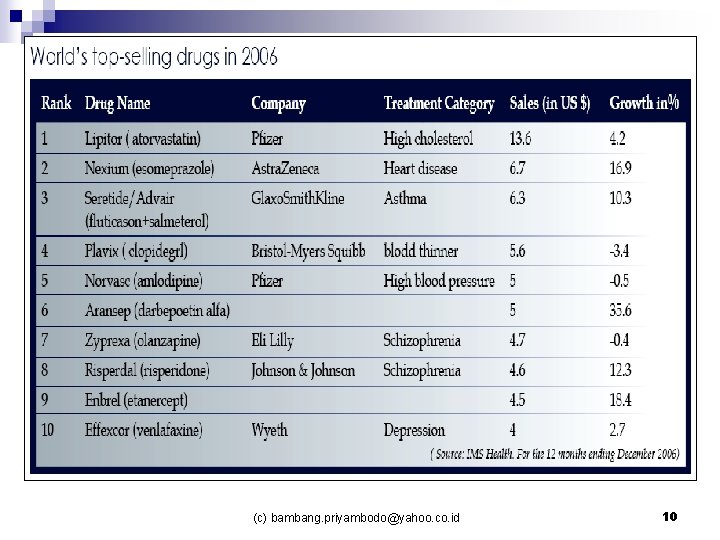
(c) bambang. priyambodo@yahoo. co. id 10
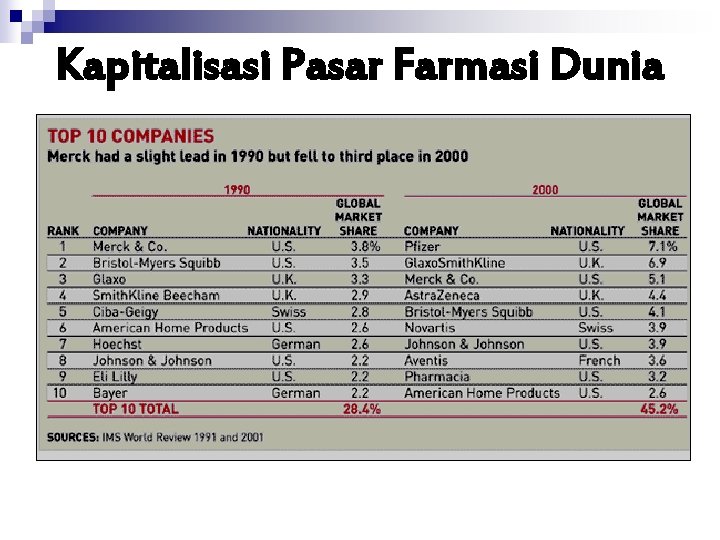
Kapitalisasi Pasar Farmasi Dunia
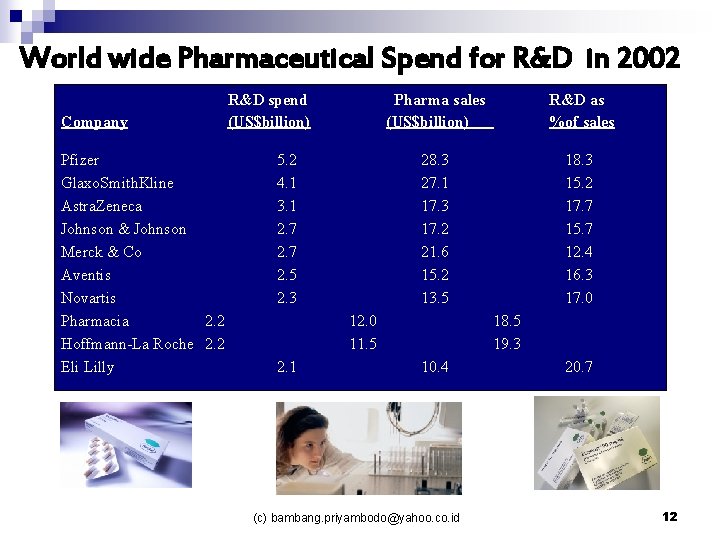
World wide Pharmaceutical Spend for R&D in 2002 Company Pfizer Glaxo. Smith. Kline Astra. Zeneca Johnson & Johnson Merck & Co Aventis Novartis Pharmacia 2. 2 Hoffmann-La Roche 2. 2 Eli Lilly R&D spend (US$billion) 5. 2 4. 1 3. 1 2. 7 2. 5 2. 3 Pharma sales (US$billion) R&D as %of sales 28. 3 27. 1 17. 3 17. 2 21. 6 15. 2 13. 5 18. 3 15. 2 17. 7 15. 7 12. 4 16. 3 17. 0 12. 0 11. 5 2. 1 18. 5 19. 3 10. 4 (c) bambang. priyambodo@yahoo. co. id 20. 7 12

Pengeluaran Industri Untuk R&D (c) bambang. priyambodo@yahoo. co. id 13
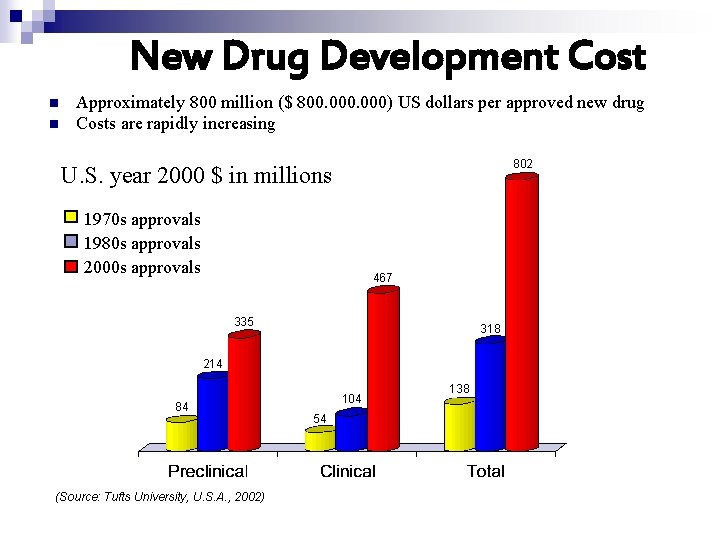
New Drug Development Cost n n Approximately 800 million ($ 800. 000) US dollars per approved new drug Costs are rapidly increasing 802 U. S. year 2000 $ in millions 1970 s approvals 1980 s approvals 2000 s approvals 467 335 318 214 84 (Source: Tufts University, U. S. A. , 2002) 104 54 138
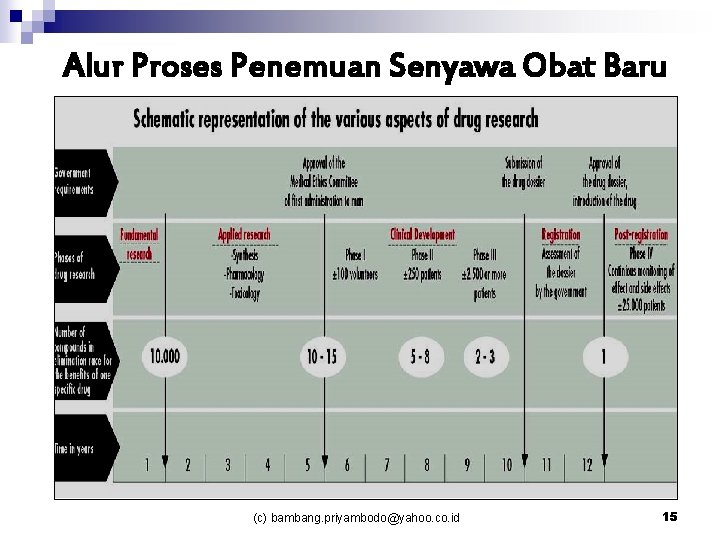
Alur Proses Penemuan Senyawa Obat Baru (c) bambang. priyambodo@yahoo. co. id 15
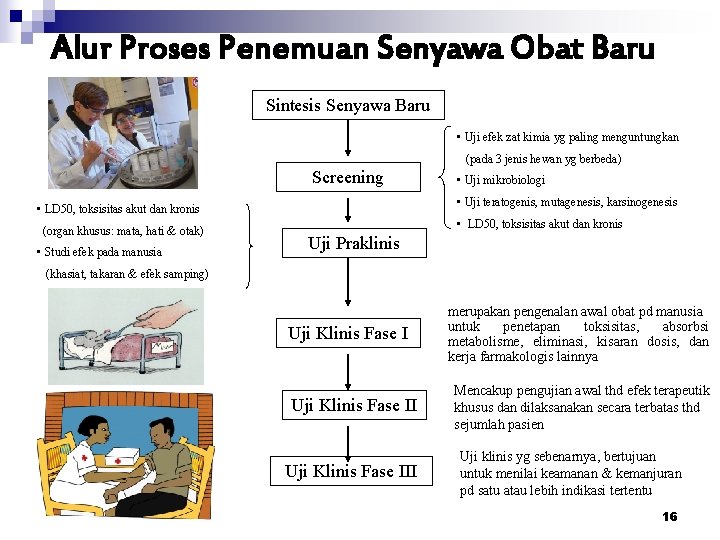
Alur Proses Penemuan Senyawa Obat Baru Sintesis Senyawa Baru • Uji efek zat kimia yg paling menguntungkan (pada 3 jenis hewan yg berbeda) Screening • Uji teratogenis, mutagenesis, karsinogenesis • LD 50, toksisitas akut dan kronis (organ khusus: mata, hati & otak) • Studi efek pada manusia • Uji mikrobiologi • LD 50, toksisitas akut dan kronis Uji Praklinis (khasiat, takaran & efek samping) Uji Klinis Fase III merupakan pengenalan awal obat pd manusia untuk penetapan toksisitas, absorbsi metabolisme, eliminasi, kisaran dosis, dan kerja farmakologis lainnya Mencakup pengujian awal thd efek terapeutik khusus dan dilaksanakan secara terbatas thd sejumlah pasien Uji klinis yg sebenarnya, bertujuan untuk menilai keamanan & kemanjuran pd satu atau lebih indikasi tertentu 16
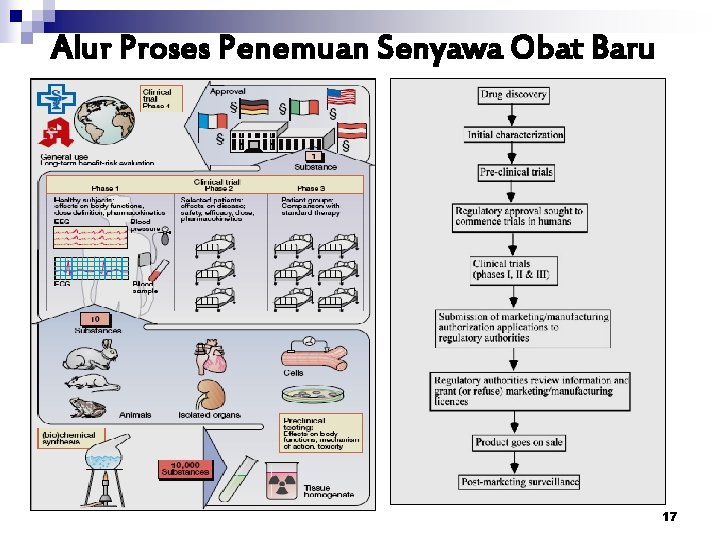
Alur Proses Penemuan Senyawa Obat Baru 17

Research & Development (R&D) 100, 000 molecules in laboratories 1 registered drugs at pharmacy development costs of 4 registered drugs are recovered 1 blockbuster (mega-seller) (c) bambang. priyambodo@yahoo. co. id 18

Ciri Industri Farmasi Ciri-ciri industri farmasi yang perlu diperhatikan : 1. Industri Farmasi merupakan industri yang diatur secara ketat, baik secara Nasional maupun Internasional (seperti registrasi obat, cara produksi obat yang baik/CPOB, distribusi dan perdagangan produk yang dihasilkan) 2. Industri farmasi, disamping menghasilkan obat untuk penderita, juga merupakan suatu industri yang berorientasi untuk memperoleh keuntungan (tidak hanya aspek sosial tapi juga ada aspek ekonomi) 3. Industri farmasi adalah satu industri beresiko tinggi, karena bukan tidak mungkin kelak dikemudian hari kalau terbukti bahwa terjadi akibat yang tidak diinginkan karena penggunaan obat, industri farmasi tersebut dituntut dan membayar ganti rugi (contoh : Industri farmasi penghasil Thalidomide ditutup karena tidak mampu lagi membayar tuntutan ganti rugi) 4. Industri Farmasi adalah industri berbasis riset yang selalu memerlukan inovasi, karena usia hidup obat relatif singkat ( lebih kurang 25 tahun) dan sesudah itu akan ditemukan obat generasi baru yang lebih baik, lebih aman dan lebih efektif (fenomena merger beberapa perusahaan farmasi raksasa dunia , seperti Glaxo Smith. Kline -Becheem, Aventis, Novartis Biochemie, Roche-Bayer, dll) (c) bambang. priyambodo@yahoo. co. id 19

Product Life Cycle (c) bambang. priyambodo@yahoo. co. id 20
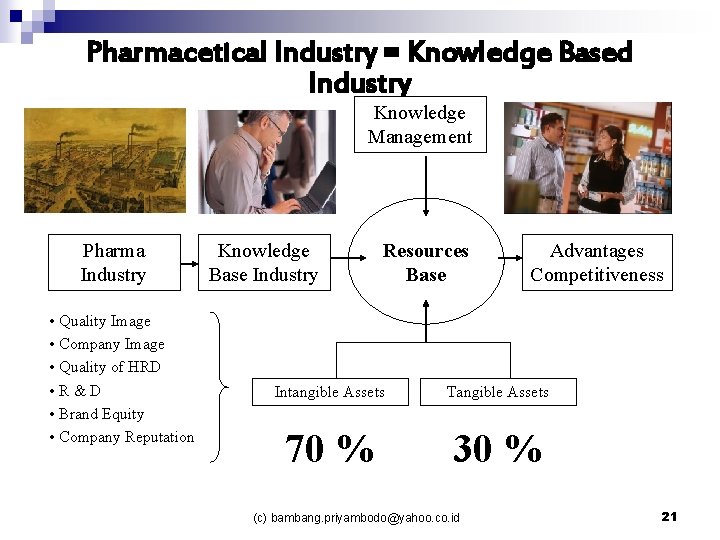
Pharmacetical Industry = Knowledge Based Industry Knowledge Management Pharma Industry • Quality Image • Company Image • Quality of HRD • R&D • Brand Equity • Company Reputation Knowledge Base Industry Resources Base Advantages Competitiveness Intangible Assets Tangible Assets 70 % 30 % (c) bambang. priyambodo@yahoo. co. id 21
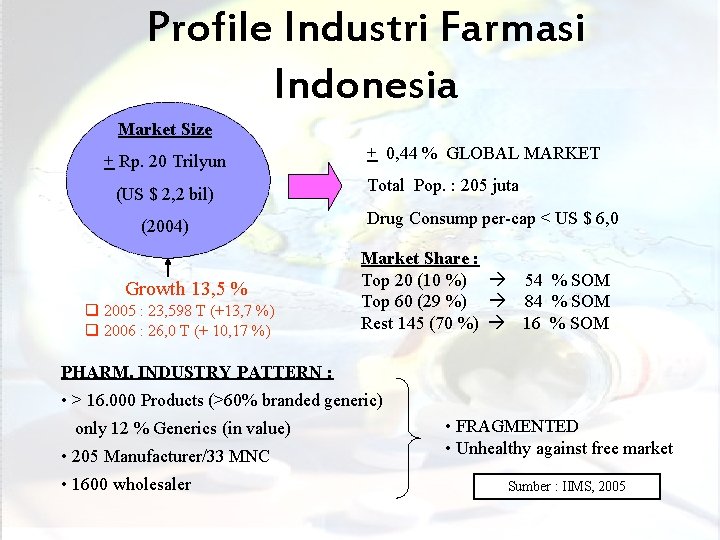
Profile Industri Farmasi Indonesia Market Size + 0, 44 % GLOBAL MARKET + Rp. 20 Trilyun Total Pop. : 205 juta (US $ 2, 2 bil) Drug Consump per-cap < US $ 6, 0 (2004) Growth 13, 5 % q 2005 : 23, 598 T (+13, 7 %) q 2006 : 26, 0 T (+ 10, 17 %) Market Share : Top 20 (10 %) 54 % SOM Top 60 (29 %) 84 % SOM Rest 145 (70 %) 16 % SOM PHARM. INDUSTRY PATTERN : • > 16. 000 Products (>60% branded generic) only 12 % Generics (in value) • 205 Manufacturer/33 MNC • FRAGMENTED • Unhealthy against free market • 1600 wholesaler Sumber : IIMS, 2005 (c) bambang. priyambodo@yahoo. co. id 22
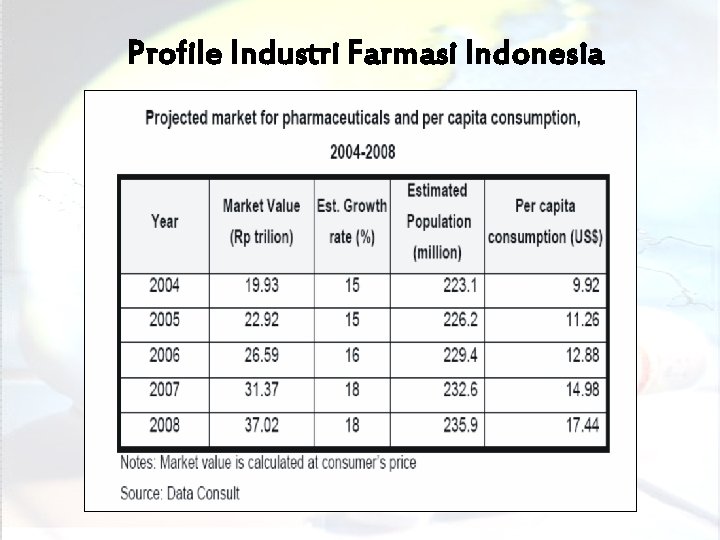
Profile Industri Farmasi Indonesia
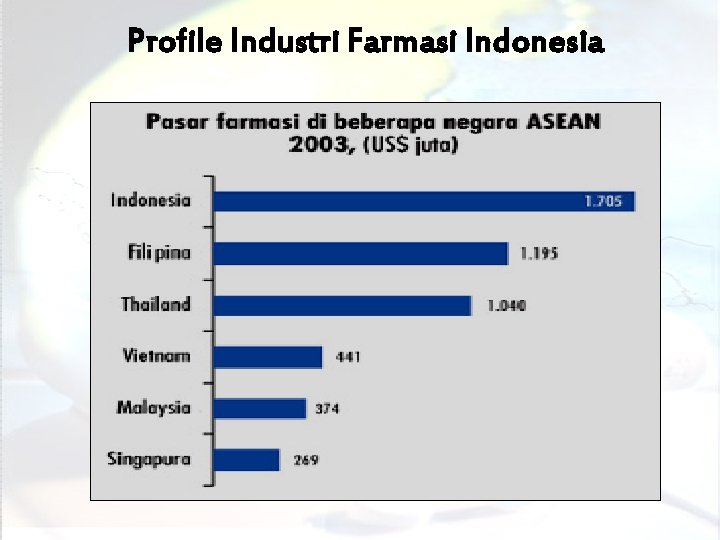
Profile Industri Farmasi Indonesia
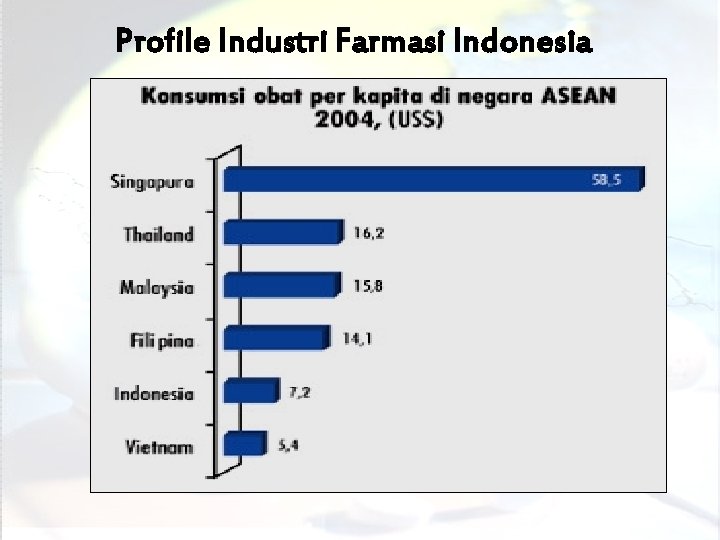
Profile Industri Farmasi Indonesia

Profile Industri Farmasi Indonesia Sumber : Badan POM 2004 (c) bambang. priyambodo@yahoo. co. id 26

Profile Industri Farmasi Indonesia (c) bambang. priyambodo@yahoo. co. id 27

Profile Industri Farmasi Indonesia Sumber : Badan POM 2004 (c) bambang. priyambodo@yahoo. co. id 28

Profile Industri Farmasi Indonesia Sumber : Badan POM 2004 (c) bambang. priyambodo@yahoo. co. id 29

Profile Industri Farmasi Indonesia

Permasalahan Industri Farmasi Indonesia 1. 2. 3. 4. Pemberdayaan idle capacity industri farmasi belum menemukan solusi yg tepat (termasuk alternatif melalui toll manufacturing maupun konsep production house). Kerjasama yang erat antar industri farmasih sulit terjalin dalam menemukan strategi untuk menghadapi invasi pasar Ketergantungan bahan baku impor (95%) belum diimbangi dengan upaya pengembangan bahan baku lokal, selain memerlukan biaya investasi yang tinggi, daya dukung peralatan masih belum memadai Antisipasi penerapan aturan internasional terhadap standarisasi industri farmasi terutama menyangkut c-GMP, harmonisasi registrasi dan belum adanya koordinasi yang baik antara industri farmasi dengan pemerintah (Badan POM) Kondisi (kemampuan) industri farmasi sendiri yang tidak merata. Sebagian sudah ada yang siap menghadapi pasar bebas, sebagian besar yang lain masih belum bisa memnuhi persyaratan, baik dari segi Hardware, Software maupun Brainware (c) bambang. priyambodo@yahoo. co. id 31

Kebijakan Badan POM n n n Peningkatan compliance terhadap persyaratan & standart pharma global Industri farmasi Nasional agar lebih efisien dan fokus dalam pelaksanaan produksi obat termasuk pemilihan fasilitas produksi yg paling feasible untuk dikembangkan Penerapan CPOB yang dinamis (c-GMP) sesuai standart internasional (dateline : Des 2007) (c) bambang. priyambodo@yahoo. co. id 32

Sejarah CPOB di Indonesia 1969 WHO Konsep “Good Practices in Manufacture quality Control of Drug” n 1971 Penerapan CPOB secara sukarela n 1988 Pedoman CPOB Edisi 1, dikeluarkan & mulai penerapannya n 1989 – 1994 Batas waktu pemenuhan CPOB ¨ 1990 Sertifikasi CPOB n 2001 Pedoman CPOB Edisi 2 n 2004 Addendum IV, GMP for Human Blood & Blood Products n 2005 Draft Pedoman CPOB Edisi 3 (c-GMP) n 2006 Finalisasi Pedoman CPOB Edisi 3 (c-GMP) n 2007 Batas waktu pemenuhan c-GMP Major Revisi : • Quality Management System • Persyaratan HVAC (terutama untuk produk-produk Steril) • Persyaratan Water System n (c) bambang. priyambodo@yahoo. co. id and 33

CPOB: 1988 - 2001 Aspek - Aspek dalam CPOB 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. Ketentuan Umum Personalia Bangunan dan Fasilitas Peralatan Sanitasi & Higiene Produksi Pengawasan Mutu Inspeksi Diri Penanganan Keluhan Terhadap Obat, Penarikan Kembali Obat dan Obat Kembalian Dokumentasi (c) bambang. priyambodo@yahoo. co. id 34

Aspek CPOB Terkini (CPOB: 2006) 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. Sistem Manajemen Mutu Personalia Bangunan dan Sarana Penunjang Peralatan Sanitasi dan Higiene Produksi Pengawasan Mutu Inspeksi Diri dan Audit Mutu Penanganan Keluhan terhadap Produk, Penarikan Kembali Produk dan Produk Kembalian Dokumentasi Pembuatan dan Analisis Berdasarkan Kontrak Kualifikasi dan Validasi

Aspek CPOB Terkini (CPOB: 2006) Annex 1. 2. 3. 4. 5. 6. 7. Pembuatan Produk Steril Produksi Produk Biologi Pembuatan Gas Medisinal Pembuatan Inhalasi Dosis Terukur Bertekanan (Aerosol) Pembuatan Produk Darah Pembuatan Obat Investigasi untuk Uji Klinis Sistem Komputerisasi

PENETAPAN STRATA INDUSTRI FARMASI n n n Total terdapat 289 item check-list Temuan per-individual komponen check list dibobot dengan prosentase berdasarkan tingkat kekritisan pemenuhan Penetapan Strata Industri Farmasi: ¨ Strata A : Hardware & Software memadai serta dilaksanakan secara konsisten ¨ Strata B : Salah satu diantara Hardware/software memerlukan perbaikan minor ¨ Strata C : Hardware dan software perlu perbaikan ¨ Strata D : Hardware dan software perlu perbaikan signifikan Boleh berproduksi di fasilitas milik sendiri dg perbaikan internal Strata C Sebagian diproduksi di fasilitas sendiri, sebagian toll mfg Strata D Toll Manufacture (jangka waktu tertentu) Strata A Strata B (c) bambang. priyambodo@yahoo. co. id 37

Hasil Mapping CPOB Tahun 2004 (c) bambang. priyambodo@yahoo. co. id 38
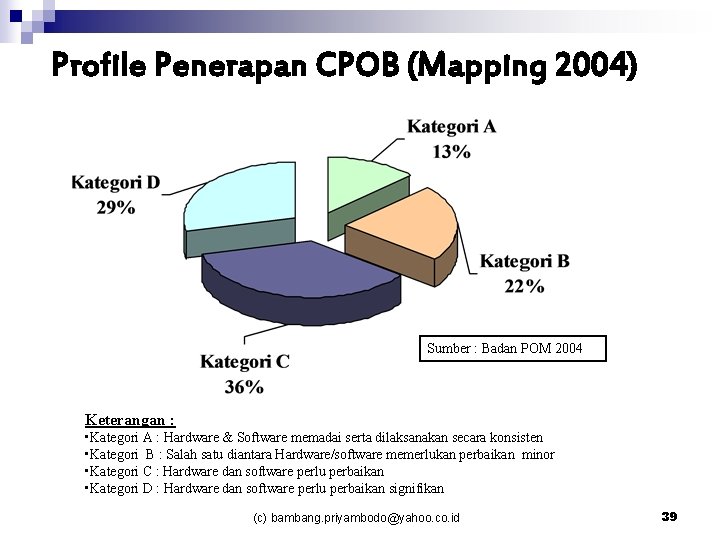
Profile Penerapan CPOB (Mapping 2004) Sumber : Badan POM 2004 Keterangan : • Kategori A : Hardware & Software memadai serta dilaksanakan secara konsisten • Kategori B : Salah satu diantara Hardware/software memerlukan perbaikan minor • Kategori C : Hardware dan software perlu perbaikan • Kategori D : Hardware dan software perlu perbaikan signifikan (c) bambang. priyambodo@yahoo. co. id 39

Profile Penerapan CPOB (Hasil Re. Mapping) Sumber : Badan POM 2008 Keterangan : • Kategori A : Hardware & Software memadai serta dilaksanakan secara konsisten • Kategori B : Salah satu diantara Hardware/software memerlukan perbaikan minor • Kategori C : Hardware dan software perlu perbaikan • Kategori D : Hardware dan software perlu perbaikan signifikan (c) bambang. priyambodo@yahoo. co. id 40
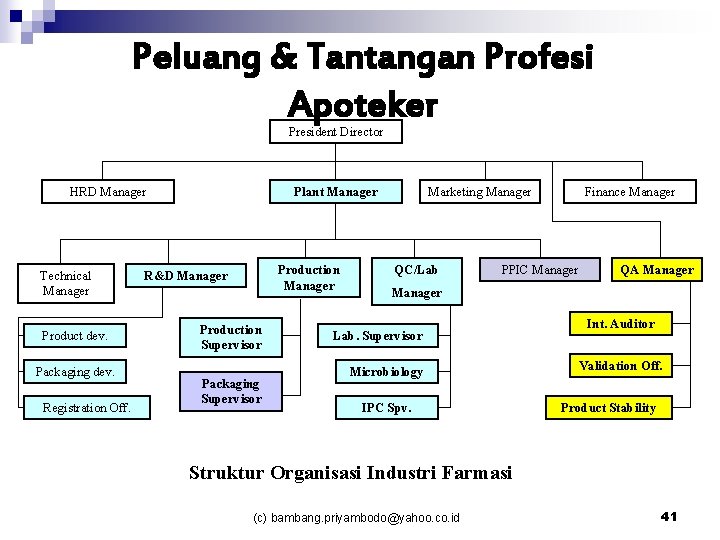
Peluang & Tantangan Profesi Apoteker President Director HRD Manager Technical Manager Product dev. Packaging dev. Registration Off. Plant Manager Production Manager R&D Manager Production Supervisor Packaging Supervisor Marketing Manager QC/Lab Finance Manager PPIC Manager QA Manager Lab. Supervisor Microbiology IPC Spv. Int. Auditor Validation Off. Product Stability Struktur Organisasi Industri Farmasi (c) bambang. priyambodo@yahoo. co. id 41

1. 2. Bidang Pengabdian Apoteker di Industri Farmasi Bidang Produksi a. Penanggung Jawab Produksi (Apoteker Penanggung Jawab) b. Perencanaan Produksi dan Pengendalian Persediaan (PPIC) c. Pengawas (Supervisor) Proses Pengolahan d. Pengawas (Supervisor) Proses Pengemasan Bidang Pengawasan Mutu a. Penanggung Jawab Pengawasan Mutu (Apoteker penanggung Jawab) b. Supervisor Laboratorium Pengujian c. Supervisor Laboratorium Pengawasan Selama Proses (IPC) d. Supervisor Laboratorium Mikrobiologi

Bidang Pengabdian Pharmacist di Industri 3. Bidang Penjaminan Mutu Farmasi 4. 5. a. Penanggung Jawab Jaminan Mutu (Apoteker Penanggung Jawab) b. Validation Officer c. Product Stability Officer d. Internal Audit Officer Bidang Penelitian dan Pengembangan a. Penanggung Jawab Penelitian dan Pengembangan b. Pengembangan Formula (Product Development Officer) c. Pengembangan Pengemasan (Packaging Development Officer) d. Standarisasi (Bahan Baku dan Bahan Pengemas) e. New Product Trial (Pengujian BA/BE) Bidang Legal dan Registrasi a. Penanggung Jawab Registrasi dan Pendaftaran Obat Jadi b. Registration Officer c. Legal Officer (patent, intellectual property right, lisensi, dll)

Apa yang perlu dikuasai oleh Mahasiswa Program Profesi Apoteker 1. 2. 3. 4. 5. 6. 7. 8. Penguasaan Teknologi Formulasi (> 80 % me too product) Penguasaan Metoda Analisa (Adopsi, Adaptasi maupun Pengembangan) Penguasaan Manajemen & Proses Produksi Penguasaan Sistem Manajemen Mutu (Quality Assurance, c. GMP, ISO 9000 series, ISO 14000 series, TQM, dll) Penguasaan Prosedur/tatacara Kalibrasi, Validasi/ Kualifikasi Mesin & Alat Produksi, Validasi Metode Analisa, Validasi Proses Produksi dan Pengemasan, dan Validasi Pembersihan Penguasaan Dokumentasi (Protap, Batch Record, Proses/ prosedur Registrasi) dan Pengembangan Produk Baru Pengetahuan Sarana Penunjang (Bangunan/peralatan, AHU, Dust Collecting System, Air Untuk Produksi, Pengolahan Limbah, dll) Penunjang : Manajemen SDM, Material Manajemen (PPIC), Marketing, dll Kurikulum Pendidikan Tinggi Farmasi ? ? ? (c) bambang. priyambodo@yahoo. co. id 44
- Slides: 44

































































