Reakcje chemiczne Krystyna Sitko Reakcje chemiczne l l




- Slides: 16

Reakcje chemiczne Krystyna Sitko

Reakcje chemiczne l l l Reakcje chemiczne są to takie przemiany, w wyniku których z jednych substancji powstają inne substancje, o zupełnie odmiennych właściwościach fizycznych i chemicznych. Substancje wchodzące w reakcje chemiczne noszą nazwę substratów. Substancje, które powstają w czasie reakcji chemicznych noszą nazwę produktów. Równanie reakcji chemicznej - zapis przebiegu procesu chemicznego za pomocą symboli pierwiastków chemicznych i wzorów związków chemicznych. Równanie reakcji chemicznej jest bardzo podobne do zwykłego równania matematycznego.

Ogólny zapis równania reakcji chemicznej Najczęściej substraty zapisujemy po lewej, a produkty po prawej stronie równania. Jeśli produkty reagują ze sobą, tworząc z powrotem substraty, to mówimy że reakcja jest odwracalna. Substraty i produkty to reagenty.

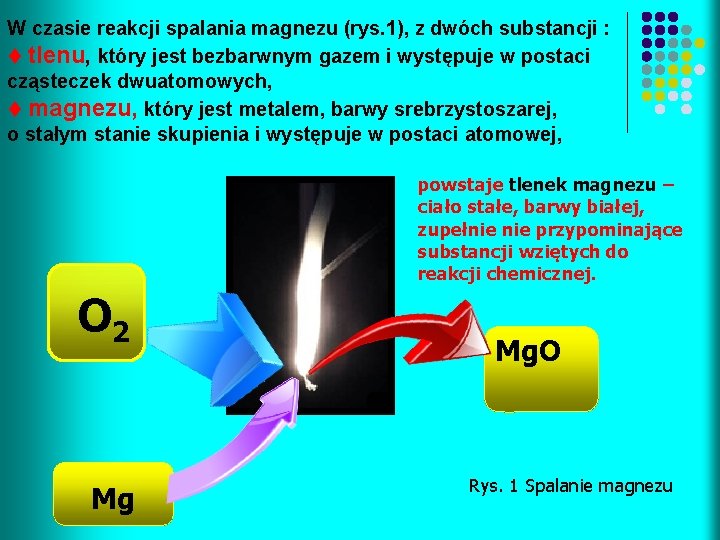
W czasie reakcji spalania magnezu (rys. 1), z dwóch substancji : t tlenu, który jest bezbarwnym gazem i występuje w postaci cząsteczek dwuatomowych, t magnezu, który jest metalem, barwy srebrzystoszarej, o stałym stanie skupienia i występuje w postaci atomowej, powstaje tlenek magnezu – ciało stałe, barwy białej, zupełnie przypominające substancji wziętych do reakcji chemicznej. O 2 Mg Mg. O Rys. 1 Spalanie magnezu

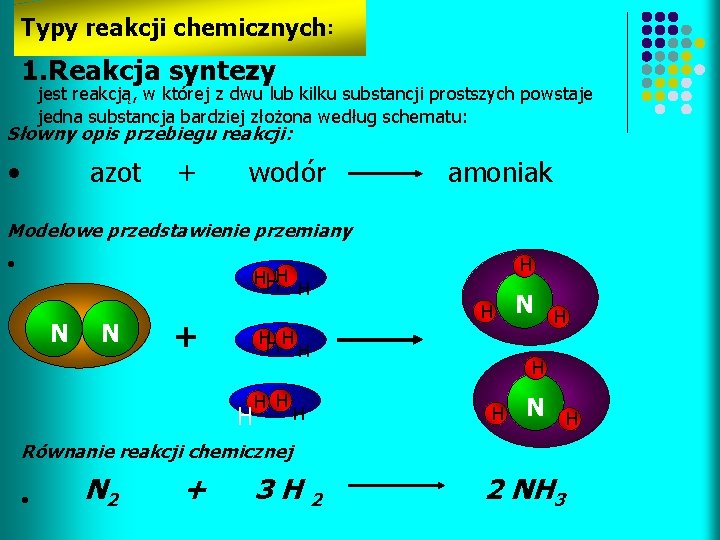
Typy reakcji chemicznych: 1. Reakcja syntezy jest reakcją, w której z dwu lub kilku substancji prostszych powstaje jedna substancja bardziej złożona według schematu: Słowny opis przebiegu reakcji: • azot + wodór amoniak Modelowe przedstawienie przemiany • H HHH N N H H + HH H H H N Równanie reakcji chemicznej • N 2 + 3 H 2 2 NH 3 H

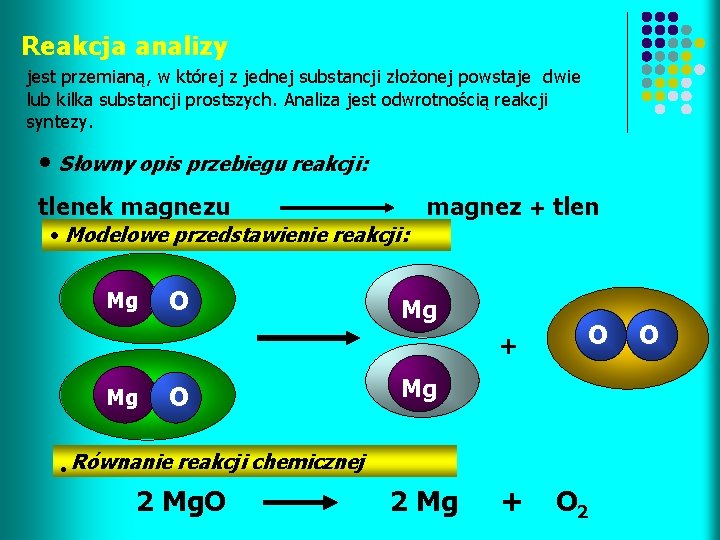
Reakcja analizy jest przemianą, w której z jednej substancji złożonej powstaje dwie lub kilka substancji prostszych. Analiza jest odwrotnością reakcji syntezy. • Słowny opis przebiegu reakcji: tlenek magnezu magnez + tlen • Modelowe przedstawienie reakcji: Mg O Mg + Mg • O O Mg Równanie reakcji chemicznej 2 Mg. O 2 Mg + O 2 O

Reakcja wymiany jest najczęściej spotykanym typem reakcji. W procesie tym następuje wymiana składników pomiędzy substancjami reagującymi. Wyróżnia się reakcje wymiany: • pojedynczej, Wymiana pojedyncza • podwójnej. Wymiana podwójna A + BC Kierunek reakcji AC + B Zn + 2 HCl ---> Zn. Cl 2 + H 2 2 K + 2 H 2 O ---> 2 KOH + H 2 AB + CD Kierunek reakcji AC + BD Mg. SO 4 + Na 2 CO 3 ---> Mg. CO 3 + Na 2 SO 4 H 2 SO 4 + Ca(OH)2 ---> Ca. SO 4 + 2 H 2 O

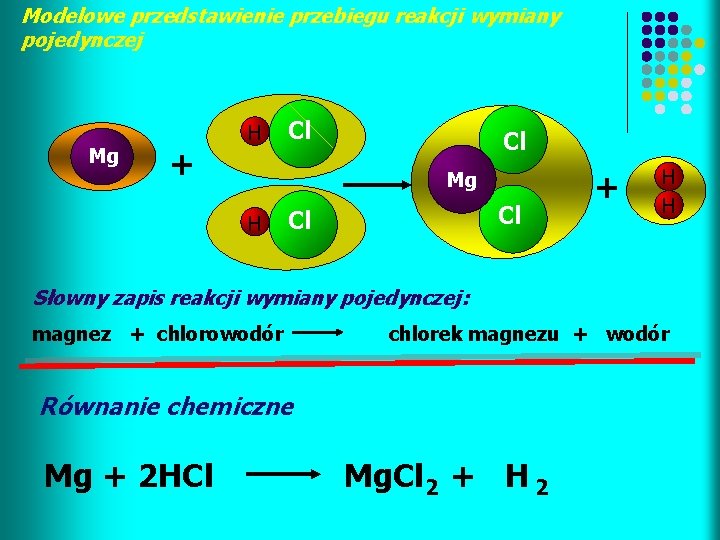
Modelowe przedstawienie przebiegu reakcji wymiany pojedynczej Mg + H Cl Cl Mg H Cl Cl + H H Słowny zapis reakcji wymiany pojedynczej: magnez + chlorowodór chlorek magnezu + wodór Równanie chemiczne Mg + 2 HCl Mg. Cl 2 + H 2

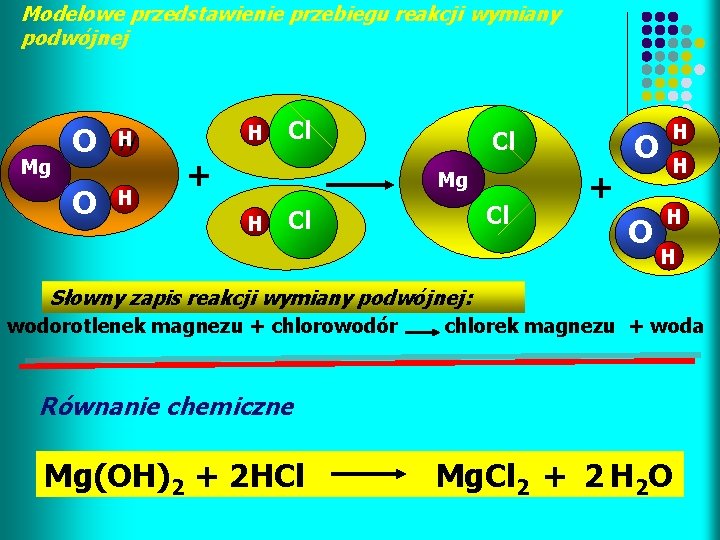
Modelowe przedstawienie przebiegu reakcji wymiany podwójnej Mg O O H H Cl + Cl Mg H Cl Cl O H + H H Słowny zapis reakcji wymiany podwójnej: wodorotlenek magnezu + chlorowodór chlorek magnezu + woda Równanie chemiczne Mg(OH)2 + 2 HCl Mg. Cl 2 + 2 H 2 O

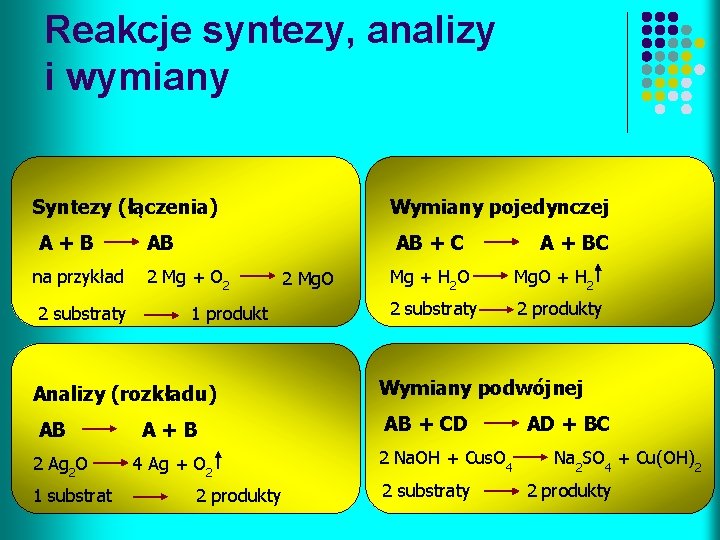
Reakcje syntezy, analizy i wymiany Syntezy (łączenia) Wymiany pojedynczej A+B AB + C na przykład 2 substraty AB 2 Mg + O 2 1 produkt 2 Mg. O A + BC Mg + H 2 O Mg. O + H 2 2 substraty 2 produkty Analizy (rozkładu) Wymiany podwójnej AB AB + CD 2 Ag 2 O 1 substrat A+B 4 Ag + O 2 2 produkty 2 Na. OH + Cus. O 4 2 substraty AD + BC Na 2 SO 4 + Cu(OH)2 2 produkty

na z - tr zo ną eg ew z Energia w reakcjach chemicznych Spalanie na przykład magnezu czy siarki w tlenie wymaga dostarczenia energii do zapoczątkowania reakcji. Potem proces spalania zachodzi gwałtownie z wydzieleniem energii cieplnej i świetlnej. Niektórym reakcjom mogą towarzyszyć również efekty akustyczne (wybuch). Takie reakcje przebiegające z wydzieleniem energii do otoczenia noszą nazwę reakcji egzoenergetycznych. Otrzymywanie tlenu z manganianu (VII) potasu zachodzi tylko wtedy, gdy dostarczamy przez cały czas energii. Reakcja chemiczna do której przebiegu konieczne jest ciągłe dostarczanie energii nosi nazwę reakcji endoenergetycznej end o wnę - do trza W życiu codziennym przykładem reakcji egzoenergetycznych jest spalanie drewna lub węgla kamiennego.

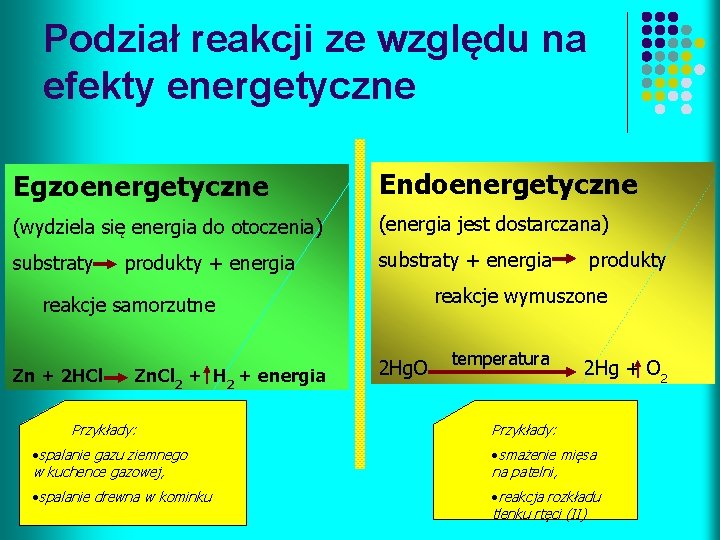
Podział reakcji ze względu na efekty energetyczne Egzoenergetyczne Endoenergetyczne (wydziela się energia do otoczenia) (energia jest dostarczana) substraty + energia produkty + energia reakcje wymuszone reakcje samorzutne Zn + 2 HCl Zn. Cl 2 + H 2 + energia Przykłady: produkty 2 Hg. O temperatura 2 Hg + O 2 Przykłady: • spalanie gazu ziemnego w kuchence gazowej, • smażenie mięsa na patelni, • spalanie drewna w kominku • reakcja rozkładu tlenku rtęci (II)

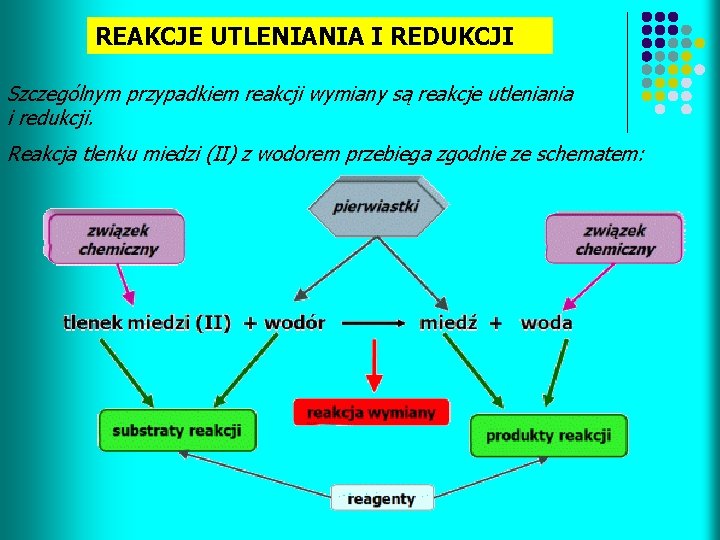
REAKCJE UTLENIANIA I REDUKCJI Szczególnym przypadkiem reakcji wymiany są reakcje utleniania i redukcji. Reakcja tlenku miedzi (II) z wodorem przebiega zgodnie ze schematem:

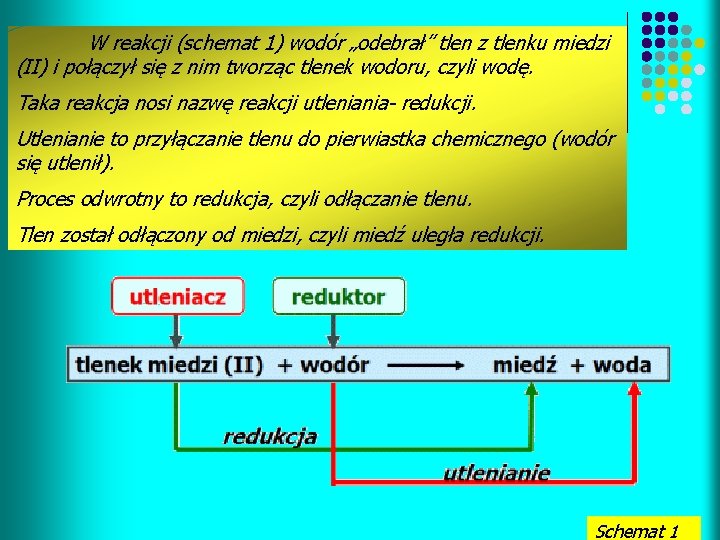
W reakcji (schemat 1) wodór „odebrał” tlen z tlenku miedzi (II) i połączył się z nim tworząc tlenek wodoru, czyli wodę. Taka reakcja nosi nazwę reakcji utleniania- redukcji. Utlenianie to przyłączanie tlenu do pierwiastka chemicznego (wodór się utlenił). Proces odwrotny to redukcja, czyli odłączanie tlenu. Tlen został odłączony od miedzi, czyli miedź uległa redukcji. Schemat 1

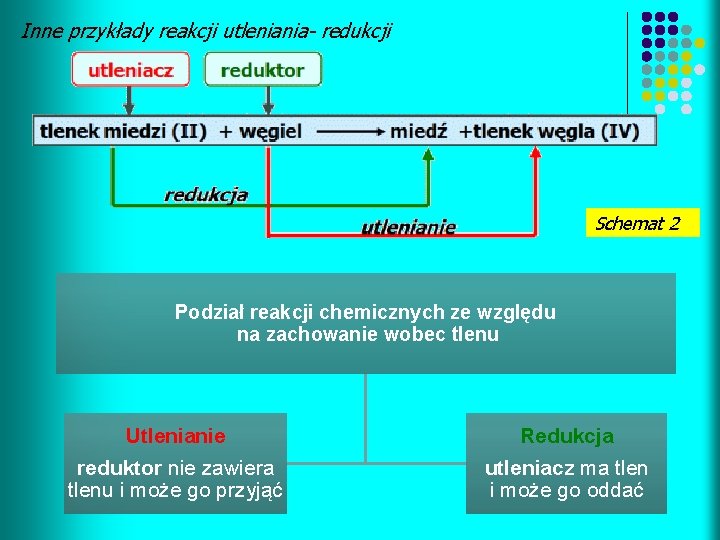
Inne przykłady reakcji utleniania- redukcji Schemat 2 Podział reakcji chemicznych ze względu na zachowanie wobec tlenu Utlenianie reduktor nie zawiera tlenu i może go przyjąć Redukcja utleniacz ma tlen i może go oddać

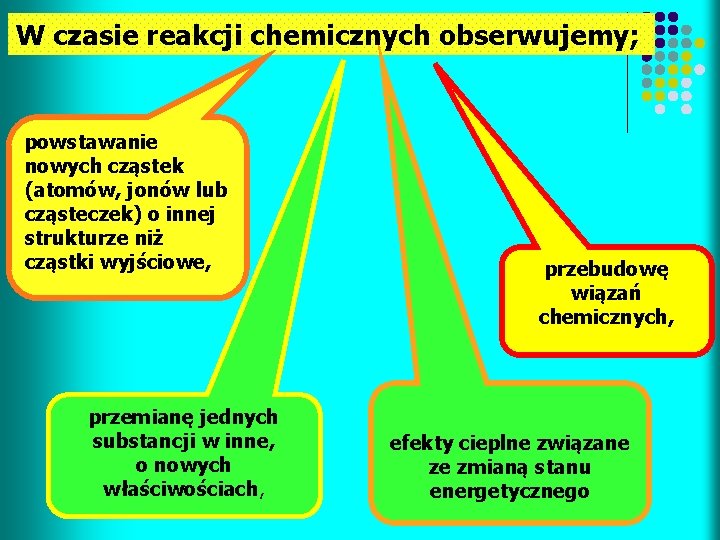
W czasie reakcji chemicznych obserwujemy; powstawanie nowych cząstek (atomów, jonów lub cząsteczek) o innej strukturze niż cząstki wyjściowe, przemianę jednych substancji w inne, o nowych właściwościach, przebudowę wiązań chemicznych, efekty cieplne związane ze zmianą stanu energetycznego