Mied i srebro oraz ich zwizki Wystpowanie i

Miedź i srebro oraz ich związki Występowanie i Otrzymywanie miedzi oraz srebra, - Właściwości fizyczne miedzi i srebra, - Właściwości chemiczne miedzi i srebra, - ważniejsze związki miedzi i srebra -

Występowanie i otrzymywanie miedzi 1. - Występowanie – w przyrodzie występuje w stanie rodzimym oraz w związkach, główne minerały to: Chalkozyn – Cu 2 S, Chalkopiryt – Cu. Fe. S 2, Kowelin – Cu. S, Kupryt – Cu 2 O, Malachit – Cu 2 CO 3(OH)2, Azuryt – Cu 3(CO 3)3(OH)2
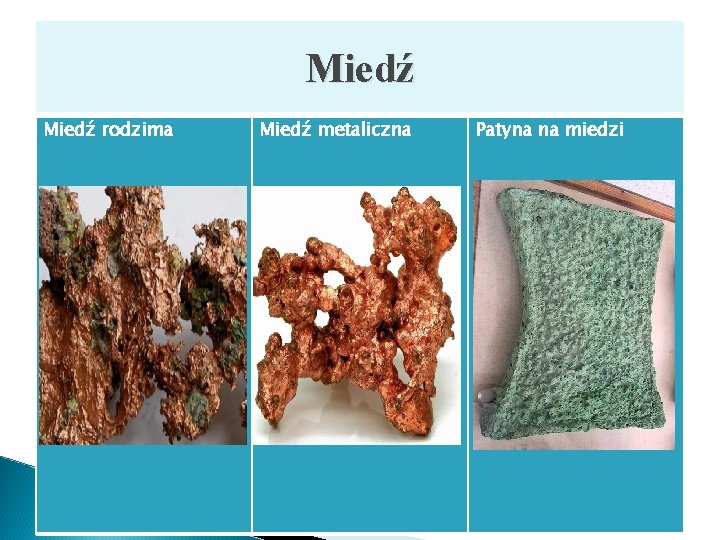
Miedź rodzima Miedź metaliczna Patyna na miedzi

Występowanie i otrzymywanie miedzi - cd 2. Otrzymywanie miedzi metalicznej Prażenie rud siarczkowych w obecności powietrza, produktem przejściowym jest tlenek miedzi(I) i siarczek miedzi(I), które reagują ze sobą dając tzw. miedź surową: - Cu 2 S + 2 Cu 2 O 6 Cu + SO 2 Redukcja rud tlenkowych i węglanowych węglem - Cu 2 O + C 2 Cu + CO 2 Surową miedź poddaje się rafinacji w procesie elektrolizy elektrolitu zawierającego rozcieńczony H 2 SO 4 i Cu. SO 4, anodą jest surowa miedź, natomiast katodą czysta miedź: - A(+): Cu 2+ + 2 e- K(-): Cu 2+ + 2 e- Cu

Występowanie i otrzymywanie srebra 1. W przyrodzie srebro występuje w postaci rodzimej oraz w minerałach Ag 2 S – argentyt, Ag. Cl – srebro rogowe (domieszki rud cynku, ołowiu, miedzi). 2. Srebro metaliczne otrzymuje się w procesie elektrolizy, w procesie elektrolizy miedzi srebro nie ulega rozpuszczeniu i opada na dno elektrolizera w postaci szlamu anodowego, szlam przerabia się elektrolitycznie i chemicznie [rozpuszczenie w Na. CN, powstające związki kompleksowe (cyjanki) są dobrze rozpuszczalne w wodzie] w celu otrzymania srebra oraz innych metali o wyższym potencjale standardowym niż potencjał miedzi, na 1000 kg miedzi surowej przypada 2 kg srebra i 50 g złota.

Właściwości fizyczne miedzi i srebra 1. Miedź – metal barwy „różowej”, miękki, ciągliwy i kowalny, jest bardzo dobrym przewodnikiem ciepła oraz prądu elektrycznego (drugi po srebrze), domieszki innych metali zwiększają jej opór właściwy. 2. Srebro – metal biały, silnie błyszczący, miękki, kowalny, ciągliwy (z 1 kg srebra można wyciągnąć drut o długości 2 km – nitka srebrna) najlepszy spośród metali przewodnik ciepła i prądu elektrycznego.

Srebro rodzime Srebro metaliczne

Właściwości chemiczne miedzi i jej związki Reakcja z tlenem w suchym powietrzu – pokrywa się warstewką tlenków miedzi o barwie czerwonobrązowej, które łatwo można usunąć metanolem, Reakcje w wilgotnym powietrzu – pod wpływem wody, CO 2 i tlenków siarki powstaje zielona patyna – mieszanina hydroksosoli: Cu 2 CO 3(OH)2 i Cu 2(OH)2 SO 4 [(Cu. OH)2 CO 3; (Cu. OH)2 SO 4] W podwyższonej temperaturze reaguje z tlenem (w zależności od warunków reakcji powstaje Cu 2 O lub Cu. O) , fluorowcami i siarką.

Właściwości chemiczne miedzi i jej związki - cd 1. Miedź nie reaguje z wodą i z kwasami nieutleniającymi (miedź posiada wysoki, dodatni standardowy potencjał elektrodowy). 2. Reakcje z kwasami utleniającymi (HNO 3 i stężony H 2 SO 4): - Cu + 4 HNO 3(stęż) Cu(NO 3)2 + 2 NO 2 + 2 H 2 O - 3 Cu + 8 HNO 3(rozc) 3 Cu(NO 3)2 + 2 NO + 4 H 2 O - Cu + 2 H 2 SO 4(stęż) Cu. SO 4 + SO 2 + 2 H 2 O - Powstające roztwory soli mają barwę niebieską pochodzącą od kationu Cu 2+, w reakcji ze stężonym HNO 3 roztwór ma początkowo barwę zieloną, ale po rozcieńczeniu przyjmuje barwę niebieską. 3. Kationy Cu+ w roztworze wodnym są nietrwałe i ulegają dysproporcjonowaniu: 2 Cu+ Cu 2+ + Cu

Właściwości chemiczne miedzi i jej związki - cd 1. Tlenki miedzi – mają charakter amfoteryczny, Cu 2 O – marchewkowo-czerwony, Cu. O – czarny 2. Otrzymywanie Termiczny rozkład: Cu(OH)2 Cu. O + H 2 O Reakcja z tlenem w podwyższonej temperaturze, Redukcja Cu. O miedzą: Cu. O + Cu 2 O Tlenek miedzi(II) ma dość silne właściwości utleniające, stosuje się jako łagodne utleniacze w chemii organicznej: utlenianie alkoholi, utlenianie aldehydów (próba Trommera).

Właściwości chemiczne miedzi i jej związki - cd Wodorotlenek miedzi(II) – niebieski, nierozpuszczalny w wodzie, ma charakter amfoteryczny Otrzymywanie – reakcja wymiany podwójnej, wytrącenie kationów Cu 2+ roztworem zasady - Cu 2+ + 2 OH- Cu(OH)2 - Cu(OH)2 + 2 H+ Cu 2+ + 2 H 2 O - Cu(OH)2 + 2 HO- [Cu(OH)4]2 - (anion tetrahydroksomiedzianu(II) barwy granatowej Cu(OH)2 – tworzy związki kompleksowe z alkoholami polihydroksylowymi i cukrami barwy niebieskofioletowej, stosowany jest do ich wykrywania.
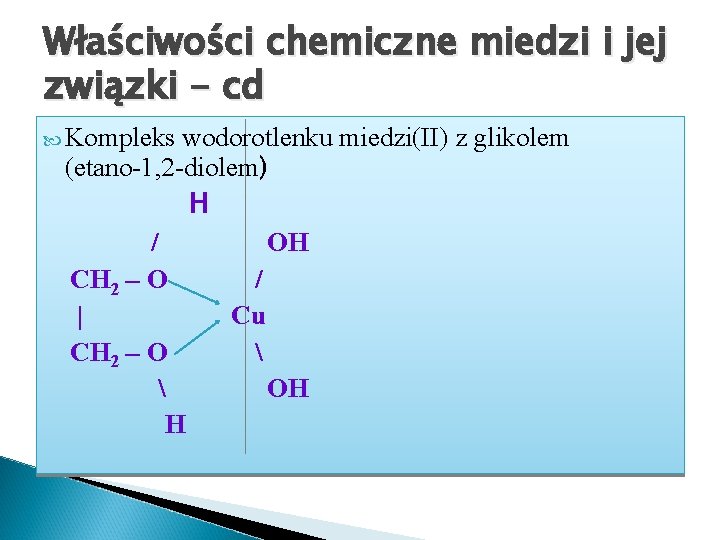
Właściwości chemiczne miedzi i jej związki - cd Kompleks wodorotlenku miedzi(II) z glikolem (etano-1, 2 -diolem) H / OH CH 2 – O / | Cu CH 2 – O OH H
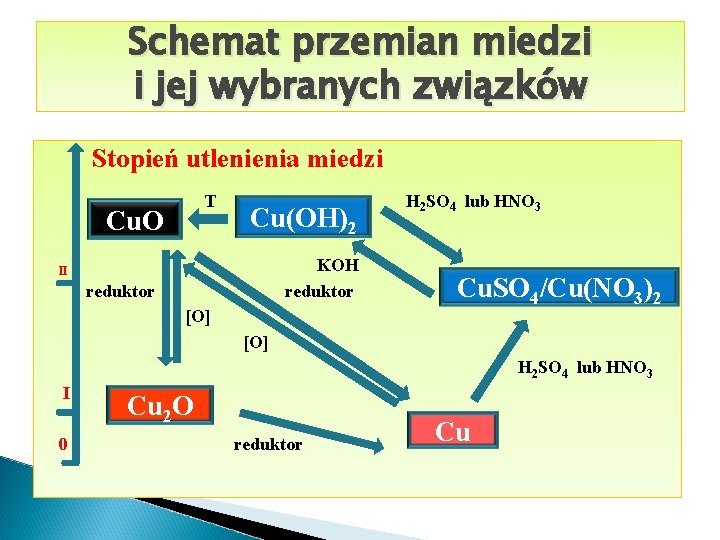
Schemat przemian miedzi i jej wybranych związków Stopień utlenienia miedzi T Cu. O Cu(OH)2 KOH reduktor II reduktor [O] H 2 SO 4 lub HNO 3 Cu. SO 4/Cu(NO 3)2 [O] H 2 SO 4 lub HNO 3 I 0 Cu 2 O reduktor Cu

Właściwości chemiczne srebra i jego związki Reakcja z siarką lub siarkowodorem w obecności tlenu – srebro matowieje i pokrywa się czarnym nalotem Ag 2 S, Nie reaguje z wodą i nieutleniającymi kwasami (patrz Cu) Ulega roztworzeniu w reakcji z kwasami utleniającymi: - Ag + 2 HNO 3(stęż) Ag. NO 3 + NO 2 + 2 H 2 O - 3 Ag + 4 HNO 3(rozc) 3 Ag. NO 3 + NO + H 2 O - 2 Ag + 2 H 2 SO 4(stęż) Ag 2 SO 4 + SO 2 + 2 H 2 O W reakcji azotanu(V) srebra z roztworami wodorotlenków litowców powstaje wodorotlenek srebra(I) barwy brązowej, który natychmiast ulega rozkładowi do tlenku srebra(I): 2 Ag+ 2 OH- ↓Ag 2 O + H 2 O

Właściwości chemiczne srebra i jego związki - cd Reakcja Ag+ z wodą amoniakalną – powstaje rozpuszczalny w wodzie wodorotlenek diaminasrebra(I), nazywany również amoniakalnym roztworem tlenku srebra(I) : [Ag(NH 3)2](OH). Powyższy wodorotlenek ma łagodne właściwości utleniające, ma zastosowanie w chemii organicznej do wykrywania aldehydów, cukrów aldoz – reakcja lustra srebrnego (próba Tollensa), ponadto stosuje się do srebrzenia bombek oraz w produkcji luster srebrnych.

Właściwości chemiczne srebra i jego związki - cd Proces fotograficzny – chlorek, bromek i jodek srebra są solami, które ulegają rozkładowi pod wpływem światła. Klisza jest pokryta emulsją – zawiesiną żelatyny i w/w soli srebra Naświetlenie kliszy; następuje rozkład Ag. Br, atomy bromu wiązane są przez żel a atomy srebra tworzą skupiska – ziarna. Wywołanie kliszy przy użyciu łagodnego reduktora (hydrochinonu) polega na redukcji kationów srebra wokół ziaren srebra Utrwalenie kliszy – działanie utrwalaczem (tiosiarczanem(VI) sodu), który usuwa z kliszy nierozłożoną światłoczułą substancję poprzez związanie srebra w rozpuszczalne w wodzie związki kompleksowe – powstaje negatyw Pozytyw – naświetlenie poprzez negatyw papieru z odwrotnym rozłożeniem światła i cienia, dalsza obróbka tak jak przy wywołaniu i utrwaleniu kliszy.

Materiały źródłowe: 1. Adam Bielański – Chemia ogólna i nieorganiczna 2. M. Grębosz, S. Zapotoczny – Słownik szkolny – Chemia 3. A. Bogdańska Zarembina, E. I. Matusewicz, J. Matusewicz – Chemia dla szkół średnich 4. R. Hassa, A. Mrzigod, J. Mrzigod, W. Sułkowski – Chemia – podręcznik i zbiór zadań w jednym 5. M. Litwin, S. Styka – Wlazło, J. Szymońska – Chemia ogólna i nieorganiczna 6. J. Sawicka, A. Janich-Kilian, W. Cejner-Mania, G. Urbańczyk – Tablice chemiczne 7. K. M. Pazdro – Chemia podręcznik do kształcenia rozszerzonego w liceach Materiał zdjęciowy: 1. Wikipedia 2. Zdjęcia własne
- Slides: 17