Reakcje zwizkw organicznych wglowodory Reakcje alkanw Reakcje alkenw

- Slides: 8

Reakcje związków organicznych – węglowodory -Reakcje alkanów -Reakcje alkenów -Reakcje alkinów -Reakcje arenów

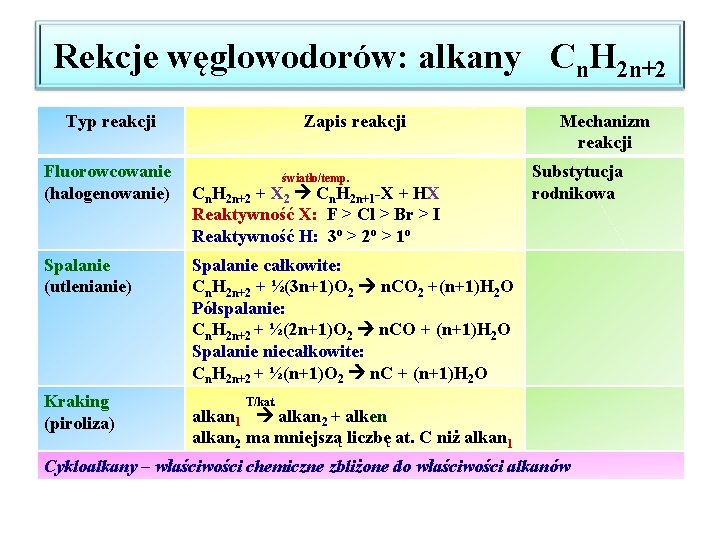
Rekcje węglowodorów: alkany Cn. H 2 n+2 Typ reakcji Fluorowcowanie (halogenowanie) Spalanie (utlenianie) Kraking (piroliza) Zapis reakcji światło/temp. Cn. H 2 n+2 + X 2 Cn. H 2 n+1 -X + HX Reaktywność X: F > Cl > Br > I Reaktywność H: 3 o > 2 o > 1 o Mechanizm reakcji Substytucja rodnikowa Spalanie całkowite: Cn. H 2 n+2 + ½(3 n+1)O 2 n. CO 2 +(n+1)H 2 O Półspalanie: Cn. H 2 n+2 + ½(2 n+1)O 2 n. CO + (n+1)H 2 O Spalanie niecałkowite: Cn. H 2 n+2 + ½(n+1)O 2 n. C + (n+1)H 2 O T/kat. alkan 1 alkan 2 + alken alkan 2 ma mniejszą liczbę at. C niż alkan 1 Cykloalkany – właściwości chemiczne zbliżone do właściwości alkanów

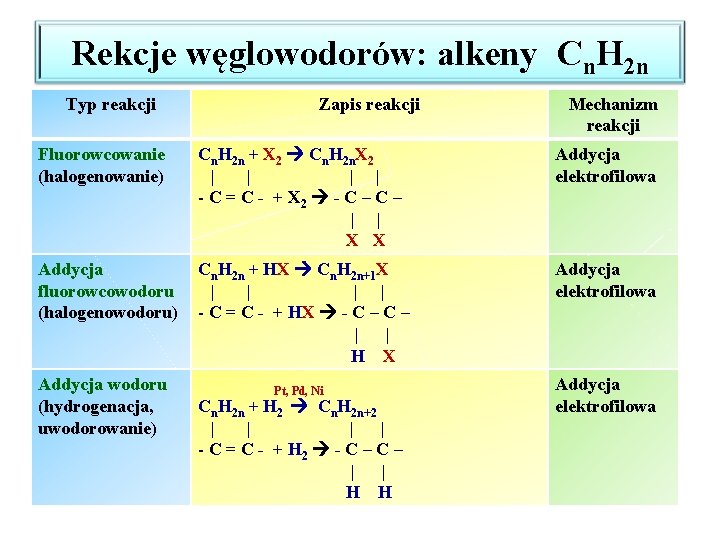
Rekcje węglowodorów: alkeny Cn. H 2 n Typ reakcji Zapis reakcji Mechanizm reakcji Fluorowcowanie (halogenowanie) Cn. H 2 n + X 2 Cn. H 2 n. X 2 | | - C = C - + X 2 - C – | | X X Addycja elektrofilowa Addycja fluorowcowodoru (halogenowodoru) Cn. H 2 n + HX Cn. H 2 n+1 X | | - C = C - + HX - C – | | H X Addycja elektrofilowa Addycja wodoru (hydrogenacja, uwodorowanie) Pt, Pd, Ni Cn. H 2 n + H 2 Cn. H 2 n+2 | | - C = C - + H 2 - C – | | H H Addycja elektrofilowa

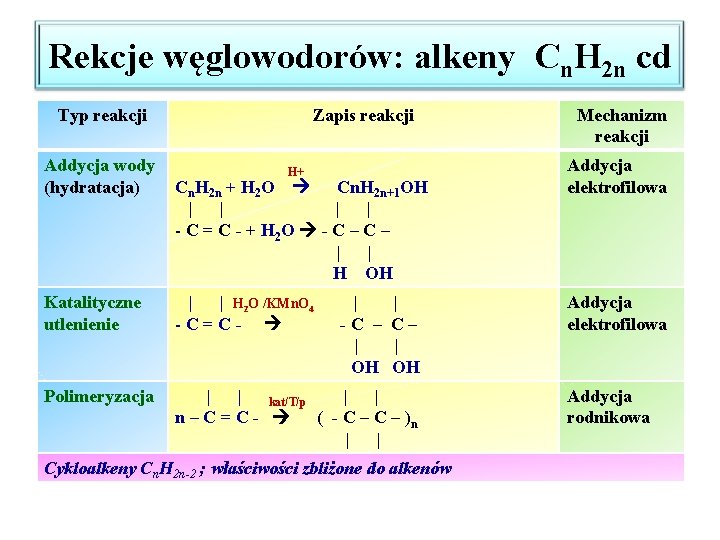
Rekcje węglowodorów: alkeny Cn. H 2 n cd Typ reakcji Addycja wody (hydratacja) Zapis reakcji H+ Cn. H 2 n + H 2 O Cn. H 2 n+1 OH | | - C = C - + H 2 O - C – | | H OH Katalityczne utlenienie | | H 2 O /KMn. O 4 -C=C- | -C – | OH | C– | OH Polimeryzacja | | kat/T/p n–C=C- ( - C – )n | | Cykloalkeny Cn. H 2 n-2 ; właściwości zbliżone do alkenów Mechanizm reakcji Addycja elektrofilowa Addycja rodnikowa

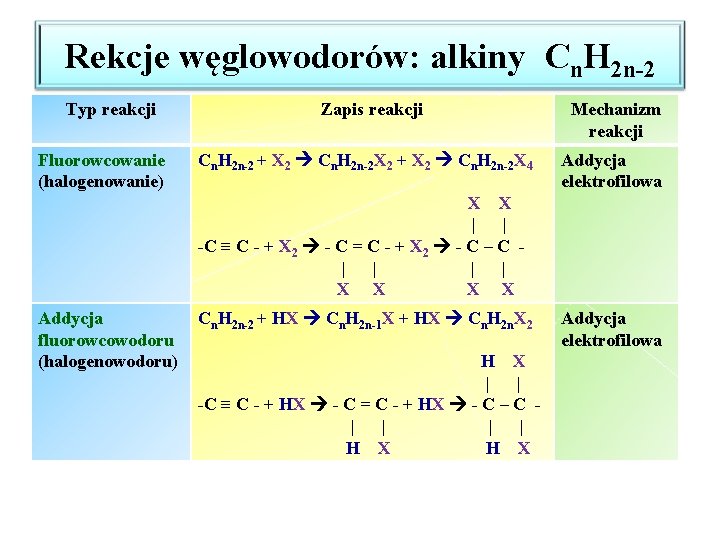
Rekcje węglowodorów: alkiny Cn. H 2 n-2 Typ reakcji Fluorowcowanie (halogenowanie) Zapis reakcji Cn. H 2 n-2 + X 2 Cn. H 2 n-2 X 4 Mechanizm reakcji Addycja elektrofilowa X X | | -C ≡ C - + X 2 - C = C - + X 2 - C – C | | X X Addycja fluorowcowodoru (halogenowodoru) Cn. H 2 n-2 + HX Cn. H 2 n-1 X + HX Cn. H 2 n. X 2 H X | | -C ≡ C - + HX - C = C - + HX - C – C | | H X Addycja elektrofilowa

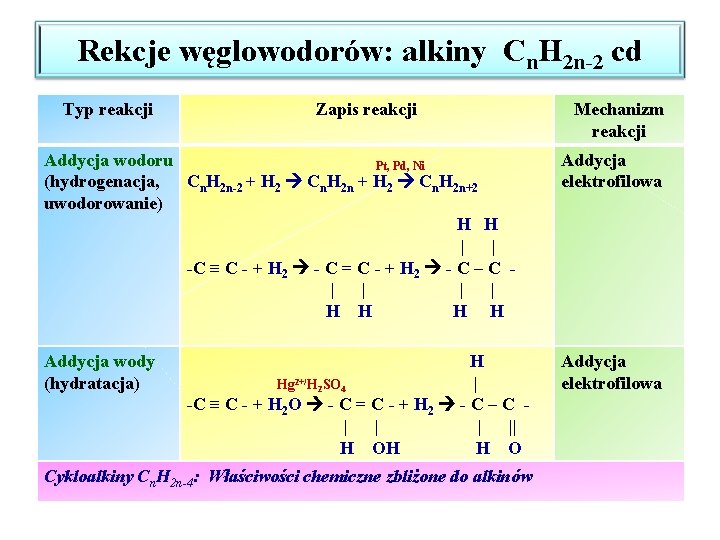
Rekcje węglowodorów: alkiny Cn. H 2 n-2 cd Typ reakcji Zapis reakcji Mechanizm reakcji Addycja wodoru Pt, Pd, Ni (hydrogenacja, Cn. H 2 n-2 + H 2 Cn. H 2 n+2 uwodorowanie) H H | | -C ≡ C - + H 2 - C = C - + H 2 - C – C | | H H Addycja elektrofilowa Addycja wody (hydratacja) Addycja elektrofilowa H Hg 2+/H 2 SO 4 | -C ≡ C - + H 2 O - C = C - + H 2 - C – C | || H OH H O Cykloalkiny Cn. H 2 n-4: Właściwości chemiczne zbliżone do alkinów

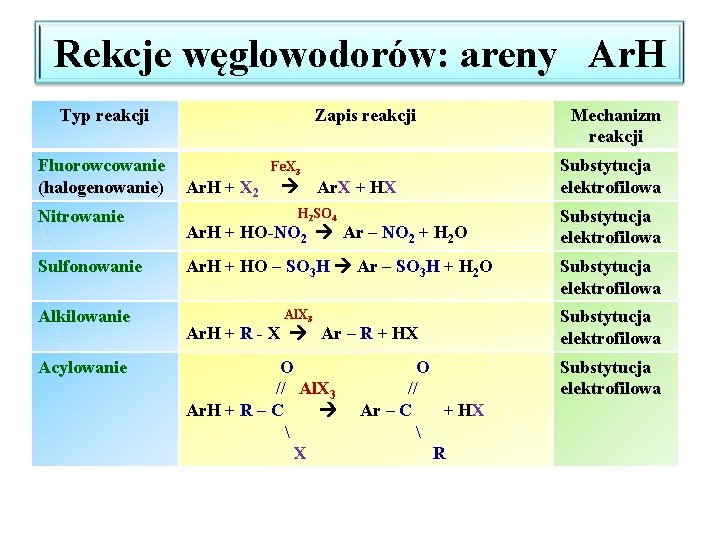
Rekcje węglowodorów: areny Ar. H Typ reakcji Fluorowcowanie (halogenowanie) Nitrowanie Sulfonowanie Alkilowanie Acylowanie Zapis reakcji Fe. X 3 Ar. H + X 2 Ar. X + HX H 2 SO 4 Ar. H + HO-NO 2 Ar – NO 2 + H 2 O Ar. H + HO – SO 3 H Ar – SO 3 H + H 2 O Al. X 3 Ar. H + R - X Ar – R + HX O // Al. X 3 Ar. H + R – C X O // Ar – C + HX R Mechanizm reakcji Substytucja elektrofilowa Substytucja elektrofilowa

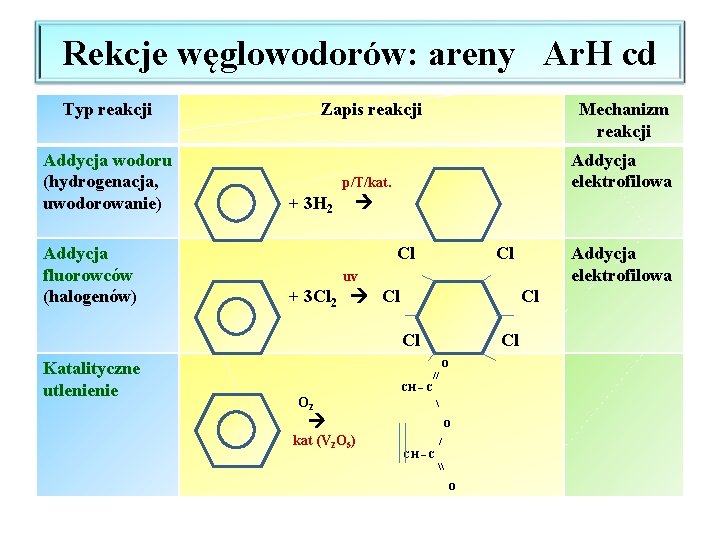
Rekcje węglowodorów: areny Ar. H cd Typ reakcji Addycja wodoru (hydrogenacja, uwodorowanie) Addycja fluorowców (halogenów) Zapis reakcji Mechanizm reakcji Addycja elektrofilowa p/T/kat. + 3 H 2 Cl Cl uv + 3 Cl 2 Cl Cl Cl Katalityczne utlenienie Addycja elektrofilowa Cl O // CH – C O 2 kat (V 2 O 5) O / CH – C \ O