Radiothrapie des cancers du sein p T 1




















- Slides: 37

Radiothérapie des cancers du sein p. T 1 a, b « Groupe : petites tumeur » Yazid Belkacémi, David Coeffic, Paul Cottu, Florence Dalenc, William Jacot et Magali Lacroix-Triki

Conflits d’intérêts : Aucun

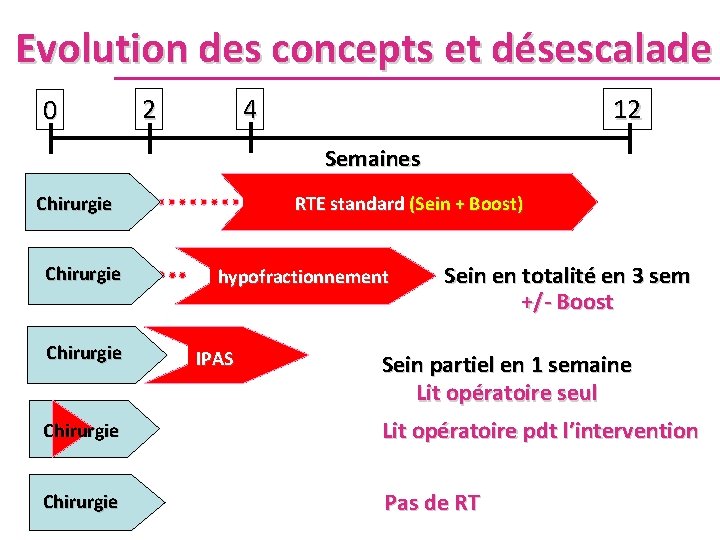
Evolution des concepts et désescalade 0 2 4 12 Semaines Chirurgie RTE standard (Sein + Boost) hypofractionnement IPAS Sein en totalité en 3 sem +/- Boost Sein partiel en 1 semaine Lit opératoire seul Chirurgie Lit opératoire pdt l’intervention Chirurgie Pas de RT

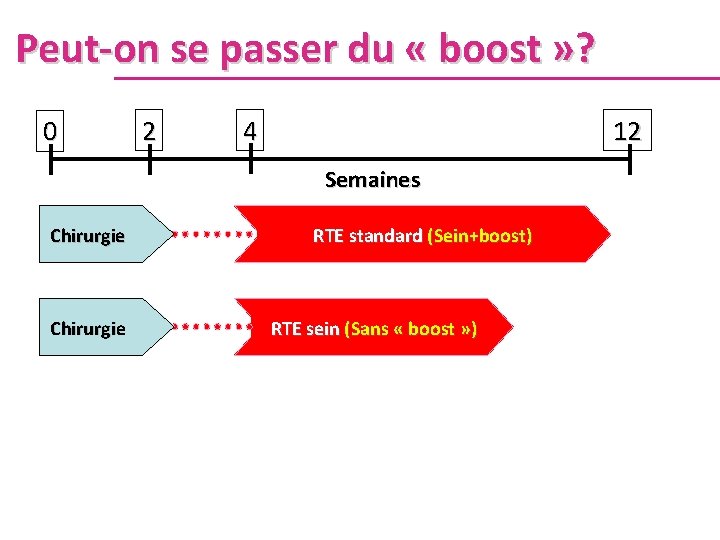
Peut-on se passer du « boost » ? 0 2 4 12 Semaines Chirurgie RTE standard (Sein+boost) RTE sein (Sans « boost » )

La méta analyse TRT conservateur : bénéfice en contrôle local Réduction du risque absolu de RL de 20% à 5 ans Réduction de mortalité par cancer : 5% à 15 ans n Méta analyse (dans l’hypothèse d’absence d’autres causes de DC) « 4 rechutes locales évitées à 5 ans : 1 décès par cancer du sein évité à 15 ans» Pas de sous-groupes qui ne bénéficient pas de la RT

Saint Paul-de-Vence L’IRRADIATION DE LA TOTALITE DE LA GLANDE MAMMAIRE DOIT ETRE SYSTEMATIQUE APRES CHIRURGIE CONSERVATRICE n Sein : 50 Gy + boost 16 Gy n Aucune exception!!! Niveau 1 - Grade A Belkacemi Y et al. CROH 2010

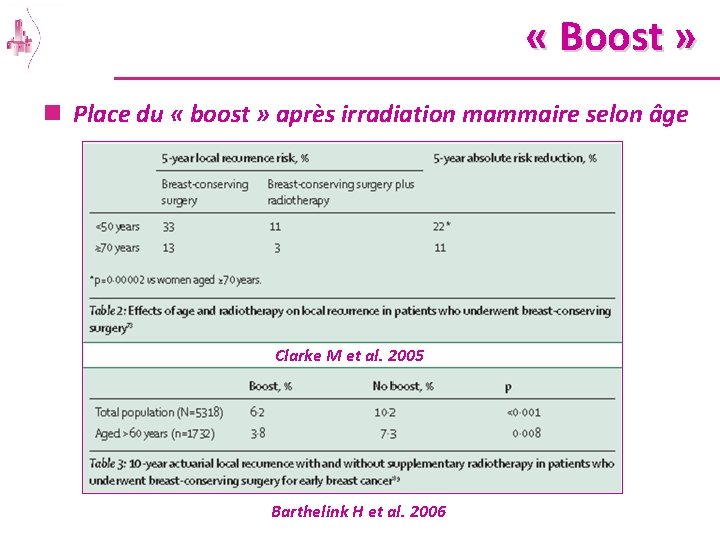
« Boost » n Place du « boost » après irradiation mammaire selon âge Clarke M et al. 2005 Barthelink H et al. 2006

« Boost » n Place du « boost » selon l’âge et autre facteurs pronostiques “Postoperative breast irradiation should therefore be considered in all patients undergoing breast-conserving surgery, irrespective of age. For women aged over 70 years with a low risk of recurrence (eg, small tumours < 2 cm, clear margins, N-, HR+), the absolute reductions in local recurrence tend to be slight and mortality is usually associated with non-breast-cancer related conditions”.

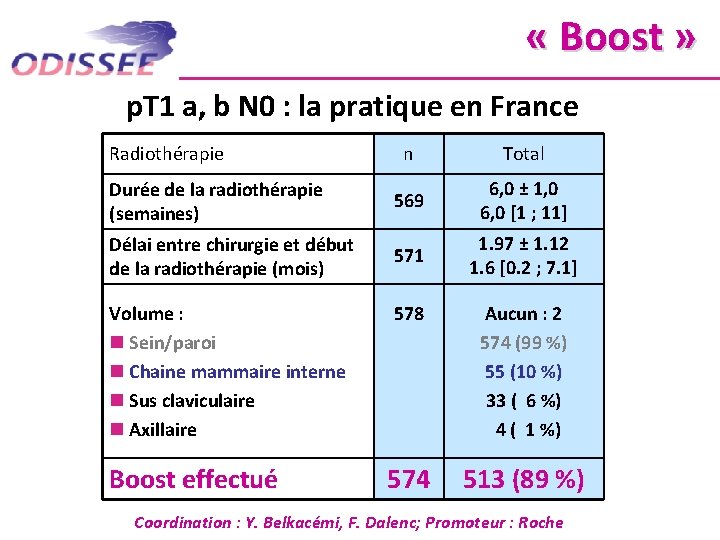
« Boost » p. T 1 a, b N 0 : la pratique en France Radiothérapie n Total Durée de la radiothérapie (semaines) 569 6, 0 ± 1, 0 6, 0 [1 ; 11] Délai entre chirurgie et début de la radiothérapie (mois) 571 1. 97 ± 1. 12 1. 6 [0. 2 ; 7. 1] Volume : n Sein/paroi n Chaine mammaire interne n Sus claviculaire n Axillaire Boost effectué 578 Aucun : 2 574 (99 %) 55 (10 %) 33 ( 6 %) 4 ( 1 %) 574 513 (89 %) Coordination : Y. Belkacémi, F. Dalenc; Promoteur : Roche

Conclusion q 2 Essais randomisés : Ø « boost » : niveau de preuve + Ø Effet indépendant de l’âge (après 60 ans) q Après 70 ans : Ø Pas d’étude pour le boost mais RT vs RT+TAM Ø Bénéfice moindre (pour la RT de façon générale) Ø Sélection : tenir compte des paramètres (bas grade, RH+, N-. . ? )

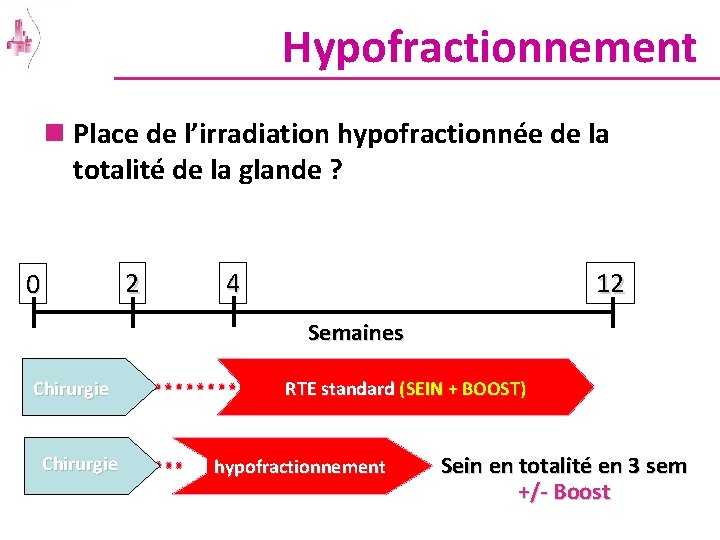
Hypofractionnement n Place de l’irradiation hypofractionnée de la totalité de la glande ? 2 0 4 12 Semaines Chirurgie RTE standard (SEIN + BOOST) hypofractionnement Sein en totalité en 3 sem +/- Boost

Hypofractionnement Schéma Canadien 50 Gy en 25 fractions en 5 semaines vs 42. 5 Gy in 16 fractions en 3 semaines Stratification : âge (50); T (< 2 cm); TRT adjuvant et centre

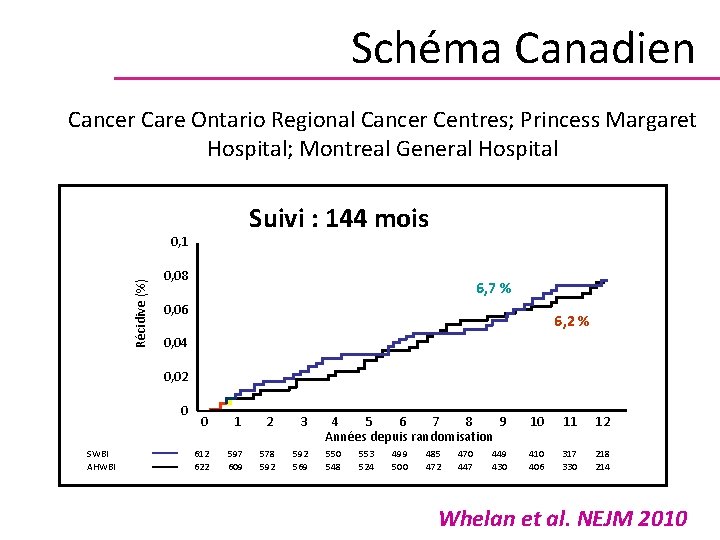
Schéma Canadien Cancer Care Ontario Regional Cancer Centres; Princess Margaret Hospital; Montreal General Hospital Suivi : 144 mois Récidive (%) 0, 1 0, 08 6, 7 % 0, 06 6, 2 % 0, 04 0, 02 0 SWBI AHWBI 0 1 2 3 612 622 597 609 578 592 569 4 5 6 7 8 9 Années depuis randomisation 10 11 12 550 548 410 406 317 330 218 214 553 524 499 500 485 472 470 447 449 430 Whelan et al. NEJM 2010

Schéma Canadien Commentaires : résultats extrapolables à toutes ? Stratification sur l’âge < 2 cm Pas de boost, ni RT ganglionnaire Pas d’inclusion des N+ Pas de seins volumineux Peu de CT adjuvante Meilleure esthétique Impact de l’âge et T Whelan et al. NEJM 2010

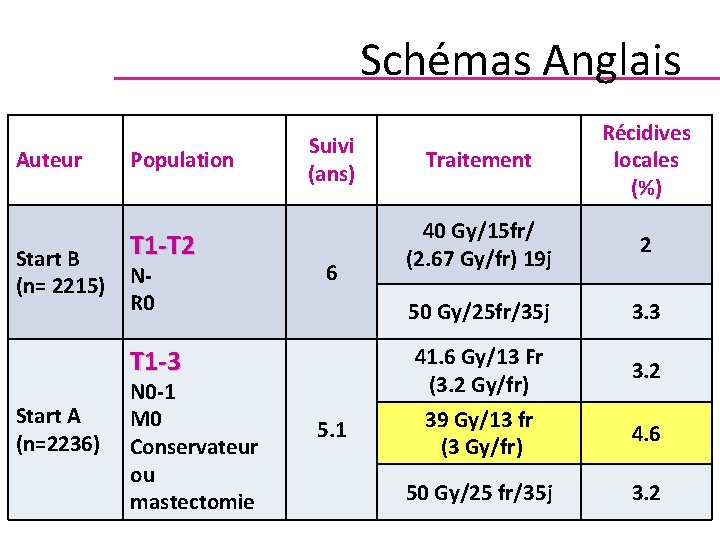
Schémas Anglais

Schémas Anglais Auteur Start B (n= 2215) Population T 1 -T 2 NR 0 Suivi (ans) 6 T 1 -3 Start A (n=2236) N 0 -1 M 0 Conservateur ou mastectomie 5. 1 Traitement Récidives locales (%) 40 Gy/15 fr/ (2. 67 Gy/fr) 19 j 2 50 Gy/25 fr/35 j 3. 3 41. 6 Gy/13 Fr (3. 2 Gy/fr) 3. 2 39 Gy/13 fr (3 Gy/fr) 4. 6 50 Gy/25 fr/35 j 3. 2

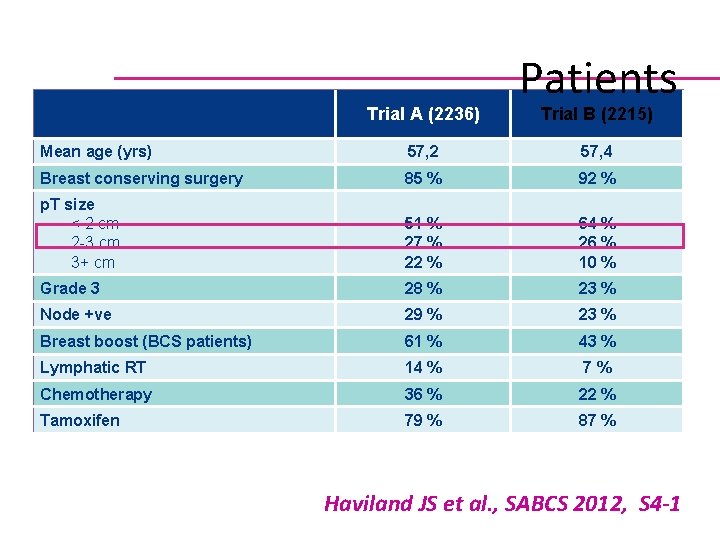
Trial A (2236) Patients Trial B (2215) Mean age (yrs) 57, 2 57, 4 Breast conserving surgery 85 % 92 % p. T size < 2 cm 2 -3 cm 3+ cm 51 % 27 % 22 % 64 % 26 % 10 % Grade 3 28 % 23 % Node +ve 29 % 23 % Breast boost (BCS patients) 61 % 43 % Lymphatic RT 14 % 7% Chemotherapy 36 % 22 % Tamoxifen 79 % 87 % Haviland JS et al. , SABCS 2012, S 4 -1

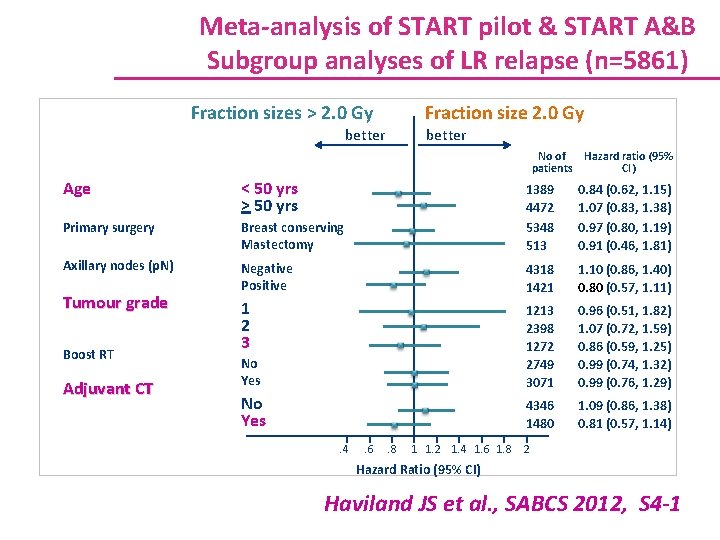
Meta-analysis of START pilot & START A&B Subgroup analyses of LR relapse (n=5861) Fraction size 2. 0 Gy Fraction sizes > 2. 0 Gy better No of Hazard ratio (95% patients CI) Age < 50 yrs > 50 yrs Primary surgery Axillary nodes (p. N) Tumour grade Boost RT Adjuvant CT Breast conserving Mastectomy 1389 4472 5348 513 0. 84 (0. 62, 1. 15) 1. 07 (0. 83, 1. 38) 0. 97 (0. 80, 1. 19) 0. 91 (0. 46, 1. 81) Negative Positive 4318 1421 1. 10 (0. 86, 1. 40) 0. 80 (0. 57, 1. 11) 1 2 3 No Yes 1213 2398 1272 2749 3071 0. 96 (0. 51, 1. 82) 1. 07 (0. 72, 1. 59) 0. 86 (0. 59, 1. 25) 0. 99 (0. 74, 1. 32) 0. 99 (0. 76, 1. 29) No Yes 4346 1480 1. 09 (0. 86, 1. 38) 0. 81 (0. 57, 1. 14) . 4 . 6 . 8 1 1. 2 1. 4 1. 6 1. 8 2 Hazard Ratio (95% CI) Haviland JS et al. , SABCS 2012, S 4 -1

Conclusion q 3 Essais randomisés : Ø Hypofractionné : niveau de preuve + Ø Résultats non extrapolables aux N+ q Stratification : Ø Taille < 2 cm : 50 -65% des patientes q Hypofractionné dans p. T 1 a, b N 0 : Ø Conforme : essai Canadien, START B Ø Tenir compte des autres paramètres o Efficacité : grade, âge, CT. . ? o Toxicité : volume mammaire, RT ganglionnaire

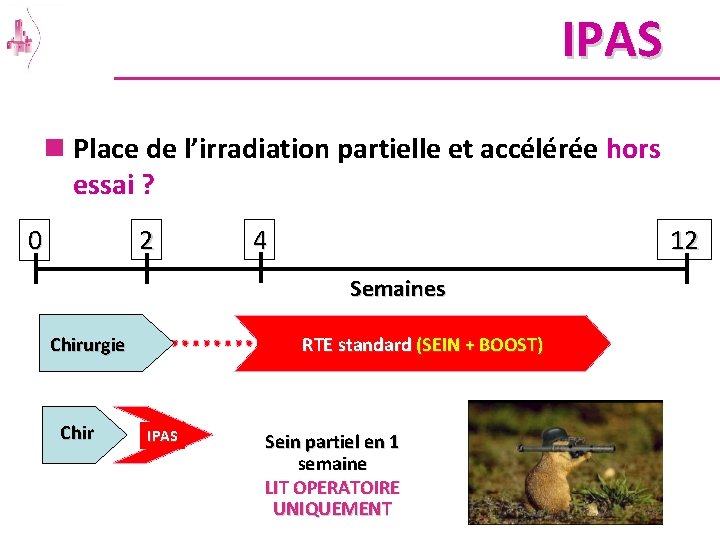
IPAS n Place de l’irradiation partielle et accélérée hors essai ? 2 0 4 12 Semaines Chirurgie Chir RTE standard (SEIN + BOOST) IPAS Sein partiel en 1 semaine LIT OPERATOIRE UNIQUEMENT

Sélection des patientes APBI consensus statement from the ASTRO ― Based on 645 original research articles ― 4 published randomized clinical trials ― 38 published prospective single arm studies n “Suitable” group n “Cautionary” group n “Unsuitable” group Smith BD et al. IJROBP, 2009

APBI consensus statement from the ASTRO consensus statement guidelines regarding patient selection for accelerated partial breast irradiation off clinical trial Smith BD et al. IJROBP, 2009

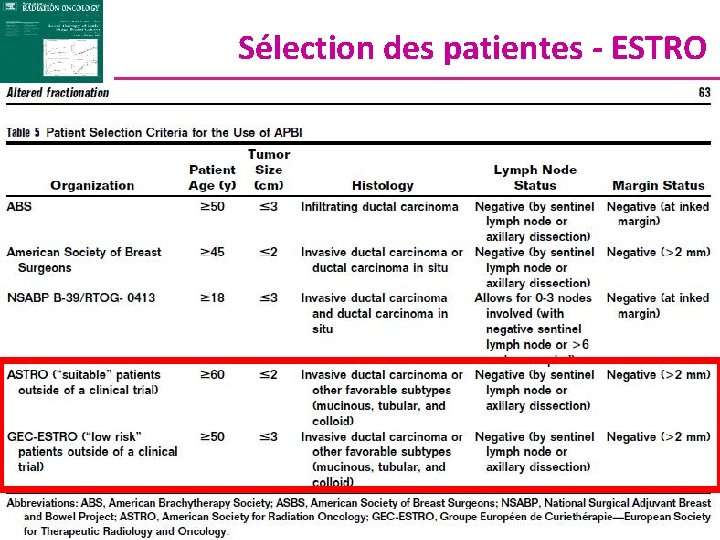
Sélection des patientes - ESTRO

Conclusion q Données prospectives monocentriques : Ø Abondantes, suivi < 10 ans q 4 essais randomisés : Ø Points critiques q Consensus américain et européen : Ø “Suitable group ” > 60 ans p. T 1 CCI et autres histologies favorables berges > 2 mm RH+

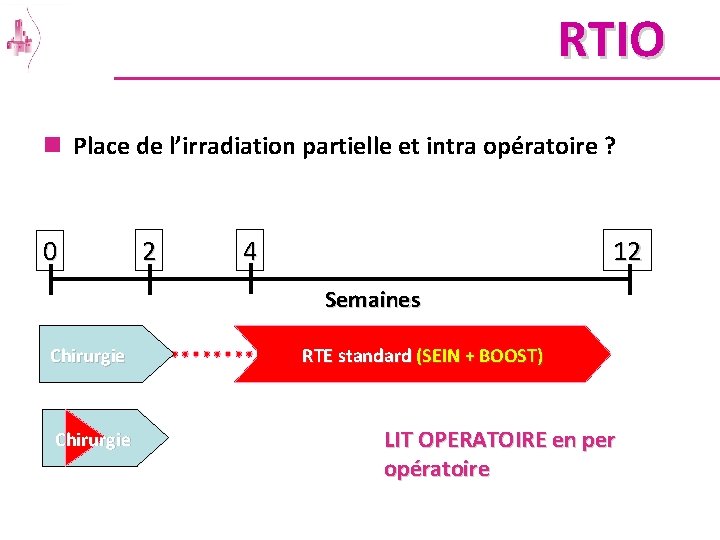
RTIO n Place de l’irradiation partielle et intra opératoire ? 0 2 4 12 Semaines Chirurgie RTE standard (SEIN + BOOST) LIT OPERATOIRE en per opératoire

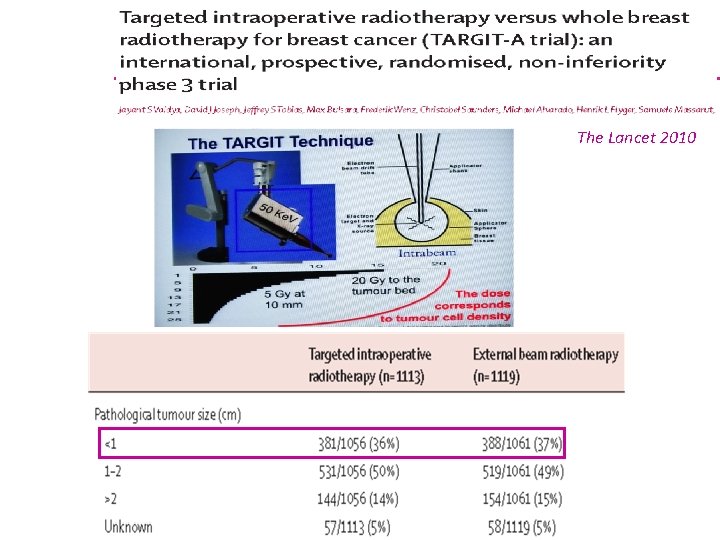
The Lancet 2010

Essai TARGIT-A n Publié en résultats préliminaires en 2010 4 Lancet 2010; 376: 91 -102 n 2232 patientes randomisées à 4 ans : 495 % de Survie Sans Récidive pour l’ensemble de la population, sans différence significative entre les 2 groupes 4 Bras TARGIT = 1, 2% de récidives 4 Bras RT sein = 0, 95% de récidives l P=NS

San Antonio 2012 n Actualisation des données 4 Sur la population définitive de 3451 patientes 41721 dans le bras INTRABEAM 41730 dans le bras radiothérapie externe 41010 patientes ont un suivi minimum de 4 ans 4611 patientes ont un suivi minimum de 5 ans n Les évènements locaux ont augmenté de 13 à 34 depuis 2010 n Le taux de récidives locales à 5 ans est en défaveur du RTIO : 423 (3, 3%) vs 11 (1, 3%), p=0, 042 Vaidya J. S et al. , SABCS 2012, S 4 -2

Conclusion n Données monocentriques (utilisant les électrons) 4 Patientes sélectionnées bon Pc : taux de récidives rassurants 4 Résultats de l’essai de MILAN n Essai TARGIT (Rx basses énérgies) 4 Taux de récidives en défaveur de INTRABEAM ! 4 La sélection des patientes est primordiale ? (> 60 ans, RH+, tumeur < 2 cm, GS-) Vaidya J. S et al. , SABCS 2012, S 4 -2

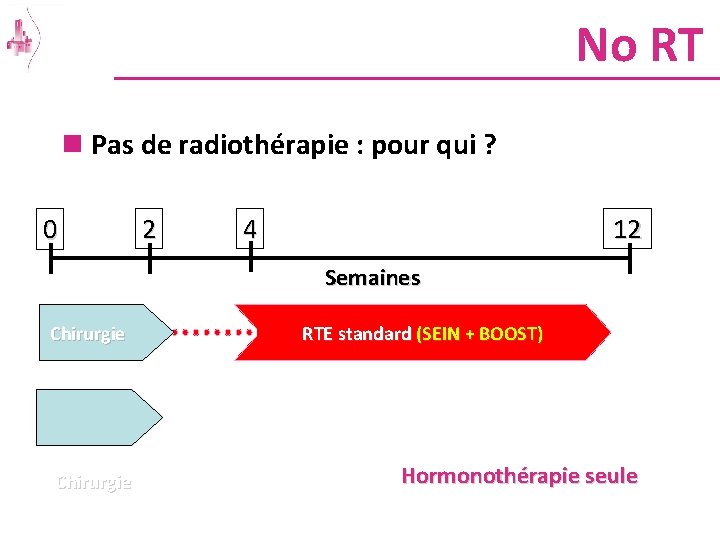
No RT n Pas de radiothérapie : pour qui ? 0 2 4 12 Semaines Chirurgie RTE standard (SEIN + BOOST) Hormonothérapie seule

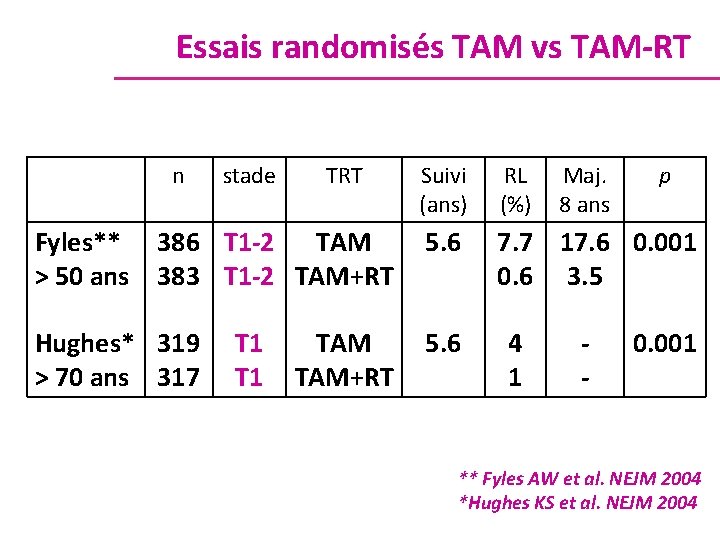
Essais randomisés TAM vs TAM-RT n stade Suivi (ans) RL (%) Fyles** 386 T 1 -2 TAM > 50 ans 383 T 1 -2 TAM+RT 5. 6 7. 7 17. 6 0. 001 0. 6 3. 5 Hughes* 319 > 70 ans 317 5. 6 T 1 TRT TAM+RT 4 1 Maj. 8 ans - p 0. 001 ** Fyles AW et al. NEJM 2004 *Hughes KS et al. NEJM 2004

Essais randomisés TAM vs TAM-RT Age > 50 y TAM vs TAM+RT T 1 cm, RH+ (n = 611) TAM + RT RL à 5 ans Métastases S/groupe RL à 5 ans p 0. 6% 0. 002 4% NS Age > 60 ans TAM+RT 0% TAM 7. 7% 4. 5% < 10 mm RH+ TAM 1. 2% p = 0. 16 Fyles A et al. NEJM 2004

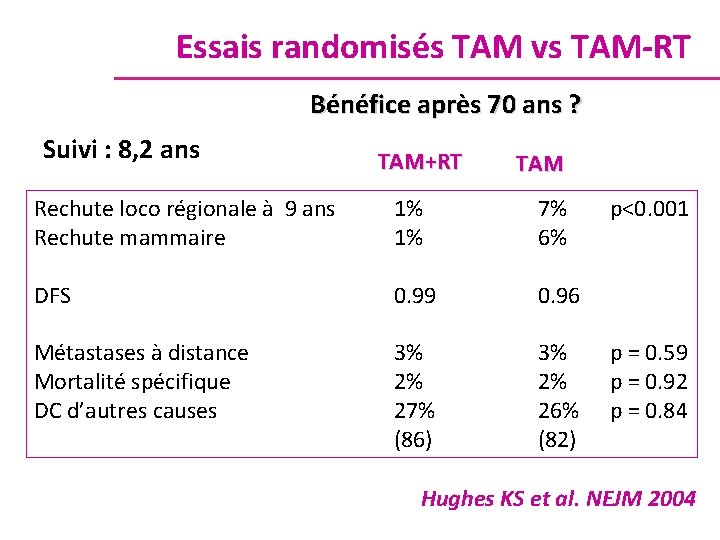
Essais randomisés TAM vs TAM-RT Bénéfice après 70 ans ? Suivi : 8, 2 ans TAM+RT TAM Rechute loco régionale à 9 ans Rechute mammaire 1% 1% 7% 6% DFS 0. 99 0. 96 3% 2% 27% (86) 3% 2% 26% (82) Métastases à distance Mortalité spécifique DC d’autres causes p<0. 001 p = 0. 59 p = 0. 92 p = 0. 84 Hughes KS et al. NEJM 2004

Données registre Bénéfice après 70 ans ? n SEER n = 8724 n ≥ 70 ans (med 77) n T 1 N 0, RE+ Pas de RT : 27% n Taux de RL 5 ans 8 ans RT 5% 8% RT+ 1% p < 0. 001 2. 3% Patientes 70 -79 ans avec «minimal comorbidity » Bénéfice maximal Smith B et al. JNCI 2006

Etude prospective pts > 70 ans n = 354 Chirurgie conservatrice, berges saines TAM seul Pas de CA ni RT Rechute locale Taux global Mortalité par cancer du sein DC Causes autres que le cancer 4, 2% (p. T 1 : 4%) 17% n 268 222 % 83

Conclusion

Merci