Przydatno diagnostyczna oznaczania niebiakowych zwizkw azotowych mocznik kreatynina

Przydatność diagnostyczna oznaczania niebiałkowych związków azotowych (mocznik, kreatynina, kwas moczowy, amoniak) Gabriela Czechura III rok, OAM

Mocznik • głównym azotowy produkt katabolizmu białek w ludzkim organizmie, • powstaje w przebiegu cyklu mocznikowego zachodzącego w hepatocytach, • wydalany głównie przez nerki (90%). Reszta (10%) usuwana przez skórę (z potem) lub degradowana w przewodzie pokarmowym przez bakterie jelitowe. Wartości prawidłowe: 2, 9 - 6, 4 mmol/l (niższe stężenie u dzieci)
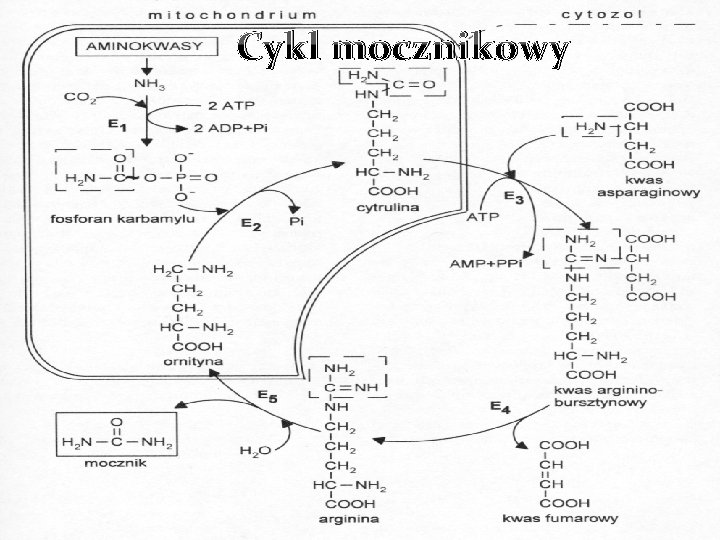
Cykl mocznikowy
Wątroba Nerki Mocz • wydalanie mocznika z moczem jest wprost proporcjonalne do wielkości przesączania kłębuszkowego (GFR), • to proces ciągły i dlatego we krwi znajduje się zazwyczaj niewielka, stała ilość azotu mocznikowego (BUN), • większość chorób nerek lub wątroby może mieć wpływ na stężenie mocznika we krwi. Jeżeli w wyniku znacznego uszkodzenia wątroby zaburzeniu ulegają procesy syntezy mocznika, wówczas stężenie BUN może się obniżyć.

BUN Tzw. blood urea nitrogen (BUN)- określa ilość azotu zawartą w moczniku krwi. Wartości są używane zamiennie i można je prosto przeliczać: mg azotu mocznika x 2, 146= mg mocznika (60/28= 2, 146) mg azotu mocznika x 0, 0357= mmol mocznika

Stężenie mocznika w surowicy jest zależne od: • perfuzji nerek i wielkości diurezy, • wielkości GFR, • szybkości syntezy mocznika związanej bezpośrednio z dzienną podażą białka w diecie i katabolizmem białkowym. ! Stężenie mocznika w surowicy nie może być bezkrytycznie używane do oceny przesączania kłębuszkowego (-funkcji nerek). Wskazania do oznaczania stężenie mocznika w surowicy: • · różnicowanie przednerkowej i pozanerkowej azotemii (za pomocą współczynnika mocznik/kreatynina), • · ocena nasilenia toksemii mocznicowej u chorych z terminalną niewydolnością nerek, • · u chorych dializowanych do oceny stanu metabolicznego chorego i nasilenia katabolizmu białkowego.

Zmiany stężenia mocznika w surowicy Azotemia a) Przednerkowa: • upośledzenie perfuzji nerkowej hipoproteinemie, utrata ECF, zawał serca) • łagodne odwodnienie, • wzmożony katabolizm białkowy (zabieg operacyjny, ekstremalne głodzenie), • dieta wysokobiałkowa, • terapia kortyzolem b) Nerkowa: • Ostra, przewlekła niewydolność nerek, gdy spada filtracja kłębkowa c) Ponerkowa: • Dowolna przyczyna obstrukcji przepływu moczu (np. obecność kamieni, przerost prostaty, zwężenia nowotworowe).

Zmiany stężenia mocznika w surowicy Niskie stężenie mocznika: • Obniżona synteza np. za mało aa do deaminacjii (głodzenie, złe wchłanianie), • Choroby wątroby (uszkodzona synteza), • Zatrzymanie wody, • Rozcieńczenie surowicy wlewami dożylnymi.

Współczynnik mocznik/kreatynina W diagnostyce chorób nerek znalazł zastosowanie współczynnik będący stosunkiem stężenia mocznika do stężenia kreatyniny w surowicy, za pomocą którego można różnicować przyczyny azotemii. Prawidłowa wartość tego współczynnika: · dla stężeń mocznika i kreatyniny wyrażonych w mmol/l wynosi około 35 · dla wartości wyrażonych w mg/dl wynosi około 25 · dla zależności BUN/kreatynina w mg/dl około 12


Metody oznaczania mocznika v. Ureaza- dehydrogenaza glutaminowa (GLDH) spektrofotometryczna analiza mocznika: mocznik ureaza NH 4+ + α- ketoglutaran + NADH • Używana najczęściej, • Bardzo swoista, • Szybka. (NH 4)2 CO 3 GLDH NAD+ + glutaminian

Kreatynina • Jest cyklicznym bezwodnikiem kreatyny, • produkowana i wydzielana w stałej ilości, synteza zachodzi w nerkach, wątrobie i w trzustce, w 2 reakcjach enzymatycznych • transportowana jest do różnych tkanek (np. do mięśni i mózgu) gdzie ulega fosforylacji do fosfokreatyny, • stężenie kreatyniny w surowicy zależy od: -całkowitej masy mięśniowej - płci (u mężczyzn jest wyższe niż u kobiet) - od rodzaju diety (dieta bogatomięsna może podwyższyć stężenie kreatyniny w surowicy nawet o 30%- w 1 kg mięsa znajduje się 2 -5 g kreatyny). Mimo tych zależności poziom kreatyniny w surowicy zdrowego człowieka jest wartością stosunkowo niezmienną (wahania dobowe nie przekraczają 15% wartości).

Wartości prawidłowe dla kreatyniny są zależne od zastosowanej metody. Typowy zakres: 80 - 115 µmol/l (mężczyźni) 53 - 97 µmol/l (kobiety) Stężenie we krwi jest odwrotnie proporcjonalne do klirensu nerkowego (GFR) !

Kreatynina jest wydalana z organizmu tylko przez nerki. Do znamiennego podwyższenia stężenia kreatyniny w osoczu dochodzi dopiero wtedy, gdy znaczna część nefronów ulegnie uszkodzeniu i GFR obniży się do około połowy wartości prawidłowej. Zastosowanie kreatyniny w diagnostyce laboratoryjnej chorób nerek
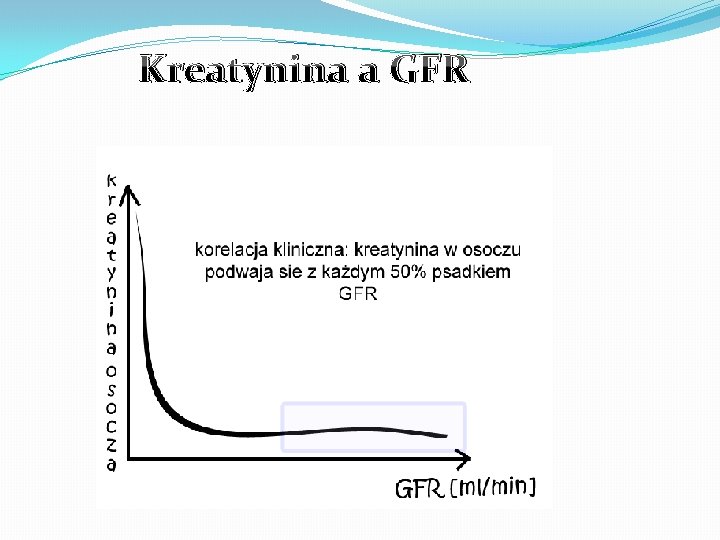
Kreatynina a GFR
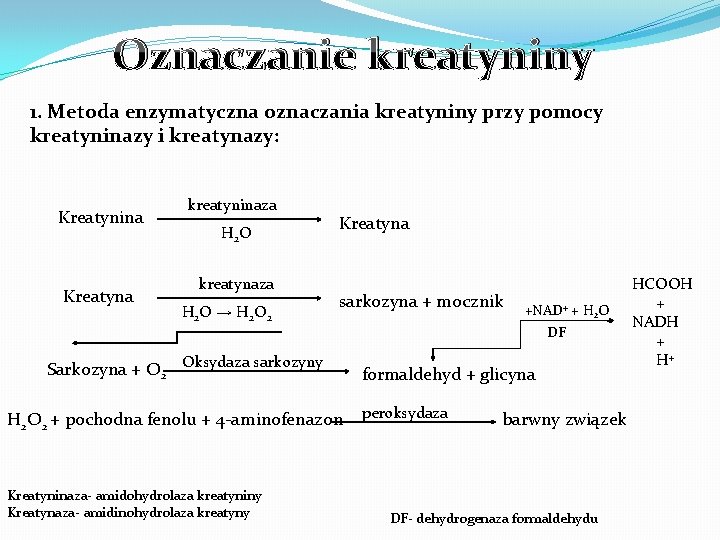
Oznaczanie kreatyniny 1. Metoda enzymatyczna oznaczania kreatyniny przy pomocy kreatyninazy i kreatynazy: Kreatynina Kreatyna kreatyninaza H 2 O kreatynaza H 2 O → H 2 O 2 Kreatyna sarkozyna + mocznik Sarkozyna + O 2 Oksydaza sarkozyny H 2 O 2 + pochodna fenolu + 4 -aminofenazon Kreatyninaza- amidohydrolaza kreatyniny Kreatynaza- amidinohydrolaza kreatyny HCOOH + +NAD+ + H 2 O NADH DF + H+ formaldehyd + glicyna peroksydaza barwny związek DF- dehydrogenaza formaldehydu
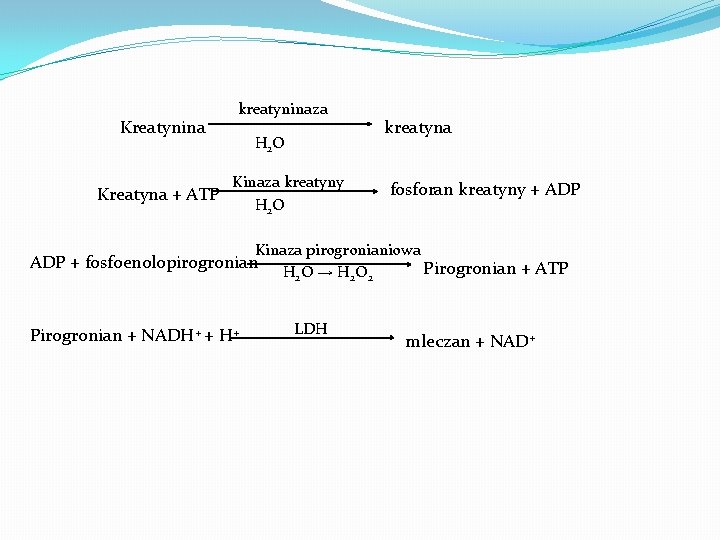
Kreatynina kreatyninaza H 2 O Kinaza kreatyny Kreatyna + ATP H 2 O kreatyna fosforan kreatyny + ADP Kinaza pirogronianiowa Pirogronian + ATP H 2 O → H 2 O 2 ADP + fosfoenolopirogronian Pirogronian + NADH+ + H+ LDH mleczan + NAD+

2. Sucha chemia. Metody oznaczania kreatyniny: • Enzymatyczna z deminazą kreatyniny → amoniak + błękit bromofenolowy (pomiar- 600 nm) • Enzymatyczna z kreatyninazą i kreatynazą • Reakcja z kwasem 3, 5 - dinitrobenzoesowym

Wskaźniki do oznaczania stężenia kreatyniny w surowicy: – ostre i przewlekłe choroby nerek – zaburzenia przemiany materii, choroby układowe: cukrzyca, hiperurykemia, choroby tkanki łącznej – nadciśnienie tętnicze – niewydolność krążenia, stan wstrząsu, ostra utrata krwi lub płynów ustrojowych – terapia lekami nefrotoksycznymi lub wydalanymi głównie przez nerki – uszkodzenie nerek wywołane zatruciem egzogennym, hemolizą, miolizą

Ograniczenia interpretacji wyników: 1)kreatynina ↑ w okresie dojrzewania, potem spada z wiekiem (tak jak GFR) 2)Czynniki mające wpływ na poziom kreatyniny (wiek, płeć, rasa, masa ciała, dieta, leki) 3)Przedział wartości referencyjnych nie koreluje dobrze z wczesną chorobą nerek

Nieprawidłowe wyniki stężenia kreatyniny: Wzrost stężenia kreatyniny: • Bez znaczenia fizjologicznego: - dieta bogata w mięso -intensywne ćwiczenia - wpływ leków (np. salicylany) - interferencje analityczne (np. antybiotyki, cefalosporyny) • Patologia: - choroby nerek (dowolna przyczyna obniżonego GFR)

Spadek stężenia kreatyniny: • Fizjologicznie: - poród • Patologia: - spadek masy mięśni (głodzenie, choroby wyniszczające, terapia sterydowa)

GFR Współczynnik przesączania kłębuszkowego (GFR, z ang. glomerular filtration rate) Ilość osocza przefiltrowana w jednostce czasu przez kłębuszki nerkowe do tzw. moczu pierwotnego. Zwykle podawany jest w ml/min lub w ml/(min× 1, 72 m²) (czyli po przeliczeniu na standardową powierzchnię ciała). Współczynnik GFR pozwala na ocenę stopnia wydolności nerek. Oceniany na podstawie klirensu egzogennych lub endogennych substancji

Badanie GFR jest wykorzystywane do: • Wykrycia przewlekłej choroby nerek CDK • Oceny stopnia zaawansowania CDK • Ustalenia dawkowania leków wydalanych drogą przesączania kłębuszkowego • Badania innych metod terapeutycznych lub wpływu leków na funkcje nerek Czynniki wpływające na wartość GFR: • Zmienność dobowa GFR- najniższe w nocy, najwyższe rano • Długotrwała wyprostowana pozycja ciała • Ciąża • Cukrzyca • Dożylna infuzja dopaminy

Idealny marker GFR �Jest wydalany wyłącznie drogą przesączania kłębuszkowego �Nie wiąże się z białkami osocza i nie wnika do erytrocytów �Nie podlega wchłanianiu zwrotnemu i sekrecji w kanalikach �Nie ulega przemianom metabolicznym w ustroju �Nie jest wychwytywany przez inne tkanki �Obojętny dla ustroju i środowiska �Tani i łatwo dostępny �Istnieje prosta i dokładna metoda oznaczania

Metody oznaczania GFR Złoty standard: klirens nerkowy inuliny (po przesączeniu do pramoczu nie ulega reabsorpcji ani wydzielaniu w kanalikach nerkowych) Srebrne standardy: klirens nerkowy lub osoczowy 51 Cr-EDTA, 125 I- talaminianu jobeksolu Metoda z wyboru: - Klirens kreatyniny z 24 h zbiórki moczu Testy przesiewowe - Obliczanie GFR na podstawie stężenia kreatyniny w surowicy Stężenie cystatyny C
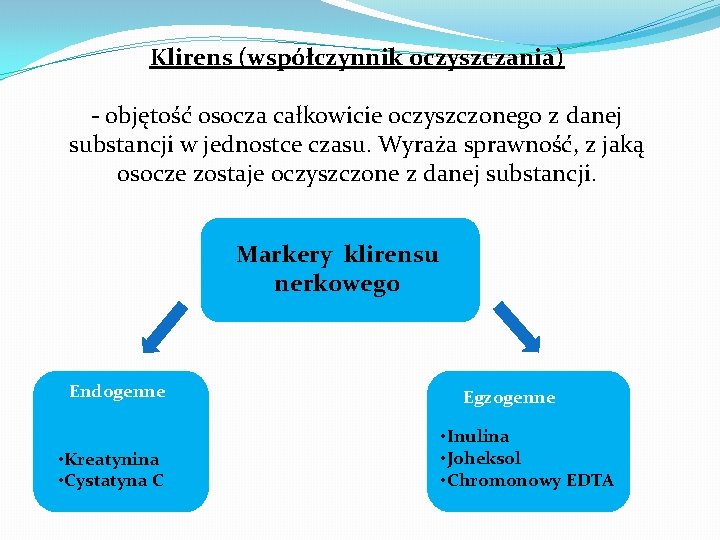
Klirens (współczynnik oczyszczania) - objętość osocza całkowicie oczyszczonego z danej substancji w jednostce czasu. Wyraża sprawność, z jaką osocze zostaje oczyszczone z danej substancji. Markery klirensu nerkowego Endogenne • Kreatynina • Cystatyna C Egzogenne • Inulina • Joheksol • Chromonowy EDTA

Kreatynina jako marker GFR: -niska czułość diagnostyczna -stężenie zależne od masy mięśniowej, jest wyższe u mężczyzn, osób młodych, rasy czarnej -jest eliminowana drogą sekrecji kanalikowej, sekrecja nasila się w miarę spadku GFR - jest degradowana w jelitach, eliminacja pozanerkowa nasila się wraz ze spadkiem GFR -metabolizm i wydzielanie cewkowe są zmieniane przez wiele leków. -stosowana rutynowo metoda Jaffe’go ma niską swoistość -duże zróżnicowanie metodyczne powoduje dużą zmienność międzylaboratoryjną

Obliczanie klirensu kreatyniny 1. Wzór Cockcrofta-Gaulta:

2. Wzór MDRD– wzór stworzony na podstawie danych dla pacjentów z przewlekłą niewydolnością nerek (uczestników programu Modification of Diet in Renal Disease ) dla zdrowych ludzi wyraźnie niedoszacowuje GFR, natomiast znacznie lepiej od wzoru CG szacuje GFR dla bardziej zaawansowanych stadiów PCh. N. MDRD Sudy- 4 - parametrowe oznaczenie GFR dla osób powyżej 18 r. ż. -kreatynina w surowicy -wiek -płeć -rasa GFR (ml/min/1. 73 m 2 ) = 186* x kreatynina (surowica) -1, 154 x wiek x 0, 742 (jeżeli ♀)/ x 1, 210 (Afroamerykanie) ***186 - dla tradycyjnych kalibratorów 175 - dla kalibratorów odnoszących się do IDMS

Ograniczenia: • Wiek 18 -70 lat, rasa biała i Afroamerykanie z GFR <90 m. L/min/ 1, 73 m 2 - dobrze wychodzi u cukrzyków • Gorsza zgodność z mierzonym GFR dla: - populacji szpialnej - ostrej niewydolności nerek - prawidłowej funkcji nerek • Walidacja obecnie udoskonalana

Cystatyna C Lizosomalna proteinaza cysteinowa, produkowana we wszystkich komórkach ze stałą szybkością. o Swobodnie filtrowana przez kłębuszki, nie wydzielana przez kanaliki proksymalne, o. Jej stężenie w osoczu ↑ w dysfunkcjach cewek nerkowych, o. Niezależna od masy mięśniowej i diety, marker dla GFR

• Na jej stężenie wpływa: -dysfunkcja tarczycy, - glikokortykoidy - prawdopodobnie również inne czynniki - wiek (↑ stężenia po 50 r. ż. ), - rasa, - płeć • Stosowana w: - pediatrii, - geriatrii, - w przypadku łagodnego upośledzenia GFR, - w warunkach braku możliwości zastosowania kreatyniny

• Ograniczenia Cystatyny C jako markera GFR: - małe zróżnicowanie metodyczne, - brak międzynarodowego wzorca Cystatyny C, - wysoka cena, - wpływ różnych czynników na jej stężenie

Kwas moczowy • Inaczej 2, 6, 8 -trioksypuryna • Powstaje w wyniku degradacji (oksydacji) puryn (adeniny i guaniny) w hepatocytach. Puryny z katabolizmu kwasów nukleinowych (dieta) są zamieniane bezpośrednio do kwasu moczowego. Katabolizm puryn u człowieka: Adenozyna → inozyna → hipoksantyna→ kwas moczowy Guanozyna→ guanina→ ksantyna→ kwas moczowy

Wartości referencyjne: • dzieci: 120 - 320 µmol/l • mężczyźni: 210 - 420 µmol/l • kobiety: 130 -350 µmol/l

Zmiany poziomu kwasu moczowego we krwi Przyczyny obniżonego poziomu : - ciężki alkoholizm, połączony z chorobami wątroby -niedobór oksydazy ksantyny - wysokie dawki salicylanów i witaminy C -Allopurinol - kortykosterydy - choroba Fanconi’ego - galaktozemia

Przyczyny podwyższonego poziomu krwi: - wzrost spożycia (dieta mięsna)- fizjologiczne -wzrost produkcji moczanów: Dna moczanowa, leczenie chorób mieloproliferacyjnych cytotoksycznymi lekami -obniżone wydalania: kwasica mleczanowa, choroby spichrzowania glikogenu typu, podawanie leków, zatrucia np. ołów, alkohol - defekty enzymatyczne: choroba Lesh- Nyhan

• Zdrowy człowiek wytwarza 0, 4 g nukleozydów purynowych i przyjmuje z dietą dodatkowe 0, 3 g dziennie. Pacjenci z artretyzmem i zespołem odkładania się moczanów w tkankach mogą mieć pulę nukleozydów purynowyh rzędu 19 -30 g. Zasady purynowe mogą też wchodzić w reakcję odtwarzania nukleotydów purynowych. • Kwas moczowy jest eliminowany z organizmu przez: ü przewód pokarmowy- 30%, ü nerki-70% (filtracja, reabsorbcja, wydzielanie; w rezultacie cewka wydziela 6 - 12% przefiltrowanego kwasu moczowego) Wydalanie z moczem: 250 -270 mg/ dzień Jego stężenie w surowicy zależy od wielkości filtracji kłębuszkowej, z tego względu może służyć do monitorowania funkcji nerek.

p. H moczu >5, 57 Kwas moczowy zdysocjowany, stosunkowo dobrze rozpuszczalny ↓ p. H moczu Kwas moczowy w formie niezdysocjowanej o gorszej rozpuszczalności. ↓ reabsorpcji moczanów w cewkach moczowych → wytrącania się kryształów i tworzenia kamieni moczowych.

Zmiany ilości wydalanego kwasu moczowego Hiperurykemia: -niewydolność nerek, -dna moczanowa, -nadprodukcja puryn (zespoły mieloproliferacyjne, masywny rozpad tkanki nowotworowej podczas chemioterapii), -specyficzne defekty enzymatyczne (np. choroba Lesch- Nyhana), -leki (diuretyki, salicylany, etambutol, pirazynamid), -zatrucie ołowiem i alkoholem, -niedoczynność tarczycy, -nadczynność przytarczyc, -kwasica mleczanowa

Artretyzm (podagra, dna moczanowa) krystalizacja kryształków moczanu sodowego w płynach z jam ciała np. stawowych i depozyty kryszałków w tkankach otaczających staw. W cięższych przypadkach następuje dalsze wytrącanie kryształków w tkankach miękkich. Depozyty te mogą być powodem rozwijającego się stanu zapalnego (nacieki leukocytarne). Zaburzenia nerek: -depozyty moczanów w parenchymie - depozyty kryształków moczanowych w cewkach i moczowodach→ kamica moczanowa Dna może być: -pierwotna (zwykle związana z nadprodukcją kwasu moczowego) -wtórna (niedostateczne wydalanie kwasu moczowego w chorobach nerek, wpływ leków, kwasów organicznych itp. ).

Wrodzony defekt- choroba Lesh- Nyhana Jest spowodowana zablokowaniem drogi powrotnego przekształcania zasad purynowych w nukleotydy powoduje opóźnienia w rozwoju umysłowym, dysfunkcję ruchową, zaburzenia neurologiczne związane z wysokim poziomem kwasu moczowego we krwi.

Hipourykemia: - stosowanie niektórych leków (wysokie dawki salicylanów, witaminy C), - ciężki alkoholizm, schorzenia wątroby, - zespół Fanconiego (upośledzenie reabsorpcji przez komórki kanalików nerkowych), -chemioterapia z użyciem inhibitorów syntezy puryn (6 merkaptopuryna), - allopurinol (hamuje oksydazę) - kortykosterydy, - galaktozemia.

Metody oznaczania kwasu moczowego: • Z kwasem fosfomolibdenowym: 1. Etapem wstępnym jest odbiałczanie próbki (kwas fosfomolibdenowy powodowałby wytrącenie się białka z roztworu). Odbiałczanie prowadzi się mieszaniną siarczanu cynku- wodorotlenek baru. 2. Do supernatantu dodaje się kwasu fosfomolibdenowego który ulega redukcji do błękitu molibdenowego przez kwas moczowy w środowisku zasadowym (odczyt 650 - 700 nm). Z metodą interferują: §glukoza, § kwas askorbinowy, § glutation, § cysteina, §leki (acetaminofenon, kwas acetylosalicylowy i pochodne), § inne puryny (teobromina, kofeina, teofilina).

Kwas moczowy urikaza alantoina + H 2 O 2 + CO 2 (odczyt 293 nm) • Oznaczanie powstałęgo nadtlenku wodoru: H 2 O 2+ DHBS + 4 - aminofenazon → pochodna benzochinonoiminy (czerwona) (520 nm) (DHBS= 3, 5 - dichloro-2 -hydroksy- benzenosulfonian) • Inne metody oznaczania powstałego nadtlenku wodoru: peroksydaza substrat + H 2 O 2 barwny produkt Zakresy wartości referencyjnych kwasu moczowego zależą od metody, wartości te dla metod oznaczania kwasu moczowego z kwasem fosforowolframowym są wyższe.

Amoniak syntetyzowany jest we wszystkich organach, głównie powstaje w przewodzie pokarmowym: • Degradacja aminokwasów • Utlenianie aminokwasów • Hydroliza glutaminy i asparaginy W żyle wrotnej stężenie amoniaku jest 5 - 10 razy wyższe niż w krążeniu ogólnym. W normalnych warunkach amoniak ulega przemianie do mocznika, bo jest toksyczny dla OUN (amoniak pasywnie pokonuje barierę krew- mózg). W fizjologicznym p. H występuje jako NH 4+.

Amoniak jest neurotoksyczny! → przechodzi przez barierę krew-mózg Wartości prawidłowe: 16 -65 µmol/l, (noworodki 100 µmol/l) nieprawidłowy amoniak -> dysfunkcje metaboliczne Znaczenie kliniczne: Zaburzenie syntezy mocznika: -nabyte (np. : ciężkie schorzenia wątroby, choroba Reya-> podwyższony amoniak u noworodków (500 - 1000 umol/l), marskość), -genetyczne (defekt jednego z enzymów cyklu mocznikowego)

Hiperamonemia: • Wrodzone defekty metaboliczne enzymów z cyklu mocznikowego • Wrodzone defekty metabolizmu lizyny i ornityny • Wrodzony defekt metabolizmu kwasów organicznych- propionowego, metylomalonowego, izowalerianowego itd. • WZW • Toksyczne zapalenie wątroby • Marskość wątroby • Encefalopatia przebiegu marskości (dodatkowo krwawienie do przewodu pokarmowego powoduje degradację białek krwi z wytworzeniem amoniaku lub dieta wysokobiałkowa) Nefropatia powoduje ↑ poziomu mocznika we krwi, wydzielanie do światła jelita, rozkład do amoniaku

Oznaczanie amoniaku 1. Błędy przedlaboratoryjne: • Palenie papierosów podnosi poziom amoniaku- 1 papieros wypalony 1 h przed pobranie materiału podwyższa o 100% poziom amoniaku • Atmosfera laboratorium powinna być wolna od oparów amoniaku i dymu papierosowego. • Osocze krwi jest materiałem z wyboru (w surowicy poziom amoniaku jest wyższy) • Zahamowanie katabolizmu aminokwasów przez natychmiastowe ochłodzenie próbki krwi w lodzie, szybkie wirowanie krwi. • Pobieranie krwi na skrzep • Pobieranie krwi na antykoagulant

2. Pobieranie materiału: -EDTA (sól dipotasowa)→osocze (we krwi wynaczynionej deaminacja) -transport w lodzie -zamknięta probówka (amoniak z powietrza zawyża wynik)

a) enzymatyczna (pomiar amoniaku/ jonu amonowego we krwi) Kwas szczawiobursztynowy + NH + + NAD(P)H + H+ 4 Dehydrogenaza kwasu glutaminowego Kwas glutaminowy + H 2 O + NAD(P)+ (pomiar 340 nm) Najpopularniejsza, stosowana w automatach, precyzyjna i dokładna. Manualna lub półmanualna. b) inne: Conway’a, Seligsona, wymieniacz jonowy, elektroda jonoselektywna

Dziękuję
- Slides: 53