PENGELOMPOKAN UNSURUNSUR BERDASARKAN ADANYA KEMIRIPAN SIFATSIFATNYA o Dapat

PENGELOMPOKAN UNSUR-UNSUR BERDASARKAN ADANYA KEMIRIPAN SIFAT-SIFATNYA


o Dapat menghantarkan panas dan listrik o Mudah dibentuk o Berkilap o Umumnya berwujud padat pada suhu kamar o Bersifat reduktor o Tidak dapat menghantarkan panas dan listrik o Yang berwujud padat umumnya rapuh o Tidak mengkilap o Ada yang berwujud padat, cair, atau gas pada suhu kamar o Bersifat oksidator HOME

JOHN WOLFGANG DOBREINER (1817) Bila tiga unsur yang sifatnya sama diurutkan menurut kenaikan massa atomnya (nomor massa), maka massa atom yang ditengah merupakan rata-rata massa atom yang pertama dan ketiga
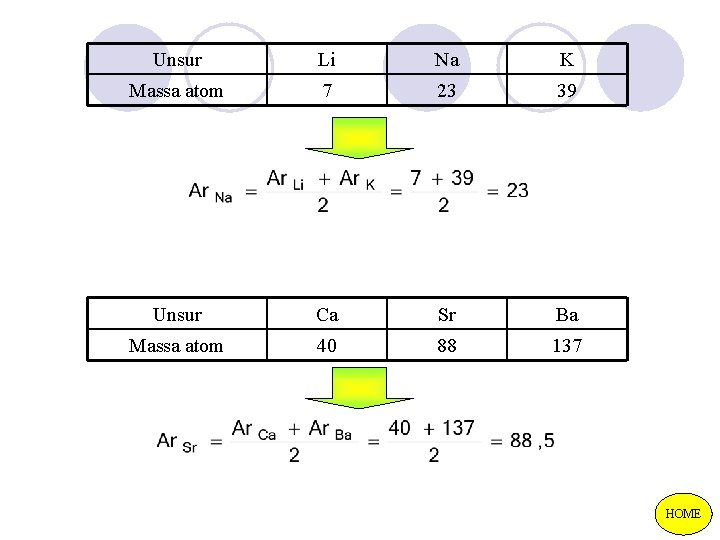
Unsur Li Na K Massa atom 7 23 39 Unsur Ca Sr Ba Massa atom 40 88 137 HOME

A. R. NEWLANDS (1864) Bila unsur dikelompokkan berdasarkan kenaikan massa atom (nomor massa), maka sifat unsur ke delapan mempunyai sifat yang mirip dengan unsur yang pertama.

o Hanya cocok untuk unsur dengan massa atom kecil o Terdapat beberapa unsur yang berhimpitan (dalam satu tempat terdapat dua unsur) HOME
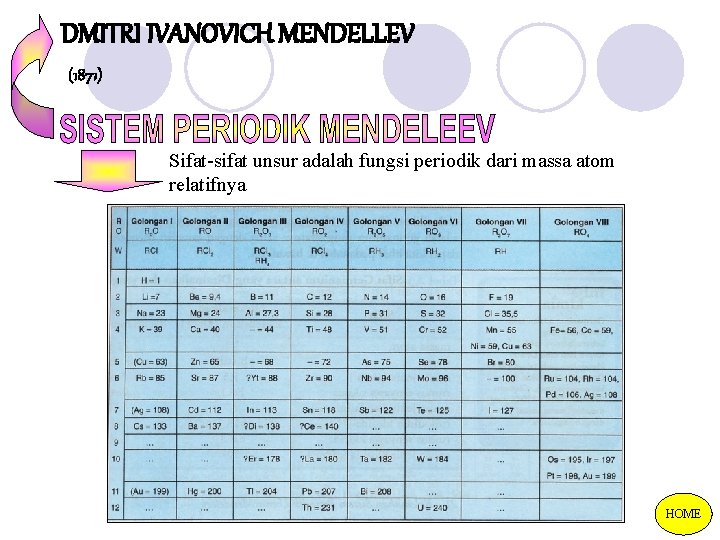
DMITRI IVANOVICH MENDELLEV (1871) Sifat-sifat unsur adalah fungsi periodik dari massa atom relatifnya HOME

HENRY MOSELEY (1887 – 1915) (1913) Sifat-sifat unsur merupakan fungsi periodik dari nomor atom
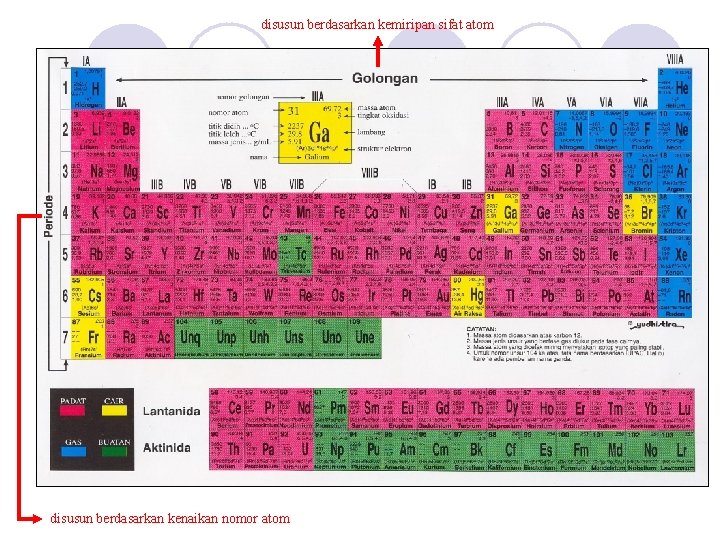
disusun berdasarkan kemiripan sifat atom disusun berdasarkan kenaikan nomor atom
v Golongan IA : golongan Alkali v Golongan IIA : golongan Alkali Tanah v Golongan VIIA : golongan Halogen v Golongan VIIIA : golongan Gas Mulia v Lantanida (golongan IIIB – periode 6) v Aktinida (golongan IIIB – periode 7)

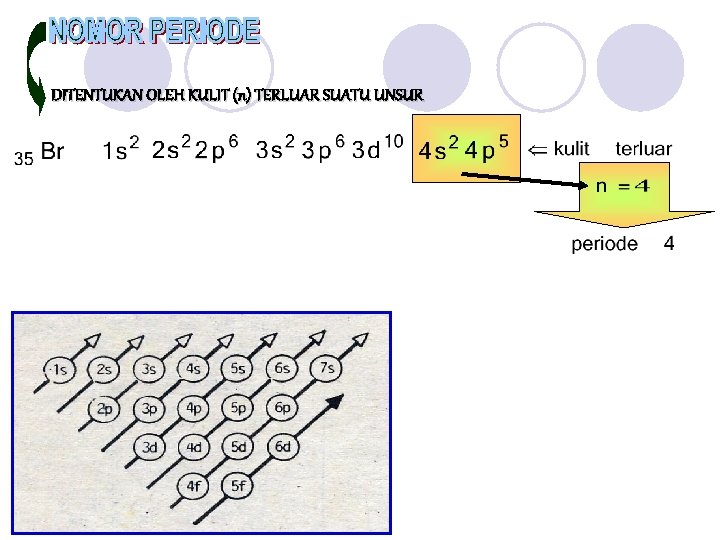
DITENTUKAN OLEH KULIT (n) TERLUAR SUATU UNSUR

DITENTUKAN OLEH JUMLAH ELEKTRON PADA KULIT TERLUAR (ELEKTRON VALENSI) SUATU UNSUR YANG KULIT TERLUARNYA SEDANG MENGISI SUB-KULIT s dan p DIMASUKKAN KE DALAM GOLONGAN A UNSUR YANG KULIT TERLUARNYA SEDANG MENGISI SUB-KULIT d dan f DIMASUKKAN KE DALAM GOLONGAN B

go to


go to


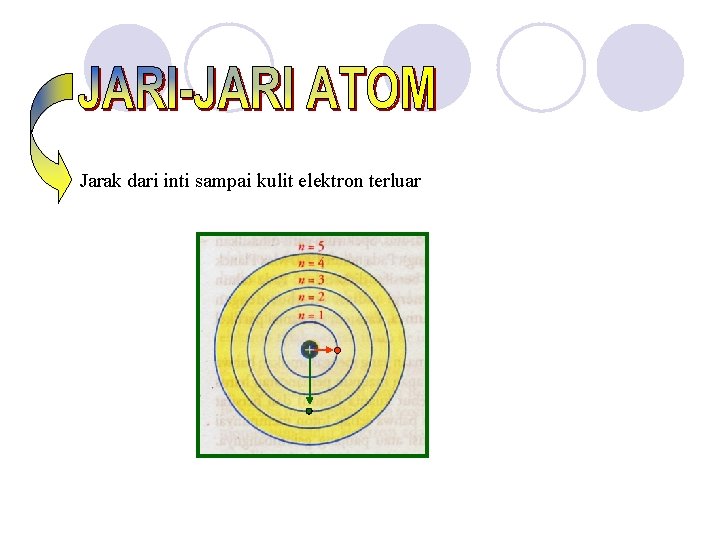
Jarak dari inti sampai kulit elektron terluar
IA r 1 H 0, 29 3 Li 1, 55 11 Na 1, 90 19 K 2, 35 37 Rb 2, 48 55 Cs 2, 67 Jari-jari atom dalam satu golongan dari atas ke bawah makin panjang


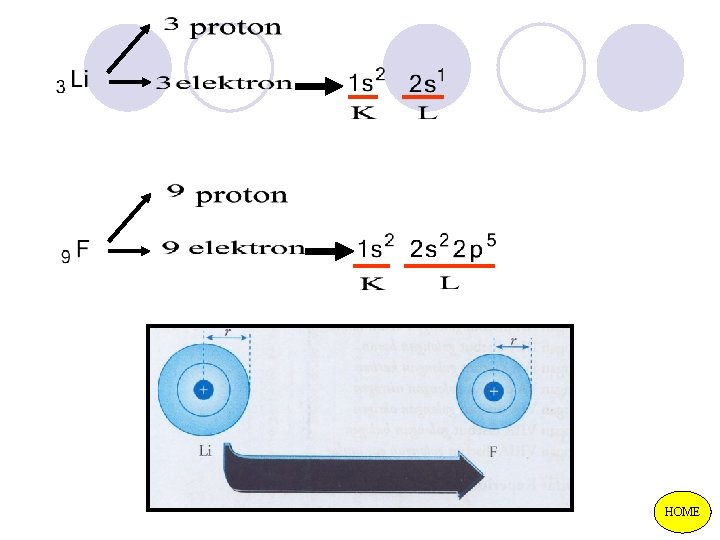
Per 2 3 Li 4 Be 5 B 6 C 7 N 8 O 9 F 10 Ne r 1, 55 1, 12 0, 98 0, 77 0, 70 0, 66 0, 64 - Jari-jari atom dalam satu periode dari kiri ke kanan makin pendek
HOME

Energi minimum yang dibutuhkan atom untuk melepaskan satu elektron yang terikat paling lemah dari suatu atom netral dalam wujud gas Dipengaruhi Jari-jari atom Nomor atom (besarnya muatan inti)

IA r (A) EI 1 H 0, 29 1312 3 Li 1, 55 520 11 Na 1, 90 496 19 K 2, 35 419 37 Rb 2, 48 403 55 Cs 2, 67 376 Energi ionisasi atom dalam satu golongan dari atas ke bawah makin kecil

Per 2 3 Li 4 Be 5 B 6 C 7 N 8 O 9 F 10 Ne proton 3 4 5 6 7 8 9 10 EI 520 900 800 1086 1402 1314 1681 2080 Energi ionisasi atom dalam satu periode dari kiri ke kanan makin besar HOME

Besarnya energi yang dilepas atau diserap jika satu elektron ditambahkan ke dalam atom netral dalam wujud gas untuk membentuk ion negatif Jika pada saat atom menangkap elektron dilepaskan energi, maka afinitas elektron berharga negatif Jika pada saat atom menangkap elektron diserap energi, maka afinitas elektron berharga positif Makin negatif harga afinitas elektron, makin mudah atom tersebut menerima elektron dan ion negatif yang terbentuk makin stabil
VIIA r (A) AE 9 F 0, 29 -328 17 Cl 1, 55 -348 35 Br 1, 90 -325 53 I 2, 35 -295 85 At 2, 48 -270 Afinitas elektron atom dalam satu golongan dari atas ke bawah makin kecil (makin positif), berarti makin sulit atom menangkap elektron

Per 2 3 Li 4 Be 5 B 6 C 7 N 8 O 9 F 10 Ne proton 3 4 5 6 7 8 9 10 AI -60 -+100 -27 -122 -+9 -141 -328 -29 Afinitas elektron atom dalam satu periode dari kiri ke kanan makin besar (makin negatif), berarti makin mudah atom menangkap elektron HOME

Ukuran kecenderungan suatu atom untuk menarik elektron ke pihaknya dalam suatu ukuran
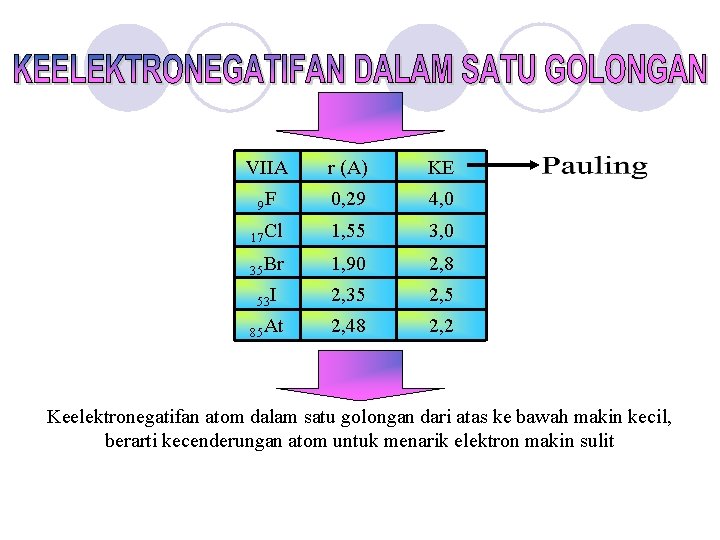
VIIA r (A) KE 9 F 0, 29 4, 0 17 Cl 1, 55 3, 0 35 Br 1, 90 2, 8 53 I 2, 35 2, 5 85 At 2, 48 2, 2 Keelektronegatifan atom dalam satu golongan dari atas ke bawah makin kecil, berarti kecenderungan atom untuk menarik elektron makin sulit
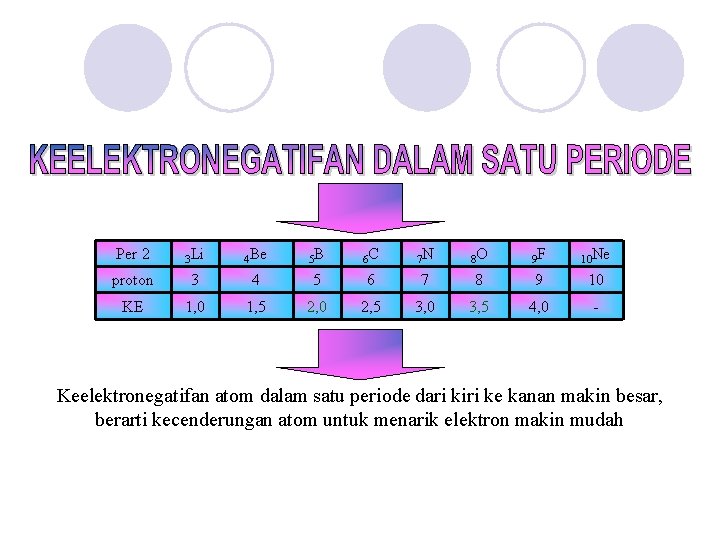
Per 2 3 Li 4 Be 5 B 6 C 7 N 8 O 9 F 10 Ne proton 3 4 5 6 7 8 9 10 KE 1, 0 1, 5 2, 0 2, 5 3, 0 3, 5 4, 0 - Keelektronegatifan atom dalam satu periode dari kiri ke kanan makin besar, berarti kecenderungan atom untuk menarik elektron makin mudah

- Slides: 34