Myeloproliferativa sjukdomar Mattias Carlsten MD Ph D STlkare























































- Slides: 85

Myeloproliferativa sjukdomar Mattias Carlsten, MD, Ph. D ST-läkare Hematologiskt Centrum Karolinska

Kroniska myeloproliferativa sjukdomar Polycythemia vera (PV) Essentiell trombocytemi (ET) Primär myelofibros (PMF) BCR-ABL negativa kroniska myeloproliferativa sjukdomar Myeloproliferative neoplasm unclassified (MPN-U, MPN UNS) Kroniska myeloisk leukemi BCR-ABL pos

Myeloproliferativa neoplasmer (MPN) • PV – ET – PMF ( – MPN-U*) • en grupp klonala benmärgssjukdomar med ökad eller minskad produktion av hematopoes • ca 350 nya fall/år i Sverige, prevalensen hög. • PV och ET vanligast, PMF mer ovanligt • medelålder vid diagnos: 65 -70 år *MPN-U/MPN UNS är en heterogen grupp som inkluderar både patienter i tidig och sen sjukdomsstadium som inte uppfyller kriterierna för PV, ET, eller PMF. Dessa har i snitt en sämre prognos än PV och ET, men bättre än PMF.

Upplägg på föreläsningen Del 1: Symtom, diagnostik och etiologi för PV, ET, PMF Komplikationer och prognos Del 2: Behandlingar – nuvarande och kommande Patientfall

Polycytemia vera (PV)

PV - Diagnoskriterier enligt WHO Major criteria: • Hb >185 g/L hos män >165 g/L hos kvinnor Eller hematokrit (EVF) >0, 52 hos män >0, 48 hos kvinnor • JAK 2 mutation (>95%) Minor criteria: • Hypercellulär benmärg-panmyelos (alla cellinjer) • Lågt s-erytropoetin • Endogenous erythroid colony formation in vitro För diagnos: båda major och 1 minor eller första major och 2 minor

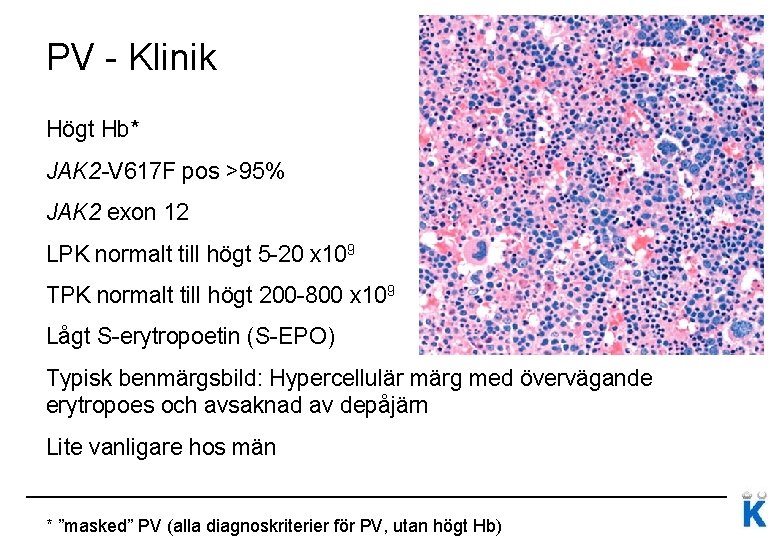
PV - Klinik Högt Hb* JAK 2 -V 617 F pos >95% JAK 2 exon 12 LPK normalt till högt 5 -20 x 109 TPK normalt till högt 200 -800 x 109 Lågt S-erytropoetin (S-EPO) Typisk benmärgsbild: Hypercellulär märg med övervägande erytropoes och avsaknad av depåjärn Lite vanligare hos män * ”masked” PV (alla diagnoskriterier för PV, utan högt Hb)

PV - Symptom Arteriell eller venös trombos - 20 % innan eller vid debut Normal-förstorad mjälte (75% i vissa studier) Klåda Mikrovaskulära störningar Yrsel och huvudvärk Trötthet Nedsatt livskvalitet

PV - Utredning • Blodstatus med differentialräkning • Järnstatus • ASAT, ALAT, bilirubin, kreatinin, urat, LD • S-erytropoetin • JAK 2 -V 617 F mutation • JAK 2 exon 12 mutation hos JAK 2 -V 617 F-negativa patienter • Benmärgsbiopsi • Kliniskt status, inklusive palpation av mjälten • Kartlägg kardiovaskulära riskfaktorer För utredningsalgoritm se Nordic MPN guidelines www. nmpn. org

Diff diagnoser vid högt Hb Förvärvade Medfödda Dehydrering Hjärtfel, hjärtsjukdom Hb variant med hög syrgasaffinitet Lungsjukdom EPO-receptor mutation Rökning? Mutationer i syragasavkännande system (VHL, PHD 2, Chuvash) Njursjukdom EPO-användning Testosteron, dopning Relativ erytrocytos (pseudopolycytemi)

Essentiell trombocytemi (ET)

ET - Diagnoskriterier enligt WHO • Varaktig trombocytos TPK >450 x 109/L • Ökad mängd stora megakaryocyter i BM • Frånvaro av kriterier för PV, PMF, KML eller andra myeloida maligniteter • JAK 2 -V 617 F mutation (50 -60%) eller annan klonal markör, om JAK 2 neg – uteslut sekundär orsak till trombocytos Alla kriterier måste vara uppfyllda

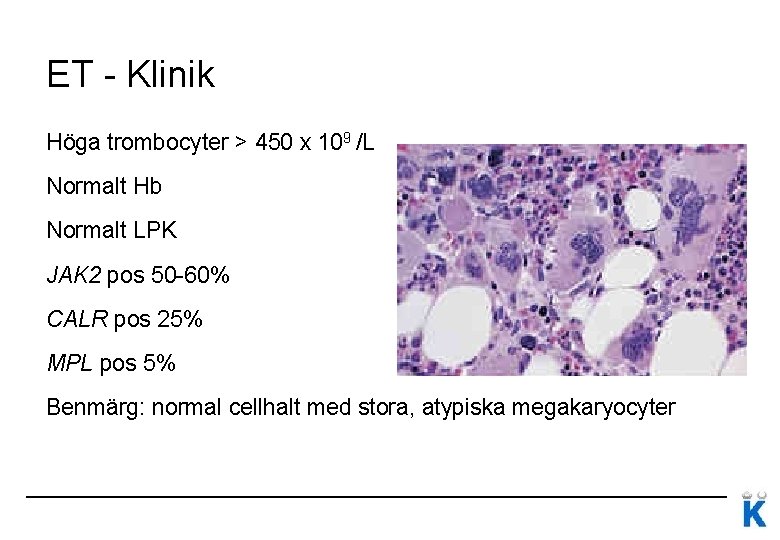
ET - Klinik Höga trombocyter > 450 x 109 /L Normalt Hb Normalt LPK JAK 2 pos 50 -60% CALR pos 25% MPL pos 5% Benmärg: normal cellhalt med stora, atypiska megakaryocyter


ET - Klinik och symptom Lite vanligare hos kvinnor Ofta asymptomatiska Arteriell och venös trombos - 20 % innan eller vid debut Trötthet Erytromelalgi – mikrovaskulär påverkan

ET - Utredning • Blodstatus med differentialräkning • ASAT, ALAT, bilirubin, kreatinin, urat, LD, CRP, SR, elfores • JAK 2 -V 617 F mutation • CALR, MPL och/eller BCR-ABL hos JAK 2 -V 617 F-negativa patienter • Benmärgsbiopsi • Kliniskt status, inklusive palpation av mjälten • Kartlägg kardiovaskulära riskfaktorer

Reaktiv trombocytos - betydligt vanligare än ET Stess: Postoperativt, trauma, blödning Kronisk järnbrist Maligniteter Kronisk infektion, ex TB Kronisk inflammation, ex PMR, RA, SLE

Primär myelofibros (PMF)

Primär myelofibros (PMF) Tidig(prefibrotisk) – Hyperproliferativ fas – fibrotisk fas Sjukdomsprogress Höga till normala blodvärden • Låga blodvärden • Förstorad mjälte • Konstitutionella symptom

PMF - Diagnoskriterier enligt WHO Major criteria: • Megakaryocytproliferation med atypi och ökad fibermängd i benmärgen • Inga tecken på PV, KML, MDS eller annan benmärgssjukdom • JAK 2 -V 617 F mutation (50 -60%) eller i frånvaro av klonal markör skall annan orsak till fibros uteslutas Minor criteria: • • ”Benmärgsdiff” (förstadier i blodet) Högt LD Anemi Splenomegali För diagnos krävs samtliga 3 major kriterier samt 2 minor kriterier

Andra orsaker till benmärgsfibros Infektion Autoimmun sjukdom Systeminflammation Hårcellsleukemi eller annan lymfoid neoplasm Metastatisk malignitet Toxisk benmärgspåverkan

PMF - Utredning • Blodstatus med differentialräkning • Järnstatus • ASAT, ALAT, bilirubin, kreatinin, urat, LD • JAK 2 -V 617 F mutation • CALR, MPL och/eller BCR-ABL hos JAK 2 -V 617 F-negativa patienter • Benmärgsbiopsi • Kliniskt status, inklusive palpation av mjälten • Kartlägg kardiovaskulära riskfaktorer

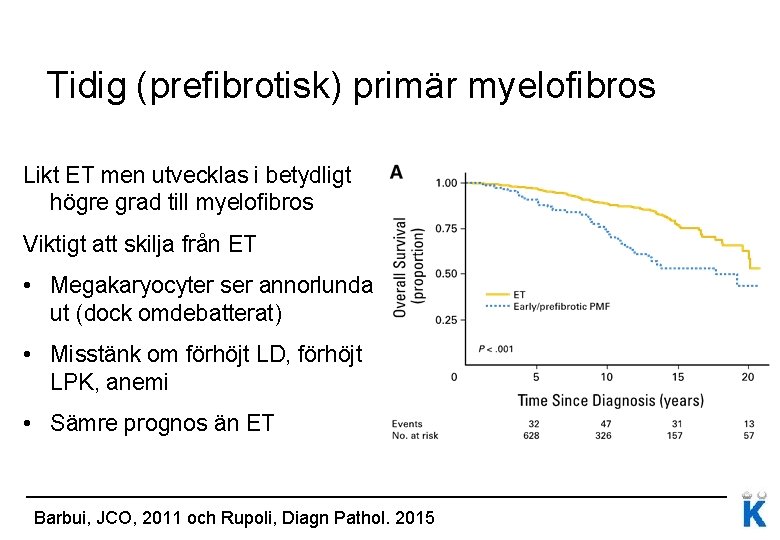
Tidig (prefibrotisk) primär myelofibros Likt ET men utvecklas i betydligt högre grad till myelofibros Viktigt att skilja från ET • Megakaryocyter ser annorlunda ut (dock omdebatterat) • Misstänk om förhöjt LD, förhöjt LPK, anemi • Sämre prognos än ET Barbui, JCO, 2011 och Rupoli, Diagn Pathol. 2015

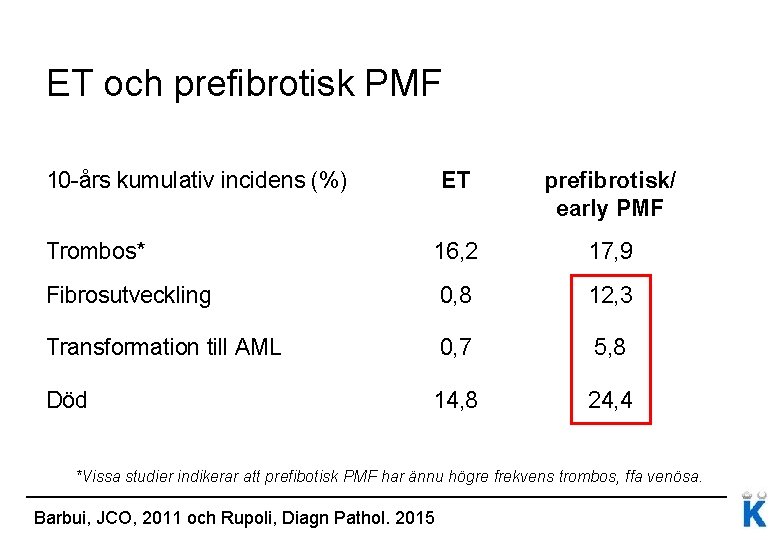
ET och prefibrotisk PMF 10 -års kumulativ incidens (%) ET prefibrotisk/ early PMF Trombos* 16, 2 17, 9 Fibrosutveckling 0, 8 12, 3 Transformation till AML 0, 7 5, 8 Död 14, 8 24, 4 *Vissa studier indikerar att prefibotisk PMF har ännu högre frekvens trombos, ffa venösa. Barbui, JCO, 2011 och Rupoli, Diagn Pathol. 2015

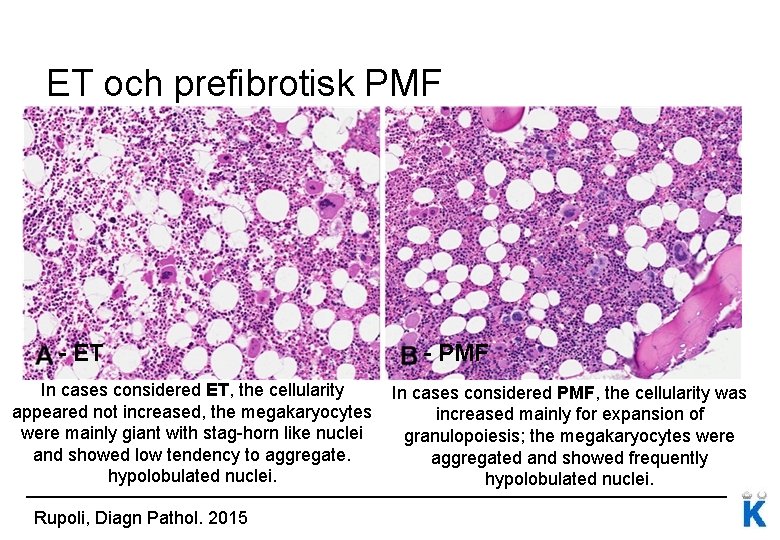
ET och prefibrotisk PMF - ET In cases considered ET, the cellularity appeared not increased, the megakaryocytes were mainly giant with stag-horn like nuclei and showed low tendency to aggregate. hypolobulated nuclei. Rupoli, Diagn Pathol. 2015 - PMF In cases considered PMF, the cellularity was increased mainly for expansion of granulopoiesis; the megakaryocytes were aggregated and showed frequently hypolobulated nuclei.

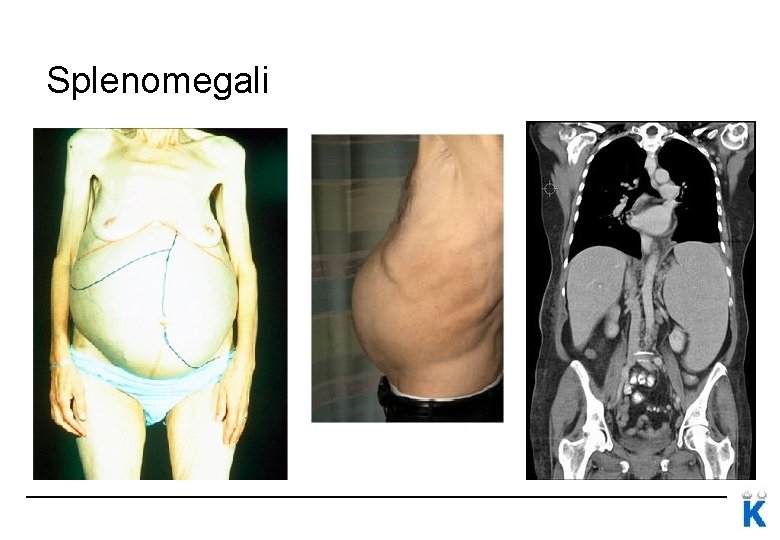
Uttalat fibrotisk MF • Anemi • Benmärgssvikt låga trombocyter och låga vita • Extramedullär blodbildning (mjälte, lever) • Splenomegali • Leukoerytroblastisk blodbild (förstadier i blodet) • Konstitutionella symptom (B-symptom) • Kakexi

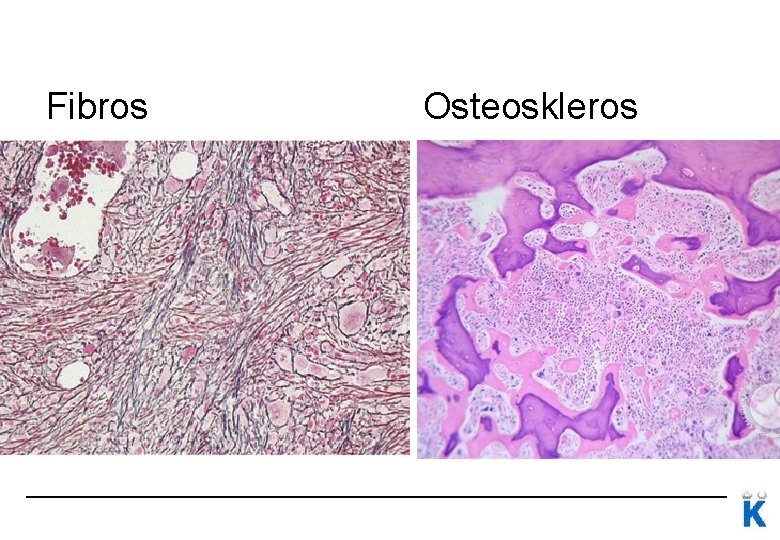
Fibros Osteoskleros

Splenomegali

Komplikationer och prognos vid MPN

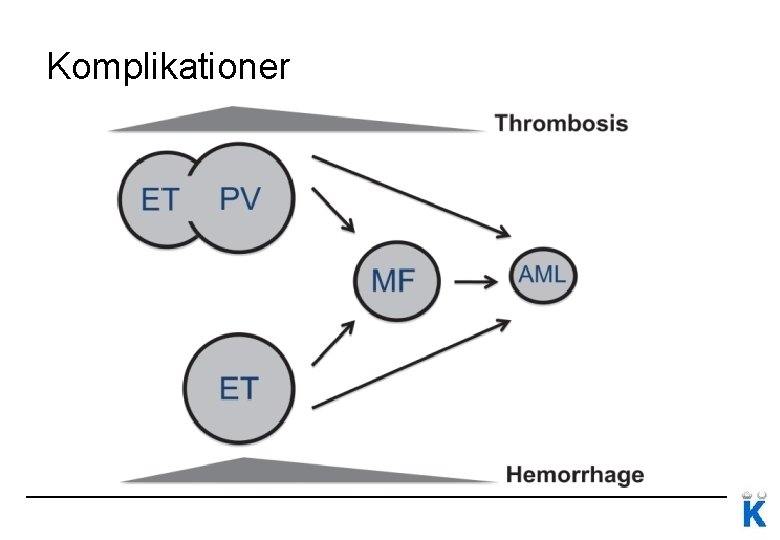
Komplikationer

Komplikationer PV ET PMF 40% ca 45% som ET? Fibrosutveckling på 10 år 10 -15% 1% - Transformation till akut leukemi 6 -15% <5% 5 -30% Trombos* Ökad risk för blödningar, framförallt vid TPK >1500 x 109 *1) Arteriella tromboser > venösa tromboser. 2) Utbredda buktromboser – tänk MPN

Riskfaktorer för transformation till MF PV: hög ålder (>60 år), leukocytos, reticulin+ fibros, splenomegali och hög JAK 2 -V 617 F allel börda ET: hög ålder (>60 år), leukocytos, anemi, reticulin+ fibros, avsaknad av JAK 2 -V 617 F, ASXL 1 mutation. Behandling med anagrelide. Cerquozzi et al. Blood Cancer Journal 2015

Riskfaktorer för transformation till AML PV: hög ålder (>61 -70 år), leukocytos (>10 -15), reticulin+ fibros, splenomegali, abnormal karyotyp, TP 53 eller RUNX 1 mutationer, behandling med radiofosfor (P 32) eller busulfan. Kvinnligt kön? ET: hög ålder (>60 år), leukocytos (>10), anemia, trombocytos (extrem), reticulin+ fibros, TP 53 eller RUNX 1 mutationer. Cerquozzi et al. Blood Cancer Journal 2015

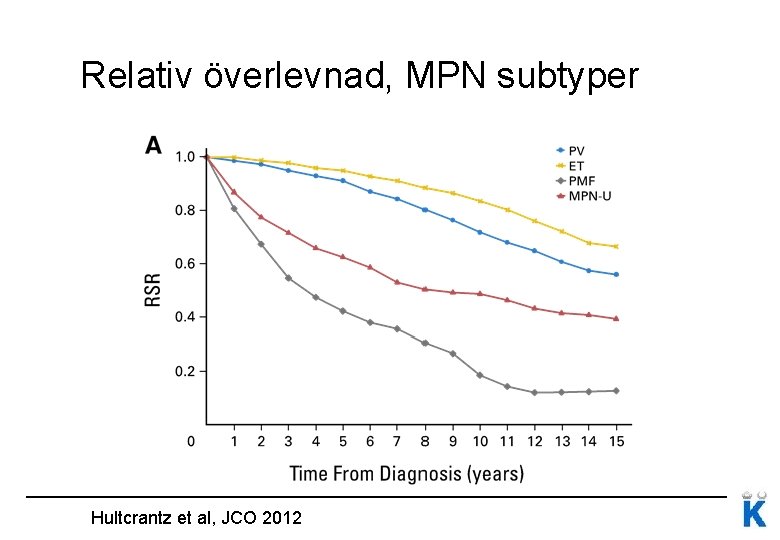
Prognos MPN Median överlevnad: PV 15 -20 år ET ej påverkad? PMF 5 år (2 -15 beroende på riskgrupp)

Relativ överlevnad, MPN subtyper Hultcrantz et al, JCO 2012

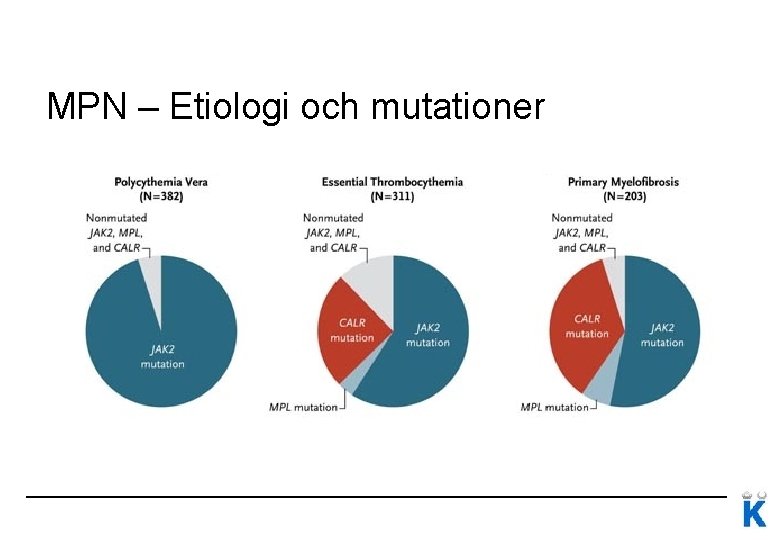
MPN etiologi och mutationer

MPN – Etiologi och mutationer Familjär koppling: 5 -7 ggr högre risk hos förstagradssläktingar Janus kinas 2 (JAK 2 -V 617 F) mutation 95% av PV 50 -60% av ET och PMF Flertal ytterligare mutationer har beskrivits JAK 2 exon 12 – PV med isolerad erytrocytos ca 2% CALR – ET 25% och PMF 35% MPL – ET 3% och PMF 6%

MPN – Etiologi och mutationer

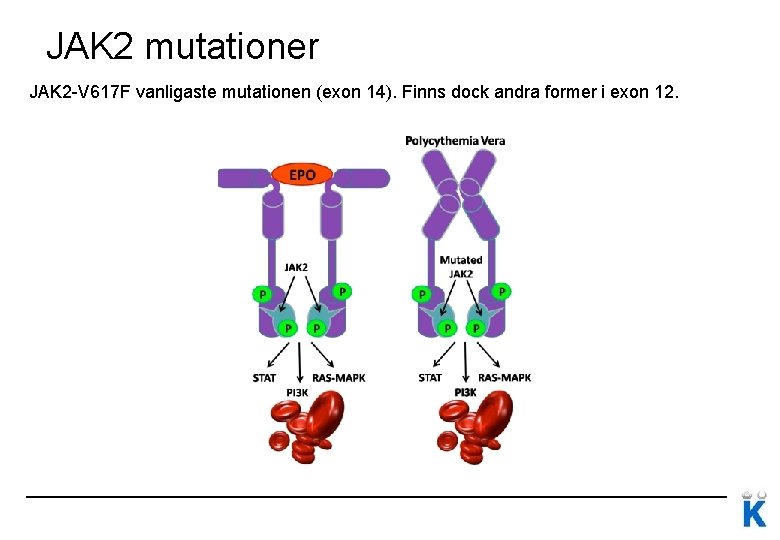
JAK 2 mutationer JAK 2 -V 617 F vanligaste mutationen (exon 14). Finns dock andra former i exon 12.

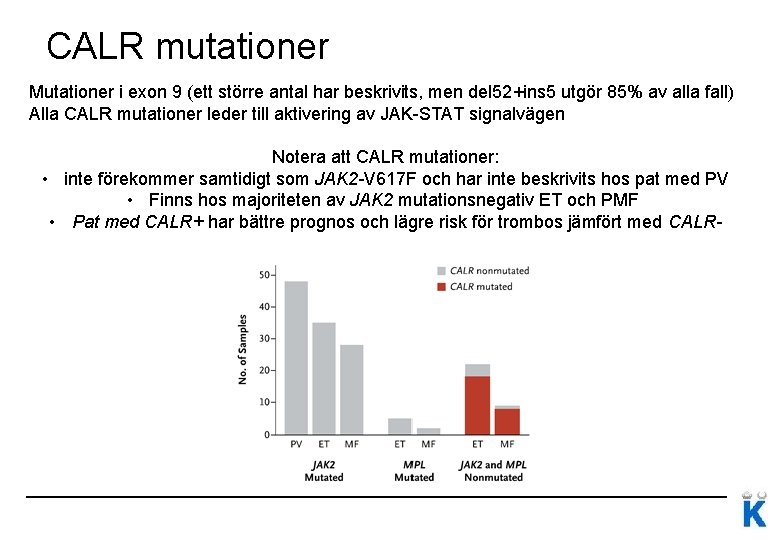
CALR mutationer Mutationer i exon 9 (ett större antal har beskrivits, men del 52+ins 5 utgör 85% av alla fall) Alla CALR mutationer leder till aktivering av JAK-STAT signalvägen Notera att CALR mutationer: • inte förekommer samtidigt som JAK 2 -V 617 F och har inte beskrivits hos pat med PV • Finns hos majoriteten av JAK 2 mutationsnegativ ET och PMF • Pat med CALR+ har bättre prognos och lägre risk för trombos jämfört med CALR-

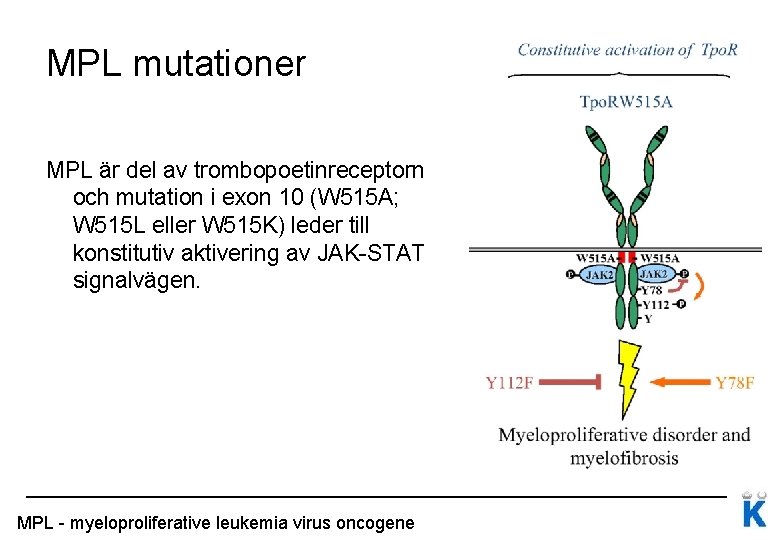
MPL mutationer MPL är del av trombopoetinreceptorn och mutation i exon 10 (W 515 A; W 515 L eller W 515 K) leder till konstitutiv aktivering av JAK-STAT signalvägen. MPL - myeloproliferative leukemia virus oncogene

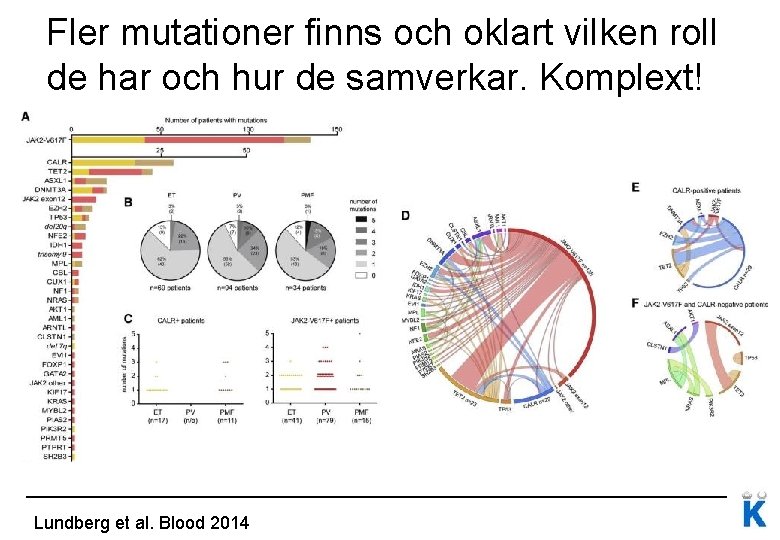
Fler mutationer finns och oklart vilken roll de har och hur de samverkar. Komplext! Lundberg et al. Blood 2014

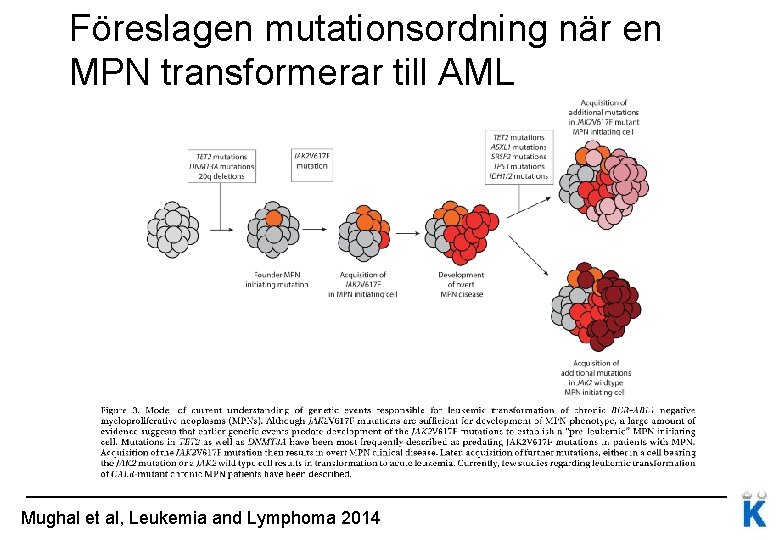
Föreslagen mutationsordning när en MPN transformerar till AML Mughal et al, Leukemia and Lymphoma 2014

Kaffepaus

Behandling av MPN

Behandling PV och ET Syftar framförallt till att förbättra symptom och minska risken för tromboembolism Blodförtunning + optimera behandling av kardiovaskulära riskfaktorer Cytoreduktiv behandling Hittills inget läkemedel som kan hindra fibros- eller leukemiutveckling Benmärgstransplantation – enda botande

Behandling PV och ET PV: Venesectio till EVF <0, 45, framkallar järnbrist och minskar trombosrisken PV och ET: Trombyl (ASA) 75 mg/dag om ej kontraindikation OBS! Trombocytantal Marchioli et al, NEJM 2013, Landolfi et al, NEJM 2004

Cytoreduktiv behandling PV och ET Indikation: • Högrisk patient • >60 år • tidigare tromboembolism • TPK >1500 x 109/L • Mikrovaskulära symptom • Högt LPK? • Hög kardiovaskulär risk Mål: normaliserade blodvärden och välmående patient

Val av cytoreduktiv behandling Hydroxyurea (Hydrea) Interferon – yngre Anagrelid – enbart trombocytsänkande Busulfan – andra handsval till äldre Radioaktivt fosfor (P 32) – tredje handsval äldre Busulfan och P 32 i höga doser ökar risken för övergång i AML Ej visat för hydroxyurea men kontroversiellt Björkholm et al, JCO 2011

Behandling PMF och sekundär MF Först klassificera enligt risk-score (IPSS, DIPSS-plus) Lågrisk och intermediär-1 Högrisk och intermediär-2 Symptomatisk behandling Allogen stamcellstransplantation? Cytoreduktiv behandling JAK 2 hämmare? Andra nya behandlingsmöjligheter?

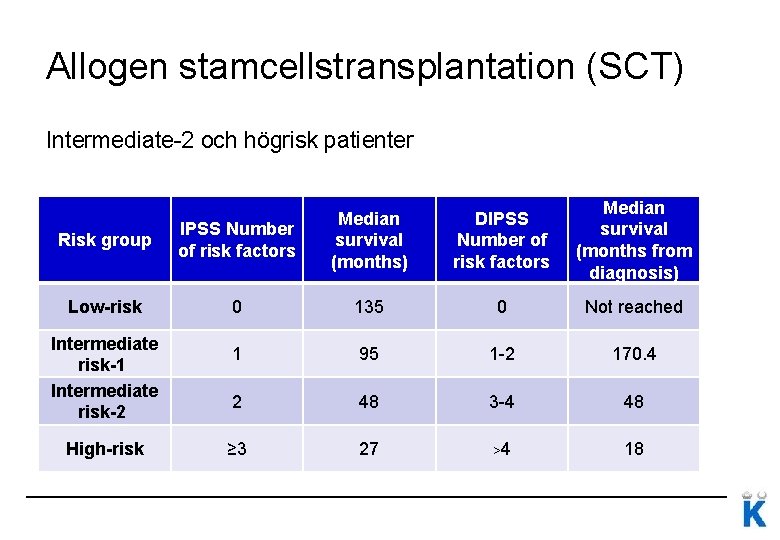
Allogen stamcellstransplantation (SCT) Intermediate-2 och högrisk patienter DIPSS Number of risk factors Median survival (months from diagnosis) Risk group IPSS Number of risk factors Median survival (months) Low-risk 0 135 0 Not reached 1 95 1 -2 170. 4 2 48 3 -4 48 ≥ 3 27 >4 18 Intermediate risk-1 Intermediate risk-2 High-risk

Behandling PMF låg och Intermediär-1 eller icke-transplantationskandidater Trombosförebyggande/behandling av höga blodvärden Behandla som ET (men utan anagrelid) Trombyl 75 mg per dag Cytoreduktiv behandling Hydroxyurea Interferon Busulfan P 32

Symptomlindrande MF Anemi Erytropoetin Androgener (Danazol) Kortison IMi. Der (+ kortison) Transfusion

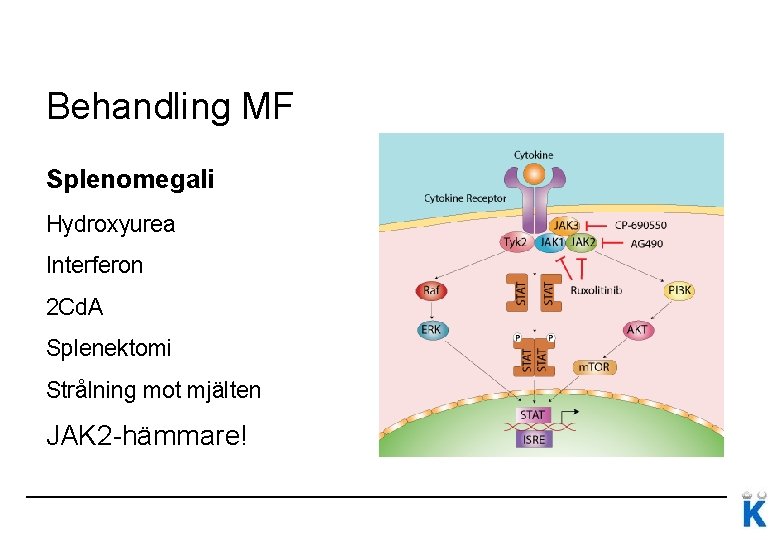
Behandling MF Splenomegali Hydroxyurea Interferon 2 Cd. A Splenektomi Strålning mot mjälten JAK 2 -hämmare!

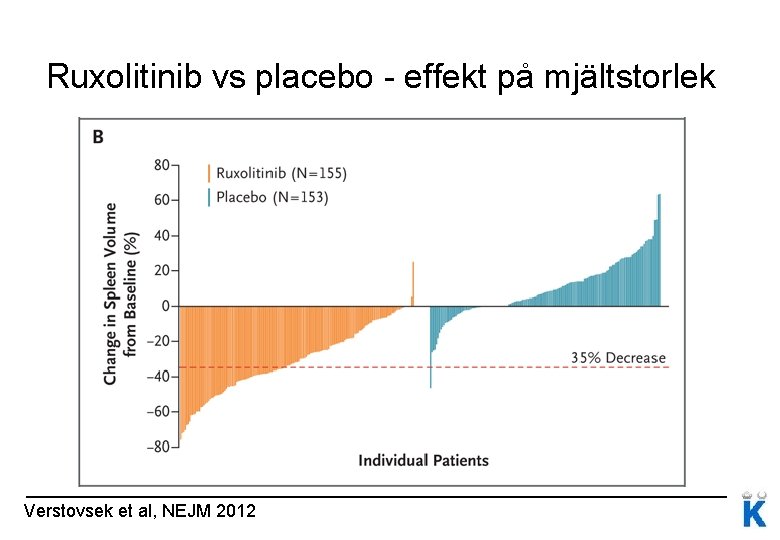
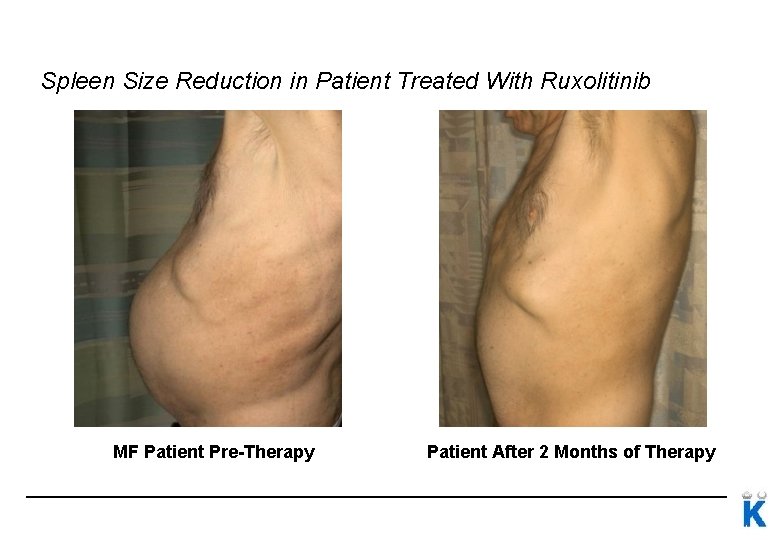
Nya behandlingar vid MF Första JAK 2 hämmaren godkänd i Sverige: ruxolitinib (Jakavi®) Fungerar oavsett om patienten är JAK 2 -positiv eller ej Minskar mjältstorleken (hos 42% minskar mjältens volym med >35% vilket motsvarar 50% minskning i palpatorisk storlek) Förbättrar konstitutionella symptom och livskvalitet Ruxolitinib - förbättrad överlevnad?

Ruxolitinib vs placebo - effekt på mjältstorlek Verstovsek et al, NEJM 2012

Spleen Size Reduction in Patient Treated With Ruxolitinib MF Patient Pre-Therapy 59 Patient After 2 Months of Therapy Photos used with permission from MD Anderson Cancer Center.

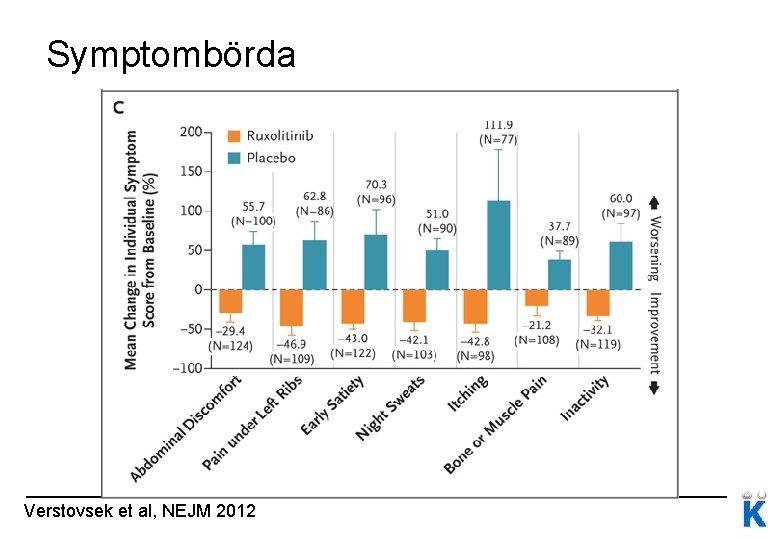
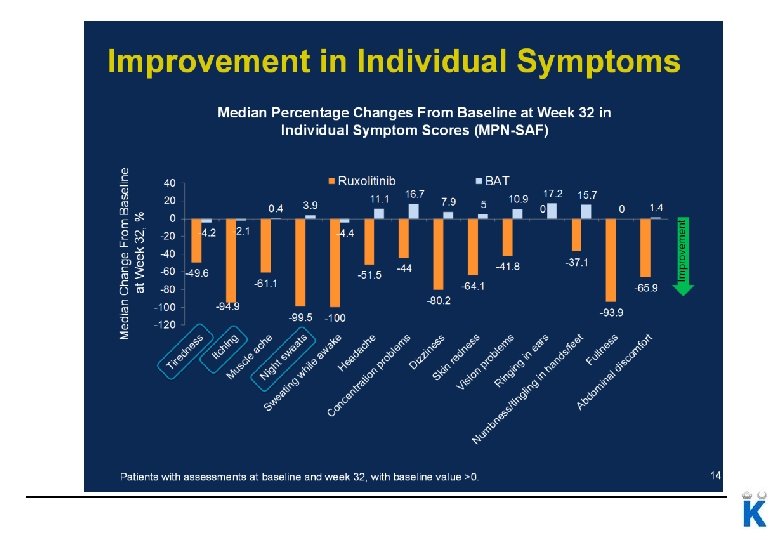
Symptombörda Verstovsek et al, NEJM 2012

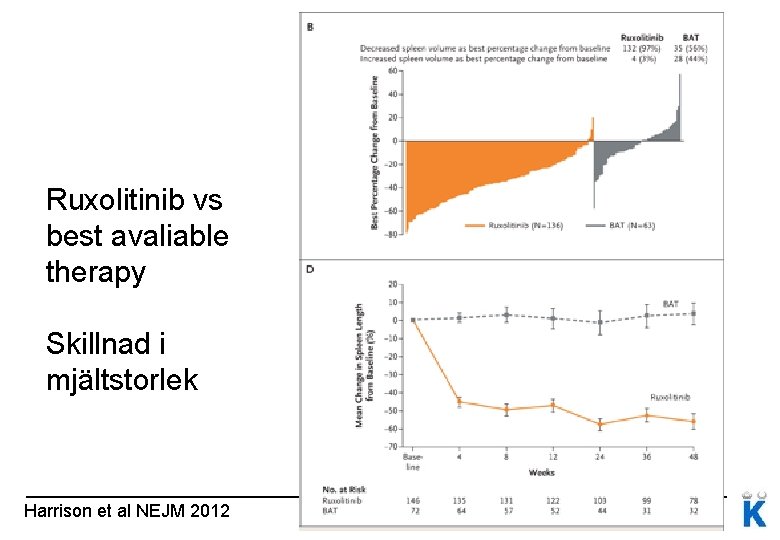
Ruxolitinib vs best avaliable therapy Skillnad i mjältstorlek Harrison et al NEJM 2012

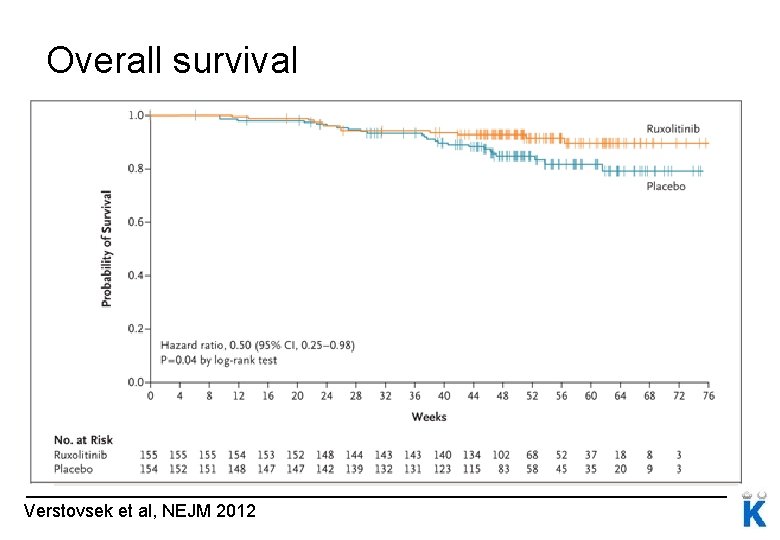
Overall survival Verstovsek et al, NEJM 2012

222 patients with JAK 2 -positive PV Resistant/intolerant to hydroxyurea Ruxolitinib vs Best Available Therapy (BAT) Outcomes: hematological response, reduction in spleen size, quality of life 2020 -12 -01 63

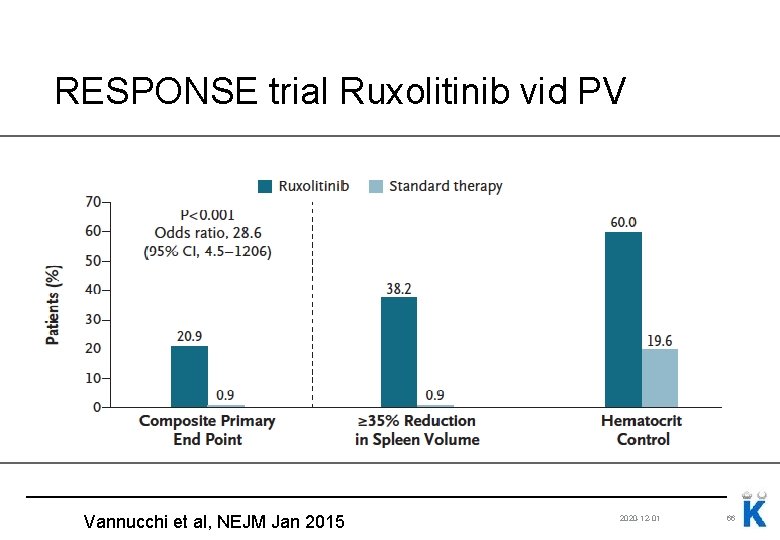
Ruxolitinib vid PV RUX vs BAT 20. 9% vs 0. 9% uppnådde primary endpoint (hematologisk kontroll och ≥ 35% minskning av mjältvolym) 60. 0% vs 19. 6% hematologiskt kontroll vid 32 veckor 38. 2% vs 0. 9% hade ≥ 35% minskning av mjältvolym 49% vs 5% BAT hade ≥ 50% mindre symptom (enligt MPN-SAF) Vannucchi et al, NEJM Jan 2015 2020 -12 -01 64

Results forts. JAK 2 allelbörda -12% RUX vs -1. 2% BAT (median -37. 5% vid v 112) Cross-over: 87. 5% av alla i BAT-arm vid v 32 Innan v 32: RUX 1 trombos och 6 tromboser i BAT-arm RUX: 3 MF och 1 AML BAT: 1 MF Vannucchi et al, NEJM Jan 2015 2020 -12 -01 65

RESPONSE trial Ruxolitinib vid PV Vannucchi et al, NEJM Jan 2015 2020 -12 -01 66


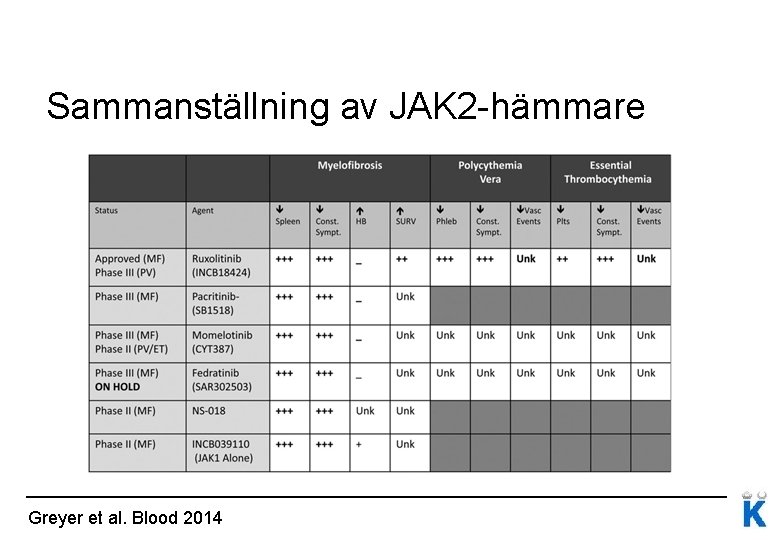
Sammanställning av JAK 2 -hämmare Greyer et al. Blood 2014

Andra nya läkemedel: Andra JAK 2 -hämmare Immunmodulerande (IMi. D) HDAC-inhibitors Telomerashämmare m. TOR-hämmare Kombinationsbehandlingar Hypometylerare mot MPN-AML (azacytidin, decitabin)

Trombos - arteriell och venös Utbredda buktromboser Budd-Chiari/portatrombos/splanchnicus Stroke Hjärtinfarkt Lungemboli/DVT Behandla som ”vanlig” tromboembolism Sänk blodvärden: venesectio, (erytraferes), trombaferes, starta cytoreduktiv behandling – hydroxyurea i första hand

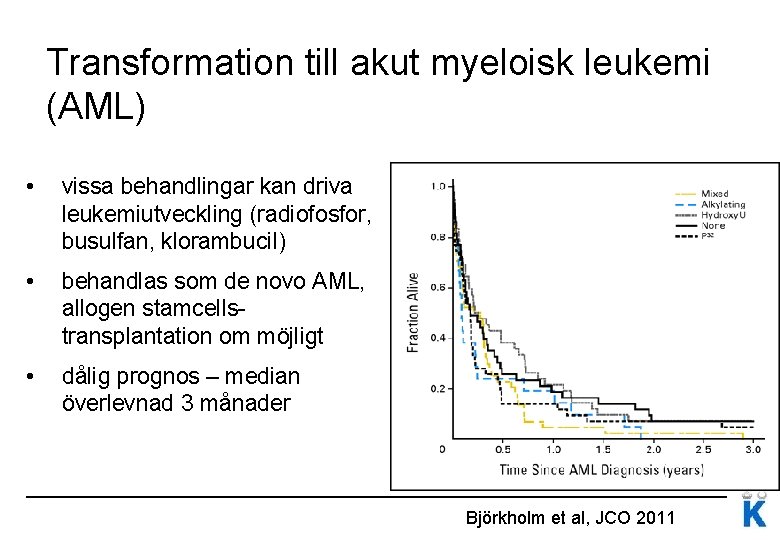
Transformation till akut myeloisk leukemi (AML) • vissa behandlingar kan driva leukemiutveckling (radiofosfor, busulfan, klorambucil) • behandlas som de novo AML, allogen stamcellstransplantation om möjligt • dålig prognos – median överlevnad 3 månader Björkholm et al, JCO 2011

Övriga komplikationer och tillstånd • Blödning • Klåda • Kirurgi • Graviditet

Sammanfattning Kroniska benmärgscancrar med varierande påverkan på livskvalitet och förväntad livslängd Ökad risk för tromboembolism (arteriell > venös) Trombosrisk minskas med behandling därför viktigt att hitta dessa sjukdomar PV och ET kan gå över i MF. Alla subtyper kan transformera till AML Ingen botande behandling förutom benmärgstransplantation Nya läkemedel på gång framförallt JAK 2 -hämmare vilka kan förbättra symptomen och troligen förlänga överlevnaden

Sammanfattning forts Tänk på MPN som diffdiagnos vid höga blodvärden, framförallt hos patienter med tromboser (buktromboser) Om högt Hb och högt EPO – utred för sekundär erytrocytos Alla med högt Hb skall inte tappas Ge inte järntillskott till patienter med PV Blödningsrisk vid TPK >1500 x 109/L Optimera kardiovaskulära riskfaktorer!

Patientfall

Fall 1. Man 51 år Diabetes typ 2 och har haft en minor stroke Hb 157 g/L LPK 7, 8 x 109/L TPK 541 x 109/L EPO 4, 2 (normalt) Tänkbar diagnos?

Fall 1. Man 51 år Utredning? Fler prover? Hb 157 g/L Behandlingsval? LPK 7, 8 x 109/L Interferon? TPK 541 x 109/L Hydrea? EPO 4, 2 (normalt) …? ASA? Benmärg: myeloprolif. sjd. JAK 2 -V 617 F neg ET som behandlas med Andra mut? ASA+Interferon CALR pos

Fall 2. Man 35 år Utredning? Kompletterande prov Hb 194 g/L Benmärg: normal EVF 0, 54 JAK 2 V 617 F neg LPK 9, 1 x 109/L EPO 113 (högt) TPK 254 x 109/L Diagnos? Ej PV Vidare utredning behövs

Fall 3. Kvinna 61 år Utredning? Hb 78 g/L LPK 3, 1 x 109/L varav neutrofila 1, 9, myelocyter 0, 3, metamyelocyter 0, 2, blaster <0, 1 TPK 93 x 109/L Konstitutionella symptom (viktnedgång, svettningar, feber) Ferritin 4672 mikrog/L Komplementerande svar Benmärg: Fibros grad II MPN som visade sig vara högrisk Behandling? Allogen stamcellstransplantation

Fall 4. Kvinna 72 år Utredning? Kompletterande svar Hb 189 g/L EPO 53 (lågt) LPK 10, 1 x 109/L varav neutrofila 8, 2 JAK 2 V 617 F pos Benmärg: bild som vid MPN TPK 265 x 109/L EVF 0, 58 MCV 94 Diagnos? PV Behandlingsval? ASA+Venesectio+Hydrea

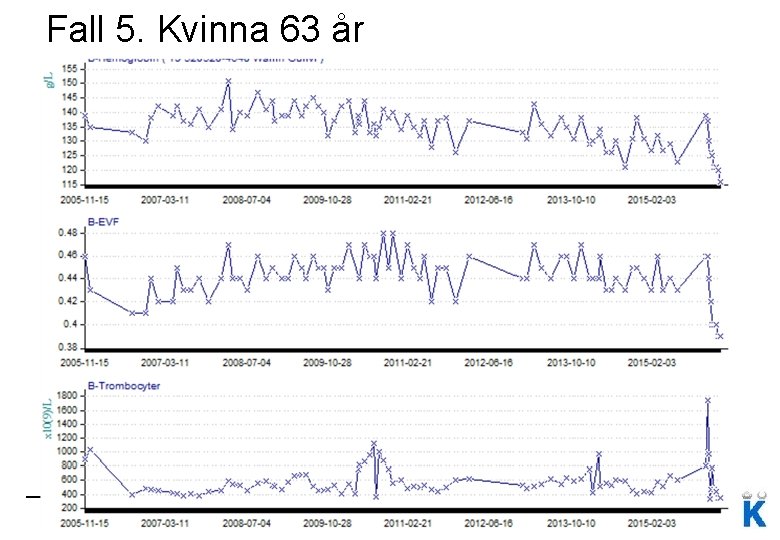
Fall 5. Kvinna 63 år 1995 - PV diagnos, högt Hb och TPK. Interferonbehandling startas (Peg. Intron). ASA. Bra svar. 2004 sept - EVF över 0. 45, första venesectio görs och utsättning av Peg. Intron då pat är trött (biverkan? ) 2004 okt - dock stigande TPK (över 1000) och EVF över 0. 45. Peg. Intron sätts in igen samt fortsatt venesectio och ASA 2005 juni - Lätt påverkade levervärden (ALP), ULJ mjälte/lever utesluter trombos. Misstanke om biverkan på Peg. Intron (? )

Fall 5. Kvinna 63 år 2005 sept - trött deprimerad, mkt på jobbet. Sjukskriven 50%. Biverkan av Peg. Intron kan ej uteslutas. 2006 jan – Hydreabehandling startas trots att pat är under 60 år, TPK under 1500 (1000). Peg. Intron prövat. JAK 2 mutations analys beställs. Fortsatt venesectio och ASA. 2006 april - TPK 292, ingen uppenbar biverkan av Hydrea, möjligvis ledstelhet morgontid. Remiss skickas till reumatologen. 2006 sept - Reumatologen sätter diagnos Sjögren 2006 – 2010 - Hydrea + Venesectio + ASA.

Fall 5. Kvinna 63 år 2010 april – Pat vill avsluta Hyrdea. Görs på prov, men redan inom någon månad är TPK över 1000 igen. Åter Hydrea 10 tabl/vecka 2011 - Mår ej bra, yrsel och ostadighetskänsla. CT skalle ua 2014 – Hydreadosen höjs då TPK ej ligger under målvärde 400 2015 dec - stigande TPK ses, Hydrea höjs till 18 tabletter/vecka med plan om omkontroll av prover om 3 veckor. 11 dagar senare söker pat akutmott pga tryck över bröstet. Tolkas som GERD, får Lundgrens blandning utan effekt. Omeprazol, hem

Fall 5. Kvinna 63 år 2015 28/12 – Venesectio, TPK 1740 (TPK 800 15/12). Vad skall man tänka på här? Ökad blödningsrisk. 2016 4/1 - Blir uppringd av Dr. Ungerstedt. Pat har känt sig flåsig och haft nervösa besvär sista tiden. Höjer Hydrea till 30/vecka. 2016 5/1 - Ny kontakt, obehag I buken framkommer utöver angivna symtom. Vad skall man tänka på här? CT buk beställs. CT angio visar trombos I höger och mellersta leverloben. Budd. Chiari. Ingen trombos I mjälten som mäter 13. 5 cm. Insätts på Fragmin i tvådos då TPK över 1700. Ej Waran. Feb 2016, TPK I sjunkande. Sura uppstötningar, får PPI med effekt.

Fall 5. Kvinna 63 år

Tack! Frågor? Hör gärna av er om ni har frågor: mattias. carlsten@ki. se

Rekommenderad läsning MPN Nordic guidelines www. nmpn. org/guidelines, www. sfhem. se WHO klassifikationen, Swerdlow 2008 ELN-guidelines, Barbui et al JCO 2011, Philadelphia-Negative Classical Myeloproliferative Neoplasms: Critical Concepts and Management. Recommendations From European Leukemia Net How I treat PV/ET/PMF i Blood Artiklar i Läkartidingen; Johansson – PV, Andreasson – ET, Merup – PMF Hultcrantz – Högt Hb-värde, inte alltid polycytemia vera