MITTEMETALLID Martin Saar GAG 2008 1 Mittemetallidest ldiselt























- Slides: 25

MITTEMETALLID Martin Saar GAG 2008

1. Mittemetallidest üldiselt • Mittemetallid on. . . – koondunud perioodilisussüsteemis üles paremale: • IIIA – VIIA rühm (VIIIA – väärisgaasid) – välisel elektronkihil palju elektrone (4 -7) – aatomiraadius suhteliselt väike – elektronegatiivsus võrdlemisi kõrge – Keemilistes reaktsioonides nii redutseerijad kui ka oksüdeerijad (va fluor ja tavaliselt hapnik) – oa ühendites võib olla nii positiivne kui negatiivne • Va: F – alati –I; O – tavaliselt –II

1. Mittemetallidest üldiselt • Mittemetallilised omadused tugevnevad: – Rühmas alt üles – Perioodis vasakult paremale • See on ühtlasi ka OKSÜDEERIVATE omaduste tugevnemise tendents

1. Mittemetallidest üldiselt • Mittemetallides lihtainena esineb kovalentne mittepolaarne side – Molekulaarsed: VIIA, N 2, O 2, H 2, S 8. . . – Aatomvõrega: C (teemant), Si, B • Allotroopia – keemilise elemendid esinemine mitme erineva lihtainena: – Erinev aatomite arv molekulis: dihapnik O 2 ja osoon O 3 – Erinev kristallistruktuur: teemant ja grafiit

2. FÜÜSIKALISED OMADUSED Üldised omadused – neid on vähe (erinevamad kui metallid) – halb soojus- ja elektrijuhtivus – rabedus Erinevad füüsikalised omadused: – erinev värvus – väga erinev sulamistemperatuur • lämmastik, hapnik broom teemant, grafiit, boor

3. KEEMILISED OMADUSED • Mittemetallid lihtainena käituvad keemilistes reaktsioonides kas redutseerijana või oksüdeerijana. . . • VAHEPALA meeldetuletuseks Protsess Oksüdeerumine Elektronide. . . loovutamine Oksüdatsiooniaste kasvab Osakese nimetus redutseerija Näide Redutseerumine. . . liitmine kahaneb oksüdeerija Mg 0 – 2 e- Mg. II S 0 + 2 e- S-II

3. KEEMILISED OMADUSED • Oksüdeerijana käituvad mittemetallid: – Alati metallide suhtes: • Fe + S Fe. S • 2 Na + Cl 2 2 Na. Cl • 2 Mg + O 2 2 Mg. O – Endast nõrgemate, st madalama elektronegatiivsusega mittemetallide suhtes • S + H 2 S – väävel oksüdeerija, vesinik redutseerija • O 2 + 2 H 2 O – hapnik oksüdeerija, vesinik redutseerija

3. KEEMILISED OMADUSED • Redutseerijana käituvad mittemetallid: – Endast tugevamate, st kõrgema elektronegatiivsusega mittemetallide suhtes • S + O 2 SO 2 – väävel redutseerija, hapnik oksüdeerija

3. KEEMILISED OMADUSED • Tugevam halogeen või tõrjuda nõrgema halogeeni halogeniidist välja • Mittemetallilisus ehk oksüdeerivad omadused tugevnesid rühmas alt üles! • Cl 2 + 2 Na. I 2 Na. Cl + I 2 • I 2 + Na. Cl ei toimu

4. Mittemetallide redoksomadused ühendites Kui mittemetalli oa on ühendis. . . • maksimaalne – ehk võrdne rühma numbriga, – siis saab ta käituda vaid elektrone liita – ehk käituda oksüdeerijana • minimaalne – ehk võrdne rühma number miinus 8 – siis saab ta vaid elektrone loovutada – ehk käituda vaid redutseerijana • Vahepealne, siis saab ta olla nii redutseerija kui oksüdeerija, sõltuvalt reaktsioonipartnerist

4. Mittemetallide redoksomadused ühendites Element Lämmastik Väävel V Maksimaalne Vahepealne Minimaalne VI HNO 3 SO 3 0 IV N 2 SO 2 -III -II NH 3 H 2 S

4. Mittemetallide redoksomadused ühendites jm • Mittemetallide vesinikühendid võivad seetõttu põleda oksiidideks: 2 H 2 S + 3 O 2 2 SO 2 + 2 H 2 O • Mittemetallioksiidid, kus mittemetalli oa pole maksimaalne võivad edasi oksüdeeruda: 2 SO 2 + O 2 2 SO 3 • Mitmed mittemetallioksiidid reageerivad veega, andes happe: SO 3 + H 2 O H 2 SO 4

5. Oksüdeerivate omadustega happeanioonid Metallide reageerimisel lahjendatud hapetega olid oksüdeerijateks happelahuses olevad vesinikioonid. Metallide reageerimisel lämmastikhappe ja kontsentreeritud väävelhappega on oksüdeerijaks aga happeanioon – täpsemalt selles maksimaalses oa-s olev mittemetall N või S. Seetõttu vesinikku ei eraldu, tekivad hoopis: • HNO 3 korral: NH 3 (NH 4 NO 3), N 2 O NO, NO 2 • H 2 SO 4 korral: H 2 S, S, SO 2

5. Oksüdeerivate omadustega happeanioonid Mõni võrrandike. . . 4 Mg + 5 H 2 SO 4 (konts) 4 Mg. SO 4 + 1 H 2 S + 4 H 2 O Mg 0 – 2 e- Mg. II │∙ 4 SVI + 8 e- S-II │∙ 1 1 Cu + 4 HNO 3 (konts) 1 Cu(NO 3)2 + 2 NO 2 + 2 H 2 O Cu 0 – 2 e- Cu. II │∙ 1 NV + 1 e- NIV │∙ 2 1 Cu + 2 H 2 SO 4 (konts) 1 Cu. SO 4 + 1 SO 2 + 2 H 2 O Cu 0 – 2 e- Cu. II │∙ 1 SVI + 2 e- S-IV │∙ 1

5. Elektronbilansist pisuke veel 4 Al + 3 O 2 2 Al 2 O 3 Al 0 – 3 e- Al. III O 20 + 2∙ 2 e- 2 O-II │∙ 4 │∙ 3

6. MITTEMETALLID JA NENDE ÜHENDID PRAKTIKS • HAPNIK – vajalik põlemisprotsessides (põlemine on ühinemine hapnikuga), sh hingamisel • VESINIK – plahvatusohtlik gaas, väga kerge, tulevikukütus • OSOON – veepuhastusjaamades (väga tugev oksüdeerija atomaarne hapnik vabaneb) • ARGOON – elektripirnides intertse keskkonna tekitamiseks • LÄMMASTIK – väga stabiilne molekul (tugev kolmikside) • KLOOR – mürgine kollakasroheline gaas • BROOM – ainus vedel mittemetall, punakaspruun • VÄÄVEL – põletatakse nt kasvuhoonete ja keldriruumide desinfitseerimiseks, tekib SO 2 • JOOD – meditsiinis haavade desinfitseerimiseks. . .

6. MITTEMETALLID JA NENDE ÜHENDID PRAKTIKS • NO 2 – punakaspruun mürgine gaas • N 2 O – naerugaas • CO 2 – tekib täielikul põlemisel, ei põle ega soodusta põlemist, tulekustutites • CO – väga mürgine, tekib mittetäielikul põlemisel • H 2 O 2 – vesinikperoksiid, haavade puhastamiseks, hapniku saamiseks • SO 2 – mürgine teravalõhnaline gaas, happesademete põhjustaja • . . .

7. KESKKONNAST. . . • Happesademeid põhjustavad: – happelised oksiidid, peamiselt SO 2, NOx, . . . • Kasvuhooneefekti põhjustavad: – peamiselt CO 2, CH 4 • Mittemetalliühenditest põhjustavad veekogude kinnikasvamist (eutrofeerumist) lämmastikuühendeid sisaldavad väetised

ÜLESANDED • Määra reaktsioonides oksüdatsiooniastmed, kirjuta elektronvõrrandid ja tuvasta oksüdeerija, redutseerija. – 2 Al + 3 Br 2 2 Al. Br 3 – 2 Mg + O 2 2 Mg. O – 3 Ca + 2 H 3 PO 4 Ca 3(PO 4)2 + 3 H 2 – Fe 2 O 3 + 3 CO 2 Fe + 3 CO 2 – 2 KCl. O 3 2 KCl + 3 O 2

ÜLESANDED • Kirjuta elektronvõrrandid: – Kaltsiumi aatomi oksüdeerumine kaltsiumiooniks – Vesinikiooni redutseerumine vesiniku aatomiks – Hapniku aatomi redutseerumine oksiidiooniks – Raud(II)iooni oksüdeerumine raud(III)iooniks

ÜLESANDED • Millisel juhul lämmastik oksüdeerub, millisel juhul redutseerub, millisel juhul pole tegemist redoksreaktsiooniga? – NH 3 N 3– NO 3 - NO 2 – N 2 NO – NO 3 - NH 4+

ÜLESANDED • Kirjuta reaktsioonivõrrand, kus. . . – Hapnik oleks oksüdeerija – Broom oleks oksüdeerija – Lämmastik oleks redutseerija – Vesinik oleks oksüdeerija – Vesinik oleks redutseerija

ÜLESANDED • Kirjuta kolme süsinikühendi valem, kus. . . – Süsinik saab olla vaid redutseerija – Süsinik saab olla vaid oksüdeerija – Süsinik saab olla nii oksüdeerija kui redutseerija

ÜLESANDED • Kuidas võivad redoksreaktsioonides käituda järgmised osakesed? N 3 NO 3 Süsinik CH 4 -s Br. VII SO 32 Cl. PH 3 HNO 3 S Cl. III S 2 HNO 2

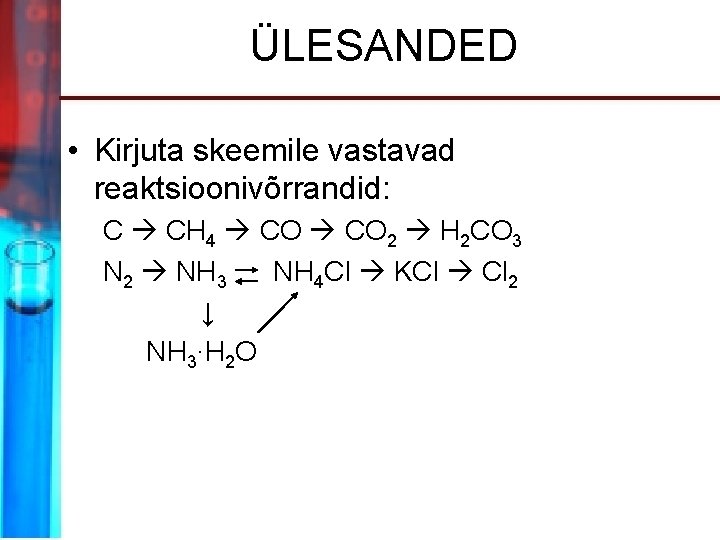
ÜLESANDED • Kirjuta skeemile vastavad reaktsioonivõrrandid: C CH 4 CO 2 H 2 CO 3 N 2 NH 3 NH 4 Cl KCl Cl 2 ↓ NH 3∙H 2 O