MATA KULIAH SKS PRASYARAT Kimia Organik Fisik KI




- Slides: 18


MATA KULIAH SKS PRASYARAT : Kimia Organik Fisik (KI 702) : 2 : - Perkuliahan ini diharapkan dapat meningkatkan pemahaman secara komprehensip terhadap kontrol dan mekanisme reaksi senyawa organik berdasarkan pada kajian struktur senyawa organik, sifat kimia dan fisika, termodinamika dan kinetika kimia. Lingkup perkuliahan meliputi struktur senyawa organik, hubungan struktur dan kereaktifan, sifat dan kedudukan keadaan transisi, zat antara reaktif, kontrol reaksi senyawa organik, asam basa (elektrofil dan nukleofil), gugus pergi, pengaruh gugus tetangga, dan mekanisme senyawa organik. Referensi utama: Issacs, N. S. (1987) Physical Organic Chemistry; Isaacs, N. S. , (1975). Reactive Intermediates in Organic Chemistry, Kitson, T. M. (1988) Organic Chemistry (A Guide to Common Themes)

RINCIAN MATERI TIAP PERTEMUAN Pertemuan 1 : Deskripsi dan silabus perkuliahan, cakupan dan overview perkuliahan Kimia Organik Fisik Pertemuan 2 : Efek Induksi Pertemuan 3 : Efek Resonansi Pertemuan 4 : Karbokation Pertemuan 5 : Karbanion Pertemuan 6 : Radikal Bebas Pertemuan 7 : Tes Unit I Pertemuan 8 : Kontrol Kinetik dan Kontrol Termodinamik Reaksi Senyawa Organik Pertemuan 9 : Penyerangan Eelektrofilik Pertemuan 10 : Penyerangan Nukleofilik Pertemuan 11 : Pembentukan Ikatan C-C Pertemuan 12 : Tes Unit II Pertemuan 13 : Reaksi asam/basa Pertemuan 14 : Gugus pergi dan pengaruh gugus tetangga Pertemuan 15 : Persamaan Hammet Pertemuan 16 : Ujian Akhir Semester (UAS)

Konsep-konsep yang diperlukan dalam mempelajari struktur molekul senyawa organik: 1. Elektronegativitas 2. Ikatan hidrogen 3. Gaya Van der Waals 4. Polarizabilitas 5. Gugus fungsi 6. Efek induksi 7. Resonansi 8. Hiperkonyugasi 9. Tautomeri 10. Regangan ruang

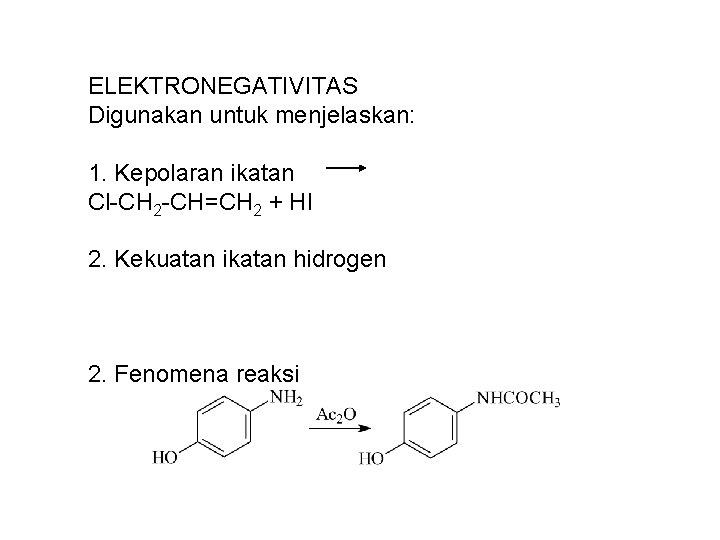
ELEKTRONEGATIVITAS Digunakan untuk menjelaskan: 1. Kepolaran ikatan Cl-CH 2 -CH=CH 2 + HI 2. Kekuatan ikatan hidrogen 2. Fenomena reaksi

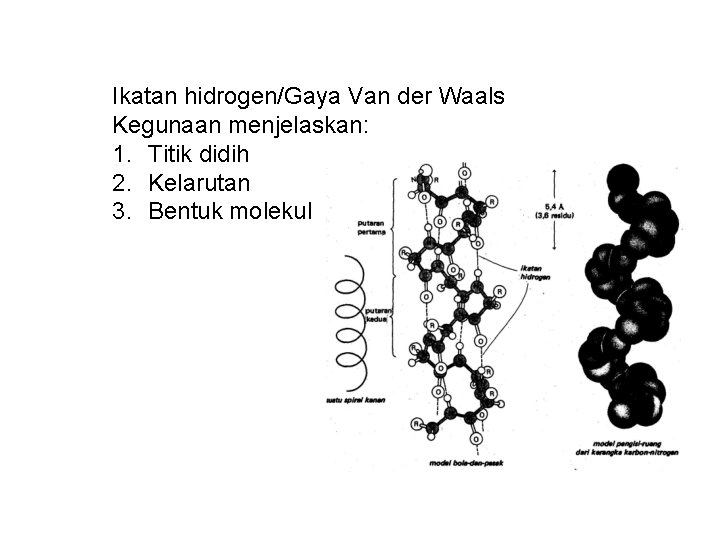
Ikatan hidrogen/Gaya Van der Waals Kegunaan menjelaskan: 1. Titik didih 2. Kelarutan 3. Bentuk molekul

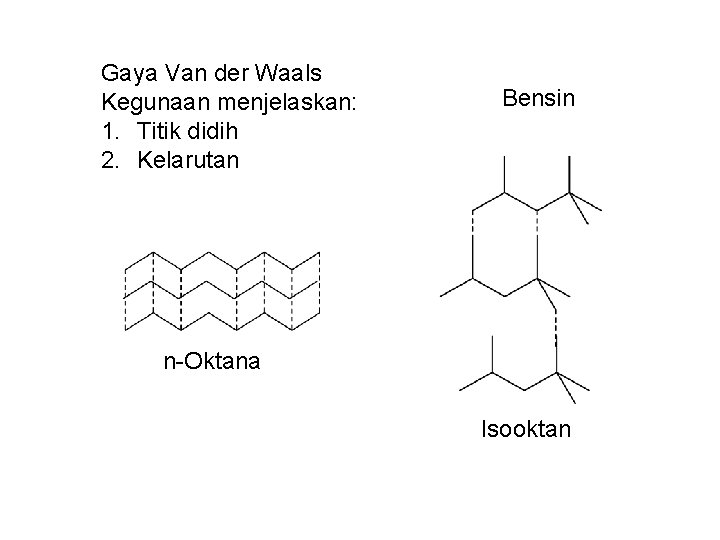
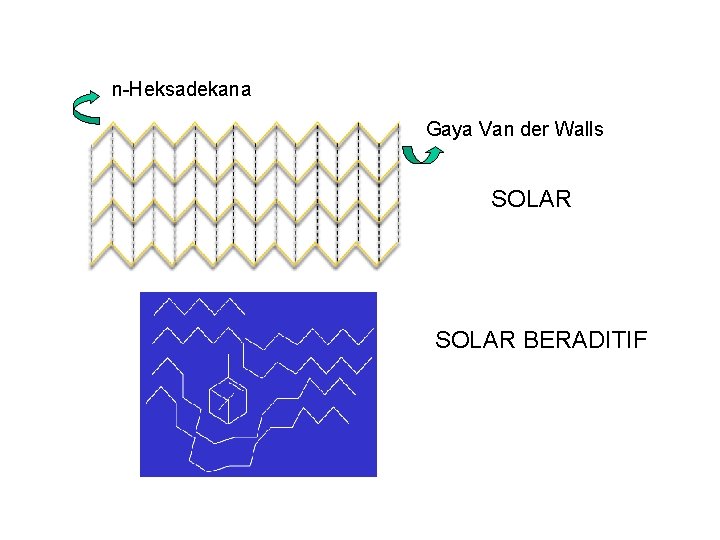
Gaya Van der Waals Kegunaan menjelaskan: 1. Titik didih 2. Kelarutan Bensin n-Oktana Isooktan

n-Heksadekana Gaya Van der Walls SOLAR BERADITIF

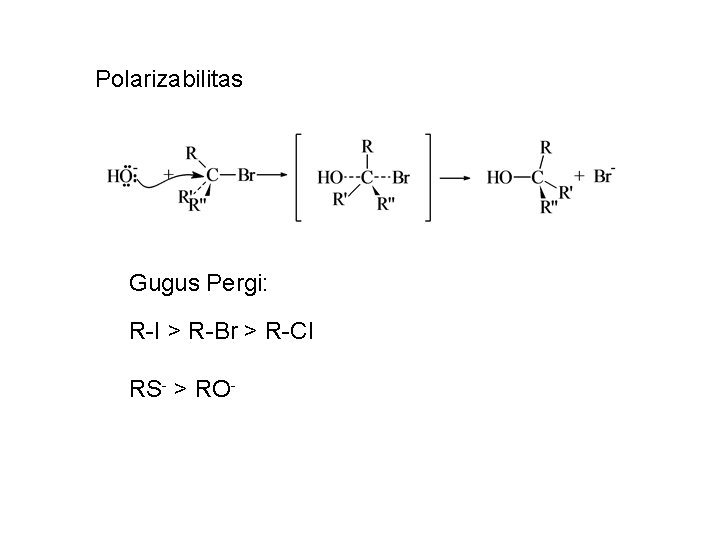
Polarizabilitas Gugus Pergi: R-I > R-Br > R-Cl RS- > RO-

Gugus Fungsi: Kedudukan kereaktifan kimia dalam suatu molekul Ciri: -Ikatan rangkap -Atom elektronegatif

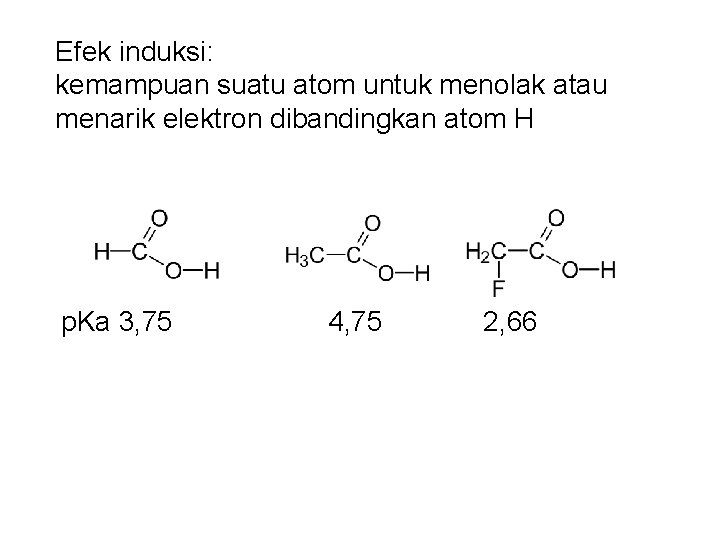
Efek induksi: kemampuan suatu atom untuk menolak atau menarik elektron dibandingkan atom H p. Ka 3, 75 4, 75 2, 66

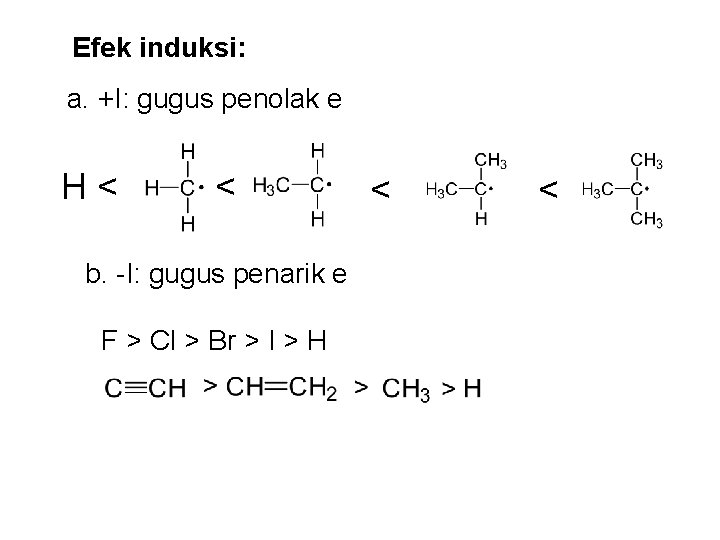
Efek induksi: a. +I: gugus penolak e H< < b. -I: gugus penarik e F > Cl > Br > I > H < <

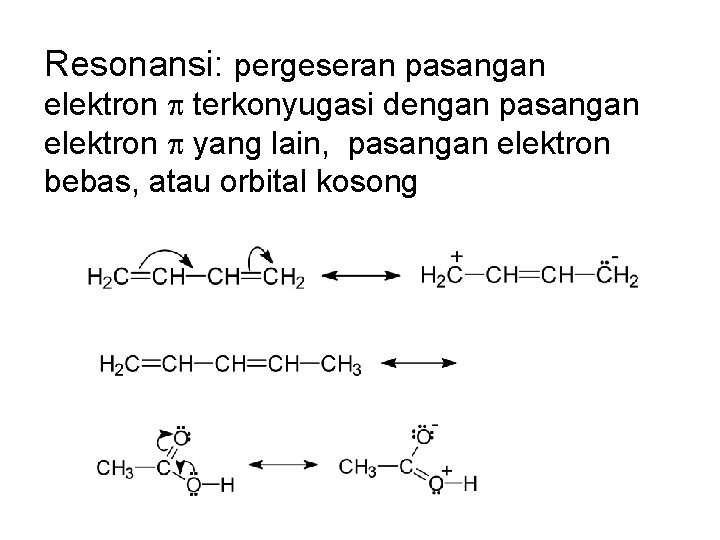
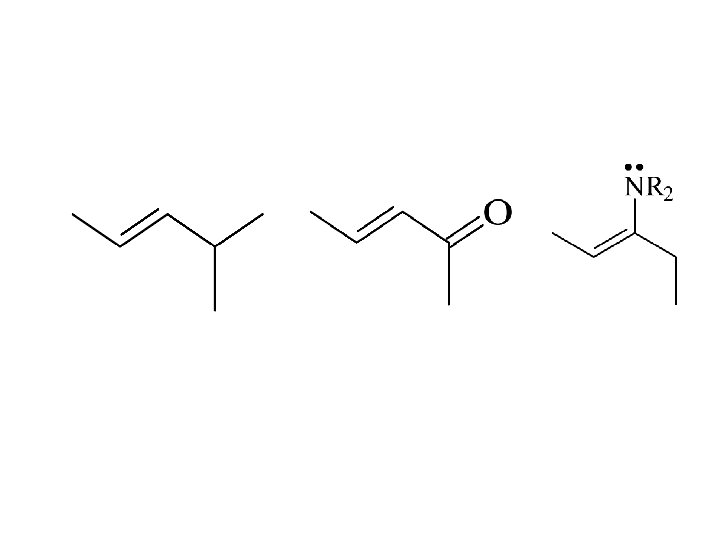
Resonansi: pergeseran pasangan elektron p terkonyugasi dengan pasangan elektron p yang lain, pasangan elektron bebas, atau orbital kosong


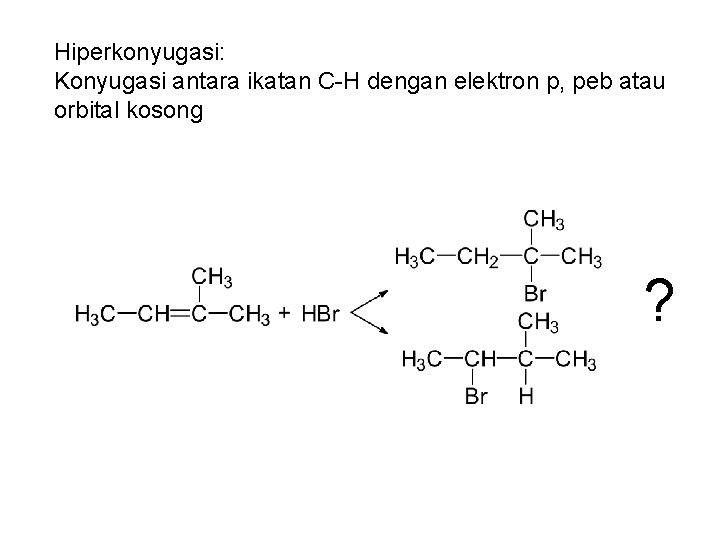
Hiperkonyugasi: Konyugasi antara ikatan C-H dengan elektron p, peb atau orbital kosong ?

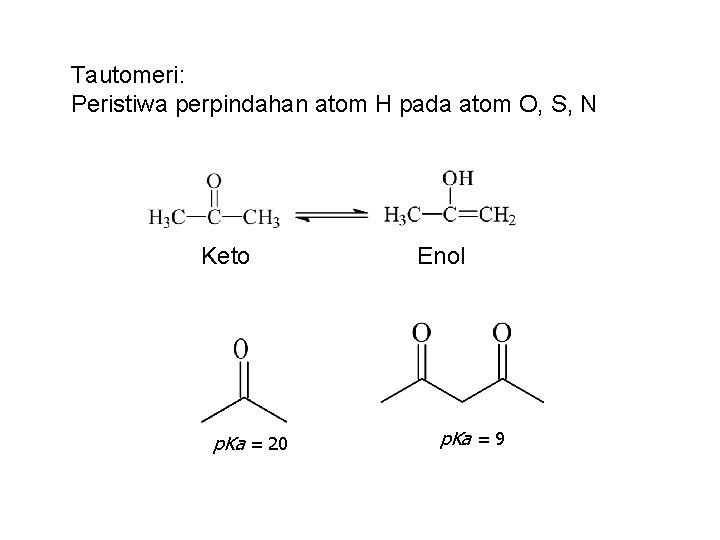
Tautomeri: Peristiwa perpindahan atom H pada atom O, S, N Keto p. Ka = 20 Enol p. Ka = 9

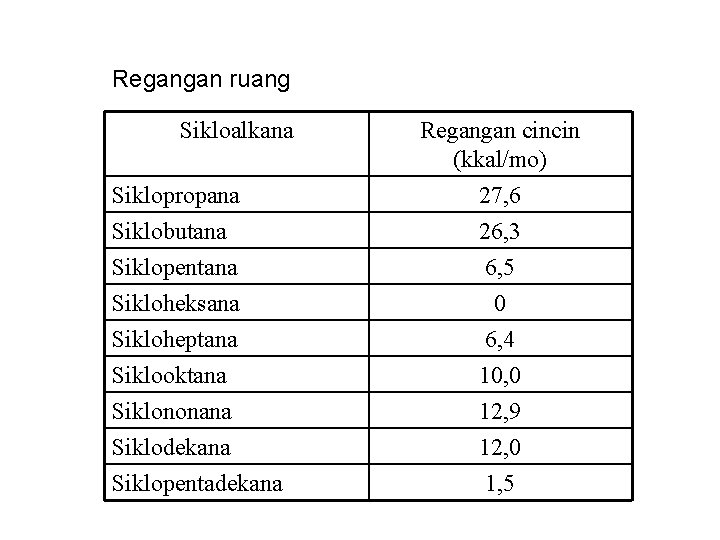
Regangan ruang Sikloalkana Siklopropana Siklobutana Siklopentana Sikloheksana Sikloheptana Siklooktana Siklononana Siklodekana Siklopentadekana Regangan cincin (kkal/mo) 27, 6 26, 3 6, 5 0 6, 4 10, 0 12, 9 12, 0 1, 5

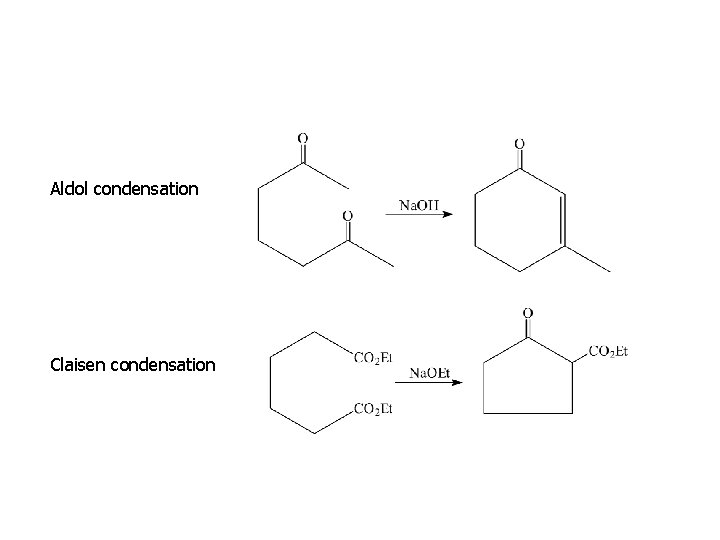
Aldol condensation Claisen condensation