Kyseliny Ing Jarmila Kirvejov Cle k se nau

























- Slides: 33

Kyseliny Ing. Jarmila Kirvejová

Cíle: • Žák se naučí : • Rozlišovat pojmy kyselý, zásaditý, neutrální. • Definovat pojem kyselina. • Vyjmenuje nejznámější kyseliny a jejich použití • Zapsat rovnici neutralizace

Kyseliny • jsou to sloučeniny, které ve vodných roztocích odštěpují kation vodíku H+ • kation H+ se spojí s molekulou vody a vzniká tzv. oxoniový kation H 3 O+

Co jsou to kyseliny? • Představ si, že si kousneš do citronu. Okamžitě se ti vybaví kyselá chuť. A v čem jsou nakládané kyselé okurky? Kyselina octová (ocet) se používá jak do okurek tak do zálivek na saláty. • A co superkyselé Bompary? Obsahují velké množství kyseliny citronové. • Minerálky, které chutnají příjemně kysele se podle toho nazývají kyselky.

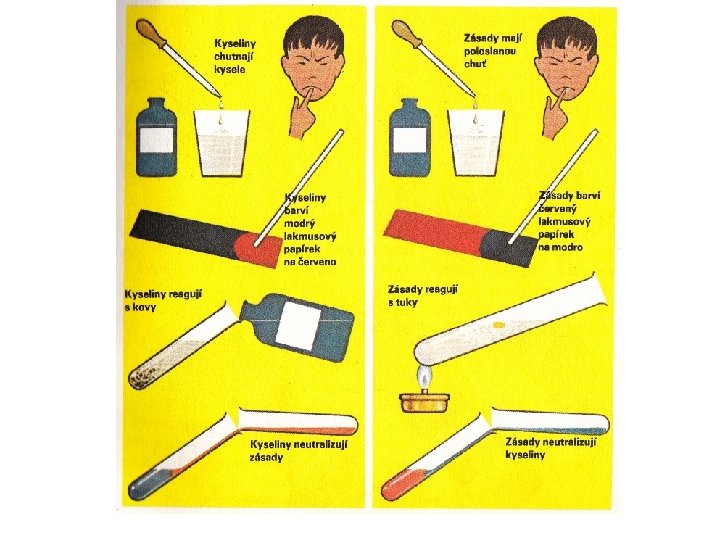
Co jsou to kyseliny? • Ne každá kyselina chutná kysele (nehledě k tomu, že ochutnávání chemikálií je životu nebezpečné). Ukážeme si vhodnější způsoby, jak zjistit, zda je látka kyselá. Protikladem kyselin jsou v chemii zásady.

Určování kyselosti a zásaditosti roztoků • K určování kyselosti nebo zásaditosti roztoků se používají tzv. indikátory (česky ukazatele). • Indikátory jsou látky, které mají jinou barvu v kyselém prostředí a jinou barvu v zásaditém prostředí. Prostředí, které není ani kyselé ani zásadité se nazývá neutrální.

Přírodní indikátor • Lakmus se získává z isladského lišejníku. Má fialovou barvu. V kyselém prostředí zčervená a v zásaditém prostředí zmodrá. Můžeme jej použít jako roztok (přikápneme ho do roztoku) nebo jako lakmusový papírek, který se do roztoku namočí.


p. H – vodíkový exponent • Vyjádření míry kyselosti (zásaditosti) roztoku – stupnice p. H • p. H = - log [H 3 O+] záporný logaritmus koncentrace vodíkových iontů • 0 --------- 7 ----------->14 • Kyselost zásaditost

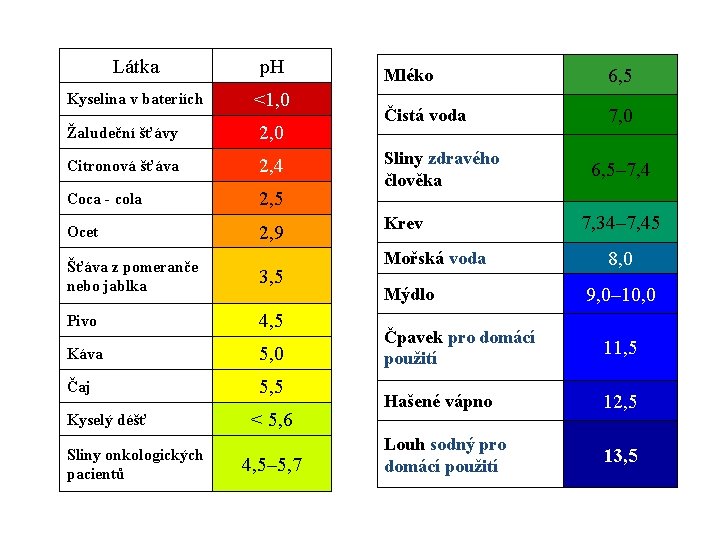
Látka p. H Kyselina v bateriích <1, 0 Žaludeční šťávy 2, 0 Citronová šťáva 2, 4 Coca - cola 2, 5 Ocet 2, 9 Šťáva z pomeranče nebo jablka 3, 5 Pivo 4, 5 Káva 5, 0 Čaj 5, 5 Kyselý déšť Sliny onkologických pacientů < 5, 6 4, 5– 5, 7 Mléko 6, 5 Čistá voda 7, 0 Sliny zdravého člověka Krev Mořská voda Mýdlo 6, 5– 7, 4 7, 34– 7, 45 8, 0 9, 0– 10, 0 Čpavek pro domácí použití 11, 5 Hašené vápno 12, 5 Louh sodný pro domácí použití 13, 5

Rozdělení kyselin 1) Bezkyslíkaté kyseliny HCl HBr 2) Kyslíkaté kyseliny H 2 SO 4 HNO 3

Bezkyslíkaté kyseliny • dvouprvkové sloučeniny, které vždy začínají písmenem H (vodík) • prvek na druhém místě dává kyselině název HCl HBr kyselina chlorovodíková kyselina bromovodíková

Bezkyslíkaté kyseliny • molekula je složená z kyselinotvorného prvku a vodíku • halogenvodíkové kyseliny – HF, HCl, HBr, HI • kys. sulfanová (sirovodíková) – H 2 S • kys. kyanovodíková -HCN

Kyslíkaté kyseliny • tříprvkové sloučeniny • na začátku vzorce je vždy H (vodík), na konci O (kyslík). Uprostřed je značka prvku, který dává kyselině pojmenování H 2 SO 4 kyselina sírová H NO 3 kyselina dusičná

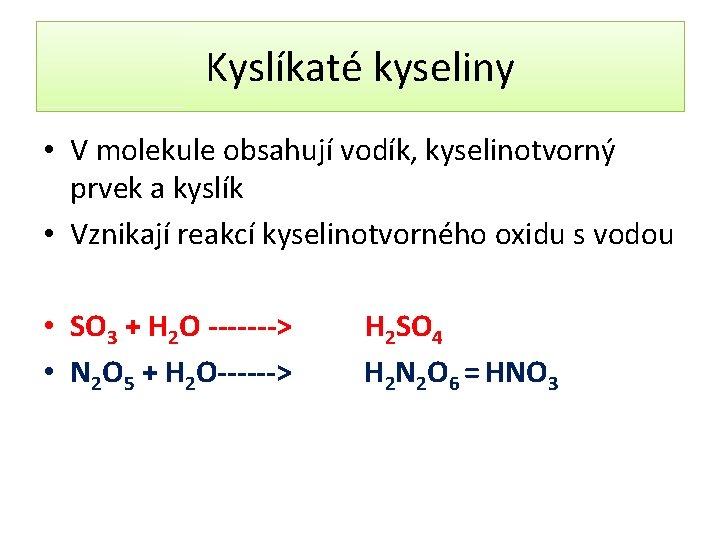
Kyslíkaté kyseliny • V molekule obsahují vodík, kyselinotvorný prvek a kyslík • Vznikají reakcí kyselinotvorného oxidu s vodou • SO 3 + H 2 O -------> • N 2 O 5 + H 2 O------> H 2 SO 4 H 2 N 2 O 6 = HNO 3

Kyselina chlorovodíková HCl kyselina solná • bezbarvá, těkavá kapalina, max. 37%; technická • zbarvena do žluta příměsmi Fe. Cl 3 • 0, 3% obsažena v žaludeční šťávě, kde se podílí na štěpení bílkovin použití: - čištění kovů před letováním - výroba plastů, barviv - v koželužském a potravinářském průmyslu

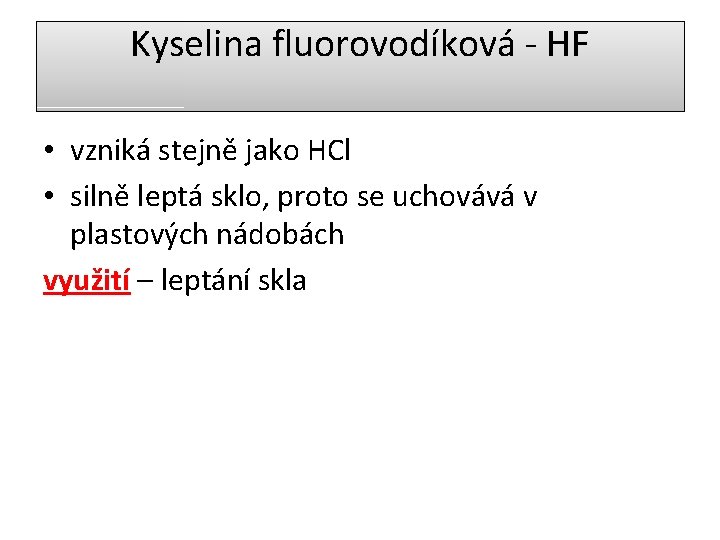
Kyselina fluorovodíková - HF • vzniká stejně jako HCl • silně leptá sklo, proto se uchovává v plastových nádobách využití – leptání skla

Další bezkyslíkaté kyseliny Sirovodíková – sulfanová H 2 S • rozpuštěním sirovodíku v H 2 O Kyanovodíková - HCN • rozpuštěním kyanovodíku v H 2 O • prudce jedovatá • její sloučenina KCN - cyankáli

Kyselina dusičná HNO 3 • bezbarvá kapalina, nestálá na světle (žloutne) • silná žíravina, max. 65% • použití: hnojiva, výbušniny, barviva • dráždí dýchací cesty • soli - dusičnany Použití - výroba barviv - výroba výbušnin - dusíkatá průmyslová hnojiva

Kyselina sírová (H 2 SO 4) • bezbarvá olejovitá kapalina • soli - sírany Použití - výroba chemikálií - průmyslová hnojiva - plasty, barviva, léčiva - výbušniny - čištění ropných produktů - úprava rud

Dehydratační účinky kyseliny sírové • Koncentrovaná kyselina sírová má schopnost odebírat látkám vodu. Všechny organické látky obsahují uhlík. Pokud organické látce odebereme vodu, zčerná (uhlík se vyloučí).

Dehydratační účinky kyseliny sírové

Kyselina fosforečná (H 3 PO 4) • soli - fosforečnany Použití - výroba průmyslových hnojiv - výroba nealkoholických nápojů (minerálky, cola…)

Další kyslíkaté kyseliny Kyselina uhličitá H 2 CO 3 – rozpouštěním CO 2 a H 2 O – snadno se rozkládá – součást perlivých nápojů Kyselina siřičitá H 2 SO 3 – rozpouštěním SO 2 a H 2 O – SO 2 spalováním fosilních paliv, ve vzduchu reaguje s vodou a vytváří kyselé deště

Kyselé deště

Ředění kyselin • Při ředění kyselin se uvolňuje velké množství tepla. • Platí pravidlo KDV – Kyselinu lijeme Do Vody (zamezíme prudkému ohřátí vody a možnému vystříknutí žíravé směsi).

Disociace (ionizace) kyselin Popisuje průběh děje, kdy kyselina ve vodném roztoku odštěpuje vodíkový iont H+. Ze zbytku molekuly se stane anion kyseliny. HCl ------- > H+ + Cl. H 2 SO 4 ----> 2 H 2+ SO 4 -2

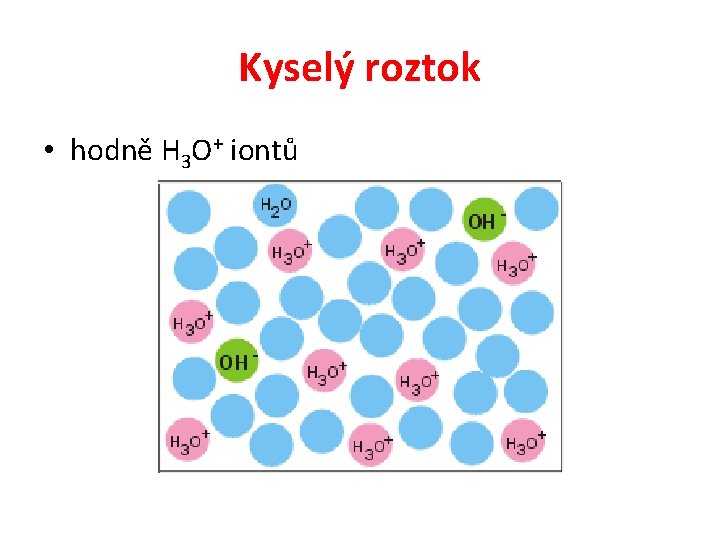
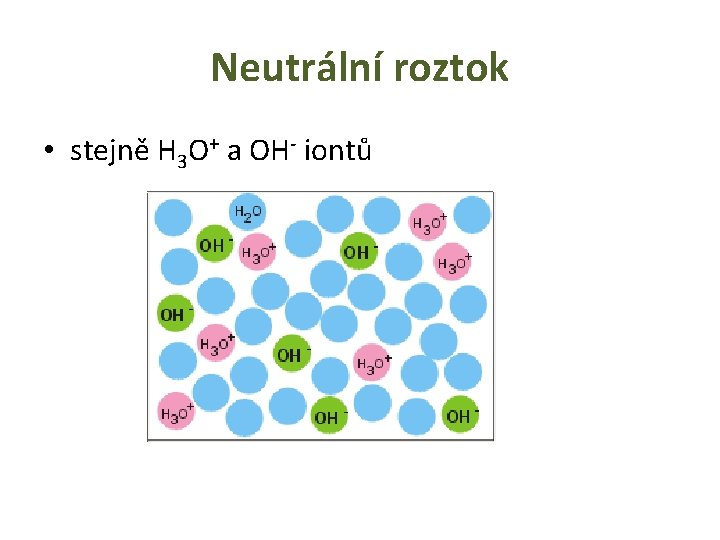
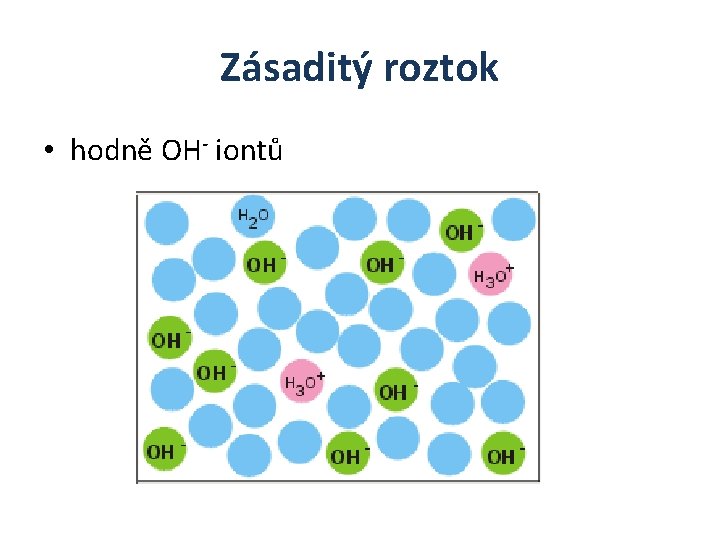
Kyselý, neutrální, zásaditý • Vodíkový (oxóniový) kation způsobuje kyselost roztoku. Čím víc je v roztoku vodíkových kationtů, tím je roztok kyselejší. Naopak anionty OH- způsobují zásaditost roztoku. Pokud je v roztoku více aniontů OHnež kationtů H 3 O+, je roztok zásaditý. Neutrální roztok obsahuje stejný počet H 3 O+ a OH- iontů.

Kyselý roztok • hodně H 3 O+ iontů

Neutrální roztok • stejně H 3 O+ a OH- iontů

Zásaditý roztok • hodně OH- iontů

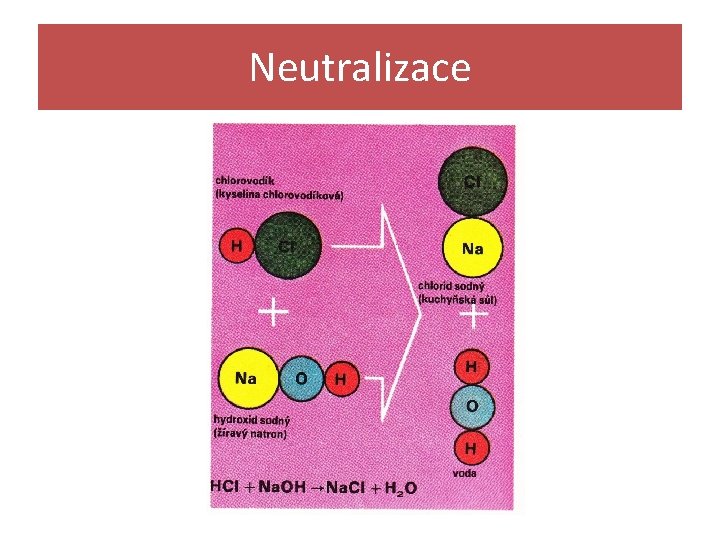
Neutralizace

Pravidla bezpečné práce s kyselinami • 1. Při práci s kyselinami používáme ochranné pomůcky. • 2. Při ředění kyselin se uvolňuje velké množství tepla, proto vždy opatrně přiléváme kyselinu do vody. • 3. Při potřísnění kyselinou postižené místo omýváme proudem tekoucí vody, popřípadě je neutralizujeme roztokem jedlé sody.