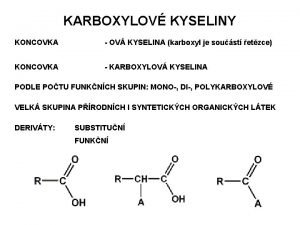
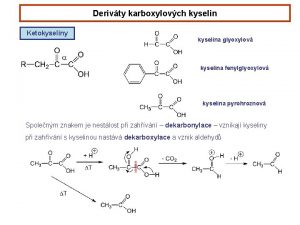
Kyseliny Anorganick bezkyslkat kyslkat Vlastnosti kyselin l l

Kyseliny Anorganické bezkyslíkaté, kyslíkaté

Vlastnosti kyselin l l jsou to sloučeniny, které ve vodných roztocích odštěpují kation vodíku H+ kation H+ se spojí s molekulou vody a vzniká tzv. oxoniový kation H 3 O+

p. H l l l je to hodnota vyjadřující koncentraci vodíkových iontů – oxoniových kationtů v roztoku pro kyseliny platí, že p. H < 7 k určování p. H slouží indikátory – látky, které mění barvu podle kyselosti prostředí

Otázky 1. 2. 3. 4. 5. 6. Proč nepoužíváme k důkazu chemických látek v laboratoři chuti? Některé kyseliny známe z přírody, např. kyselinu mravenčí, některé z domácnosti, např. kyselinu octovou, a z drogerie známe kyselinu solnou (chlorovodíkovou). Znáte ještě nějaké kyseliny? Zdůvodněte, proč pojem kation vodíku a proton mají stejný význam. Obsahuje pevná kyselina citrónová vodíkové kationty? Odpověď zdůvodni. Může být nějaký prvek kyselinou? Na lécích se většinou setkáváme s latinskými názvy chemických látek. Co asi znamená slovo acidum?

BEZKYSLÍKATÉ KYSELINY l l molekula je složená z kyselinotvorného prvku a vodíku halogenvodíkové kyseliny – HF, HCl, HBr, HI kys. sulfanová (sirovodíková) – H 2 S kys. kyanovodíková HCN

Kyselina chlorovodíková HCl ox. č. H = +I, ox. č. chloru = -I l * rozpuštěním chlorovodíku v H 2 O l ! koncentrovaná ( 37%) je silná žíravina, je těkavá a dráždí dýchací cesty, leptá pokožku ! l je obsažena v žaludeční šťávě ( 0, 3%) Použití: l k čištění klozetových mís, k čištění kovů, při pájení l k výrobě léčiv, barviv a plastů l
Kyselina fluorovodíková - HF l l l vzniká stejně jako HCl silně leptá sklo, proto se uchovává v plastových nádobách Využití – leptání skla

Další bezkyslíkaté kyseliny Sirovodíková – sulfanová H 2 S l * rozpuštěním sirovodíku v H 2 O Kyanovodíková - HCN l * rozpuštěním kyanovodíku v H 2 O l prudce jedovatá l její sloučenina KCN - cyankáli
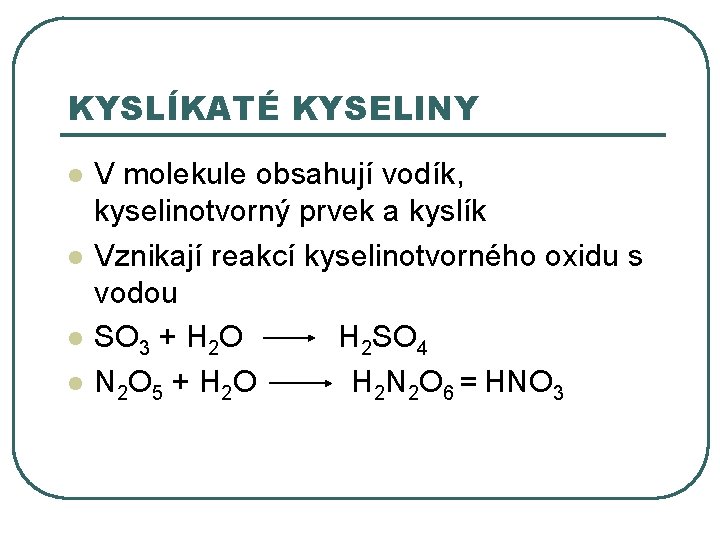
KYSLÍKATÉ KYSELINY l l V molekule obsahují vodík, kyselinotvorný prvek a kyslík Vznikají reakcí kyselinotvorného oxidu s vodou SO 3 + H 2 O H 2 SO 4 N 2 O 5 + H 2 O H 2 N 2 O 6 = HNO 3

Kyselina sírová l l koncentrovaná je hustá olejnatá kapalina má silné leptavé účinky z organických látek odebírá vodu a způsobuje jejich zuhelnatění využití • výroba barviv, léčiv, hnojiv, výbušnin • náplň olověných akumulátorů

Kyselina dusičná l l čirá bezbarvá tekutina rozkládá se na světle, vzniká směs oxidů dusíku (jedovaté) má silné leptavé účinky reaguje s většinou kovů (mimo Pt a Au)

Ředění kyselin l l Při ředění kyselin se uvolňuje velké množství tepla Platí pravidlo KDV – Kyselinu lijeme Do Vody (zamezíme prudkému ohřátí vody a možnému vystříknutí žíravé směsi)

Další kyslíkaté kyseliny l Kyselina uhličitá H 2 CO 3 l Kyselina siřičitá H 2 SO 3 • * rozpouštěním CO 2 a H 2 O • snadno se rozkládá • součást perlivých nápojů • * rozpouštěním SO 2 a H 2 O • SO 2 * spalováním fosilních paliv, ve vzduchu reaguje s vodou a vytváří kyselé deště

Další kyslíkaté kyseliny l kyselina chlorná HCl. O • * rozpouštěním Cl v H 2 O • snadno likviduje bakterie, ale sama se rychle • • rozpadá má bělící účinky využití – součást dezinfekčních prostředků (SAVO, …)

Další kyslíkaté kyseliny l Kyselina fosforečná H 3 PO 4 • součást Coca-Coly (E 338) • výroba hnojiva – superfosfát • výroba pracích prášků (obsahují fosforečnany • na změkčení vody a zlepšení účinku) Nebezpečí • P nahrazuje Ca v kostech • kyselina způsobuje zvýšenou kazivost zubů • fosforečnany jsou výživou pro řasy a sinice ve vodních nádržích

Lučavka královská l l směs koncentrované kyseliny dusičné (HNO 3) a kyseliny chlorovodíkové (HCl) v poměru 1: 3 rozpouští velmi odolné kovové prvky, jako je zlato, stříbro, platina, tantal, palladium, iridium, rhodium
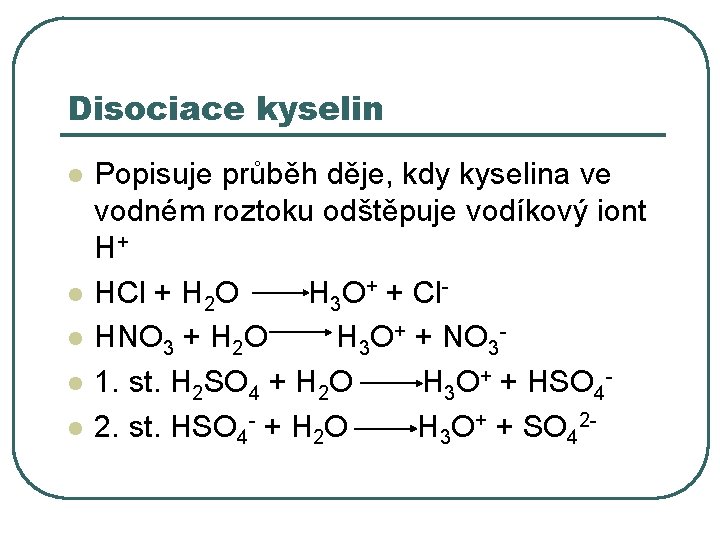
Disociace kyselin l l l Popisuje průběh děje, kdy kyselina ve vodném roztoku odštěpuje vodíkový iont H+ HCl + H 2 O H 3 O+ + Cl. HNO 3 + H 2 O H 3 O+ + NO 31. st. H 2 SO 4 + H 2 O H 3 O+ + HSO 42. st. HSO 4 - + H 2 O H 3 O+ + SO 42 -

Zdroje l l http: //www. mujweb. cz/www/cmelda/smrk y/obr_02. gif http: //cs. wikipedia. org
- Slides: 18