Kuantum Teorisi ve Atomlarn Elektronik Yaps Kaynak Fen













- Slides: 29

Kuantum Teorisi ve Atomların Elektronik Yapısı Kaynak: Fen ve Mühendislik Bilimleri için KİMYA Raymond CHANG 1

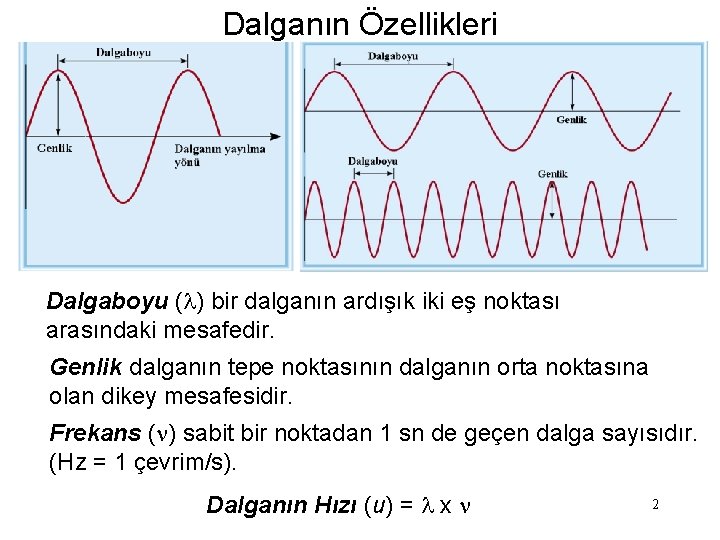
Dalganın Özellikleri Dalgaboyu (l) bir dalganın ardışık iki eş noktası arasındaki mesafedir. Genlik dalganın tepe noktasının dalganın orta noktasına olan dikey mesafesidir. Frekans (n) sabit bir noktadan 1 sn de geçen dalga sayısıdır. (Hz = 1 çevrim/s). Dalganın Hızı (u) = l x n 2

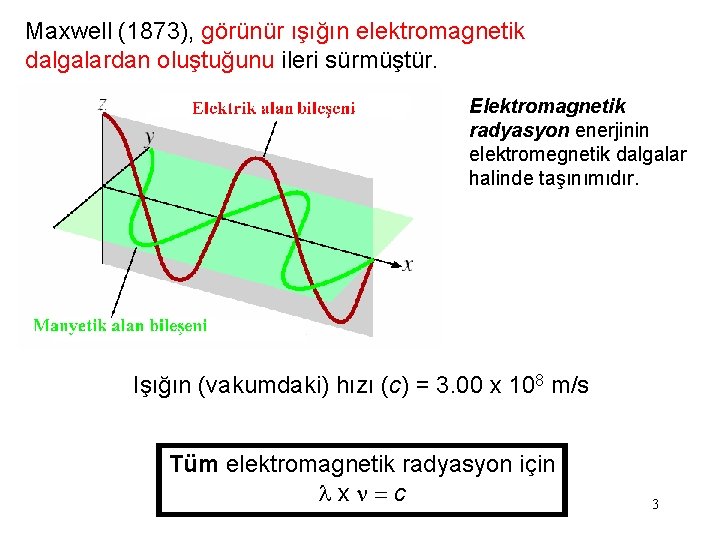
Maxwell (1873), görünür ışığın elektromagnetik dalgalardan oluştuğunu ileri sürmüştür. Elektromagnetik radyasyon enerjinin elektromegnetik dalgalar halinde taşınımıdır. Işığın (vakumdaki) hızı (c) = 3. 00 x 108 m/s Tüm elektromagnetik radyasyon için lxn=c 3

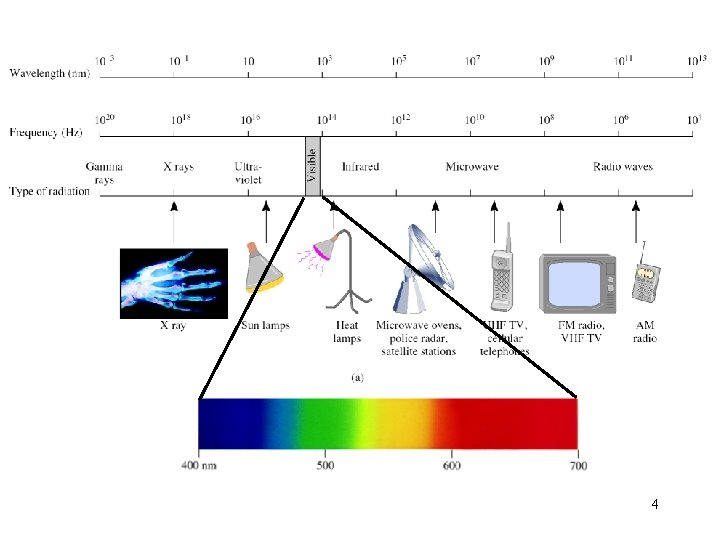
4

Bir fotonun frekansı 6. 0 x 104 Hz dir. Dalgaboyunu (λ) kaç nm dir. Bu frekans görünür bölgede midir ? lxn=c l = c/n l = 3. 00 x 108 m/s / 6. 0 x 104 Hz l = 5. 0 x 103 m l = 5. 0 x 1012 nm 5

Enerji (ışın) kesikli birimler halinde (kuantum) yayılır veya absorplanır. E=hxn Planck sabiti (h) h = 6. 63 x 10 -34 J • s 6

Bakır yüksek enerjili elektronlar ile bombardıman edildiğinde X ışınları yayılır. X ışınlarının dalgaboyu 0, 154 nm ise enerjiyi joule cinsinden hesaplayınız. E=hxn E=hxc/l E = 6. 63 x 10 -34 (J • s) x 3. 00 x 10 8 (m/s) / 0. 154 x 10 -9 (m) E = 1. 29 x 10 -15 J 7

Schrodinger Dalga Denklemi y kuantum sayıları denen 4 sayının bir fonksiyonudur. kuantum sayıları (n, l, ms) Baş kuantum sayısı n n = 1, 2, 3, 4, …. e- un çekirdeğe olan uzaklığını ifade eder. n=1 n=2 n=3 8

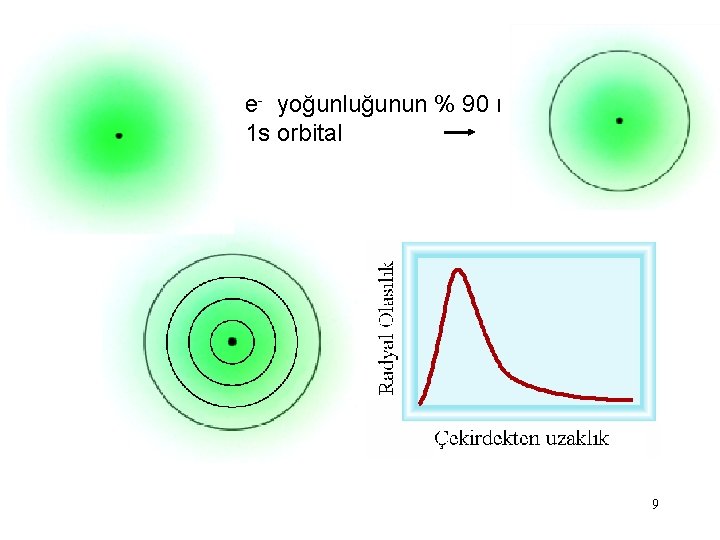
e- yoğunluğunun % 90 ı 1 s orbital 9

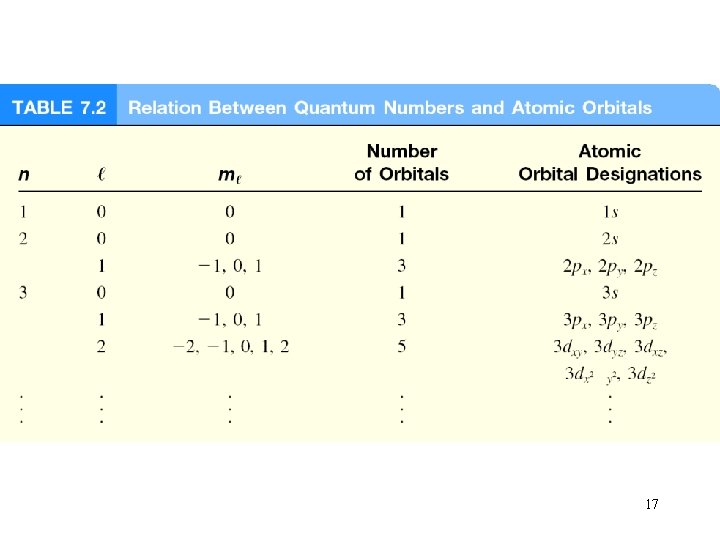
Schrodinger Dalga Denklemi kuantum sayıları: (n, l, ms) açısal momentum kuantum sayısı l Verilen bir n değeri için , l = 0, 1, 2, 3, … n-1 n = 1, l = 0 n = 2, l = 0 veya 1 n = 3, l = 0, 1, veya 2 l=0 l=1 l=2 l=3 s orbital p orbital d orbital f orbital e- nun kapladığı “hacmin” şeklini gösterir 10

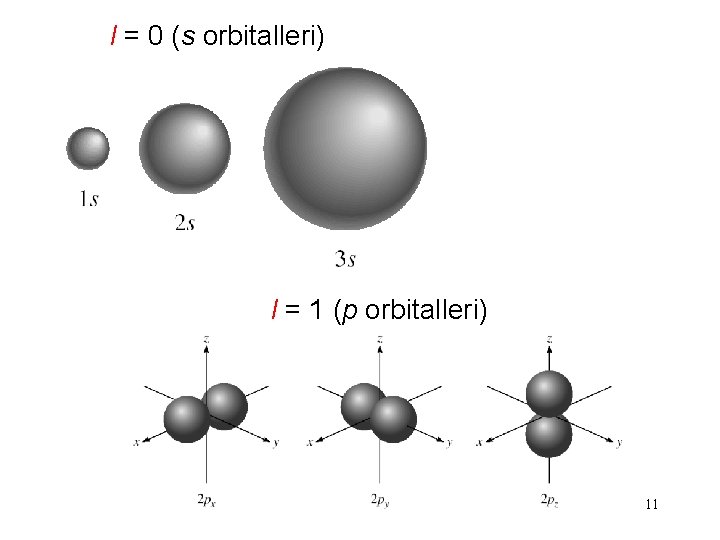
l = 0 (s orbitalleri) l = 1 (p orbitalleri) 11

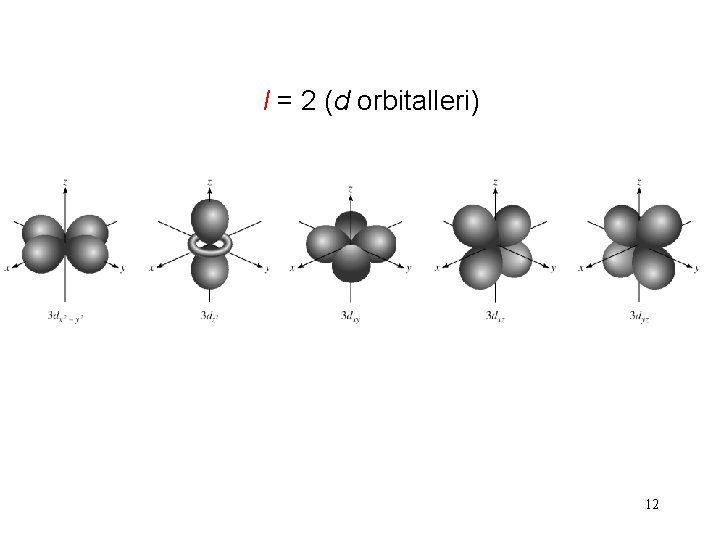
l = 2 (d orbitalleri) 12

Schrodinger Dalga Denklemi kuantum sayıları: (n, l, ms) Manyetik kuantum sayısı ml l nin verilen bir değeri için ml = -l, …. , 0, …. +l Eğer l = 1 (p orbital) ise , ml = -1, 0, veya 1 Eğer l = 2 (d orbital), ml = -2, -1, 0, 1, veya 2 Orbitallerin uzaydaki yönelimi 13

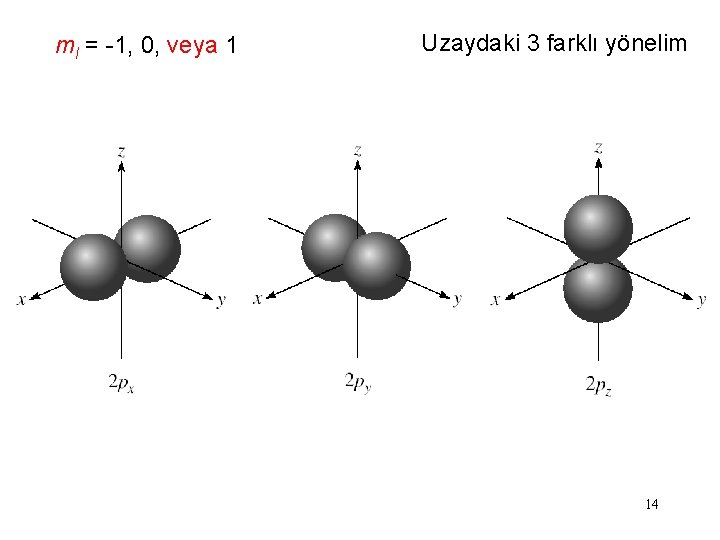
ml = -1, 0, veya 1 Uzaydaki 3 farklı yönelim 14

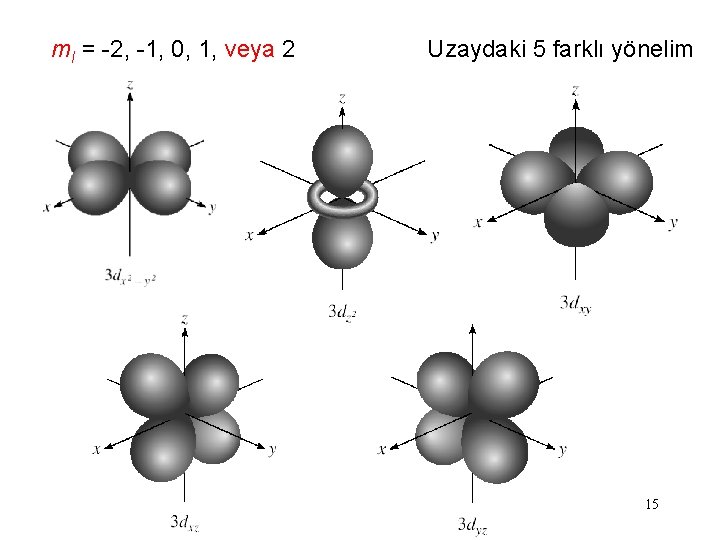
ml = -2, -1, 0, 1, veya 2 Uzaydaki 5 farklı yönelim 15

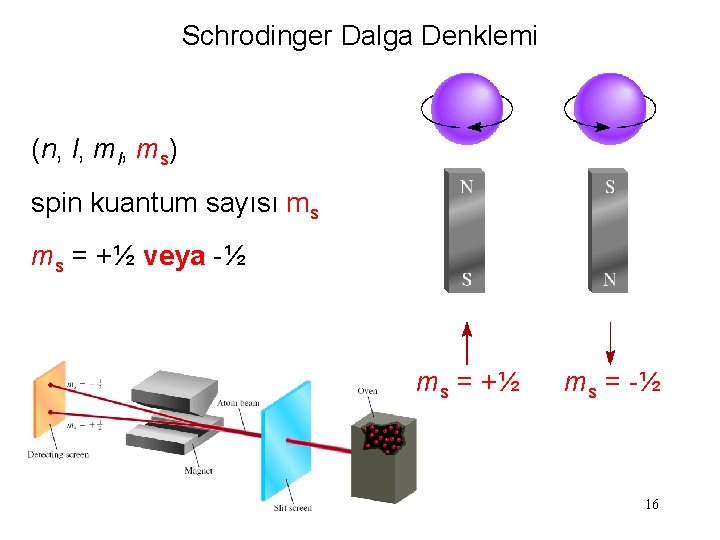
Schrodinger Dalga Denklemi (n, l, ms) spin kuantum sayısı ms ms = +½ veya -½ ms = +½ ms = -½ 16

17

Schrodinger Dalga Denklemi Kuantum sayıları: (n, l, ms) Yörünge – elektronlar aynı n değerini alır. Alt yörünge – aynı n ve l değerini alan elektronlar bulunur. Orbital – elektronlar aynı n, l, ve ml değerlerini, alır. Bir orbital kaç elektron barındırır ? Eğer n, l, ve ml aynı ise o zaman ms = ½ or - ½ y = (n, l, ml, ½) veya y = (n, l, ml, -½) Bir orbital 2 elektron bulundurur. 18

Schrodinger Dalga Denklemi kuantum sayıları: (n, l, ms) Atomdaki elektronun bulunabileceği enerji seviyeleri onun kendisine özgü Dalga fonksiyonu (Ψ) ile tanımlanır Pauli dışarlama prensibi – bir atomdaki iki elektron aynı dört kuantum sayısını alamaz Wolfgang Ernst Pauli 19

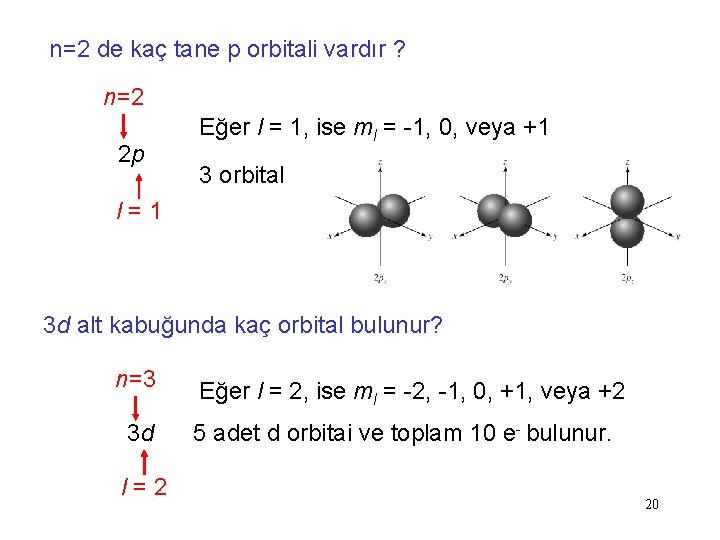
n=2 de kaç tane p orbitali vardır ? n=2 2 p Eğer l = 1, ise ml = -1, 0, veya +1 3 orbital l=1 3 d alt kabuğunda kaç orbital bulunur? n=3 3 d l=2 Eğer l = 2, ise ml = -2, -1, 0, +1, veya +2 5 adet d orbitai ve toplam 10 e- bulunur. 20

Elektronların bir alt kabuktaki en kararlı dağılımı en fazla paralel spinin olduğu haldir (Hund Kuralı). 21

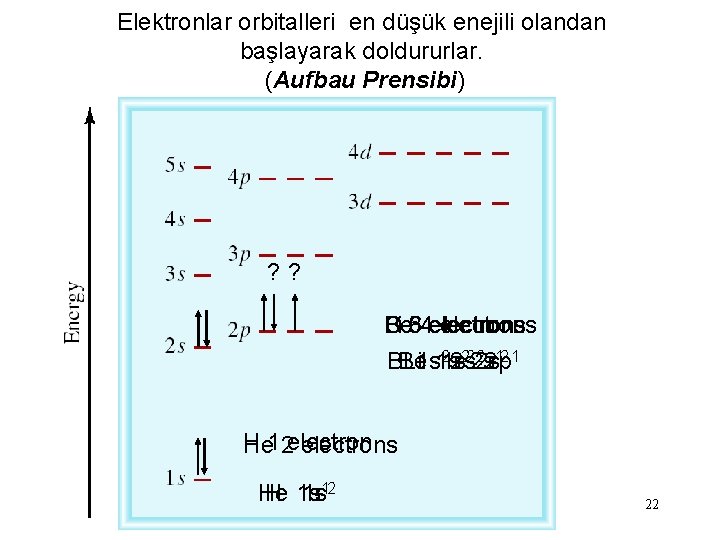
Elektronlar orbitalleri en düşük enejili olandan başlayarak doldururlar. (Aufbau Prensibi) ? ? Be Li B 5 C 3 64 electrons 22 s 22 p 12 1 BBe Li 1 s 1 s 1 s 2 s H He 12 electrons He H 1 s 1 s 12 22

Çok elektronlu bir atomda orbitallerin doldurulması 1 s < 2 p < 3 s < 3 p < 4 s < 3 d < 4 p < 5 s < 4 d < 5 p < 6 s 23

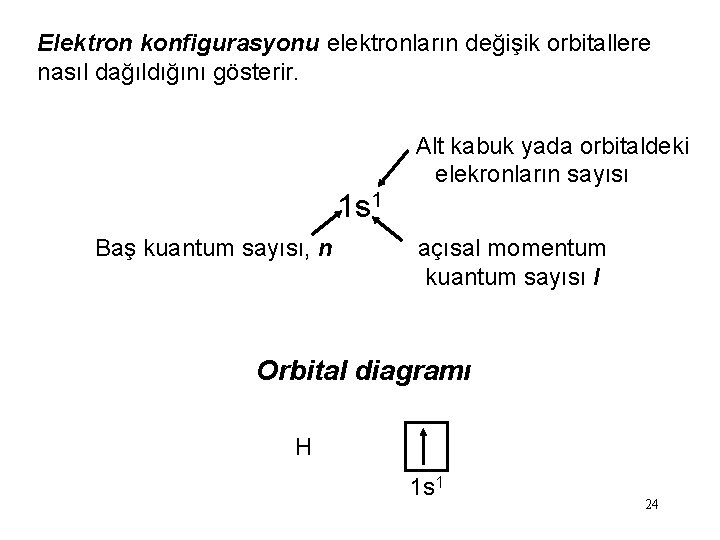
Elektron konfigurasyonu elektronların değişik orbitallere nasıl dağıldığını gösterir. Alt kabuk yada orbitaldeki elekronların sayısı 1 s 1 Baş kuantum sayısı, n açısal momentum kuantum sayısı l Orbital diagramı H 1 s 1 24

Mg un elektron konfigürasyonu nedir ? 12 Mg 1 s < 2 p < 3 s < 3 p < 4 s 1 s 22 p 63 s 2 2 + 6 + 2 = 12 electron Kısaca [Ne]3 s 2 [Ne] 1 s 22 p 6 Cl un en dış elektronunun muhtemel 4 kuantum sayısını yazınız. 17 Cl 1 s < 2 p < 3 s < 3 p < 4 s 1 s 22 p 63 s 23 p 5 2 + 6 + 2 + 5 = 17 elektron En dış (son) elektron 3 p orbitalinde bulunur. n=3 l=1 ml = -1, 0, or +1 ms = ½ or -½ 25

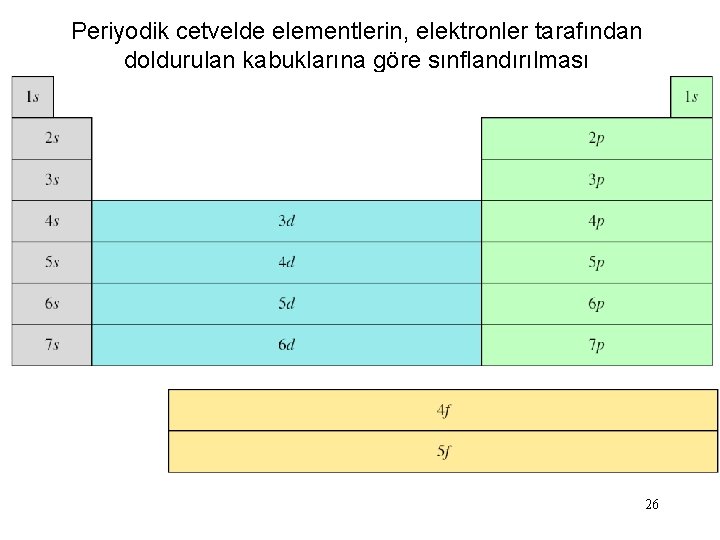
Periyodik cetvelde elementlerin, elektronler tarafından doldurulan kabuklarına göre sınflandırılması 26

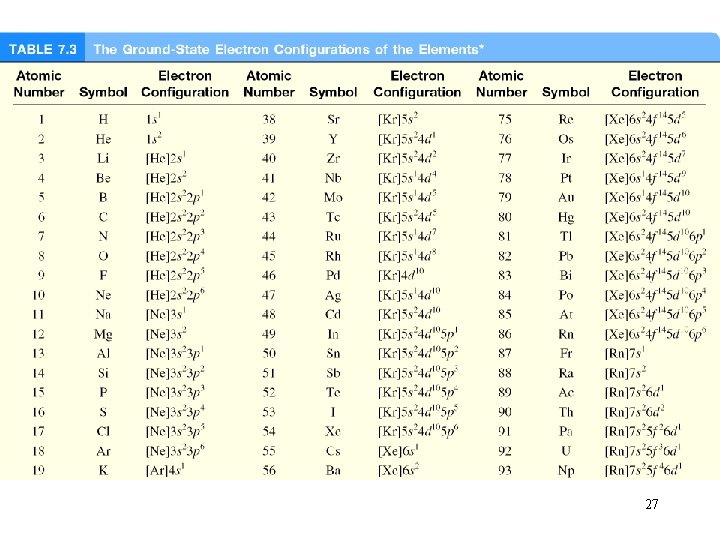
27

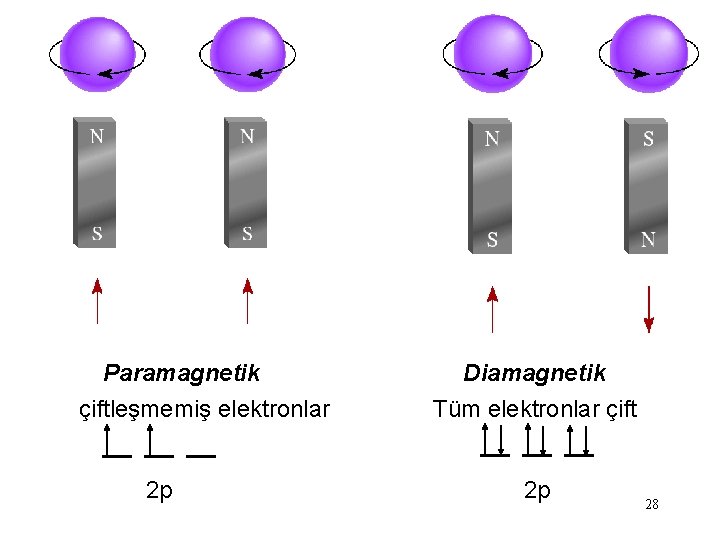
Paramagnetik çiftleşmemiş elektronlar 2 p Diamagnetik Tüm elektronlar çift 2 p 28
