2 Bilangan kuantum azimut disebut juga bilangan kuantum

2. Bilangan kuantum azimut disebut juga bilangan kuantum momentum sudut. Bilangan kuantum ini menyatakan besarnya bagian energi elektron karena mengelilingi inti atom (momentum sudut). Bilangan kuantum ini diberi lambang l (bilangan bulat) dengan harga dari 0 – (n – 1). 0 l (n-1)

Dlm. struktur elektron, bilangan kuantum azimut ini menyatakan subkulit atau orbital elektron. Orbital-orbital tsb. diberi nama sesuai dg. harga l: l = 0 : orbital s l = 1 : orbital p l = 2 : orbital d l = 3 : orbital f


Nama-nama s, p, d dan f diambil dari sifat penampakan garis spektrum, yaitu : sharp (tajam) p : principal (utama) d : diffuse (baur) f : fundamental (dasar)

3. Bilangan kuantum magnetik Otto Stern dan W. Gerlach: Percobaan pengaruh medan magnet thd. spektra Bila suatu sumber spektra diletakkan dalam medan magnet yang kuat, dan spektra yang dihasilkan diamati pada arah tegaklurus arah medan magnet, ternyata bahwa garis-garis spektrum yang tanpa medan magnet terlihat sebagai garis tunggal, terurai menjadi beberapa macam garis. Percobaan ini dikenal sebagai percobaan Stern-Gerlach.

Maka diperkenalkanlah: bilangan kuantum magnetik (m). Harga m : - l sampai dg. + l: -l m + l Contoh: l = 0 l = 1 l = 2 l = 3 m = 0 m = -1, 0, +1 m = -2, -1, 0, +1, + 2 m = -3, -2, -1, 0, +1, + 2, + 3 Bilangan kuantum m menentukan jumlah maksimum elektron dlm. suatu orbital. Satu harga m menunjukkan satu lintasan elektron.

4. Bilangan kuantum spin George E. Uhlenbeck dan Samuel A. Goudsmit: Elektron berputar pada porosnya (melakukan spin). Pengamatan spektra yang lebih teliti: Pasangan garis spektra yang berdekatan: Dua garis (doublet) Tiga garis (triplet) (multiplet) Diperkenalkan bilangan kuantum spin. Kecepatan spin: sama, Orientasinya thd. arah tertentu: berlawanan Harga bilangan kuantum spin: +1/2 (paralel) dan -1/2 (antiparalel).
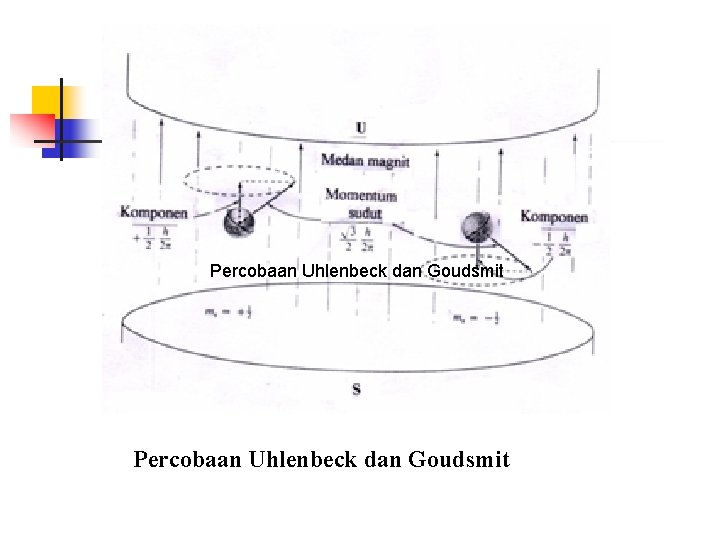
Percobaan Uhlenbeck dan Goudsmit

5. KEBERADAAN ELEKTRON DALAM ATOM 5. 1. Energi elektron dan bilangan kuantumnya Setiap elektron dalam atom berada dalam keadaan energi tertentu, yg. ditunjukkan oleh keempat bilangan kuantumnya: 1. Bilangan kuantum utama (kulit elektron) 2. Bilangan kuantum azimut (orbital elektron) 3. Bilangan kuantum magnetik (jumlah orbital tiap jenisnya) 4. Bilangan kuantum spin (jumlah maksimum elektron dalam satu orbital)

5. 2. Azas Larangan Pauli Wolfgang Pauli: Dalam sebuah atom tidak ada dua buah elektron yang mempunyai keempat bilangan kuantum yang sama. Pernyataan ini dikenal sebagai: Azas Larangan Pauli.
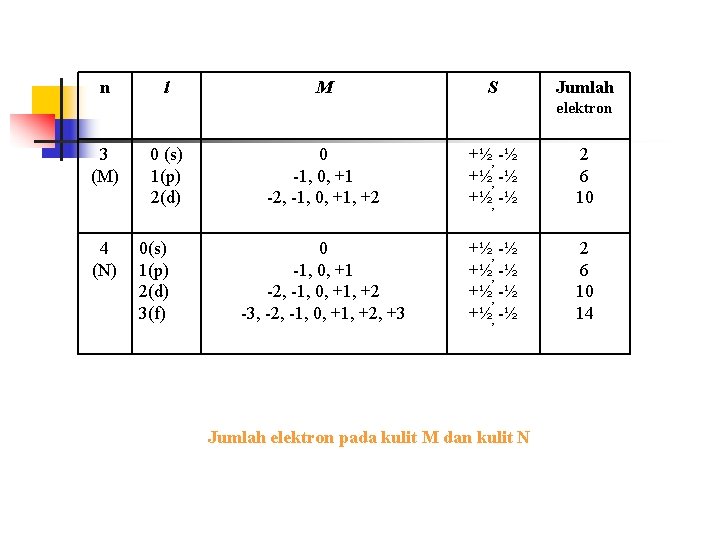
n l M S Jumlah elektron 3 (M) 4 (N) 0 (s) 1(p) 2(d) 0(s) 1(p) 2(d) 3(f) 0 -1, 0, +1 -2, -1, 0, +1, +2 +½, -½ 2 6 10 0 -1, 0, +1 -2, -1, 0, +1, +2 -3, -2, -1, 0, +1, +2, +3 +½, -½ 2 6 10 14 Jumlah elektron pada kulit M dan kulit N

Bentuk-bentuk orbital Bohr: bentuk lintasan elektron mengelilingi atom adalah lingkaran, seperti planet tatasurya mengelilingi matahari. Arnold Sommerfeld: Juga ada bentuk ellips dari lintasan elektron Bentuk lintasan elektron menurut Bohr-Sommerfeld
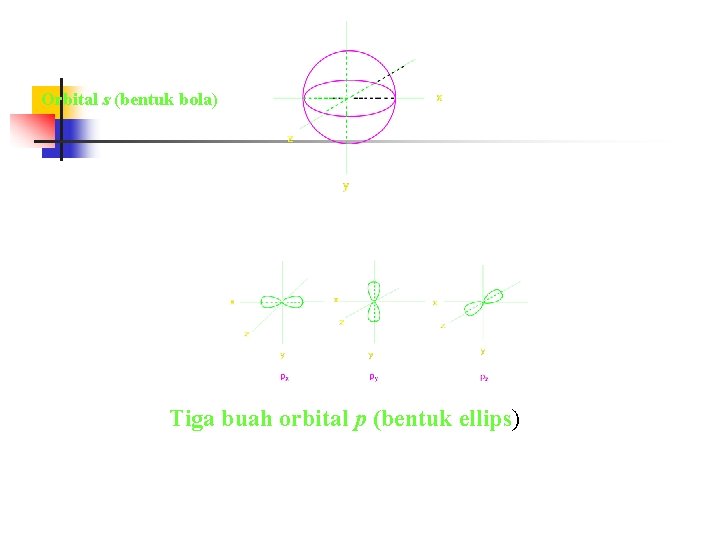
Orbital s (bentuk bola) Tiga buah orbital p (bentuk ellips)

n Gambar 3. 21. Lima buah orbital d
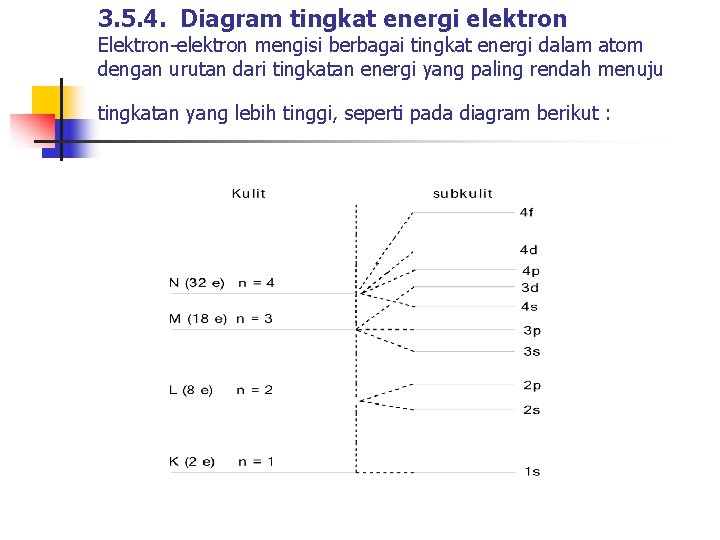
3. 5. 4. Diagram tingkat energi elektron Elektron-elektron mengisi berbagai tingkat energi dalam atom dengan urutan dari tingkatan energi yang paling rendah menuju tingkatan yang lebih tinggi, seperti pada diagram berikut :

n n n n 3. 5. 5. Urutan pengisian elektron Prinsip Aufbau Pengisian elektron seperti yang digambarkan pada diagram tingkat energi di atas secara lengkapnya diuraikan pada gambar 3. 23. Urutan pengisian elektron tersebut dikenal sebagai Prinsip Aufbau. Terdapat pengecualian dalam urutan pengisian elektron tersebut, yaitu sebelum subkulit 4 f diisi, subkulit 5 d diisi satu elektron lebih dahulu, sembilan elektron 5 d lainnya akan mengisi subkulit 5 d setelah subkulit 4 f terisi penuh dengan 14 elektron. Demikian juga halnya sebelum subkulit 5 f diisi, subkulit 6 d diisi satu elektron lebih dahulu, sembilan elektron 6 d lainnya akan mengisi subkulit 5 d setelah subkulit 5 f terisi penuh dengan 14 elektron. Aturan Hund Pada urutan pengisian elektron, dikenal Aturan Hund, yaitu : Bila dalam suatu subkulit masih ada orbital yang kosong, maka orbital lain dalam subkulit tersebut tidak akan terisi penuh (dengan elektron yang berpasangan).

Gambar 3. 23. Urutan pengisian elektron menurut prisip Aufbau

Contoh aturan Hund : Bila pada subkulit 2 p terdapat orbital p yang kosong, maka orbital 2 p yang lain tidak dapat berisi penuh. Berikut ini adalah tabel pengisian elektron dari hidrogen sampai dengan neon :

Konfigurasi elektron adalah suatu rumus yang menggambarkan elektron-elektron dalam orbital-orbital suatu atom. Dalam konfigurasi tersebut, jumlah elektron dalam suatu subkulit disebutkan. Contoh : n n n n n H He Li Be B C N O F Ne : : : : : 1 s 1 (dibaca : “satu es satu”) 1 s 2 2 s 1 1 s 2 2 s 2 2 p 1 1 s 2 2 p 2 1 s 2 2 p 3 1 s 2 2 p 4 1 s 2 2 p 5 1 s 2 2 p 6
- Slides: 19