Gradniki snovi Pripravila Tatjana Posavec Biotehniki izobraevalni center

Gradniki snovi Pripravila: Tatjana Posavec Biotehniški izobraževalni center Ljubljana Gimnazija in veterinarska šola Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

Kaj je atom? Atomos → grško nedeljiv Atom je najmanjši delec s kemijskimi lastnostmi določenega elementa, ki se pri kemijski reakciji ne spreminja. S prostim očesom atomov ne vidimo, a so zelo pomembni, ker so osnovni gradniki vse žive in nežive narave. Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

Zgradba atoma Atom je zgrajen iz jedra in elektronske ovojnice. Jedro je približno 100. 000 krat manjše od atoma, vendar je v njem skoraj vsa masa atoma. Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

Elektroni, protoni in nevtroni V jedru so protoni, ki imajo pozitiven naboj (p+) in nevtroni, ki so brez naboja (n°). V elektronski ovojnici pa se nahajajo elektroni, ki imajo negativen naboj (e-). Vsi delci atoma so zelo lahki, protoni in nevtroni imajo približno enako maso, masa elektrona pa je 1836 -krat manjša od mase protona. Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

Naboj atoma Ker je v atomu enako število elektronov in protonov, je atom nevtralen delec. Primer: atom ogljika Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

Vrstno in masno število V periodnem sistemu so atomi razporejeni glede na vrstno število → pove število protonov v jedru in elektronov v elektronski ovojnici. Masno število = število p+ + število n° Masno število je zaokrožena relativna atomska masa elementa. Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

Primer: atom natrija Simbol atoma natrija je Na. 22, 99 → relativna atomska masa Na 11→ vrstno število masno število Na = 23 → p+= 11 e- = 11 n° = 12 Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

Atom zlata Reši nalogo: 196, 97 → ? Au 79 → ? Masno število = ? Vrstno število = ? Relativna atomska masa = ? Število protonov = ? Število elektronov = ? Število nevtronov = ? Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

Izotopi so atomi istega elementa, ki imajo enako vrstno število, razlikujejo pa se v masnem številu → zato imajo različno število nevtronov. Primer: izotopi vodika 1 2 3 H H H 1 1 1 vodik devterij tricij 99, 9 % 0, 1 % neznatne količine Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

Primeri izotopov 1. Kisik ima tri izotope: 16 17 18 O O O 8 8 8 2. Železo ima štiri naravne izotope: 54 56 57 58 Fe Fe 26 26 Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

Lastnosti in razširjenost izotopov v naravi Različni izotopi so različno razširjeni v naravi, imajo različne fizikalne, a enake kemijske lastnosti. Relativna atomska masa elementa je vsota produktov med razširjenostjo in relativno atomsko maso posameznih izotopov. Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.
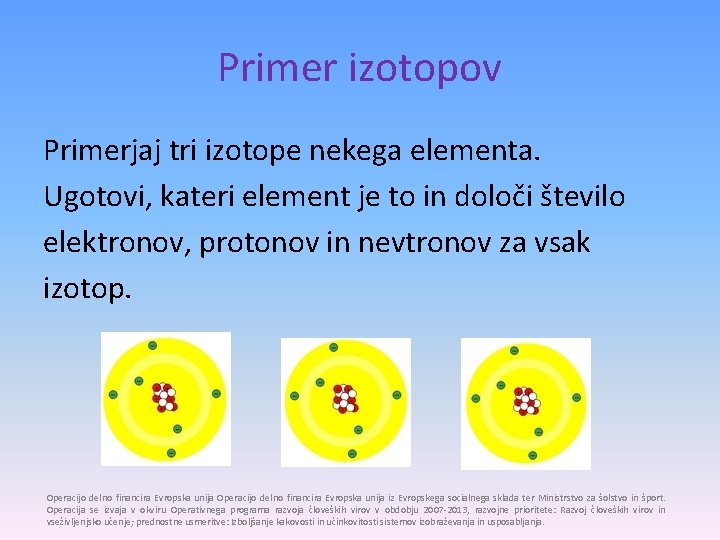
Primer izotopov Primerjaj tri izotope nekega elementa. Ugotovi, kateri element je to in določi število elektronov, protonov in nevtronov za vsak izotop. Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

Ioni Kdaj nastane ion? Ion nastane, če atom odda ali sprejme elektrone. Ioni so električno nabiti delci → kationi in anioni Kationi imajo pozitiven naboj, anioni pa negativen naboj. Kation nastane, če atom odda enega ali več elektronov, anion pa nastane, če atom sprejme enega ali več elektronov. Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.
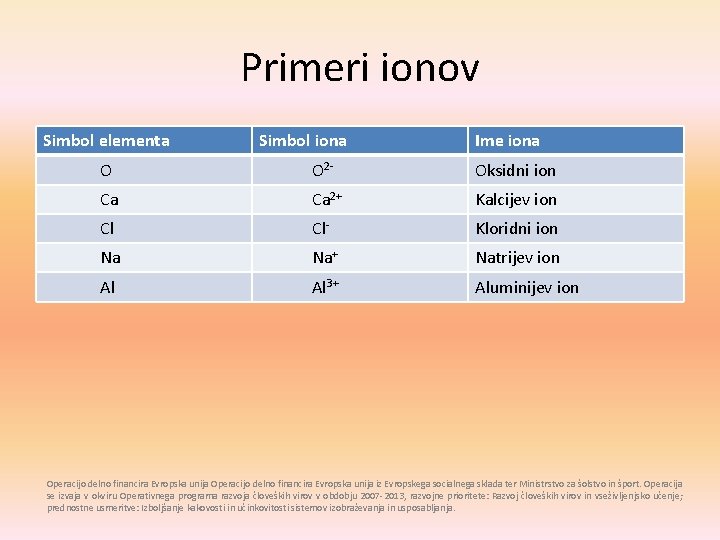
Primeri ionov Simbol elementa Simbol iona Ime iona O O 2 - Oksidni ion Ca Ca 2+ Kalcijev ion Cl Cl- Kloridni ion Na Na+ Natrijev ion Al Al 3+ Aluminijev ion Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

Elektronska ovojnica → elektroni se gibajo v prostoru okrog jedra →atomska orbitala je prostor okoli jedra atoma, v katerem je 95 % verjetnost, da se v njej nahaja elektron → vrste orbital: - s orbitale - p orbitale - d orbitale - f orbitale Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

Orbitale se razlikujejo po: → obliki → velikosti → usmerjenosti v prostoru → px, py, pz → energiji Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

Elektronska konfiguracija • razporeditev elektronov po orbitalah Elektroni so razporejeni po orbitalah v skladu s tremi pravili: → princip izgradnje → Paulijevo izključitveno načelo → Hundovo pravilo V eni orbitali sta lahko največ dva elektrona. Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

Primeri elektronske konfiguracije H 1 s 1 He 1 s 2 Li 1 s 2 2 s 1 Be 1 s 22 s 2 B 1 s 22 p 1 C 1 s 22 px 12 py 1 Na 1 s 22 p 63 s 1 - daljši način Na [Ne] 3 s 1 - krajši način Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

Viri: Andrej Smrdu: KEMIJA Snov in spremembe 1, Ljubljana, Jutro, 2006 Andrej Smrdu: Kemijo razumem, kemijo znam Ljubljana, Jutro, 2008 http: //www. osbos. si/e-kemija/e-gradivo/ http: //www. minet. si/kemija/ http: //www. ntf. uni-lj. si/ http: //education. jlab. org/qa/atom_model_03. gif http: //www. oemerhacili. com/belcika/taniyalim/image/i mage/Atomium. jpg Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 20072013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.

http: //www. osbos. si/e-kemija/e-gradivo-tmp/3 sklop/izotopi_ogljika_14. jpg http: //www. eskom. co. za/nuclear_energy/fuel/at om. jpg http: //education. jlab. org/qa/atom_model_04. gif Operacijo delno financira Evropska unija iz Evropskega socialnega sklada ter Ministrstvo za šolstvo in šport. Operacija se izvaja v okviru Operativnega programa razvoja človeških virov v obdobju 2007 -2013, razvojne prioritete: Razvoj človeških virov in vseživljenjsko učenje; prednostne usmeritve: Izboljšanje kakovosti in učinkovitosti sistemov izobraževanja in usposabljanja.
- Slides: 20