Bioloisko savienojumu monomri 2 lekcija Lekcijas saturs Organiskie

Bioloģisko savienojumu monomēri 2. lekcija

Lekcijas saturs • • • Organiskie savienojumi, to funkcionālās grupas Aminoskābes Ogļhidrāti Nukleotīdi Nekovalentās mijiedarbības

Organisko savienojumu vispārīgās īpašības • Molekulas veido oglekļa atomu ķēdes • Pie oglekļa atomiem var būt piesaistītas dažādas funkcionālās grupas • Funkcionālajām grupām ir raksturīgas noteiktas ķīmiskās īpašības • Molekulas īpašības nosaka atomu izvietojums 3

Ogļūdeņraži • Organiskie savienojumi, kuri sastāv tikai no oglekļa un ūdeņraža atomiem • Piesātinātie ogļūdeņraži (alkāni) satur tikai vienkāršās saites • Piesātinātie = piesātināti ar ūdeņradi, satur maksimālo H atomu skaitu CH 4, metāns C 2 H 6 ( CH 3 -CH 3 ), etāns C 4 H 10, ( CH 3 -CH 2 -CH 3 ), butāns 4
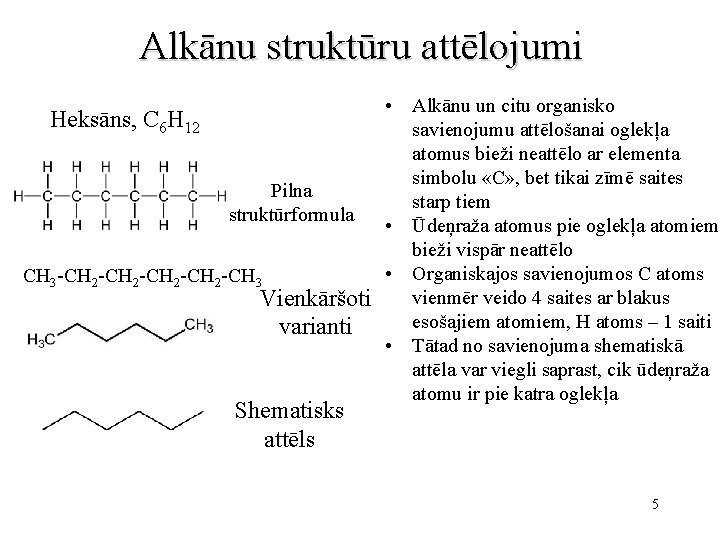
Alkānu struktūru attēlojumi • Alkānu un citu organisko Heksāns, C 6 H 12 savienojumu attēlošanai oglekļa atomus bieži neattēlo ar elementa simbolu «C» , bet tikai zīmē saites Pilna starp tiem struktūrformula • Ūdeņraža atomus pie oglekļa atomiem bieži vispār neattēlo • Organiskajos savienojumos C atoms CH 3 -CH 2 -CH 3 vienmēr veido 4 saites ar blakus Vienkāršoti esošajiem atomiem, H atoms – 1 saiti varianti • Tātad no savienojuma shematiskā attēla var viegli saprast, cik ūdeņraža atomu ir pie katra oglekļa Shematisks attēls 5
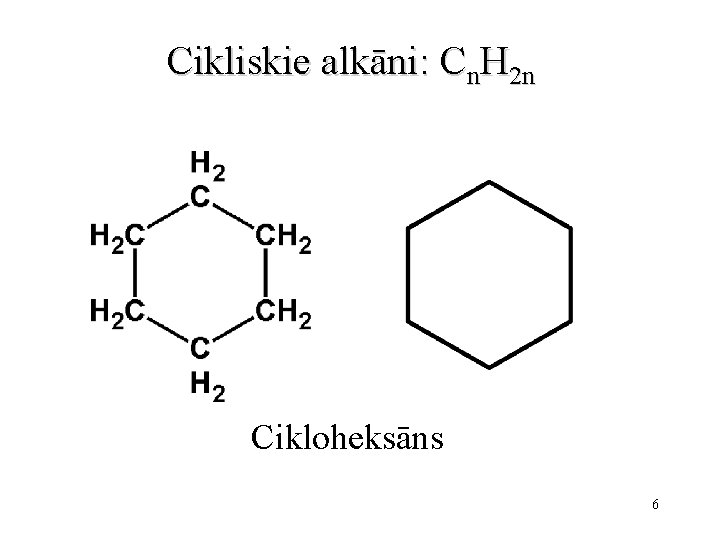
Cikliskie alkāni: Cn. H 2 n Cikloheksāns 6
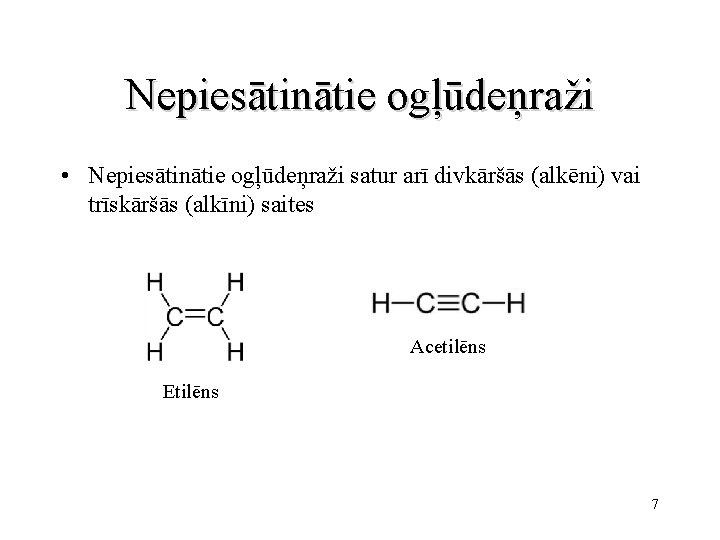
Nepiesātinātie ogļūdeņraži • Nepiesātinātie ogļūdeņraži satur arī divkāršās (alkēni) vai trīskāršās (alkīni) saites Acetilēns Etilēns 7
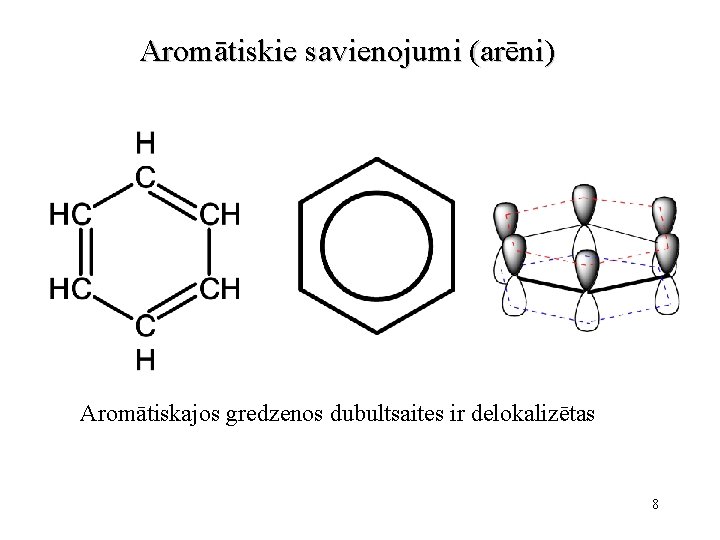
Aromātiskie savienojumi (arēni) Aromātiskajos gredzenos dubultsaites ir delokalizētas 8

Organisko savienojumu izomēri • Strukturālie izomēri – savienojumi ar vienādām kopīgajām formulām, bet dažādā secībā savienotiem atomiem • Stereoizomēri – savienojumi ar vienādām kopīgajām formulām un vienādā secībā savienotiem atomiem, bet atšķirīgu atomu telpisko novietojumu – Cis-trans izomēri – Enantiomēri jeb optiskie izomēri 9

Strukturālie izomēri • Strukturālie izomēri var būt gan ķīmiski līdzīgi, gan arī ļoti atšķirīgi • Piemērs: ir 3 savienojumi ar vispārējo formulu C 3 H 8 O, no kuriem divi ir spirti (ķīmiski līdzīgi), bet trešais – ēteris (ķīmiski atšķirīgs no spirtiem) CH 3 CH OH CH 3 CH 2 CH OH Propilspirts CH 3 CH 2 O CH 3 Metilēteris Izopropilspirts 10
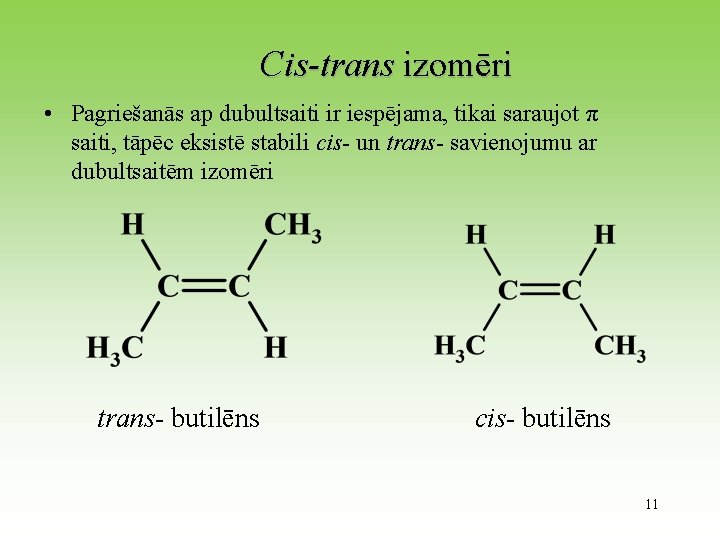
Cis-trans izomēri • Pagriešanās ap dubultsaiti ir iespējama, tikai saraujot π saiti, tāpēc eksistē stabili cis- un trans- savienojumu ar dubultsaitēm izomēri trans- butilēns cis- butilēns 11
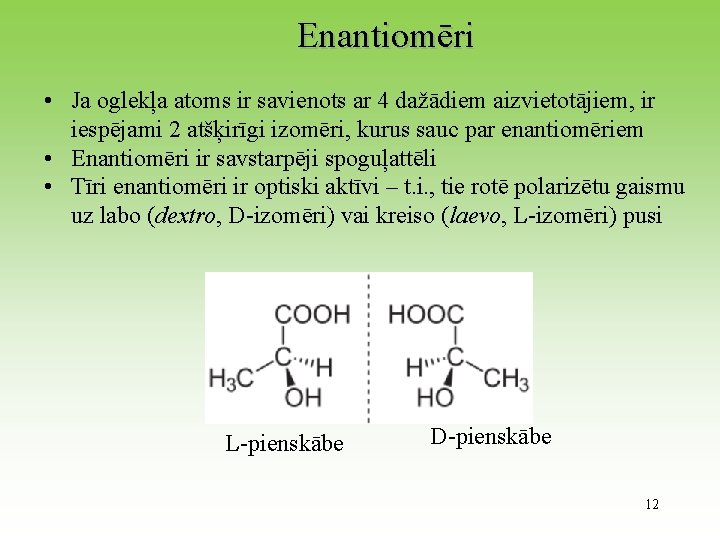
Enantiomēri • Ja oglekļa atoms ir savienots ar 4 dažādiem aizvietotājiem, ir iespējami 2 atšķirīgi izomēri, kurus sauc par enantiomēriem • Enantiomēri ir savstarpēji spoguļattēli • Tīri enantiomēri ir optiski aktīvi – t. i. , tie rotē polarizētu gaismu uz labo (dextro, D-izomēri) vai kreiso (laevo, L-izomēri) pusi L-pienskābe D-pienskābe 12
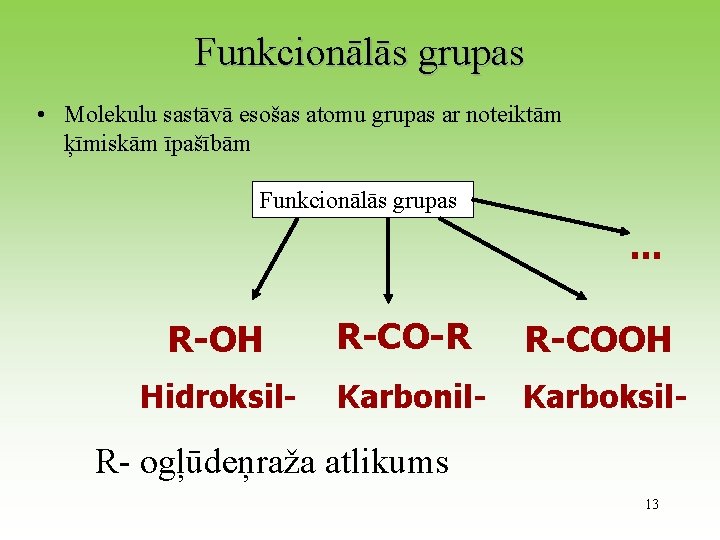
Funkcionālās grupas • Molekulu sastāvā esošas atomu grupas ar noteiktām ķīmiskām īpašībām Funkcionālās grupas . . . R-OH R-CO-R R-COOH Hidroksil- Karbonil- Karboksil- R- ogļūdeņraža atlikums 13
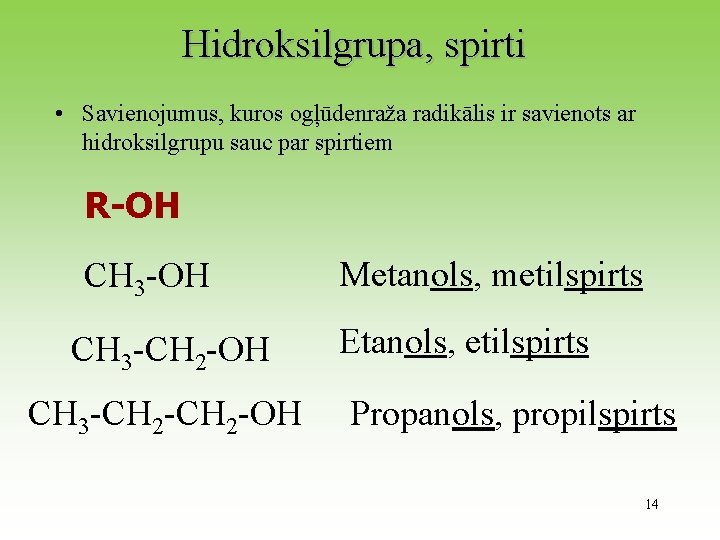
Hidroksilgrupa, spirti • Savienojumus, kuros ogļūdenraža radikālis ir savienots ar hidroksilgrupu sauc par spirtiem R-OH CH 3 -CH 2 -OH Metanols, metilspirts Etanols, etilspirts Propanols, propilspirts 14

Karbonilgrupa, aldehīdi • Savienojumus, kuros karbonilgrupa ir savienota ar vienu ūdeņraža atomu un vienu ogļūdeņraža radikāli sauc par aldehīdiem R C=O Karbonilgrupa H C=O H Metanāls, formaldehīds C=O H Aldehīds CH 3 C=O H Etanāls, acetaldehīds 15

Karbonilgrupa, ketoni • Savienojumus, kuros karbonilgrupa ir savienota ar diviem ogļūdeņražu radikāļiem sauc par ketoniem R C=O R’ Ketons CH 3 C=O CH 3 Dimetilketons, acetons 16
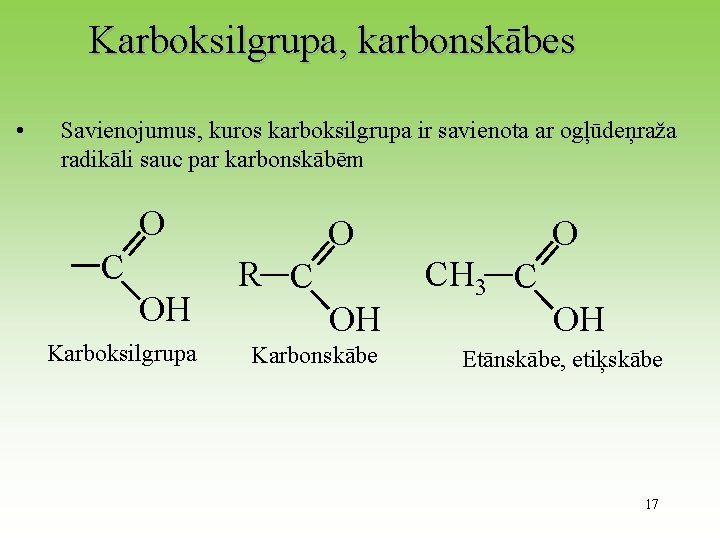
Karboksilgrupa, karbonskābes • Savienojumus, kuros karboksilgrupa ir savienota ar ogļūdeņraža radikāli sauc par karbonskābēm O C OH Karboksilgrupa O R C OH Karbonskābe O CH 3 C OH Etānskābe, etiķskābe 17

Amīni, aminogrupa • Amīni ir amonjaka atvasinājumi, kur viens, divi vai trīs ūdeņraža atomi ir aizvietoti ar ogļūdeņraža radikāli (pirmējie, otrējie un trešējie amīni) • Aminogrupa ir pirmējo amīnu sastāvā un satur vienu slāpekļa un divus ūdeņraža atomus NH 3 Amonjaks -NH 2 Aminogrupa CH 3 -NH 2 CH 3 -NH-CH 3 Metilamīns Dimetilamīns CH 3 -N-CH 3 Trimetilamīns 18

Citas funkcionālās grupas un savienojumi R-SH Sulfhidrilgrupa, merkaptāni (tioli) R-S-S-R’ Disulfīdgrupa, disulfīdi O R-O-P-OO- Fosfātgrupa, organiskie fosfāti 19
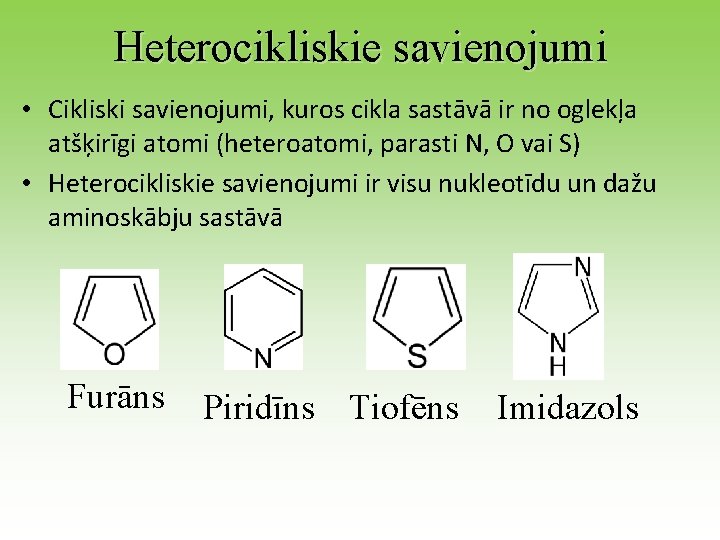
Heterocikliskie savienojumi • Cikliski savienojumi, kuros cikla sastāvā ir no oglekļa atšķirīgi atomi (heteroatomi, parasti N, O vai S) • Heterocikliskie savienojumi ir visu nukleotīdu un dažu aminoskābju sastāvā Furāns Piridīns Tiofēns Imidazols

Funkcionālo grupu reakcijas • Funkcionālās grupas spēj iesaistīties dažādās ķīmiskās reakcijās, piemēram: • Kondensācijas (savienošana, atņemot ūdens molekulu) reakcija. • Hidrolīzes (sašķelšana, pievienojot ūdens molekulu) reakcija. R -OH + OH-R R-O-R +H 2 O R -OH + OH-R 21
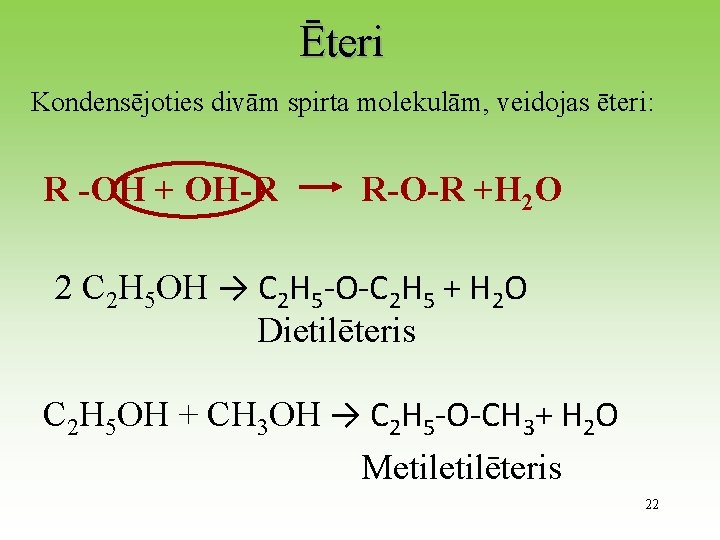
Ēteri Kondensējoties divām spirta molekulām, veidojas ēteri: R -OH + OH-R R-O-R +H 2 O 2 C 2 H 5 OH → C 2 H 5 -O-C 2 H 5 + H 2 O Dietilēteris C 2 H 5 OH + CH 3 OH → C 2 H 5 -O-CH 3+ H 2 O Metilēteris 22
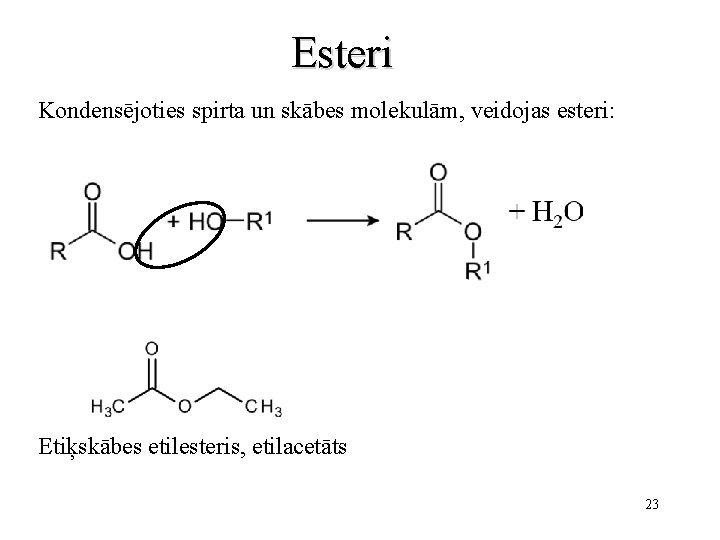
Esteri Kondensējoties spirta un skābes molekulām, veidojas esteri: Etiķskābes etilesteris, etilacetāts 23
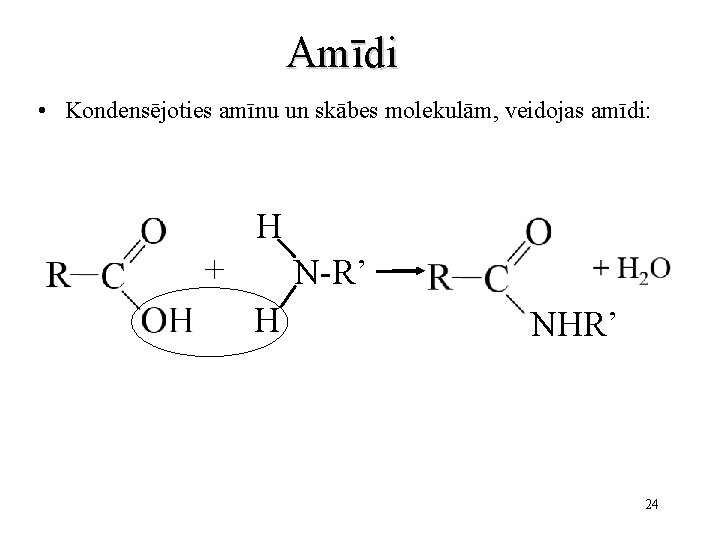
Amīdi • Kondensējoties amīnu un skābes molekulām, veidojas amīdi: H + N-R’ H NHR’ 24
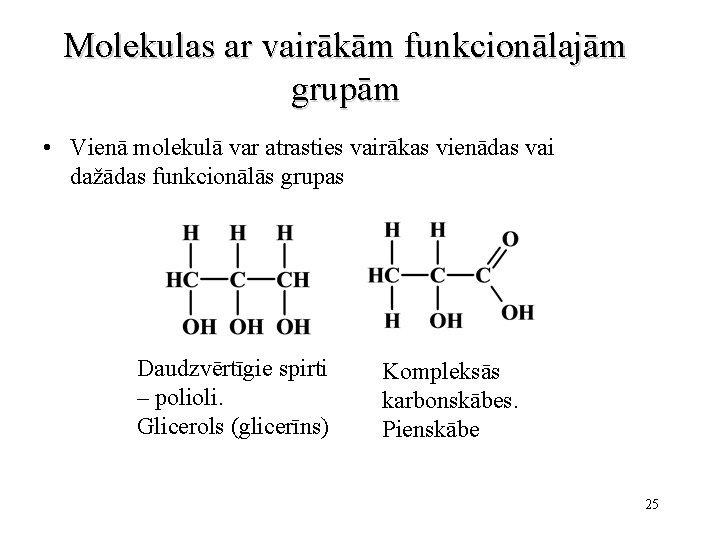
Molekulas ar vairākām funkcionālajām grupām • Vienā molekulā var atrasties vairākas vienādas vai dažādas funkcionālās grupas Daudzvērtīgie spirti – polioli. Glicerols (glicerīns) Kompleksās karbonskābes. Pienskābe 25

Aminoskābes • Organiski savienojumi ar amino- un karboksil- grupām • Proteīni sastāv no 20 dažādām aminoskābēm ar vienādu skeletu (“backbone”), bet atšķirīgām sānu ķēdēm (“R”) • Visas proteīnus veidojošās aminoskābes ir a-aminoskābes (karboksil- un amino- grupas ir pievienotas pie viena un tā paša oglekļa atoma, saukta par Ca) | H 3+N―Ca―H | R a-aminoskābe COO- | H 3+N―Ca―Cb―H | | R R’ | H 3+N―Ca―Cb―Cg―H | R | | R’ R’’ b- un g- aminoskābes (proteīnus neveido)
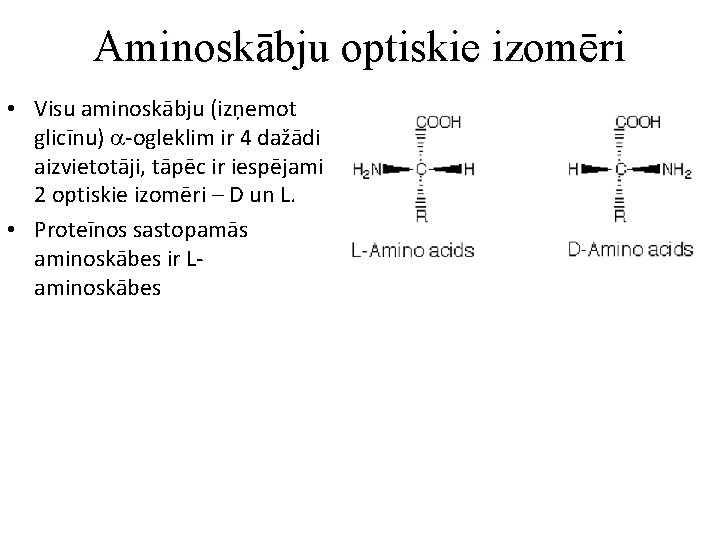
Aminoskābju optiskie izomēri • Visu aminoskābju (izņemot glicīnu) a-ogleklim ir 4 dažādi aizvietotāji, tāpēc ir iespējami 2 optiskie izomēri – D un L. • Proteīnos sastopamās aminoskābes ir Laminoskābes

Aminoskābju klasifikācija • Parasti aminoskābes klasificē pēc to sānu ķēžu polaritātes • Izdala nepolārās (hidrofobās), polārās un lādētās aminoskābes
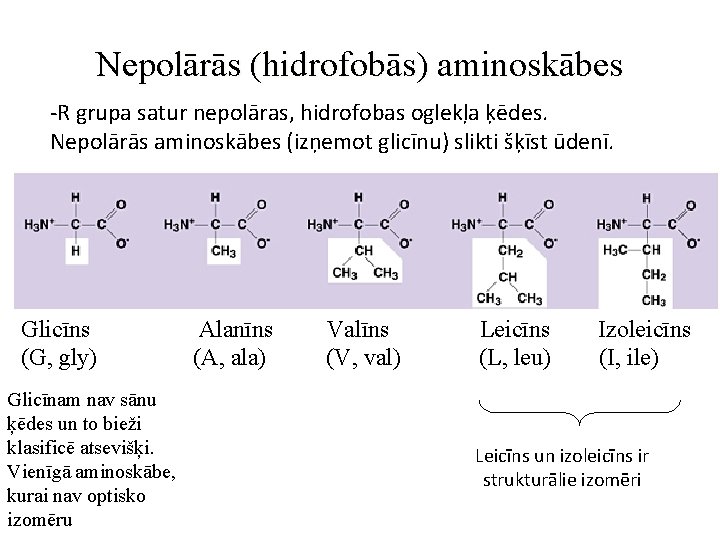
Nepolārās (hidrofobās) aminoskābes -R grupa satur nepolāras, hidrofobas oglekļa ķēdes. Nepolārās aminoskābes (izņemot glicīnu) slikti šķīst ūdenī. Glicīns (G, gly) Glicīnam nav sānu ķēdes un to bieži klasificē atsevišķi. Vienīgā aminoskābe, kurai nav optisko izomēru Alanīns (A, ala) Valīns (V, val) Leicīns (L, leu) Izoleicīns (I, ile) Leicīns un izoleicīns ir strukturālie izomēri
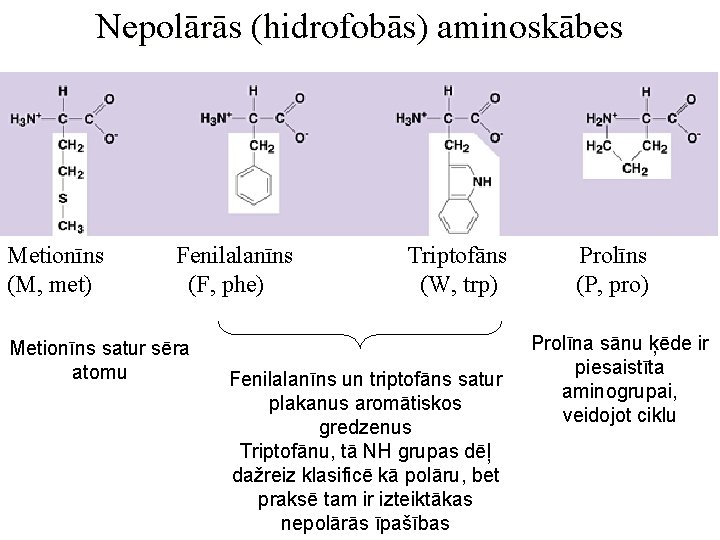
Nepolārās (hidrofobās) aminoskābes Metionīns (M, met) Fenilalanīns (F, phe) Metionīns satur sēra atomu Triptofāns (W, trp) Fenilalanīns un triptofāns satur plakanus aromātiskos gredzenus Triptofānu, tā NH grupas dēļ dažreiz klasificē kā polāru, bet praksē tam ir izteiktākas nepolārās īpašības Prolīns (P, pro) Prolīna sānu ķēde ir piesaistīta aminogrupai, veidojot ciklu

Polārās aminoskābes - R grupa sastāv no oglekļa, skābekļa, un skābekļa atomiem, kuri sānu ķēdi padara polārāku un tādejādi hidrofilāku. Polārās aminoskābes labi šķīst ūdenī. Serīns (S, ser) Treonīns (T, thr) Cisteīns (C, cys) Tirozīns (Y, tyr) Cisteīnam ir gan polāras, gan hidrofobas īpašības. Divi cisteīni var savienoties ar SH grupām Aspargīns Glutamīns (N, asn) (Q, gln)
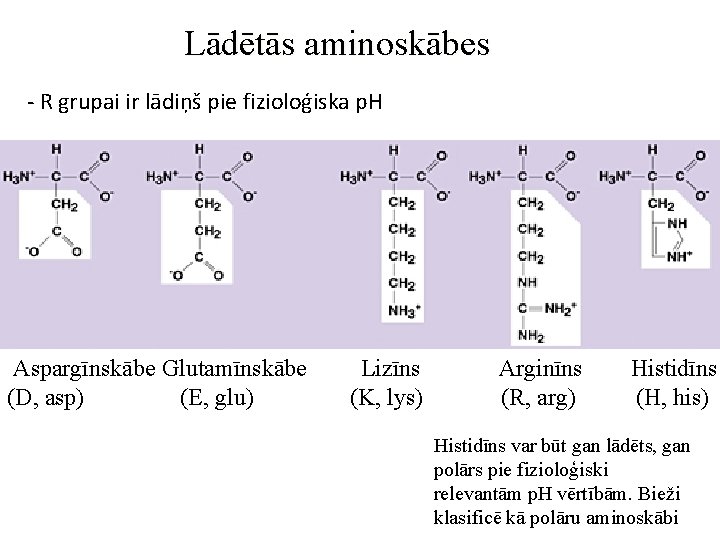
Lādētās aminoskābes - R grupai ir lādiņš pie fizioloģiska p. H Aspargīnskābe Glutamīnskābe (D, asp) (E, glu) Lizīns (K, lys) Arginīns (R, arg) Histidīns (H, his) Histidīns var būt gan lādēts, gan polārs pie fizioloģiski relevantām p. H vērtībām. Bieži klasificē kā polāru aminoskābi

Ogļhidrāti (ogļūdeņi, cukuri) • Vispārīgā ķīmiskā formula (CH 2 O)n = ogļhidrāti • Monosaharīdi: 3 – 6 C atomu ķēde + viena karbonil- un vairākas hidroksil- funkcionālās grupas • Monosaharīdu kondensācijas reakcijās veidojas di-, triun polisaharīdi 33

Monosaharīdu klasifikācija • Atkarībā no funkcionālās grupas, izšķir divus monosaharīdu veidus – aldozes un ketozes • Nosaukumos ietilpst arī oglekļa atomu skaits – piem. triozes (3 oglekļi), heksozes (6 oglekļi), u. c. • Līdzīgi aminoskabēm, monosaharīdiem ir D- un Lizomēri; dabā sastopama pārsvarā D- forma D-gliceraldehīds, aldotrioze Dihidroksiacetons, ketotrioze 34
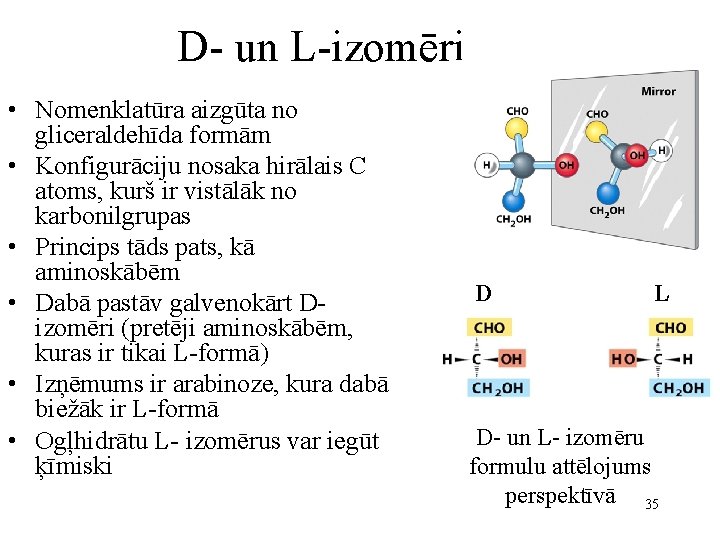
D- un L-izomēri • Nomenklatūra aizgūta no gliceraldehīda formām • Konfigurāciju nosaka hirālais C atoms, kurš ir vistālāk no karbonilgrupas • Princips tāds pats, kā aminoskābēm • Dabā pastāv galvenokārt Dizomēri (pretēji aminoskābēm, kuras ir tikai L-formā) • Izņēmums ir arabinoze, kura dabā biežāk ir L-formā • Ogļhidrātu L- izomērus var iegūt ķīmiski D L D- un L- izomēru formulu attēlojums perspektīvā 35
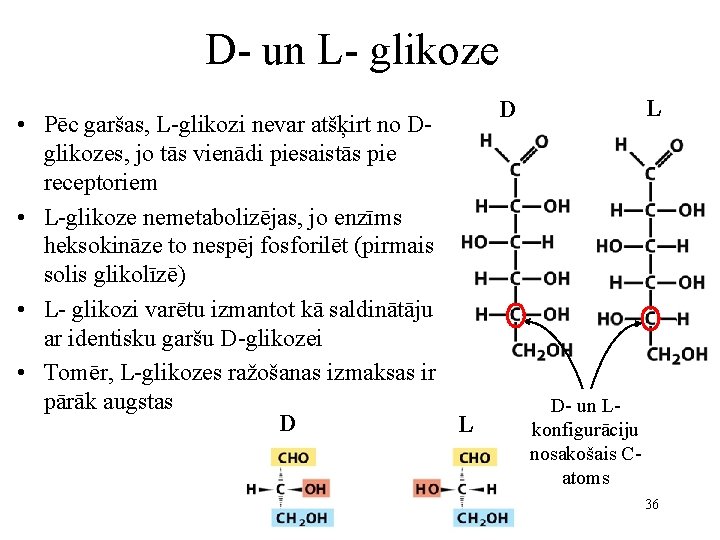
D- un L- glikoze • Pēc garšas, L-glikozi nevar atšķirt no Dglikozes, jo tās vienādi piesaistās pie receptoriem • L-glikoze nemetabolizējas, jo enzīms heksokināze to nespēj fosforilēt (pirmais solis glikolīzē) • L- glikozi varētu izmantot kā saldinātāju ar identisku garšu D-glikozei • Tomēr, L-glikozes ražošanas izmaksas ir pārāk augstas D L L D D- un Lkonfigurāciju nosakošais Catoms 36
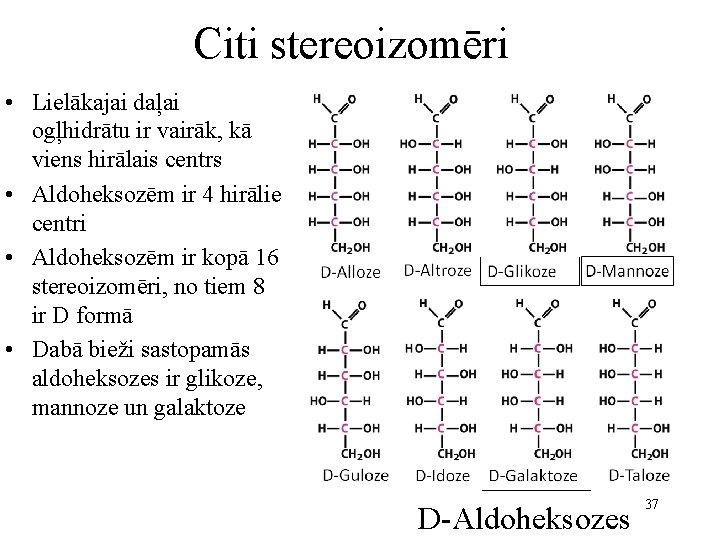
Citi stereoizomēri • Lielākajai daļai ogļhidrātu ir vairāk, kā viens hirālais centrs • Aldoheksozēm ir 4 hirālie centri • Aldoheksozēm ir kopā 16 stereoizomēri, no tiem 8 ir D formā • Dabā bieži sastopamās aldoheksozes ir glikoze, mannoze un galaktoze D-Aldoheksozes 37
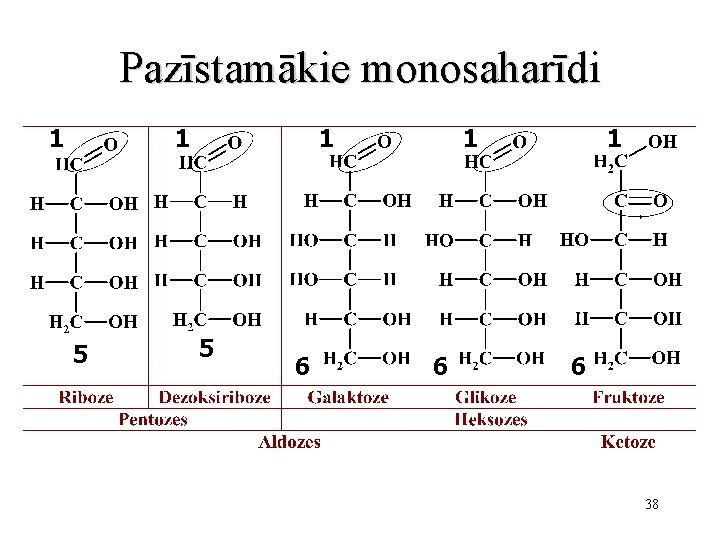
Pazīstamākie monosaharīdi 1 1 5 6 1 6 38
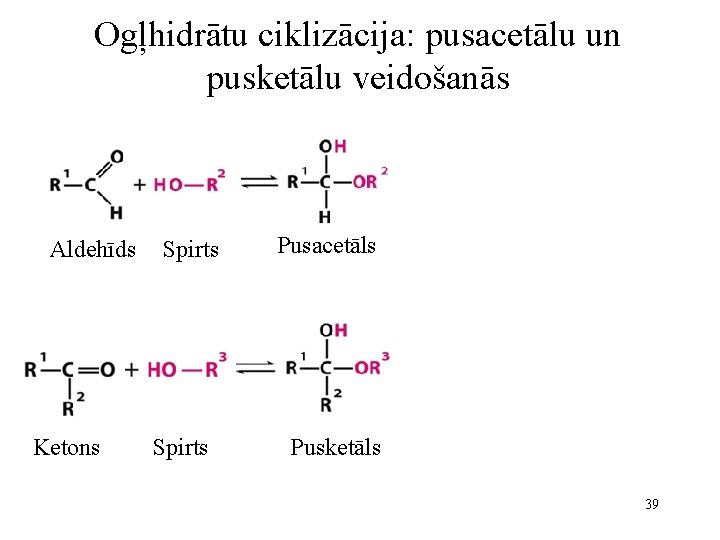
Ogļhidrātu ciklizācija: pusacetālu un pusketālu veidošanās Aldehīds Ketons Spirts Pusacetāls Pusketāls 39
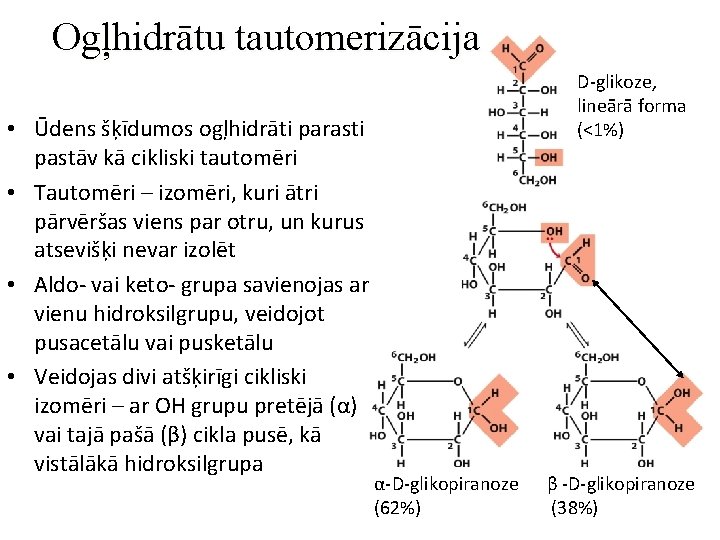
Ogļhidrātu tautomerizācija • Ūdens šķīdumos ogļhidrāti parasti pastāv kā cikliski tautomēri • Tautomēri – izomēri, kuri ātri pārvēršas viens par otru, un kurus atsevišķi nevar izolēt • Aldo- vai keto- grupa savienojas ar vienu hidroksilgrupu, veidojot pusacetālu vai pusketālu • Veidojas divi atšķirīgi cikliski izomēri – ar OH grupu pretējā (α) vai tajā pašā (β) cikla pusē, kā vistālākā hidroksilgrupa D-glikoze, lineārā forma (<1%) α-D-glikopiranoze (62%) β -D-glikopiranoze (38%)
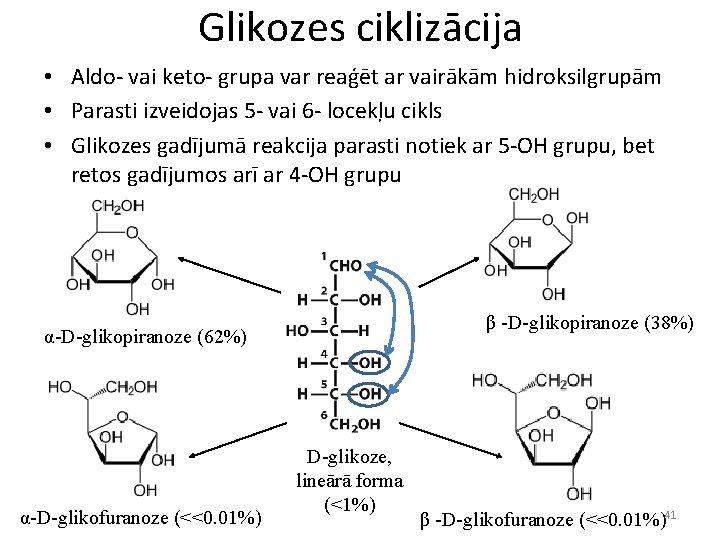
Glikozes ciklizācija • Aldo- vai keto- grupa var reaģēt ar vairākām hidroksilgrupām • Parasti izveidojas 5 - vai 6 - locekļu cikls • Glikozes gadījumā reakcija parasti notiek ar 5 -OH grupu, bet retos gadījumos arī ar 4 -OH grupu β -D-glikopiranoze (38%) α-D-glikopiranoze (62%) α-D-glikofuranoze (<<0. 01%) D-glikoze, lineārā forma (<1%) β -D-glikofuranoze (<<0. 01%)41
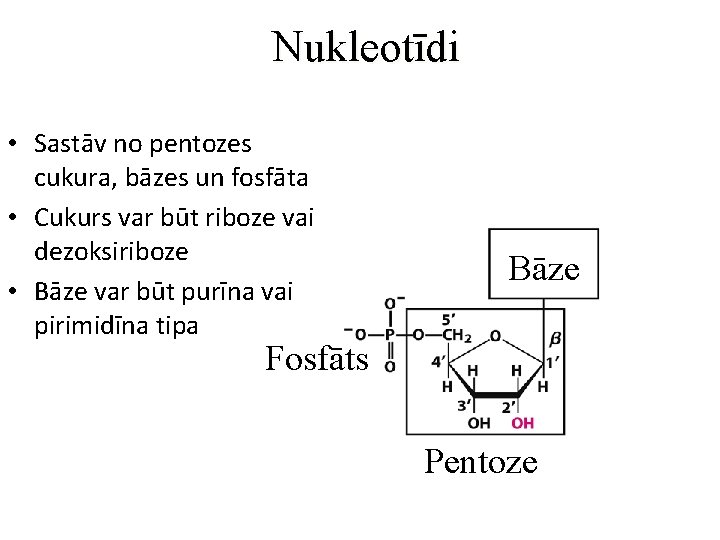
Nukleotīdi • Sastāv no pentozes cukura, bāzes un fosfāta • Cukurs var būt riboze vai dezoksiriboze • Bāze var būt purīna vai pirimidīna tipa Bāze Fosfāts Pentoze
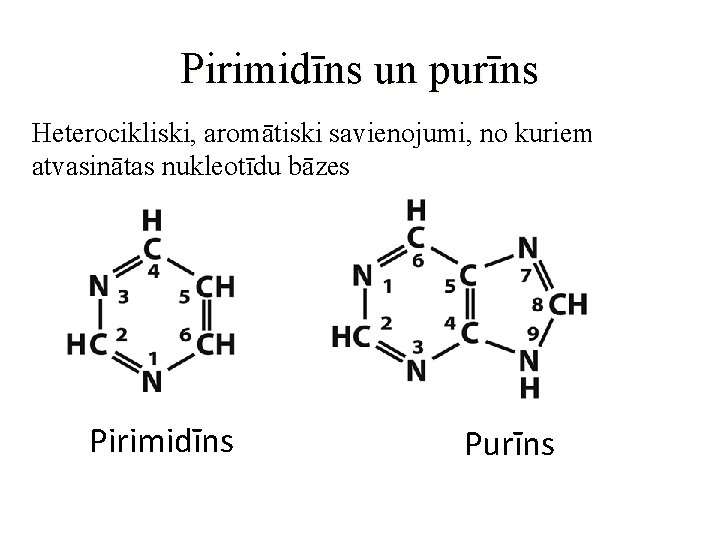
Pirimidīns un purīns Heterocikliski, aromātiski savienojumi, no kuriem atvasinātas nukleotīdu bāzes Pirimidīns Purīns
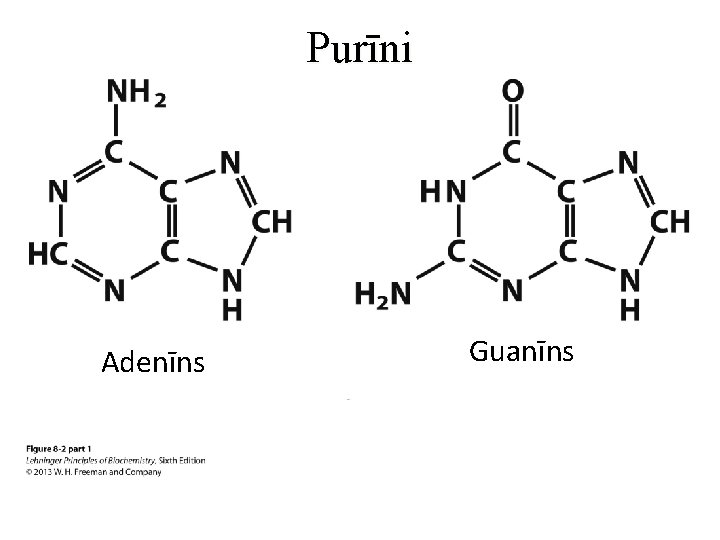
Purīni Adenīns Guanīns
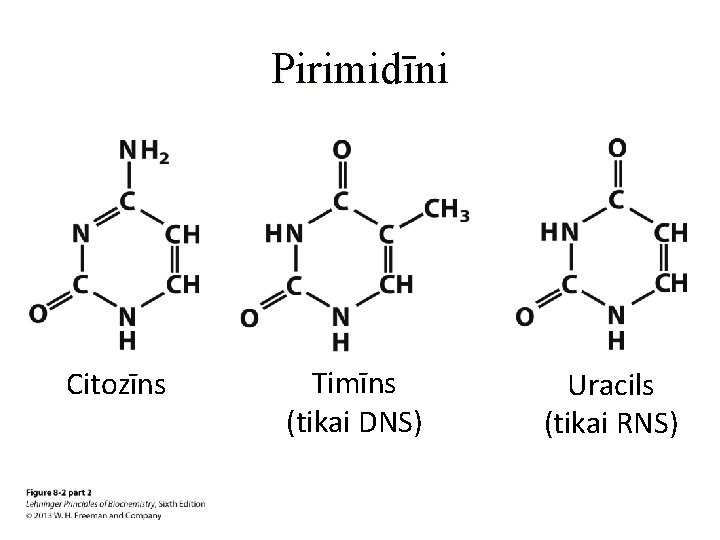
Pirimidīni Citozīns Timīns (tikai DNS) Uracils (tikai RNS)
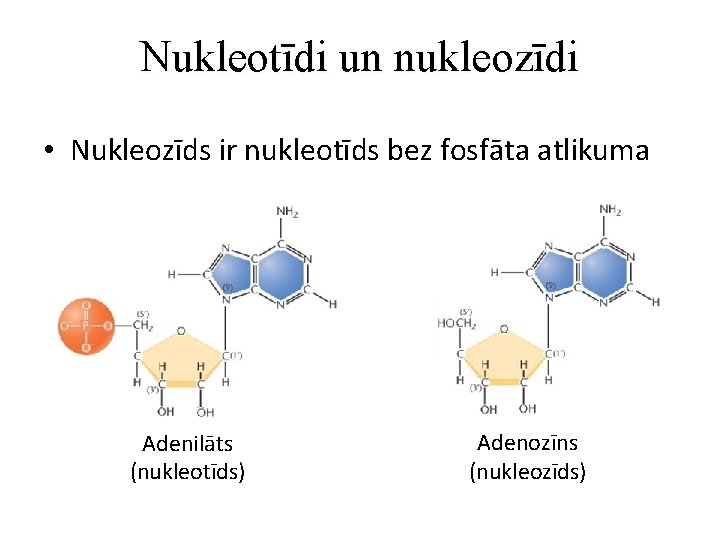
Nukleotīdi un nukleozīdi • Nukleozīds ir nukleotīds bez fosfāta atlikuma Adenilāts (nukleotīds) Adenozīns (nukleozīds)
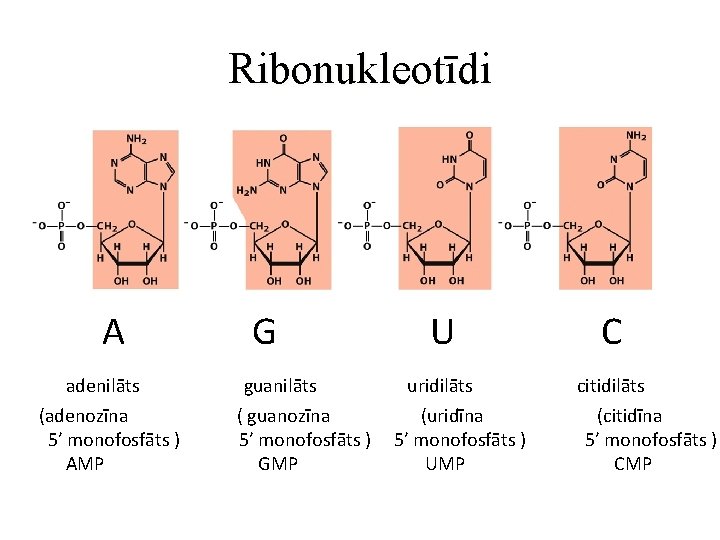
Ribonukleotīdi A adenilāts (adenozīna 5’ monofosfāts ) AMP G guanilāts ( guanozīna 5’ monofosfāts ) GMP U uridilāts (uridīna 5’ monofosfāts ) UMP C citidilāts (citidīna 5’ monofosfāts ) CMP
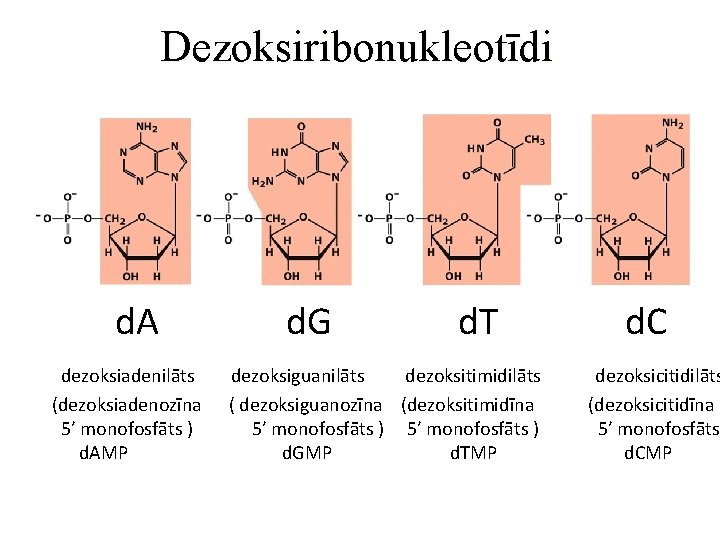
Dezoksiribonukleotīdi d. A dezoksiadenilāts (dezoksiadenozīna 5’ monofosfāts ) d. AMP d. G d. T dezoksiguanilāts dezoksitimidilāts ( dezoksiguanozīna (dezoksitimidīna 5’ monofosfāts ) d. GMP d. TMP d. C dezoksicitidilāts (dezoksicitidīna 5’ monofosfāts d. CMP
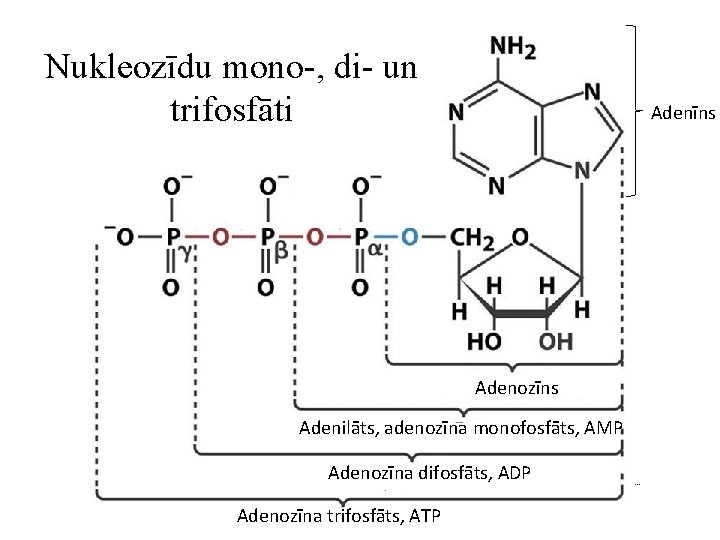
Nukleozīdu mono-, di- un trifosfāti Adenīns Adenozīns Adenilāts, adenozīna monofosfāts, AMP Adenozīna difosfāts, ADP Adenozīna trifosfāts, ATP

Nekovalentās mijiedarbības starp molekulām • Bioķīmiskajos procesos ļoti liela nozīme ir dažādām salīdzinoši vājām elektrostatiskajām mijiedarbībām starp atomiem • Bioloģiskās makromolekulas sastāv no ļoti daudziem atomiem, tāpēc atomu vājās mijiedarbības summējas un kļūst nozīmīgas 50
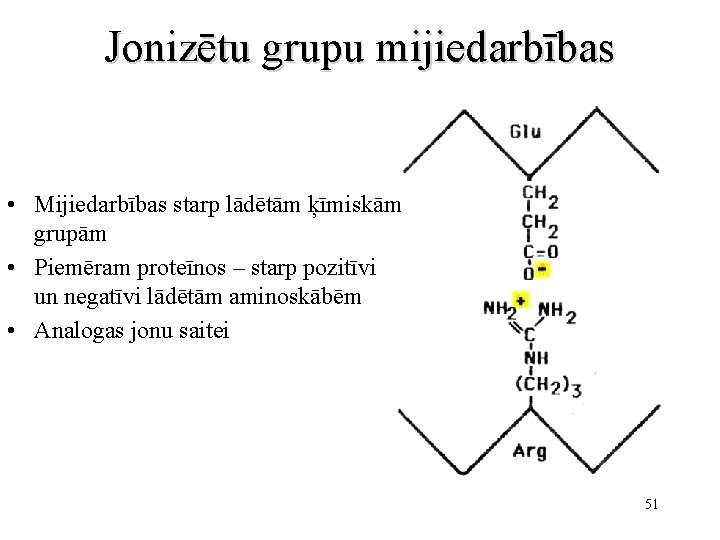
Jonizētu grupu mijiedarbības • Mijiedarbības starp lādētām ķīmiskām grupām • Piemēram proteīnos – starp pozitīvi un negatīvi lādētām aminoskābēm • Analogas jonu saitei 51

Van der Vālsa spēki • Definēti kā jebkura mijiedarbība starp molekulām, atšķirīga no kovalentās vai jonu mijiedarbības • Teorētiski H-saites arī ir van der Vālsa spēku paveids, bet tās ir daudz stiprākas par citiem van der Vālsa spēkiem, tādēļ tās parasti klasificē atsevišķi • Molekulām, kuru sastāvā ir atomi ar atšķirīgām elektronegativitātēm, veidojas permanentie dipoli ar daļējiem lādiņiem • Pat ja elektronegativitātes ir vienādas, tomēr fluktuāciju dēļ izveidojas īslaicīgi dipoli, kuri var inducēt dipolu blakus esošajā molekulā Gekonu spēja rāpties pa vertikālām, pilnīgi gludām virsmām tiek skaidrota ar van der Vālsa spēkiem 52
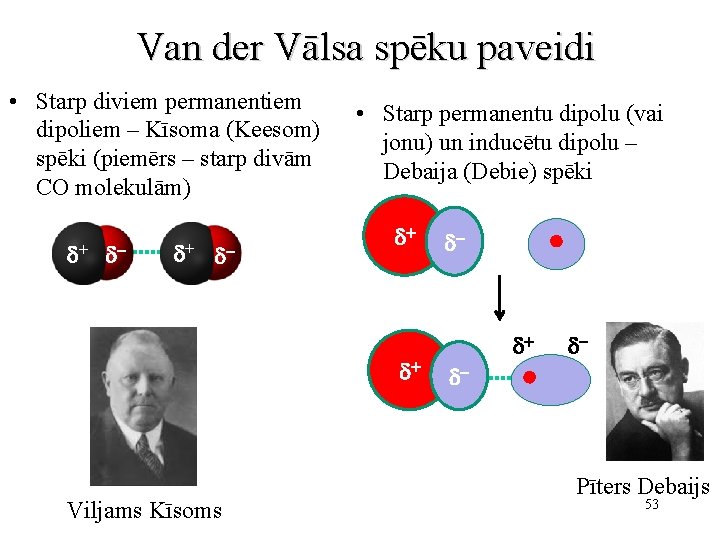
Van der Vālsa spēku paveidi • Starp diviem permanentiem dipoliem – Kīsoma (Keesom) spēki (piemērs – starp divām CO molekulām) d+ d- • Starp permanentu dipolu (vai jonu) un inducētu dipolu – Debaija (Debie) spēki d+ d+ Viljams Kīsoms d- d+ d- d- Pīters Debaijs 53
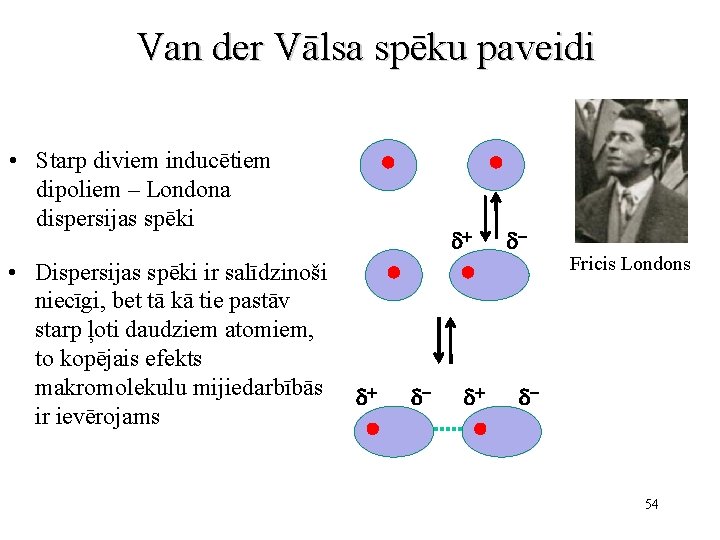
Van der Vālsa spēku paveidi • Starp diviem inducētiem dipoliem – Londona dispersijas spēki • Dispersijas spēki ir salīdzinoši niecīgi, bet tā kā tie pastāv starp ļoti daudziem atomiem, to kopējais efekts makromolekulu mijiedarbībās ir ievērojams d+ d+ d- Fricis Londons d- 54
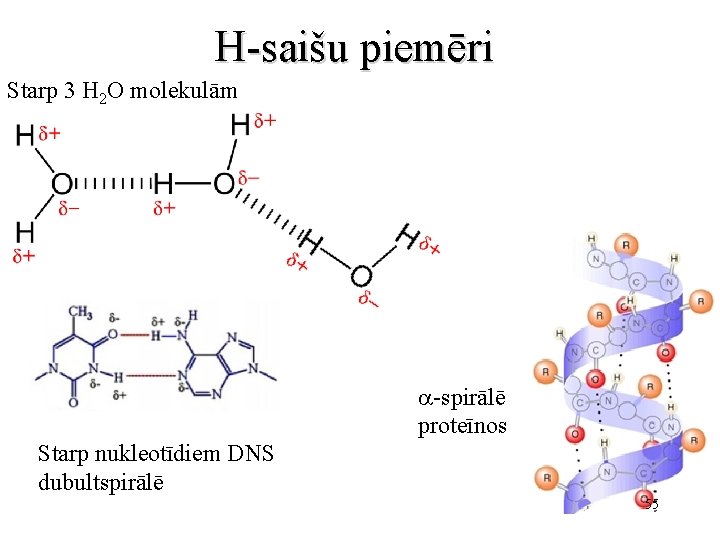
H-saišu piemēri Starp 3 H 2 O molekulām a-spirālē proteīnos Starp nukleotīdiem DNS dubultspirālē 55
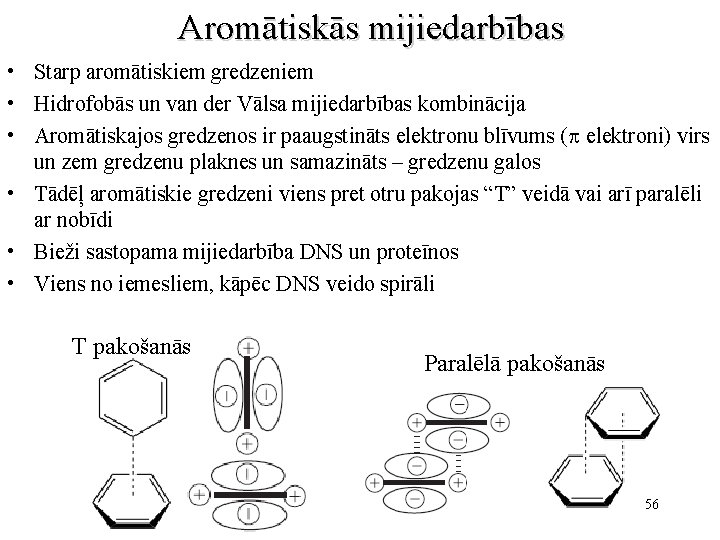
Aromātiskās mijiedarbības • Starp aromātiskiem gredzeniem • Hidrofobās un van der Vālsa mijiedarbības kombinācija • Aromātiskajos gredzenos ir paaugstināts elektronu blīvums (p elektroni) virs un zem gredzenu plaknes un samazināts – gredzenu galos • Tādēļ aromātiskie gredzeni viens pret otru pakojas “T” veidā vai arī paralēli ar nobīdi • Bieži sastopama mijiedarbība DNS un proteīnos • Viens no iemesliem, kāpēc DNS veido spirāli T pakošanās Paralēlā pakošanās 56

Hidrofobais efekts H 2 O • Hidrofobais (“bailes no ūdens”) efekts ir novērojams, jebkuru nepolāru savienojumu sajaucot ar ūdeni • Kontakti starp polārām un nepolārām molekulām ir enerģētiski neizdevīgi • Tāpēc nepolārās molekulas agregējas kopā, lai minimizētu kontaktus 57 ar polārajām molekulām

Hidrofobās mijiedarbības • Lai kādu savienojumu izšķīdinātu ūdenī, ir jāizjauc dažas H-saites starp ūdens molekulām • Izšķīdinot polāru savienojumu, veidojas jaunas H-saites ar izšķīdināto vielu, kas kompensē izjauktās saites starp ūdens molekulām • Nepolāra savienojuma gadījumā kompensējošas H-saites veidoties nevar, kas nav izdevīgi no entalpijas viedokļa • Papildus, ap nepolārā savienojuma molekulām izveidojas parakristālisku ūdens molekulu slānis, kas no entropijas viedokļa nav izdevīgi • Tādejādi, hidrofobām molekulām ir enerģētiski izdevīgāk mijiedarboties vienai ar otru, nekā ar ūdeni • Amfipātisko molekulu hidrofilā daļa var mijiedarboties ar ūdeni, bet hidrofobā daļa – ar citu molekulu hidrofobajām daļām • Rezultātā, amfipātiskas molekulas (piem. fosfolipīdi) ūdenī veido bislāņus un micellas 58
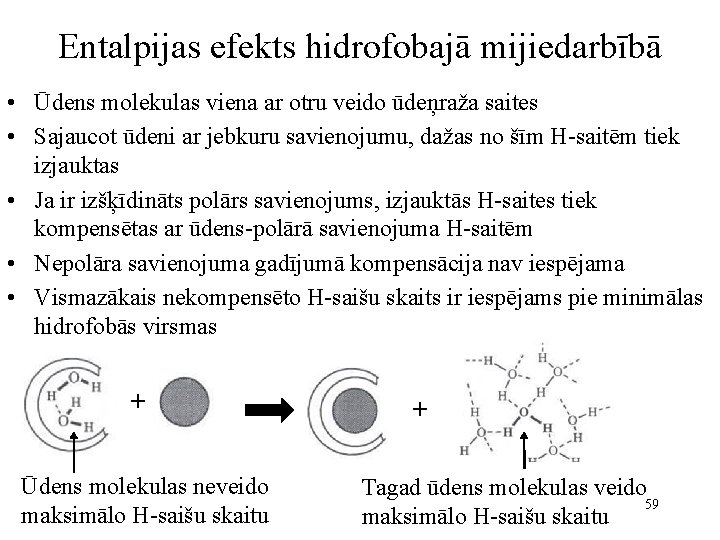
Entalpijas efekts hidrofobajā mijiedarbībā • Ūdens molekulas viena ar otru veido ūdeņraža saites • Sajaucot ūdeni ar jebkuru savienojumu, dažas no šīm H-saitēm tiek izjauktas • Ja ir izšķīdināts polārs savienojums, izjauktās H-saites tiek kompensētas ar ūdens-polārā savienojuma H-saitēm • Nepolāra savienojuma gadījumā kompensācija nav iespējama • Vismazākais nekompensēto H-saišu skaits ir iespējams pie minimālas hidrofobās virsmas + Ūdens molekulas neveido maksimālo H-saišu skaitu + Tagad ūdens molekulas veido 59 maksimālo H-saišu skaitu

Entropijas efekts hidrofobajā mijiedarbībā • Ap hidrofobām virsmām ūdenī pastāv augsti sakārtotu (parakristālisku) ūdens molekulu slānis • Divām hidrofobām virsmām mijiedarbojoties, sakārtoto ūdens molekulu slānis izjūk, kas ir entropiski izdevīgi • Hidrofobajā mijiedarbībā entropijas efekts ir daudz lielāks par entalpijas efektu +7 H 2 O 60
- Slides: 60