Dzvbas mija 2 lekcija 1 Lekcijas saturs Atoma

Dzīvības ķīmija 2. lekcija 1

Lekcijas saturs • Atoma uzbūve • Elementu periodiskā sistēma • Ķīmiskās saites • Mijiedarbības starp molekulām • Ūdens īpašības 2

Atomu uzbūves principi • Parasti atomu iztēlojas kā planetāro modeli, kur elektroni riņķo ap kodolu • Reālā situācija ir atšķirīga, bet planetārais modelis noder kā vienkārša aproksimācija • Kodols sastāv no protoniem un neitroniem • Kodols ir daudz mazāks par atoma kopējo izmēru – aptuveni 100 000 reizes • Gandrīz visa atoma masa ir sakoncentrēta kodolā 3
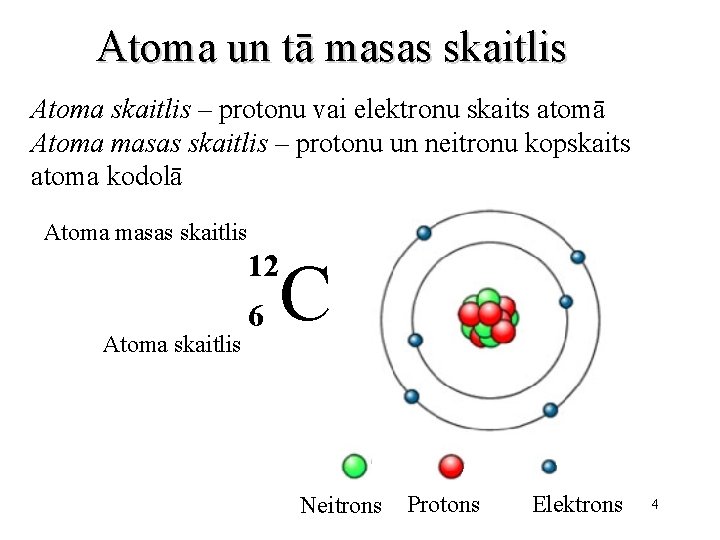
Atoma un tā masas skaitlis Atoma skaitlis – protonu vai elektronu skaits atomā Atoma masas skaitlis – protonu un neitronu kopskaits atoma kodolā Atoma masas skaitlis 12 Atoma skaitlis 6 C Neitrons Protons Elektrons 4
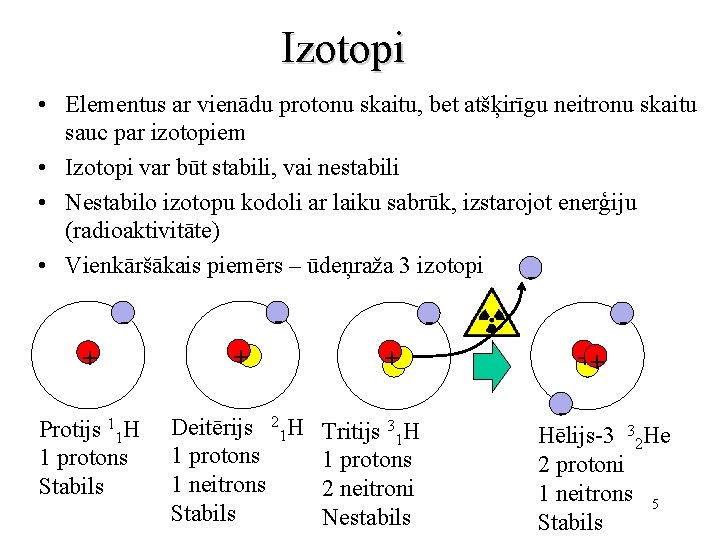
Izotopi • Elementus ar vienādu protonu skaitu, bet atšķirīgu neitronu skaitu sauc par izotopiem • Izotopi var būt stabili, vai nestabili • Nestabilo izotopu kodoli ar laiku sabrūk, izstarojot enerģiju (radioaktivitāte) • Vienkāršākais piemērs – ūdeņraža 3 izotopi - + + 1 H 1 Protijs 1 protons Stabils Deitērijs 1 protons 1 neitrons Stabils + 2 H 1 3 H 1 Tritijs 1 protons 2 neitroni Nestabils ++ Hēlijs-3 32 He 2 protoni 1 neitrons 5 Stabils
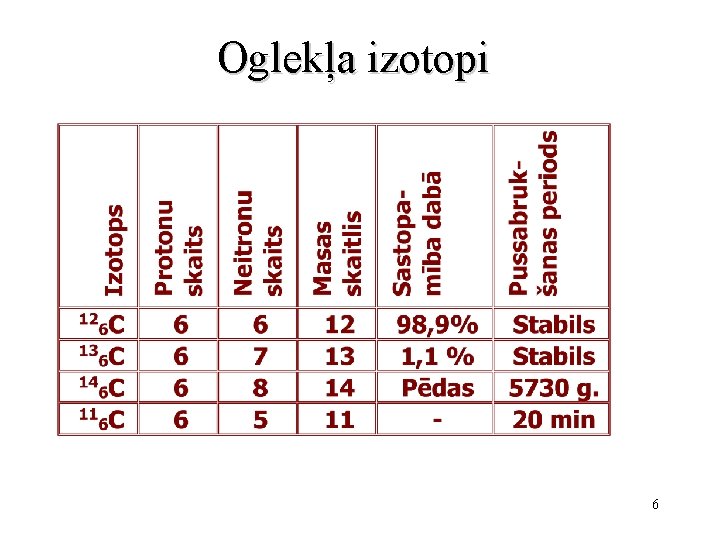
Oglekļa izotopi 6

Atomu masa • Atoma masas vienība – viena divpadsmitā daļa no oglekļa 12 C atoma masas (oglekļa vienība), aptuveni vienlīdzīga protona masai • Atoma masas vienības ekvivalents gramos: Daltons (Da) ~ 1, 66 x 10 -24 grami • Molekulas masa - molekulu veidojošo atomu masas summa • Bioloģiskās makromolekulas bieži ir ļoti lielas un to masu mēra kilodaltonos (k. Da) vai megadaltonos 7 (MDa)

Mola jēdziens • Veidojot ķīmiskās saites atomi mijiedarbojas noteiktās veselu skaitļu attiecībās: • C+O 2 → CO 2 2 H 2+O 2 → 2 H 2 O 2 Al+3 O 2 → 2 Al 2 O 3 • Lai ar ķīmisko reakciju iegūtu noteiktu daudzumu produkta, izejvielas ir jāņem proporcionāli reakcijā iesaistīto atomu vai molekulu skaitam • Atomu (arī molekulu un jonu) daudzuma mērvienība ir mols • Viens mols jebkura atoma (molekulas, jonu) satur 6, 02 x 1023 daļiņu 8

Avogadro skaitlis 6, 02 x 1023 = Avogadro skaitlis, ķīmiska konstante: oglekļa atomu skaits, kuru kopējā masa ir 12 grami. Avogadro skaitlis norāda atomu vai molekulu skaitu molā. Amadeus Avogadro (1776 - 1856) - itāļu ķīmiķis, kurš ievēroja, ka gāzes savā starpā reaģē noteiktās tilpuma attiecībās. 9

Molmasa Jebkuru 6, 02 x 1023 vienādu atomu vai molekulu masa gramos, kas ir skaitliski vienāda ar viena atoma vai molekulas masu, kas aprēķināta atoma masas vienībās (daltonos) Skābekļa molekulmasa – 32 Da Skābekļa molmasa – 32 grami Hemoglobīna molekulmasa – 60 000 Da (60 k. Da) Hemoglobīna molmasa - 60 000 g (60 kg) 1 hemoglobīna molekula transportē 4 skābekļa molekulas Tātad, lai vienlaicīgi transportētu 32 gramus skābekļa, vajag 60/4=15 kilogramus hemoglobīna 10

Atoma elektronu apvalka uzbūve Elektroni ap atoma kodolu izvietoti noteiktos enerģijas līmeņos (čaulās), kurus apzīmē ar burtiem: K; L; M; N utt. vai cipariem 1, 2, 3, 4. . . Vienu enerģijas līmeni veido 1 -4 apakšlīmeņi, kurus apzīmē ar burtiem: s; p; d; f Katru enerģijas apakšlīmeni aizpilda raksturīgas un noteikta skaita un formas elektronu orbitāles L K K- max 1 apakšlīmenis (s) 1 s 2 s 2 p L- max 2 apakšlīmeņi (s, p) M- max 3 apakšlīmeņi (s, p, d) N+ -max 4 apakšlīmeņi (s, p, d, f) s- max 2 ep- max 6 ed- max 10 ef- max 14 e 11

Enerģijas līmeņu aizpildīšanās • Līmeņi un apakšlīmeņi aizpildās pakāpeniski, maksimāli izmantojot zemākos enerģētiskos līmeņus • Atomu elektronu orbitāļu aizpildījumu var attēlot shematiski: C: 1 s 22 s 2 p 2 12
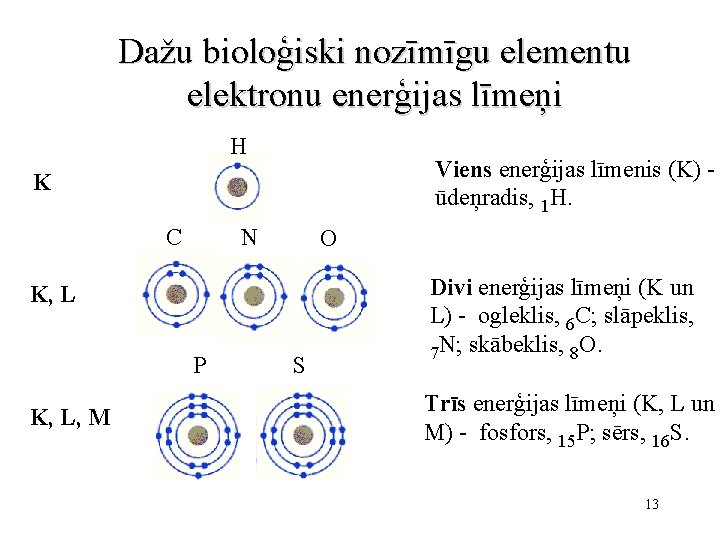
Dažu bioloģiski nozīmīgu elementu elektronu enerģijas līmeņi H Viens enerģijas līmenis (K) ūdeņradis, 1 H. K C N O K, L P K, L, M S Divi enerģijas līmeņi (K un L) - ogleklis, 6 C; slāpeklis, 7 N; skābeklis, 8 O. Trīs enerģijas līmeņi (K, L un M) - fosfors, 15 P; sērs, 16 S. 13

Elektronu orbitāles • Realitātē elektroni neriņķo ap kodolu kā planētas ap Sauli, bet aizpilda noteiktu telpas daļu • Telpas daļu, kurā ar noteiktu varbūtību atrodas elektrons, sauc par elektrona orbitāli • Vienā orbitālē vienlaikus var atrasties divi elektroni ar pretējiem magnētiskajiem griezes momentiem – spiniem • Elektroniem s, p, d un f apakšlīmeņos ir atšķirīgas orbitāļu formas 14
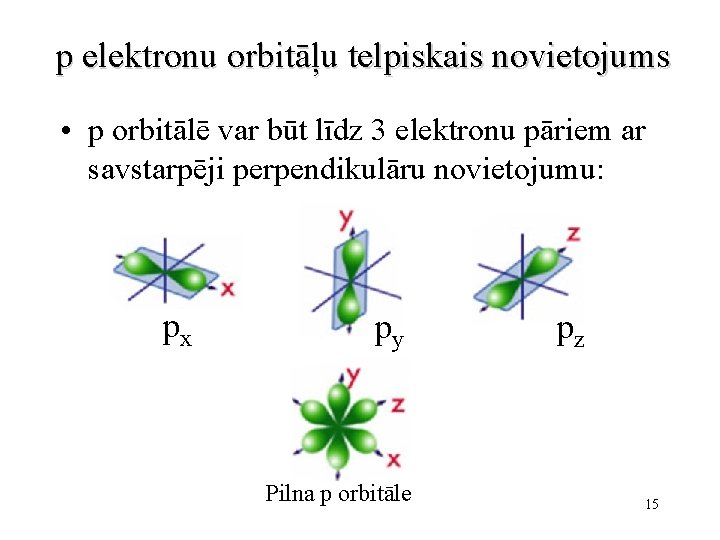
p elektronu orbitāļu telpiskais novietojums • p orbitālē var būt līdz 3 elektronu pāriem ar savstarpēji perpendikulāru novietojumu: px py Pilna p orbitāle pz 15
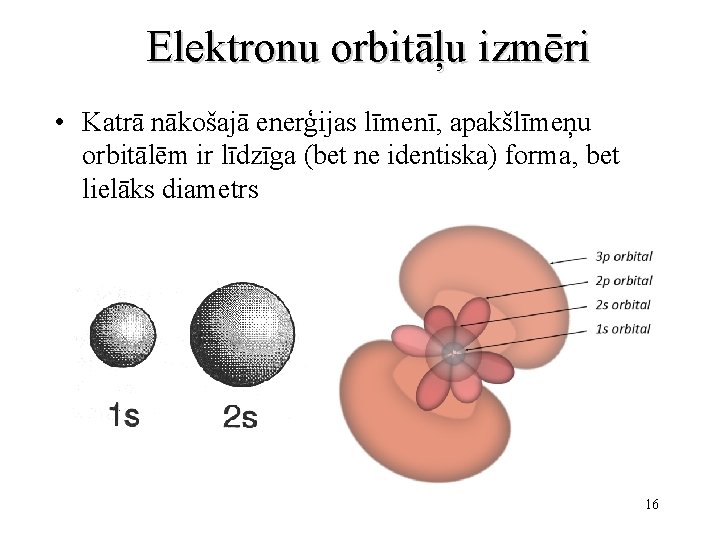
Elektronu orbitāļu izmēri • Katrā nākošajā enerģijas līmenī, apakšlīmeņu orbitālēm ir līdzīga (bet ne identiska) forma, bet lielāks diametrs 16
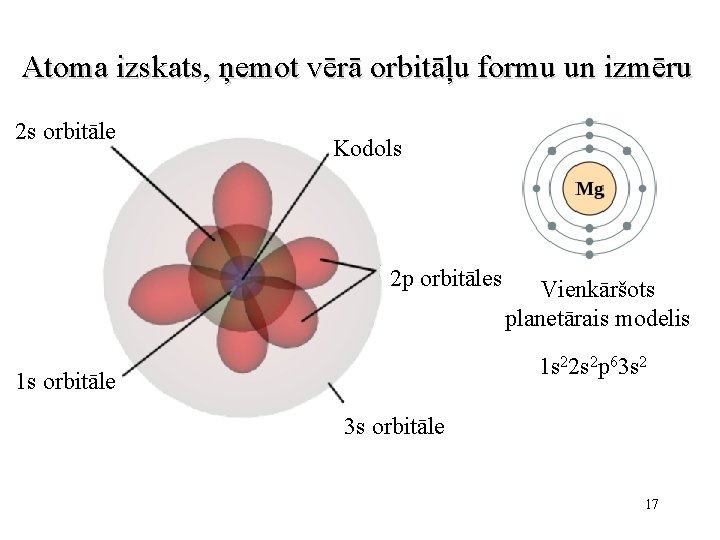
Atoma izskats, ņemot vērā orbitāļu formu un izmēru 2 s orbitāle Kodols 2 p orbitāles Vienkāršots planetārais modelis 1 s 22 s 2 p 63 s 2 1 s orbitāle 3 s orbitāle 17
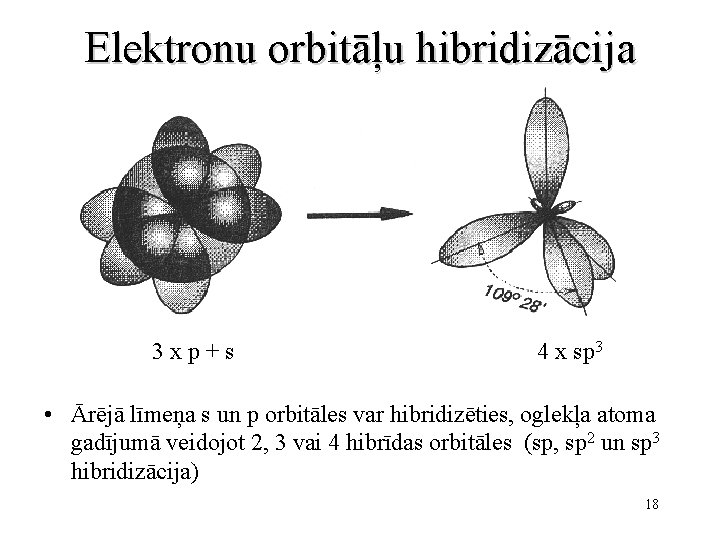
Elektronu orbitāļu hibridizācija 3 xp+s 4 x sp 3 • Ārējā līmeņa s un p orbitāles var hibridizēties, oglekļa atoma gadījumā veidojot 2, 3 vai 4 hibrīdas orbitāles (sp, sp 2 un sp 3 hibridizācija) 18

Elementu ķīmiskās īpašības un periodiskā sistēma • Elementu ķīmiskās īpašības nosaka to elektronu apvalka, īpaši ārējās čaulas uzbūve • Sakārtojot elementus elektronu enerģētisko līmeņu aizpildījuma secībā, iegūstam periodisko sistēmu 19
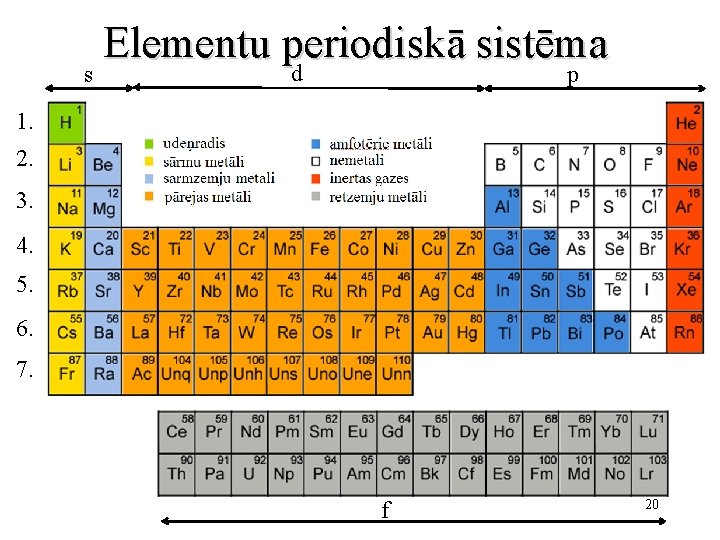
s Elementu periodiskā sistēma d p 1. 2. 3. 4. 5. 6. 7. f 20

Dabā sastopamie un biogēnie elementi • Dabā satopami 92 ķīmiskie elementi, vēl 26 elementi (118. – ununoktijs) iegūti laboratorijas apstākļos. • Dzīvās dabas objektus veido 25 – 26 elementi (biogēnie elementi) • Vēl 10 – 15 elementi ir sastopami toksisko savienojumu vai ārstniecisko preparātu sastāvā 21

Ķīmisko elementu izplatība organismos • O-65% • N-3. 3% • K-0. 4% • Cl-0. 2% • C-18. 5% • Ca-1. 5% • S-0. 3% • Mg-0. 1% • Na-0. 2% • Pārējie kopā < 0. 1% • H-9. 5% • P-1% 22

Ķīmisko elementu izplatība organismos • Četri pamatelementi – C, H, O un N sastāda aptuveni 96% šūnas masas • Makroelementi – citi elementi, kuri organismam nepieciešami samērā lielos daudzumos (Ca, P, S, K, Na, Cl, Mg, kopā ap 4% masas) • Mikroelementi – elementi, kuri ir organismam ir nepieciešami nelielos daudzumos (katrs mazāk, kā 0. 01 %) • Papildus ir elementi, kuru loma zīdītāju organismā ir varbūtēja, bet nav pierādīta (Si, B, As, V) • Fluors nav organismam nepieciešams, bet paaugstina zobu izturību, kā arī ir daudzu medikamentu sastāvā • Daži elementi ir nepieciešami noteiktiem mikroorganismiem, bet ne zīdītājiem (piem. Cd dažās aļģēs) • Cilvēka organismā ir konstatēti ap 60 ķīmiskie elementi, bet lielākā daļa tur ir nokļuvuši nejauši un ir inerti vai toksiski 23

Pamatelementu un makroelementu galvenās funkcijas organismā • • • C, H, O – visu organisko vielu sastāvā N – aminoskābju, nukleotīdu sastāvā S – dažu aminoskābju un sāļu sastāvā P – nukleotīdu un neorganiskā fosfāta (piem. kaulu) sastāvā Ca – kaulu sastāvā, dažādu signālceļu un bioķīmisko procesu regulācijā • K, Na – šūnu osmotiskā spiediena regulācijā, neironu darbībā • Cl- šūnu osmotiskā spiediena regulācijā, kuņģī – sālsskābes sastāvā • Mg- mijiedarbība ar nukleotīdiem un nukleīnskābēm, daudzu enzīmu kofaktors 24

Nozīmīgākie mikroelementi 25
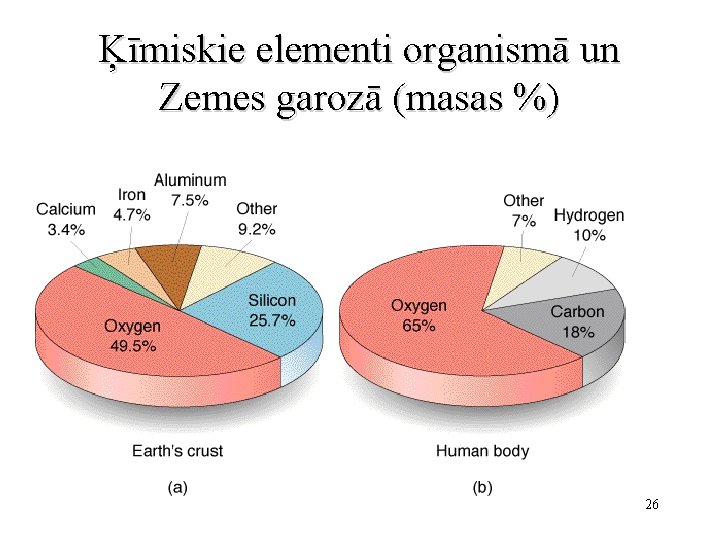
Ķīmiskie elementi organismā un Zemes garozā (masas %) 26

Kāpēc ogleklis, nevis silīcijs? • Ogleklim ir tieksme veidot polimēru ķēdītes – nepieciešams sarežģītu savienojumu izveidei • Silīcijs arī var veidot līdzīgas ķēdītes, bet. . . : • Silīcijs nespēj veidot kovalentās saites ar tik daudziem elementiem, kā ogleklis • Silīcija savienojumi ar ūdeņradi aktīvi reaģē ar ūdeni • Silīcija oksidēšanās produkts ir Si. O 2 (ļoti neaktīvs, grūti izvadīt no organisma) • Silīciju dzīvie organismi izmanto ļoti maz, cilvēks – gandrīz nemaz 27

Molekulu un jonu veidošanās • Atomi veido molekulas un jonus, izmantojot mijiedarbību starp ārējā enerģētiskā līmeņa elektroniem • Elementi ar vāji aizpildītu ārējo enerģētisko līmeni elektronus viegli atdod (piem. sārmu metāli) • Elementi ar gandrīz aizpildītu ārējo enerģētisko līmeni elektronus viegli pievieno (piem. halogēni) • Elementi ar pilnībā aizpildītu ārējo līmeni ir ķīmiski inerti (inertās gāzes) 28

Ķīmiskā saite • Vispārīgā gadījumā - 2 vairāku atomu mijiedarbība, kurā veidojas stabila daudzatomu sistēma • Parasti ar ķīmisko saiti saprot t. s. «stiprās» saites – jonu saiti, metālisko saiti un kovalento saiti • Ūdeņraža saites un van der Vālsa mijiedarbības arī ir ķīmisko saišu veidi, bet daudz vājākas par «stiprajām» saitēm 29
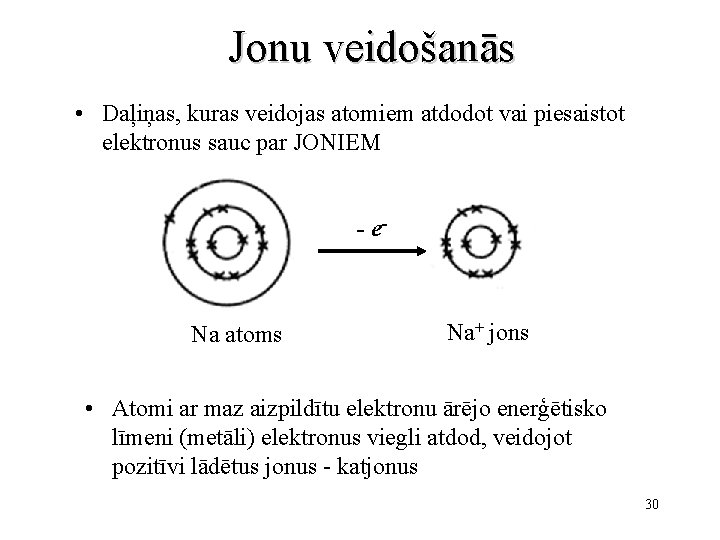
Jonu veidošanās • Daļiņas, kuras veidojas atomiem atdodot vai piesaistot elektronus sauc par JONIEM - e- Na atoms Na+ jons • Atomi ar maz aizpildītu elektronu ārējo enerģētisko līmeni (metāli) elektronus viegli atdod, veidojot pozitīvi lādētus jonus - katjonus 30
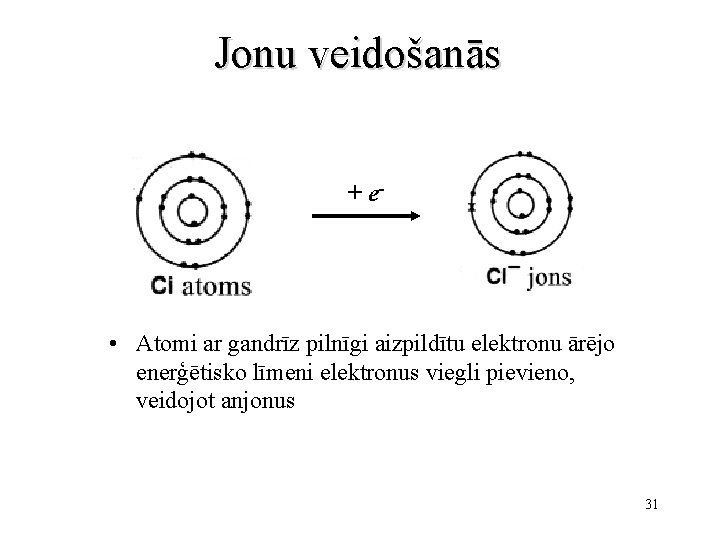
Jonu veidošanās + e- • Atomi ar gandrīz pilnīgi aizpildītu elektronu ārējo enerģētisko līmeni elektronus viegli pievieno, veidojot anjonus 31

Jonu saites veidošanās • Ārējais nātrija atoma elektrons tiek pārnests uz hlora atoma ārējo elektronu čaulu • Atdoto vai pieņemto elektronu skaits nosaka elementa vērtību • Nātrijs (vienmēr) un hlors (parasti) ir vienvērtīgi elementi • Starp lādētajiem joniem veidojas elektrostatiska mijiedarbība, kuru sauc par jonu saiti 32

Jonu saite kristāliskā stāvoklī • Cietā agregātstāvoklī nātrija hlorīda kristāla struktūru veido elektrostatiskas mijiedarbības starp pretēji lādētiem joniem. 33
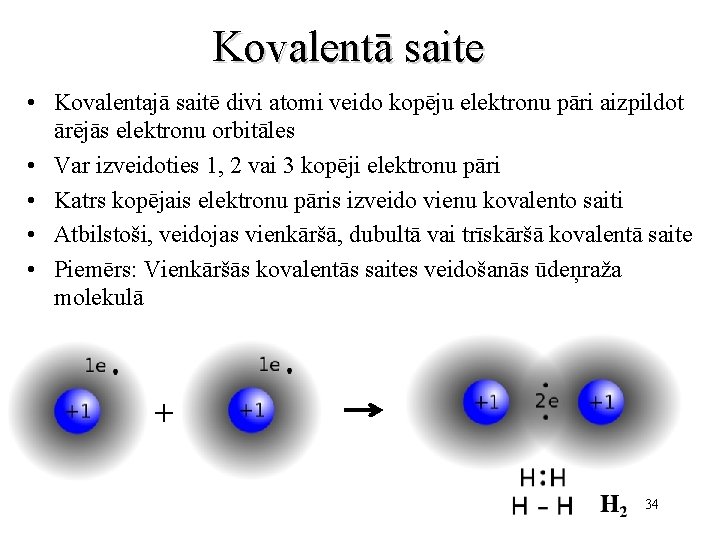
Kovalentā saite • Kovalentajā saitē divi atomi veido kopēju elektronu pāri aizpildot ārējās elektronu orbitāles • Var izveidoties 1, 2 vai 3 kopēji elektronu pāri • Katrs kopējais elektronu pāris izveido vienu kovalento saiti • Atbilstoši, veidojas vienkāršā, dubultā vai trīskāršā kovalentā saite • Piemērs: Vienkāršās kovalentās saites veidošanās ūdeņraža molekulā + 34
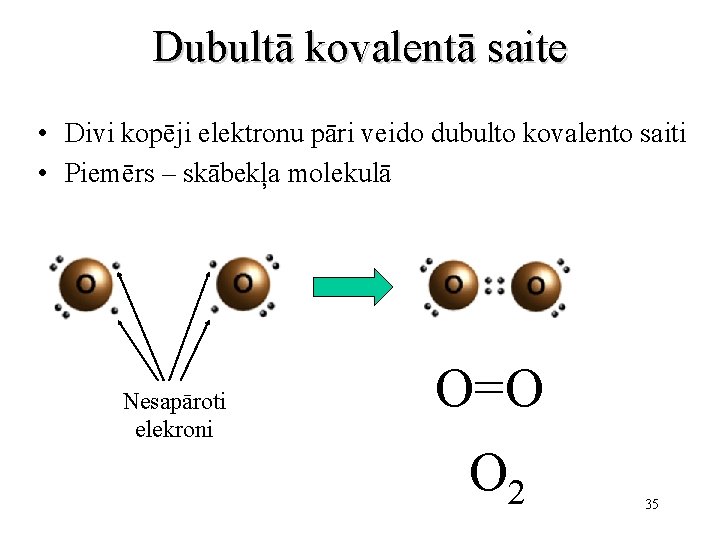
Dubultā kovalentā saite • Divi kopēji elektronu pāri veido dubulto kovalento saiti • Piemērs – skābekļa molekulā Nesapāroti elekroni O=O O 2 35
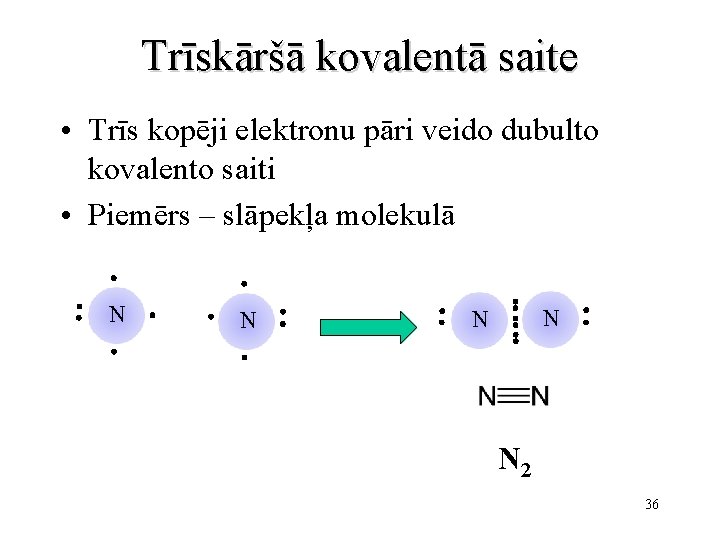
Trīskāršā kovalentā saite • Trīs kopēji elektronu pāri veido dubulto kovalento saiti • Piemērs – slāpekļa molekulā N N N 2 36
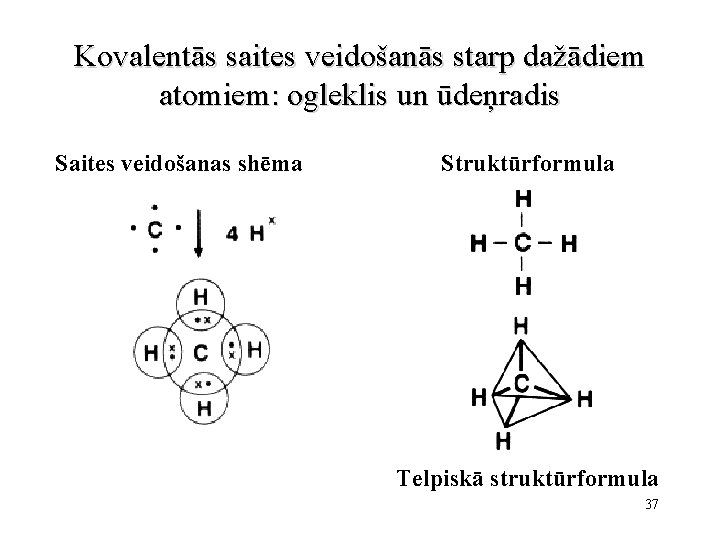
Kovalentās saites veidošanās starp dažādiem atomiem: ogleklis un ūdeņradis Saites veidošanas shēma Struktūrformula Telpiskā struktūrformula 37

Polārās un nepolārās kovalentās saites • Dažādiem atomiem piemīt dažādas elektronegativitātes – t. i. , tieksme piesaistīt elektronu • Ja kovalentā saite veidojas starp atomiem ar līdzīgām elektronegativitātēm, kopējais elektronu pāris veidojas pa vidu starp atomiem (piemēram C-C, C-H). Izveidojas nepolārā kovalentā saite • Ja abiem atomiem ir atšķirīgas elektronegativitātes, elektronu pāris nobīdās uz elektronegatīvākā atoma pusi un veidojas daļēji lādiņi (piemēram, N-H, O-H, C-O). Izveidojas polārā kovalentā saite • Ja elektronegativitātes ir ļoti atšķirīgas, veidojas jonu saite 38
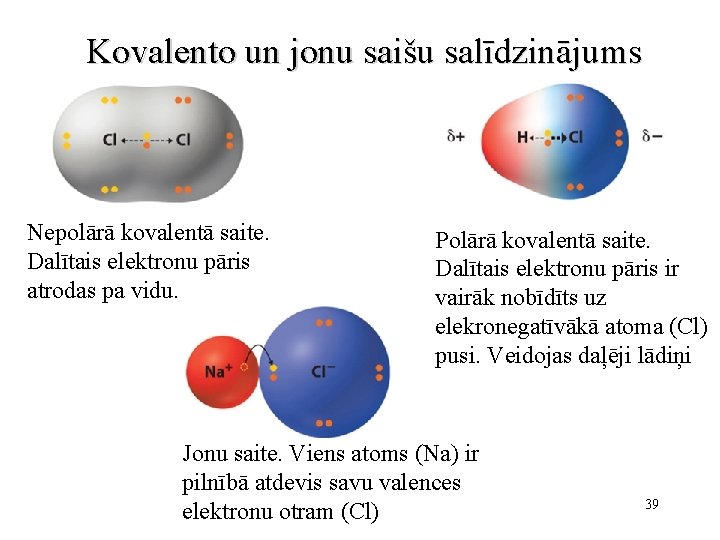
Kovalento un jonu saišu salīdzinājums Nepolārā kovalentā saite. Dalītais elektronu pāris atrodas pa vidu. Polārā kovalentā saite. Dalītais elektronu pāris ir vairāk nobīdīts uz elekronegatīvākā atoma (Cl) pusi. Veidojas daļēji lādiņi Jonu saite. Viens atoms (Na) ir pilnībā atdevis savu valences elektronu otram (Cl) 39
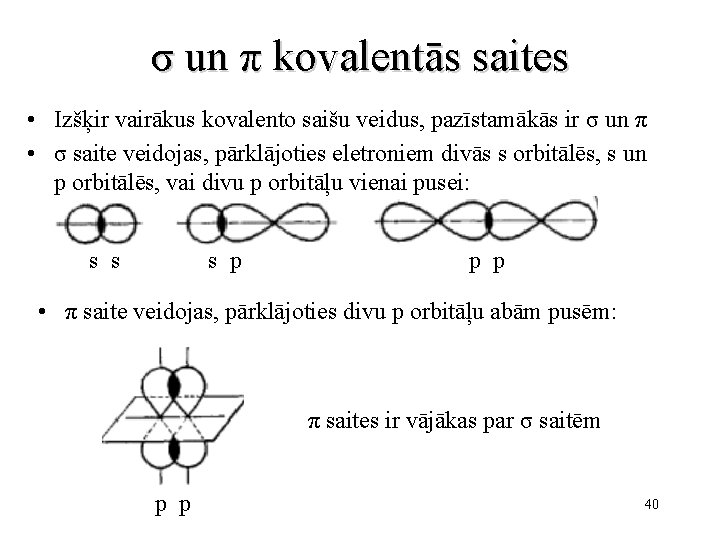
σ un π kovalentās saites • Izšķir vairākus kovalento saišu veidus, pazīstamākās ir σ un π • σ saite veidojas, pārklājoties eletroniem divās s orbitālēs, s un p orbitālēs, vai divu p orbitāļu vienai pusei: s p s s p p • π saite veidojas, pārklājoties divu p orbitāļu abām pusēm: π saites ir vājākas par σ saitēm p p 40
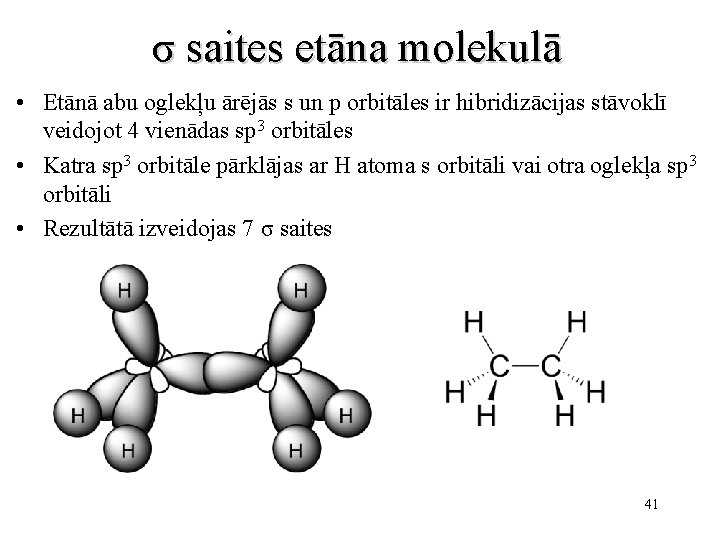
σ saites etāna molekulā • Etānā abu oglekļu ārējās s un p orbitāles ir hibridizācijas stāvoklī veidojot 4 vienādas sp 3 orbitāles • Katra sp 3 orbitāle pārklājas ar H atoma s orbitāli vai otra oglekļa sp 3 orbitāli • Rezultātā izveidojas 7 σ saites 41
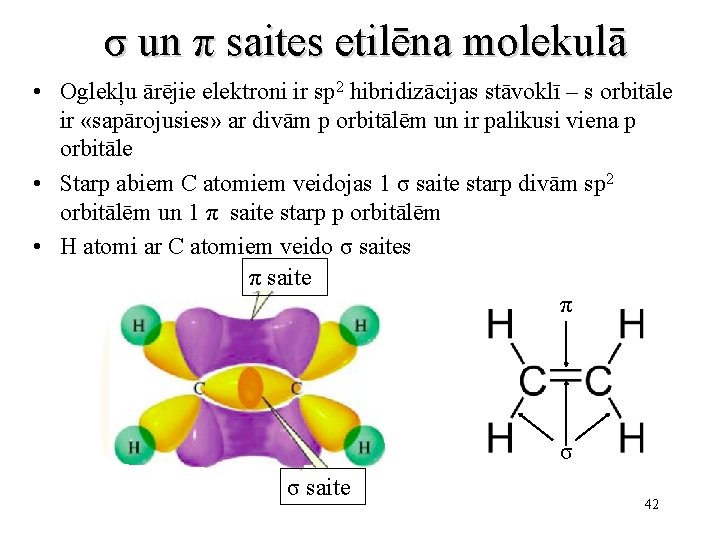
σ un π saites etilēna molekulā • Oglekļu ārējie elektroni ir sp 2 hibridizācijas stāvoklī – s orbitāle ir «sapārojusies» ar divām p orbitālēm un ir palikusi viena p orbitāle • Starp abiem C atomiem veidojas 1 σ saite starp divām sp 2 orbitālēm un 1 π saite starp p orbitālēm • H atomi ar C atomiem veido σ saites π saite π σ σ saite 42

Nekovalentās mijiedarbības starp molekulām • Bioķīmiskajos procesos ļoti liela nozīme ir dažādām salīdzinoši vājām elektrostatiskajām mijiedarbībām starp atomiem • Bioloģiskās makromolekulas sastāv no ļoti daudziem atomiem, tāpēc atomu vājās mijiedarbības summējas un kļūst nozīmīgas 43
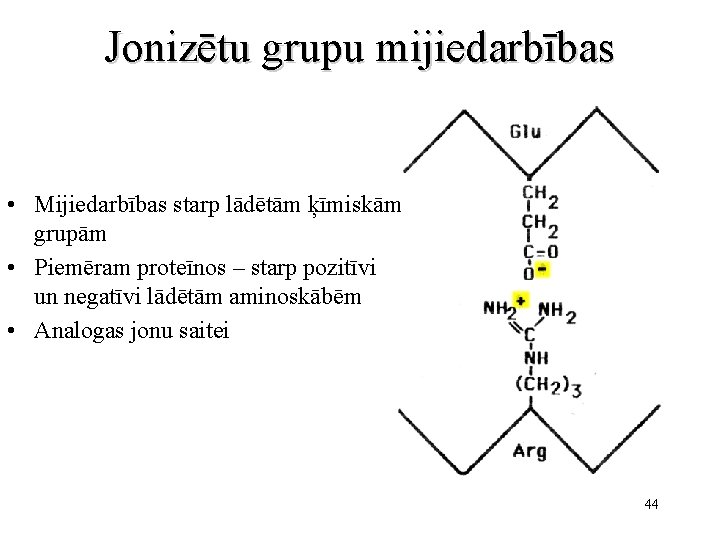
Jonizētu grupu mijiedarbības • Mijiedarbības starp lādētām ķīmiskām grupām • Piemēram proteīnos – starp pozitīvi un negatīvi lādētām aminoskābēm • Analogas jonu saitei 44

Van der Vālsa spēki • Definēti kā jebkura mijiedarbība starp molekulām, atšķirīga no kovalentās vai jonu mijiedarbības • Teorētiski H-saites arī ir van der Vālsa spēku paveids, bet tās ir daudz stiprākas par citiem van der Vālsa spēkiem, tādēļ tās parasti klasificē atsevišķi • Molekulām, kuru sastāvā ir atomi ar atšķirīgām elektronegativitātēm, veidojas permanentie dipoli ar daļējiem lādiņiem • Pat ja elektronegativitātes ir vienādas, tomēr fluktuāciju dēļ izveidojas īslaicīgi dipoli, kuri var inducēt dipolu blakus esošajā molekulā Gekonu spēja rāpties pa vertikālām, pilnīgi gludām virsmām tiek skaidrota ar van der Vālsa spēkiem 45
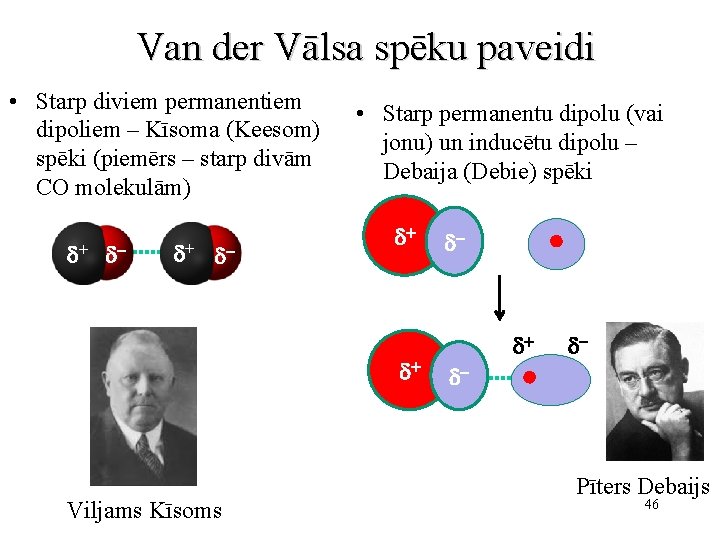
Van der Vālsa spēku paveidi • Starp diviem permanentiem dipoliem – Kīsoma (Keesom) spēki (piemērs – starp divām CO molekulām) d+ d- • Starp permanentu dipolu (vai jonu) un inducētu dipolu – Debaija (Debie) spēki d+ d+ Viljams Kīsoms d- d+ d- d- Pīters Debaijs 46
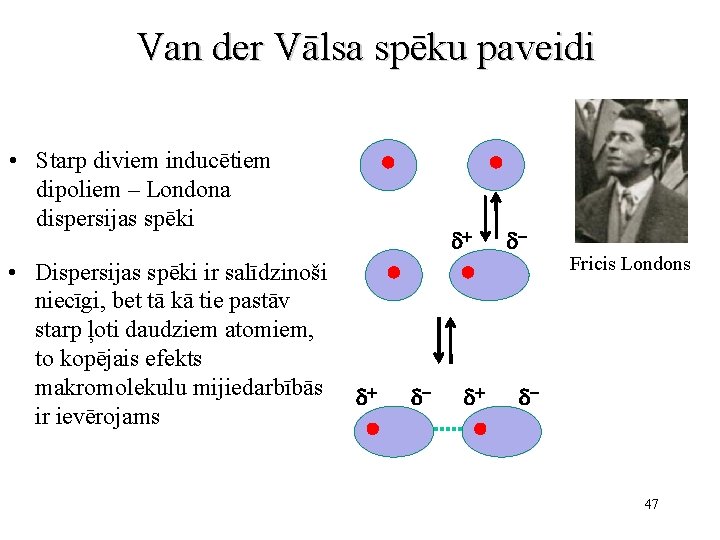
Van der Vālsa spēku paveidi • Starp diviem inducētiem dipoliem – Londona dispersijas spēki • Dispersijas spēki ir salīdzinoši niecīgi, bet tā kā tie pastāv starp ļoti daudziem atomiem, to kopējais efekts makromolekulu mijiedarbībās ir ievērojams d+ d+ d- Fricis Londons d- 47
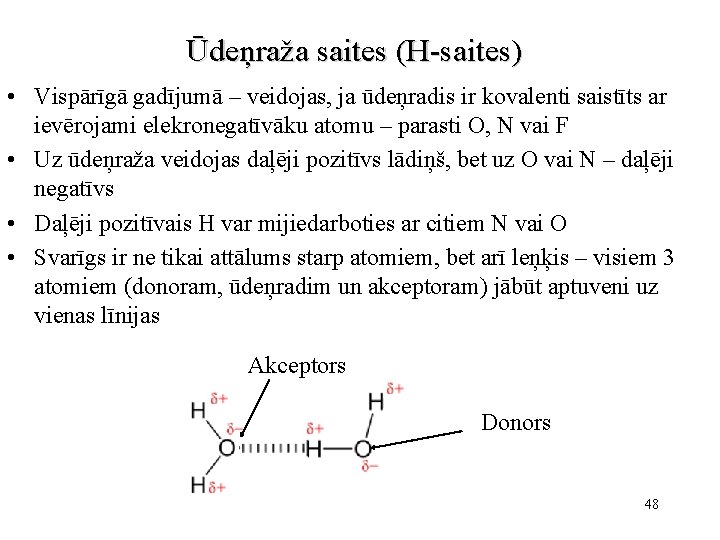
Ūdeņraža saites (H-saites) • Vispārīgā gadījumā – veidojas, ja ūdeņradis ir kovalenti saistīts ar ievērojami elekronegatīvāku atomu – parasti O, N vai F • Uz ūdeņraža veidojas daļēji pozitīvs lādiņš, bet uz O vai N – daļēji negatīvs • Daļēji pozitīvais H var mijiedarboties ar citiem N vai O • Svarīgs ir ne tikai attālums starp atomiem, bet arī leņķis – visiem 3 atomiem (donoram, ūdeņradim un akceptoram) jābūt aptuveni uz vienas līnijas Akceptors Donors 48
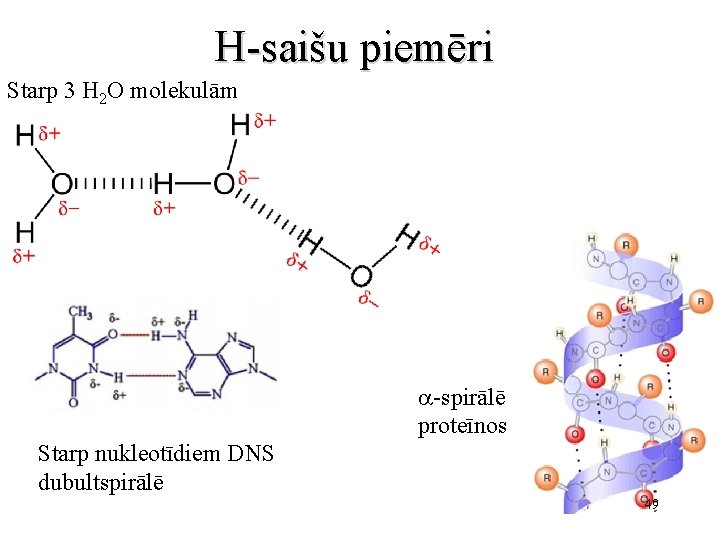
H-saišu piemēri Starp 3 H 2 O molekulām a-spirālē proteīnos Starp nukleotīdiem DNS dubultspirālē 49

Ūdens H 2 O 50
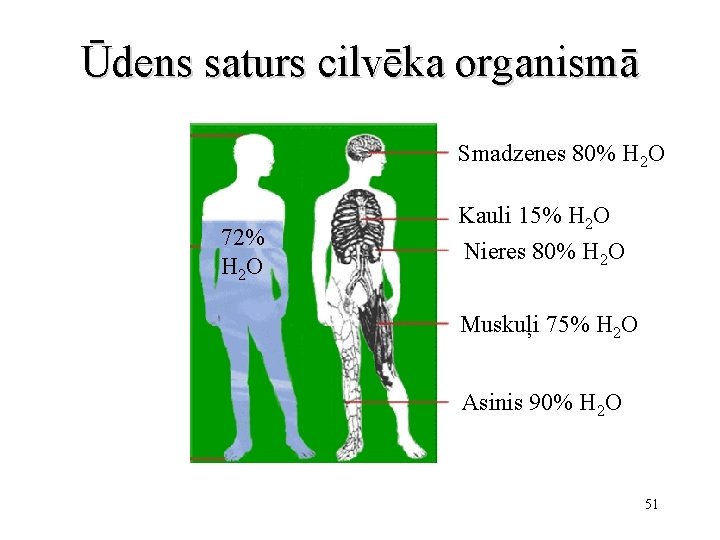
Ūdens saturs cilvēka organismā Smadzenes 80% H 2 O 72% H 2 O Kauli 15% H 2 O Nieres 80% H 2 O Muskuļi 75% H 2 O Asinis 90% H 2 O 51

Ar ko ūdens ir īpašs? • • • Polārs šķīdinātājs Šķidrs bioloģiski nozīmīgās temperatūrās Augsta siltumietilpība un iztvaikošanas siltums Augsts virsmas spraigums Cietā agregātstāvoklī vieglāks, nekā šķidrā 52
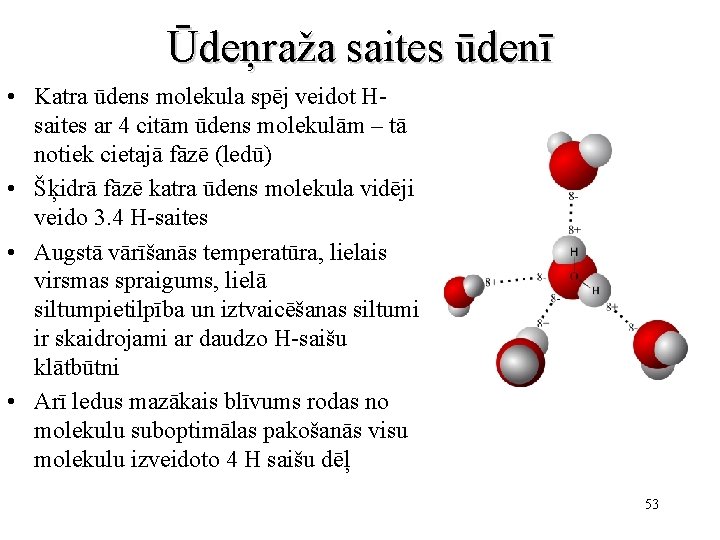
Ūdeņraža saites ūdenī • Katra ūdens molekula spēj veidot Hsaites ar 4 citām ūdens molekulām – tā notiek cietajā fāzē (ledū) • Šķidrā fāzē katra ūdens molekula vidēji veido 3. 4 H-saites • Augstā vārīšanās temperatūra, lielais virsmas spraigums, lielā siltumpietilpība un iztvaicēšanas siltumi ir skaidrojami ar daudzo H-saišu klātbūtni • Arī ledus mazākais blīvums rodas no molekulu suboptimālas pakošanās visu molekulu izveidoto 4 H saišu dēļ 53

Hidrofobais efekts H 2 O • Hidrofobais (“bailes no ūdens”) efekts ir novērojams, jebkuru nepolāru savienojumu sajaucot ar ūdeni • Kontakti starp polārām un nepolārām molekulām ir enerģētiski neizdevīgi • Tāpēc nepolārās molekulas agregējas kopā, lai minimizētu kontaktus 54 ar polārajām molekulām
- Slides: 54