EnzimoloijaMetabolisms Lekcijas saturs Brvo radiklu procesi Oksidatvais stress

Enzimoloģija/Metabolisms Lekcijas saturs: Brīvo radikālu procesi. Oksidatīvais stress. Lipīdu peroksidācija. Antioksidanti. Selenoproteīni. Slāpekļa oksīda sintāzes Molekulāras bioloģijas (bioķīmijas)katedra 2009/2010. akad. gads

Oksidoreduktāžu klasifikācija I 1. 1. Iedarbojas ar donora - OH grupu 1. 2. Iedarbojas ar donora aldehīd- vai ketogrupu 1. 2. 3. 2. Ksantīnoksidāze 1. 3. Iedarbojas uz CH-CH grupām 1. 3. 99. 1. Sukcinātdehidrogenāze 1. 9. Iedarbojas ar donora hēma grupu 1. 9. 3. 1. Citohromoksidāze 1. 11. Iedarbojas ar peroksīdu kā akceptoru 1. 1. 6. Katalāze 1. 1. 7. Peroksidāze 1. 13. Iedarbojas ar vienu donoru, ieslēdzot molekulāru skābekli - oksigenāzes (dioksigenāzes) 1. 13. 11. Triptofān -2, 3 dioksigenāze 1. 13. 11. 12. Lipoksigenāze

Oksidoreduktāžu klasifikācija II 1. 14. Iedarbojas ar diviem donoriem, ieslēdzot molekulāru skābekļa vienu atomu substrātā, bet otru “ūdenī”-monooksigenāzes 1. 14. Otrs donors ir flavoproteīns 1. 14. 1. Nespecifiskā monooksigenāze, mikrosomu P 450 1. 14. 16. Otrs donors ir pteridīns 1. 14. 16. 1. Fenīlalanīn-tetrehidrobiopterīn: O 2 -oksidoreduktāze 1. 14. 17. Otrs donors ir askorbāts 1. 14. 17. 1. Dopamīna monooksigenāze 1. 15. Darbojas uz superoksīda radikālu kā akceptoru 1. 15. 1. 1. Superoksīddismutāze 1. 19.

Reaktīvās skābekļa formas Reactive oxygen species ROS
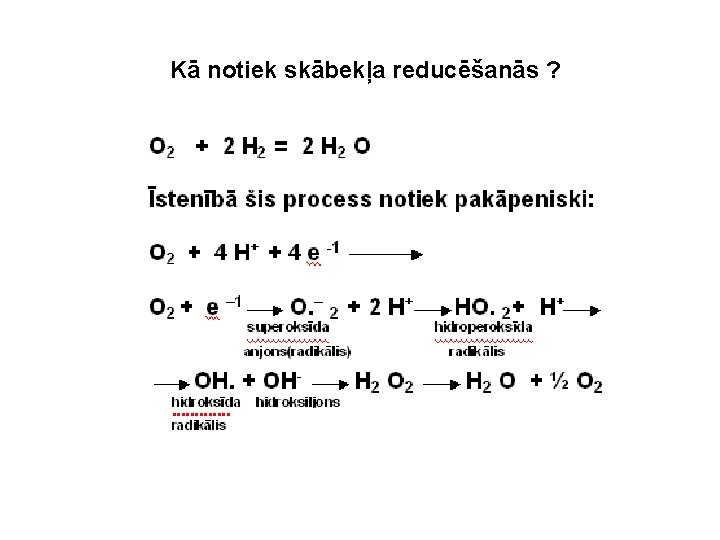
Kā notiek skābekļa reducēšanās ?

Reakciju piemēri, kurās veidojas brīvie radikāli 1. Eritrocītos pie hemoglobīna oksidācijas līdz methemoglobīnam 2. Citohroma P 450 reduktāzes gaitā 3. Ksantīnoksidāzes reakcijā (K. F. 1. 2. 3. 22)(agrāk K. F. 1. 2. 3. 2) 4. NADPH oksidāze neitrofīlajos leikocītos - nozīme fagocitozē 5. Fentona reakcija (neenzimātiska) 6. Harbera-Veisa reakcija, Fe katalizēta 7. Slāpekļa oksīda veidošanās un darbība
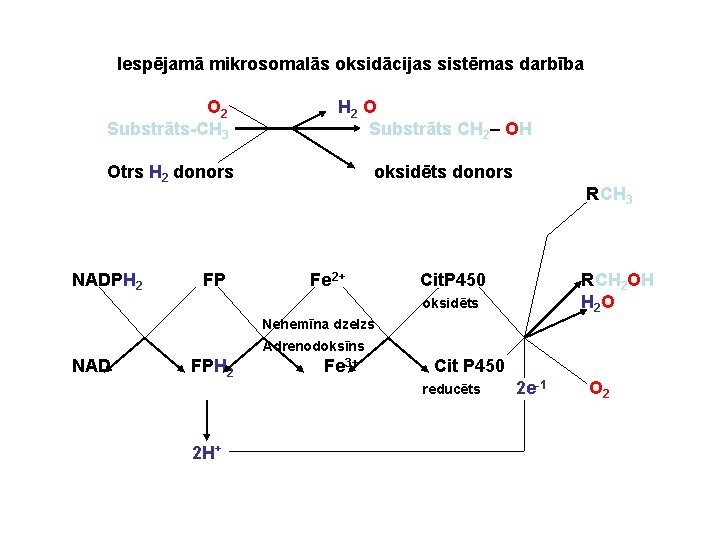
Iespējamā mikrosomalās oksidācijas sistēmas darbība O 2 Substrāts-CH 3 H 2 O Substrāts CH 2– OH Otrs H 2 donors NADPH 2 FP oksidēts donors RCH 3 Fe 2+ Cit. P 450 RCH 2 OH H 2 O oksidēts Nehemīna dzelzs Adrenodoksīns NAD FPH 2 Fe 3+ Cit P 450 reducēts 2 H+ 2 e-1 O 2

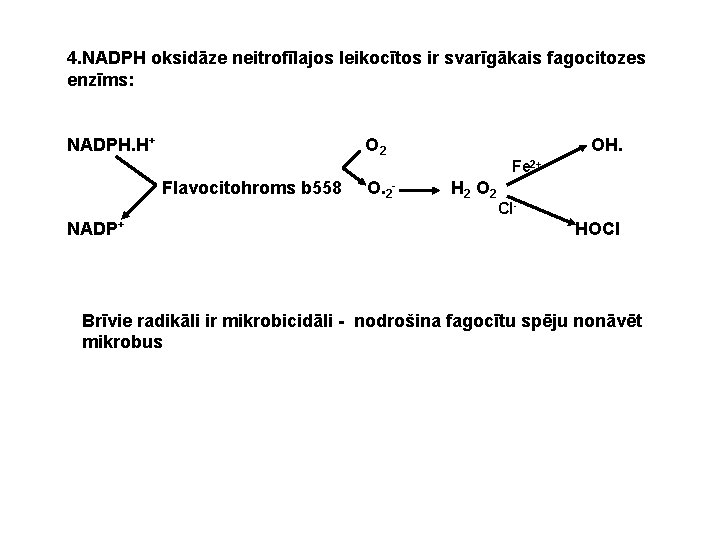
4. NADPH oksidāze neitrofīlajos leikocītos ir svarīgākais fagocitozes enzīms: NADPH. H+ O 2 OH. Fe 2+ Flavocitohroms b 558 NADP+ O. 2 - H 2 O 2 Cl- HOCl Brīvie radikāli ir mikrobicidāli - nodrošina fagocītu spēju nonāvēt mikrobus

Galvenās reakcijas, kuras eliminē brīvos radikālus 1. Spontānā dismutācija 2. Superoksīddismutāzes reakcija (K. F. 1. 15. 1. 1. ) 3. Glutationperoksidāze (K. F. 1. 1. 9. ) 4. Peroksidāze (K. F. 1. 1. 7. ) 6. Katalāze (K. F. 1. 1. 6. ) 7. Neitrofīlo leikocītu mieloperoksidāze




Selenoproteīni Visos selenoproteīnos selēns iesaistās kā selenocisteīns HSe- CH 2 CHNH 2 COOH Oksidoreduktāzēs selenocisteīns ietilpst aktīvajā centrā Atsevišķos proteīnos terminācijas kodona UGA vietā inkorporē selenocisteīnu 1. Glutationperoksidāze (GPx) ar līdzīgu aktivitāti izšķir 2 enzīmus : KF. 1. 1. 9. un KF. 1. 1. 12 eksistē arī vairākas izoformas a) cellulārā GPx b) fosfolipīdu GPx (apzīmē PH-GPx) c) ekstracellulārā GPx d) gastrointestināla Gi-GP 2. Iodtironīndejodināze KF. 3. 8. 1. 4 vismaz trīs tipi L-tiroksīns + ūdens 3, 5, 3 -trijodtironīns + jodīds 3. Tioredoksīn reduktāze KF. 1. 8. 1. 9. (Piedalās ribozes reducēšanā par dezoksiribozi) 4. Plazmas selenoproteīns P (50% plazmas selēna, satur 10 selēna atomus) 5. Muskuļu selenoproteīns W


Bioķīmiskās metodes ROS analīzēm 1. Hemiluminescences pētījumi dažādos objektos un metodes dažādie varianti 2. Konjugēto diēnu noteikšana 3. Malonskābes dialdehīda noteikšana ar tiobarbitūrskābi 5. Enzīmu aktivitātes: a) superoksīddismutāze b) katalāze c) glutationreduktāze d) glutationperoksidāze 6. Selēna daudzums

Dabīgie organisma antioksidanti

Reaktīvās slāpekļa formas Reactive nitrogen species RNS

Slāpekļa oksīda sintāzes Slāpekļa monoksīds. . NO , ko parasti sauc par slāpekļa oksīdu ir brīvais radikāls , kurš ģenerējas bioloģiskās sistēmās un darbojās kā signālmolekula daudzos fizioloģiskos procesos asinsspiediena kontrolē, kā neirotranmitters, bet augstā koncentācija kā defensīvs citotoksīns. Tas veidojas no arginīna. EC 1. 14. 13. 39 Nitrīta oksīda sintāze, NO sintetāze, NOS Zīdītajos ir trīs izoenzīmi: n. NOS - NOS 1 - 29 eksoni, 1429 -1433 ask. - smadzenēs, skeleta muskulatūrā i. NOS - NOS 2 - 27 eksoni, 1144 -1153 ask. - šķīstošs, inducējams e. NOS - NOS 1 - 26 eksoni, 1203 -1205 ask. - endotēlijā, membrānu asociēts Koenzīmi: 1) FAD 2) FMN 3) Hēms 4) Tetrahidrobiopterīns 5) Ca+- kalmodulīns (Ca. M) Katalizētā reakcija: NH 2 Arg-C +NADPH 2+O 2 Oksiarginīns-C +1/2 NADPH 2+O 2 NH N-OH . NO + citrulīns



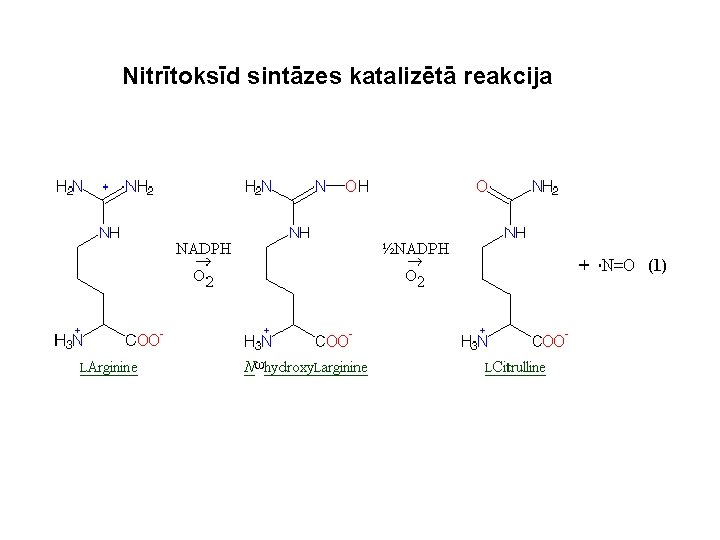
Nitrītoksīd sintāzes katalizētā reakcija

Zīdītāju nitrītoksīd sintāzes, to gēni un īpašības
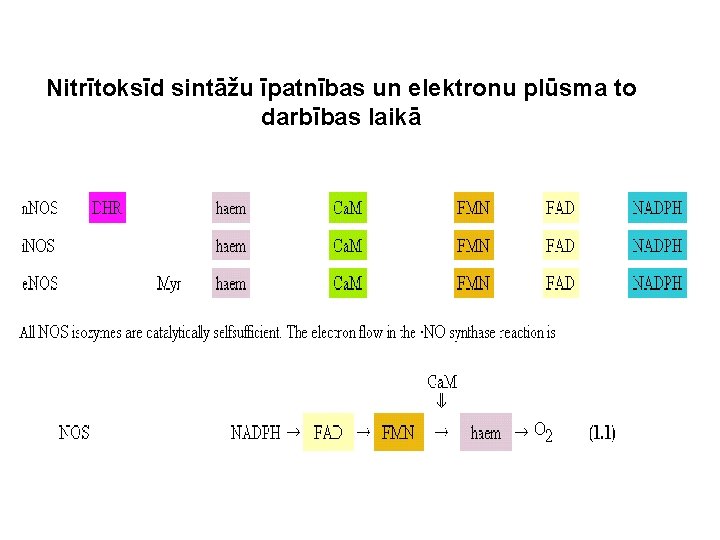
Nitrītoksīd sintāžu īpatnības un elektronu plūsma to darbības laikā
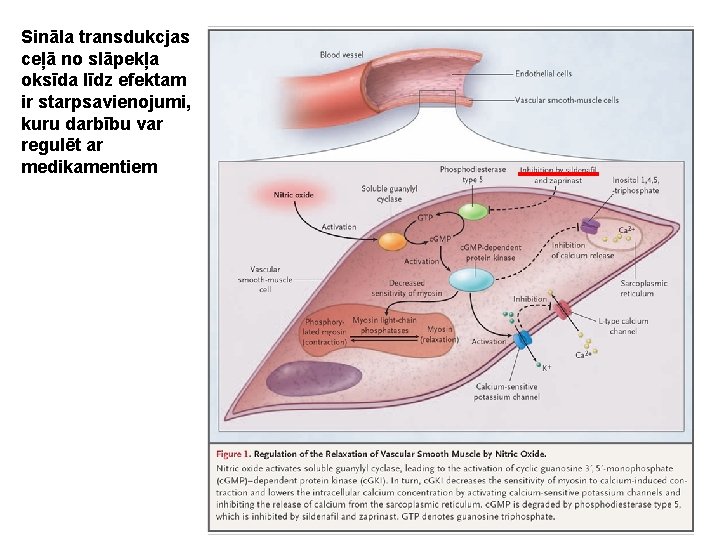
Sināla transdukcjas ceļā no slāpekļa oksīda līdz efektam ir starpsavienojumi, kuru darbību var regulēt ar medikamentiem

- Slides: 27