Dzvbas mija 3 lekcija Lekcijas saturs p H

Dzīvības ķīmija 3. lekcija

Lekcijas saturs • • • p. H, buferšķīdumi Organiskie savienojumi, to funkcionālās grupas Aminoskābes Ogļhidrāti Nukleotīdi
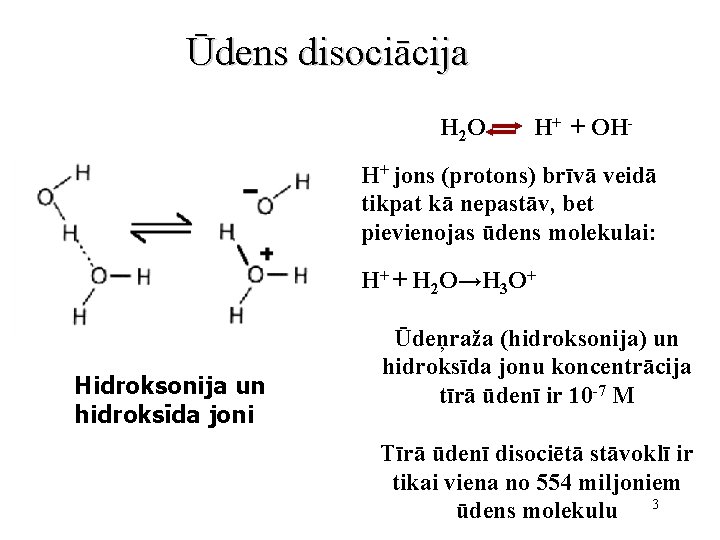
Ūdens disociācija H 2 O H+ + OH- H+ jons (protons) brīvā veidā tikpat kā nepastāv, bet pievienojas ūdens molekulai: H+ + H 2 O→H 3 O+ Hidroksonija un hidroksīda joni Ūdeņraža (hidroksonija) un hidroksīda jonu koncentrācija tīrā ūdenī ir 10 -7 M Tīrā ūdenī disociētā stāvoklī ir tikai viena no 554 miljoniem ūdens molekulu 3

Skābes • Skābes palielina H+ jonu koncentrāciju šķīdumā • Vājas skābes disociē (sadalās) jonos tikai daļēji, stipras – gandrīz pilnīgi Stipras Vājas HCl H+ + Cl. CH 3 COOH H+ + CH 3 COO- etiķskābe acetāta jons, konjugētā (saistītā) bāze 4
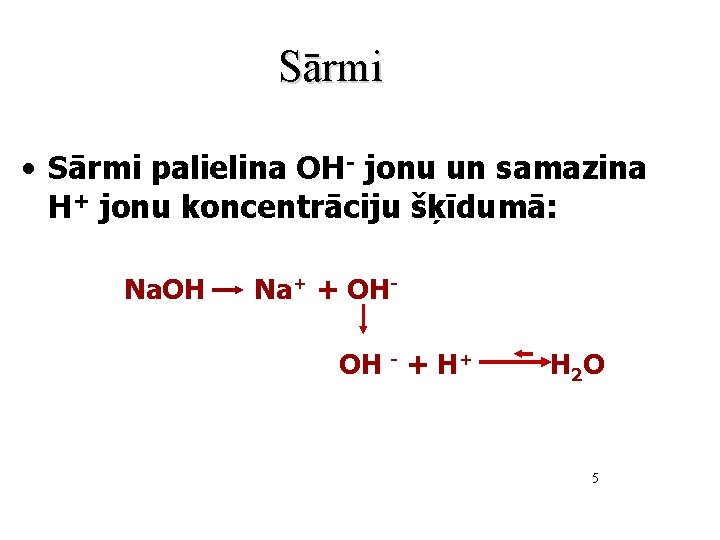
Sārmi • Sārmi palielina OH- jonu un samazina H+ jonu koncentrāciju šķīdumā: Na. OH Na+ + OHOH - + H+ H 2 O 5
![p. H • p. H = - log [H+] • Tīrā ūdenī p. H p. H • p. H = - log [H+] • Tīrā ūdenī p. H](http://slidetodoc.com/presentation_image_h2/9c1cc6b82f2d92d36542d952e64171dc/image-6.jpg)
p. H • p. H = - log [H+] • Tīrā ūdenī p. H = -log 10 -7 =7 • Pieliekot skābi, H+ jonu koncentrācija pieaug (un p. H samazinās) skābes disociācijas dēļ: • HCl → H+ + Cl • Pieliekot sārmu, H+ jonu koncentrācija samazinās (un p. H palielinās), jo: • 1) Sārms disociē: Na. OH → Na+ + OH • 2) OH- joni reaģē ar šķīdumā esošajiem H+ joniem: H+ + OH- → H 2 O 6

Ūdens jonu reizinājums • Šķīdumos H+ un OH- koncentrācija ir savstarpēji saistīta • Palielinot vienu, otra tikpat reižu samazinās • Abu koncentrāciju reizinājums ir konstants lielums: [H+] · [OH-] = 10 -14 M 2 • Tādejādi, zinot H+ jonu koncentrāciju, vienmēr var izrēķināt OH- jonu koncentrāciju un otrādi 7

p. H aprēķins stiprai skābei • Stipras skābes ūdenī disociē gandrīz pilnīgi • Tātad, H+ jonu koncentrācija ir tāda pati, kā skābei un var tieši aprēķināt p. H • Piemēram, 0. 1 M sālsskābē H+ jonu koncentrācija arī ir 0. 1 M, tātad: • p. H = -log 0. 1 = 1 8

p. H aprēķins stiprai bāzei • Stipras bāzes ūdenī disociē gandrīz pilnīgi • Tātad, OH- jonu koncentrācija ir tāda pati, kā bāzei • Zinot OH- jonu koncentrāciju, H+ jonu koncentrāciju var aprēķināt no ūdens jonu reizinājuma (10 -14 M 2) • Piemēram, 0. 1 M Na. OH OH- jonu koncentrācija arī ir 0. 1 M, tātad: • [H+] = 10 -14/0. 1 = 10 -13 • p. H = -log 10 -13 = 13 9
![Skābju stiprumu raksturo skābes disociācijas konstante p. Ka HA ↔ H+ + A- Ka=[H+][A-]/[HA] Skābju stiprumu raksturo skābes disociācijas konstante p. Ka HA ↔ H+ + A- Ka=[H+][A-]/[HA]](http://slidetodoc.com/presentation_image_h2/9c1cc6b82f2d92d36542d952e64171dc/image-10.jpg)
Skābju stiprumu raksturo skābes disociācijas konstante p. Ka HA ↔ H+ + A- Ka=[H+][A-]/[HA] p. Ka=-log[Ka] • Jo mazāks p. Ka, jo stiprāka skābe. • p. Ka ir skaitliski vienāds ar p. H, pie kura puse skābes molekulu šķīdumā ir disociētā stāvoklī • Div- un trīsvērtīgām skābēm katrai disociācijas stadijai ir savs p. Ka H 3 PO 4 H 2 PO 4 - + H+ HPO 42 - + H+ p. Ka = 1. 8 p. Ka = 7. 2 10
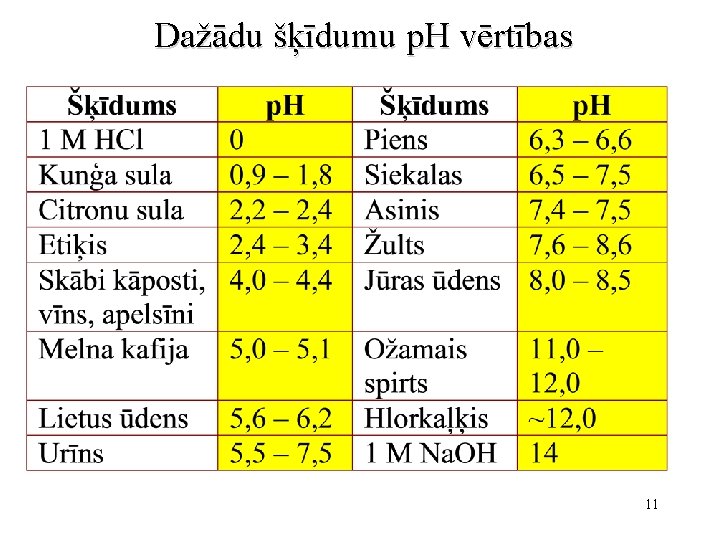
Dažādu šķīdumu p. H vērtības 11

Buferšķīdumi • Vājas skābes un saistītās (konjugētās) bāzes šķīdumi, kas spēj pretoties straujām p. H izmaiņām, pievienojot nelielus stipras skābes vai sārma daudzumus vai atšķaidot ar ūdeni • Buferšķīdumi pastāv arī bioloģiskos organismos, jo bioķīmisku reakciju norisei ir nepieciešams optimāls p. H 12

Buferēšanās iemesli Piemērs: Acetāta buferis sastāv no etiķskābes un nātrija acetāta Etiķskābe ir vāja skābe, tāpēc līdzsvars ir nobīdīts pa kreisi (t. i. šķīdumā tā vairāk ir nedisociētā formā): CH 3 COOH H+ + CH 3 COO- Papildus pieliktie acetāta joni līdzsvaru nobīda vēl vairāk pa kreisi: - CH 3 COOH CH 3 COO H+ + CH 3 COO- Rezultātā, šķīdumā ir daudz acetāta jonu, daudz nedisociētas etiķskābes un maz ūdeņraža jonu 13
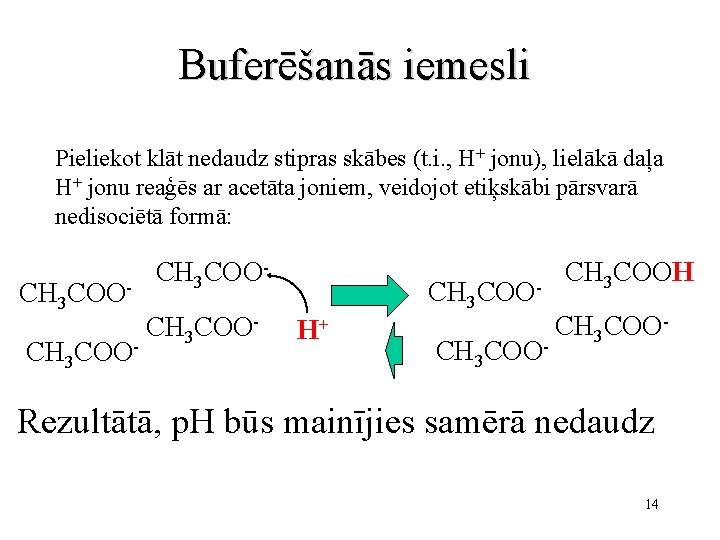
Buferēšanās iemesli Pieliekot klāt nedaudz stipras skābes (t. i. , H+ jonu), lielākā daļa H+ jonu reaģēs ar acetāta joniem, veidojot etiķskābi pārsvarā nedisociētā formā: CH 3 COO- CH 3 COOCH 3 COO- CH 3 H+ COO- CH 3 COOH CH 3 COO- Rezultātā, p. H būs mainījies samērā nedaudz 14
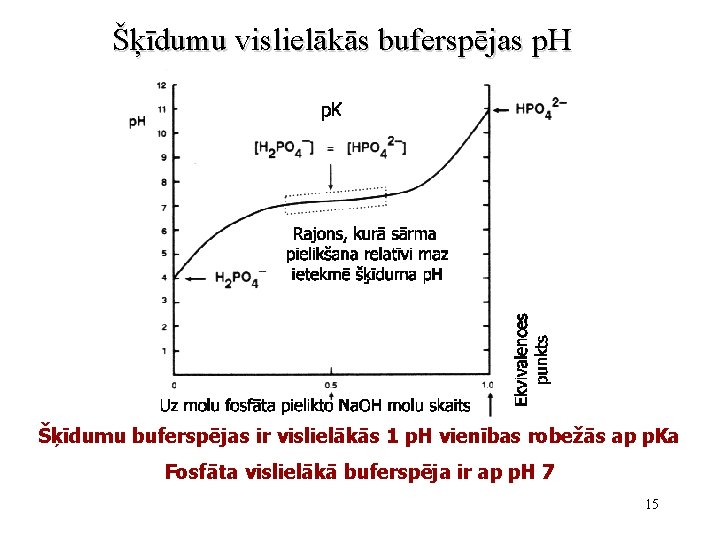
Šķīdumu vislielākās buferspējas p. H Šķīdumu buferspējas ir vislielākās 1 p. H vienības robežās ap p. Ka Fosfāta vislielākā buferspēja ir ap p. H 7 15

Bikarbonāta bufersistēma • Bikarbonāta bufersistēma notur asins p. H robežās no 7. 3 līdz 7. 5 • Dzīvībai bīstami simptomi parādās pie relatīvi nelielām izmaiņām – zem p. H 7. 0 vai virs p. H 7. 8 16

Fosfāta bufersistēma • Fosfāta bufersistēma regulē iekššūnas p. H robežās no 6. 9 līdz 7. 4 • Fosfāta bufersistēmu bieži izmanto dažādiem in vitro eksperimentiem – piemēram, enzimātiskām reakcijām 17

Organisko savienojumu vispārīgās īpašības • Molekulas veido oglekļa atomu ķēdes • Pie oglekļa atomiem var būt piesaistītas dažādas funkcionālās grupas • Funkcionālajām grupām ir raksturīgas noteiktas ķīmiskās īpašības 18

Ogļūdeņraži • Organiskie savienojumi, kuri sastāv tikai no oglekļa un ūdeņraža atomiem • Piesātinātie ogļūdeņraži (alkāni) satur tikai vienkāršās saites • Piesātinātie = piesātināti ar ūdeņradi, satur maksimālo H atomu skaitu CH 4, metāns C 2 H 6 ( CH 3 -CH 3 ), etāns C 4 H 10, ( CH 3 -CH 2 -CH 3 ), butāns 19
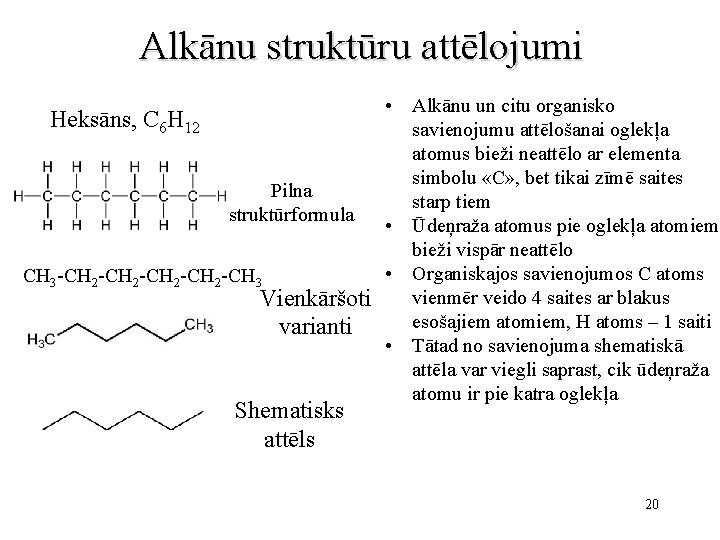
Alkānu struktūru attēlojumi • Alkānu un citu organisko Heksāns, C 6 H 12 savienojumu attēlošanai oglekļa atomus bieži neattēlo ar elementa simbolu «C» , bet tikai zīmē saites Pilna starp tiem struktūrformula • Ūdeņraža atomus pie oglekļa atomiem bieži vispār neattēlo • Organiskajos savienojumos C atoms CH 3 -CH 2 -CH 3 vienmēr veido 4 saites ar blakus Vienkāršoti esošajiem atomiem, H atoms – 1 saiti varianti • Tātad no savienojuma shematiskā attēla var viegli saprast, cik ūdeņraža atomu ir pie katra oglekļa Shematisks attēls 20
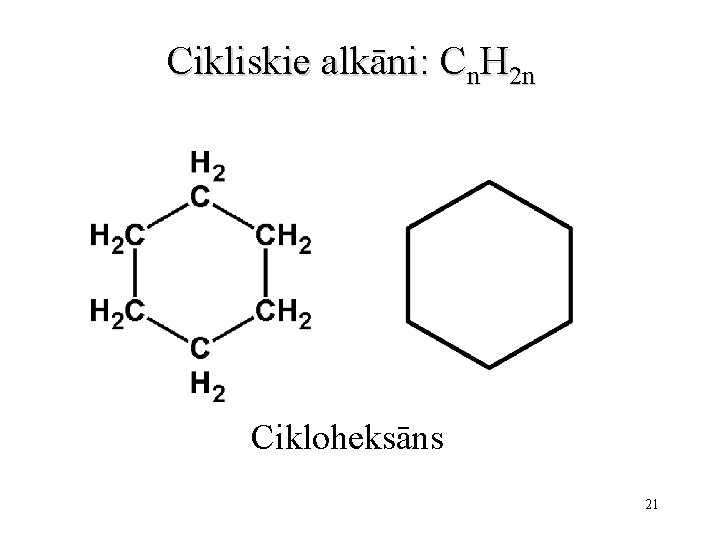
Cikliskie alkāni: Cn. H 2 n Cikloheksāns 21
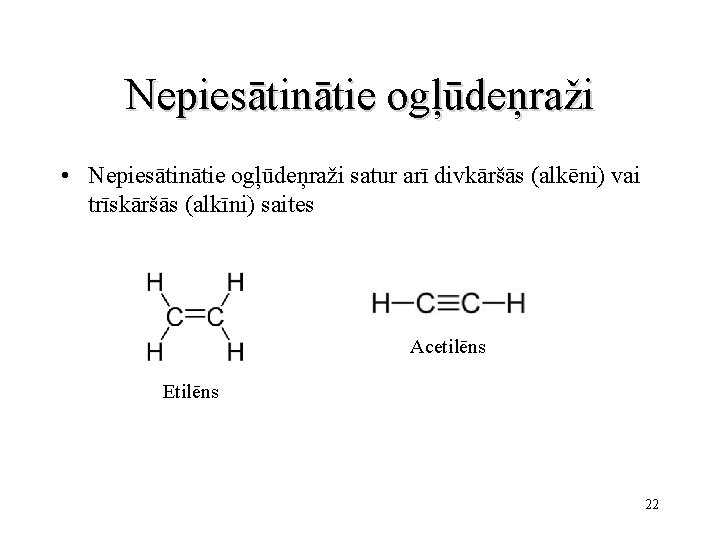
Nepiesātinātie ogļūdeņraži • Nepiesātinātie ogļūdeņraži satur arī divkāršās (alkēni) vai trīskāršās (alkīni) saites Acetilēns Etilēns 22
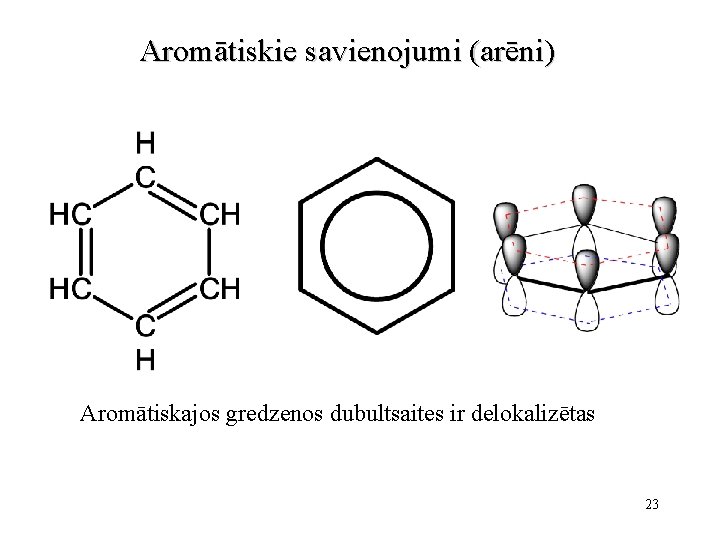
Aromātiskie savienojumi (arēni) Aromātiskajos gredzenos dubultsaites ir delokalizētas 23

Organisko savienojumu izomēri • Strukturālie izomēri – savienojumi ar vienādām kopīgajām formulām, bet dažādā secībā savienotiem atomiem • Stereoizomēri – savienojumi ar vienādām kopīgajām formulām un vienādā secībā savienotiem atomiem, bet atšķirīgu atomu telpisko novietojumu – Cis-trans izomēri – Enantiomēri jeb optiskie izomēri 24

Strukturālie izomēri • Strukturālie izomēri var būt gan ķīmiski līdzīgi, gan arī ļoti atšķirīgi • Piemērs: ir 3 savienojumi ar vispārējo formulu C 3 H 8 O, no kuriem divi ir spirti (ķīmiski līdzīgi), bet trešais – ēteris (ķīmiski atšķirīgs no spirtiem) CH 3 CH OH CH 3 CH 2 CH OH Propilspirts CH 3 CH 2 O CH 3 Metilēteris Izopropilspirts 25
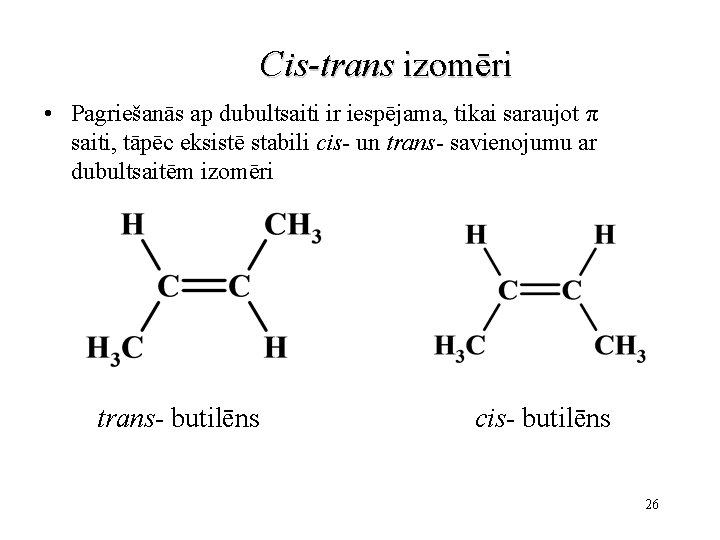
Cis-trans izomēri • Pagriešanās ap dubultsaiti ir iespējama, tikai saraujot π saiti, tāpēc eksistē stabili cis- un trans- savienojumu ar dubultsaitēm izomēri trans- butilēns cis- butilēns 26
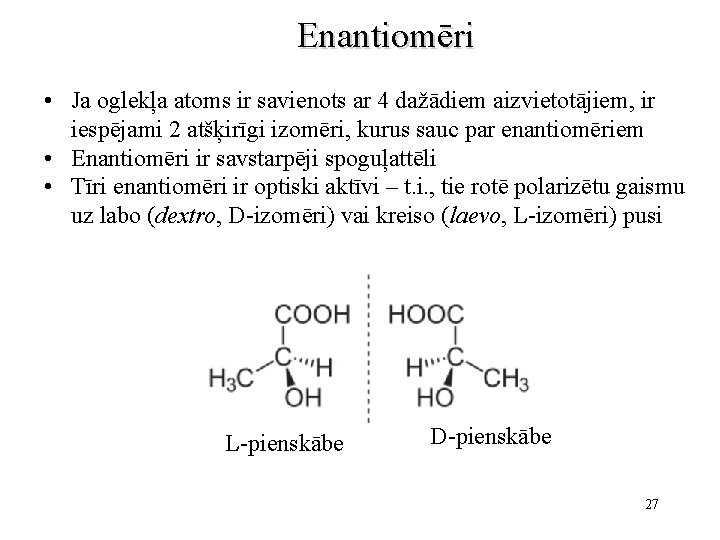
Enantiomēri • Ja oglekļa atoms ir savienots ar 4 dažādiem aizvietotājiem, ir iespējami 2 atšķirīgi izomēri, kurus sauc par enantiomēriem • Enantiomēri ir savstarpēji spoguļattēli • Tīri enantiomēri ir optiski aktīvi – t. i. , tie rotē polarizētu gaismu uz labo (dextro, D-izomēri) vai kreiso (laevo, L-izomēri) pusi L-pienskābe D-pienskābe 27
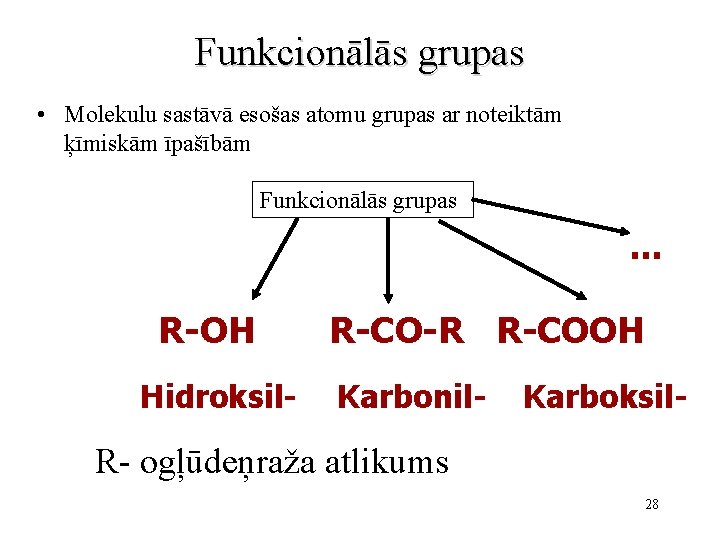
Funkcionālās grupas • Molekulu sastāvā esošas atomu grupas ar noteiktām ķīmiskām īpašībām Funkcionālās grupas . . . R-OH Hidroksil- R-CO-R R-COOH Karbonil- Karboksil- R- ogļūdeņraža atlikums 28

Hidroksilgrupa, spirti • Savienojumus, kuros ogļūdenraža radikālis ir savienots ar hidroksilgrupu sauc par spirtiem R-OH CH 3 -OH Metanols, metilspirts CH 3 -CH 2 -OH Etanols, etilspirts 29

Karbonilgrupa, aldehīdi • Savienojumus, kuros karbonilgrupa ir savienota ar vienu ūdeņraža atomu un vienu ogļūdeņraža radikāli sauc par aldehīdiem R C=O Karbonilgrupa H C=O H Metanāls, formaldehīds C=O H Aldehīds CH 3 C=O H Etanāls, acetaldehīds 30

Karbonilgrupa, ketoni • Savienojumus, kuros karbonilgrupa ir savienota ar diviem ogļūdeņražu radikāļiem sauc par ketoniem R C=O R’ Ketons CH 3 C=O CH 3 Dimetilketons, acetons 31
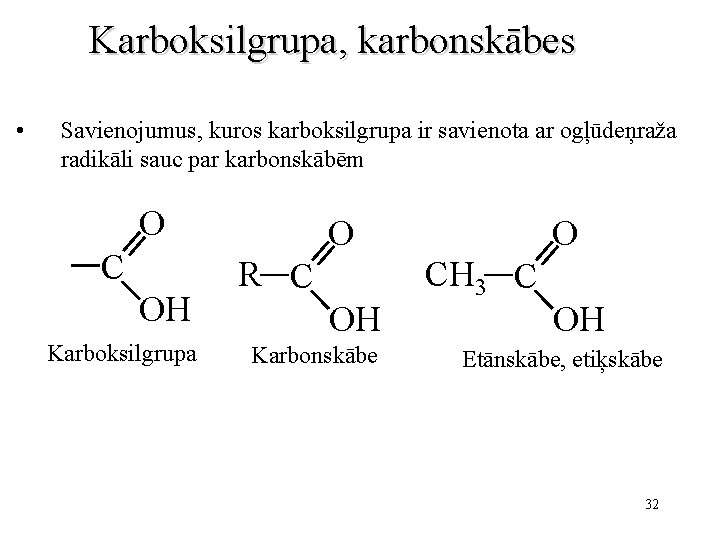
Karboksilgrupa, karbonskābes • Savienojumus, kuros karboksilgrupa ir savienota ar ogļūdeņraža radikāli sauc par karbonskābēm O C OH Karboksilgrupa O R C OH Karbonskābe O CH 3 C OH Etānskābe, etiķskābe 32

Amīni, aminogrupa • Amīni ir amonjaka atvasinājumi, kur viens, divi vai trīs ūdeņraža atomi ir aizvietoti ar ogļūdeņraža radikāli (pirmējie, otrējie un trešējie amīni) • Aminogrupa ir pirmējo amīnu sastāvā un satur vienu slāpekļa un divus ūdeņraža atomus NH 3 Amonjaks -NH 2 Aminogrupa CH 3 -NH 2 CH 3 -NH-CH 3 Metilamīns Dimetilamīns CH 3 -N-CH 3 Trimetilamīns 33

Citas funkcionālās grupas un savienojumi R-SH Sulfhidrilgrupa, merkaptāni (tioli) R-S-S-R’ Disulfīdgrupa, disulfīdi O R-O-P-OO- Fosfātgrupa, organiskie fosfāti 34
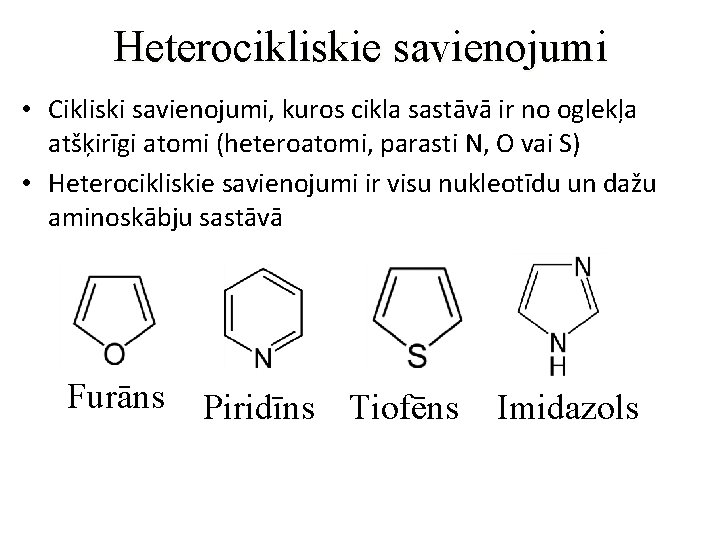
Heterocikliskie savienojumi • Cikliski savienojumi, kuros cikla sastāvā ir no oglekļa atšķirīgi atomi (heteroatomi, parasti N, O vai S) • Heterocikliskie savienojumi ir visu nukleotīdu un dažu aminoskābju sastāvā Furāns Piridīns Tiofēns Imidazols

Funkcionālo grupu reakcijas • Funkcionālās grupas spēj iesaistīties dažādās ķīmiskās reakcijās, piemēram: • Kondensācijas (savienošana, atņemot ūdens molekulu) reakcija. • Hidrolīzes (sašķelšana, pievienojot ūdens molekulu) reakcija. R -OH + OH-R R-O-R +H 2 O R -OH + OH-R 36
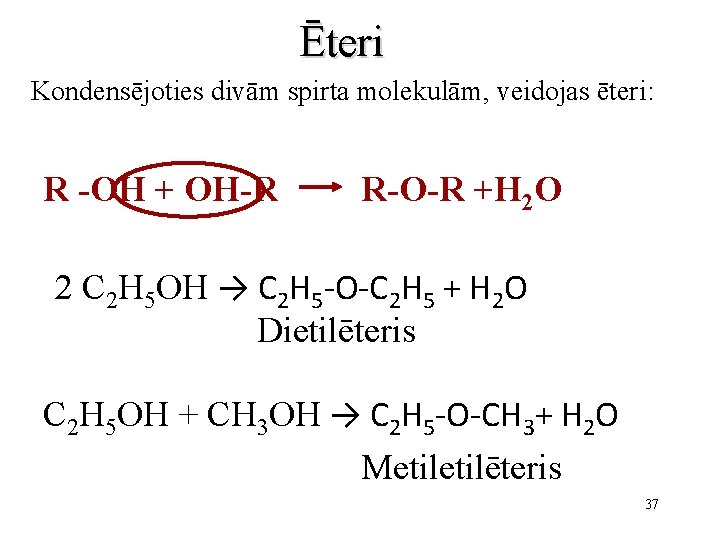
Ēteri Kondensējoties divām spirta molekulām, veidojas ēteri: R -OH + OH-R R-O-R +H 2 O 2 C 2 H 5 OH → C 2 H 5 -O-C 2 H 5 + H 2 O Dietilēteris C 2 H 5 OH + CH 3 OH → C 2 H 5 -O-CH 3+ H 2 O Metilēteris 37
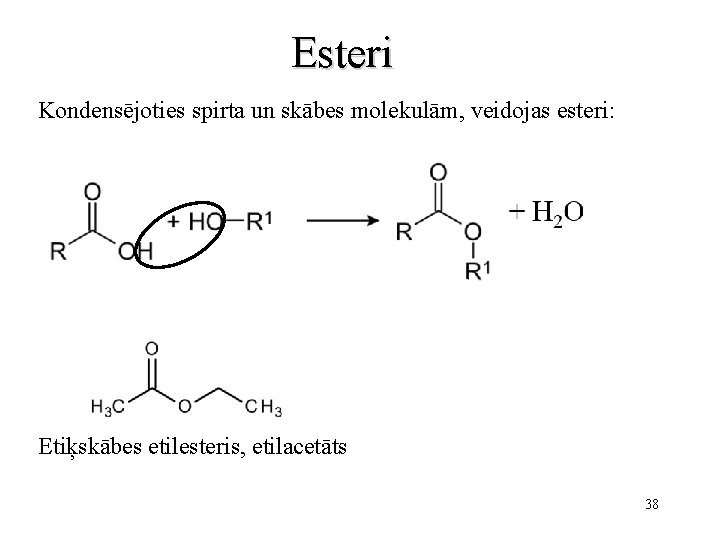
Esteri Kondensējoties spirta un skābes molekulām, veidojas esteri: Etiķskābes etilesteris, etilacetāts 38
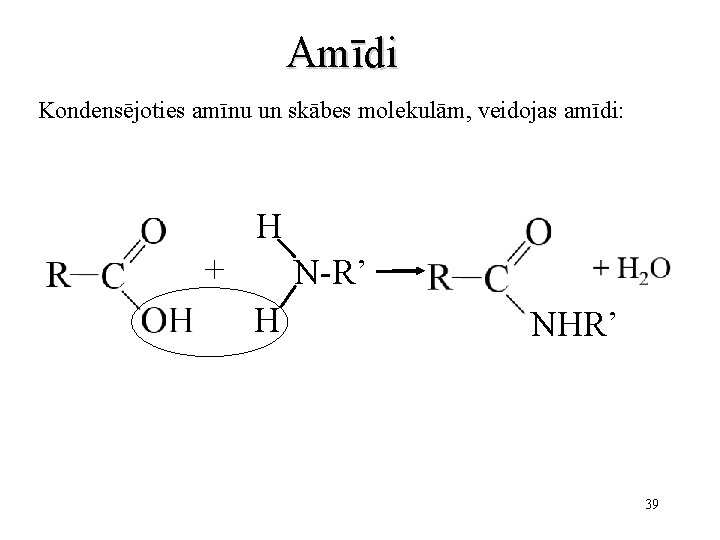
Amīdi Kondensējoties amīnu un skābes molekulām, veidojas amīdi: H + N-R’ H NHR’ 39
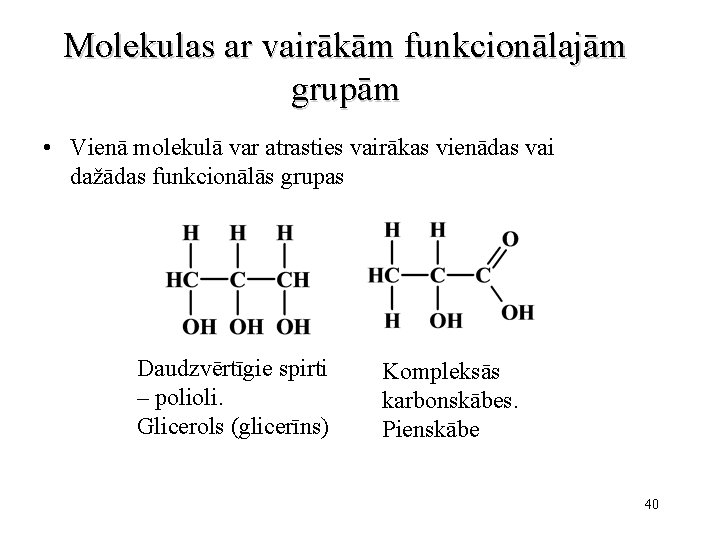
Molekulas ar vairākām funkcionālajām grupām • Vienā molekulā var atrasties vairākas vienādas vai dažādas funkcionālās grupas Daudzvērtīgie spirti – polioli. Glicerols (glicerīns) Kompleksās karbonskābes. Pienskābe 40

Aminoskābes • Organiski savienojumi ar amino- un karboksil- grupām • Proteīni sastāv no 20 dažādām aminoskābēm ar vienādu skeletu (“backbone”), bet atšķirīgām sānu ķēdēm (“R”) • Visas proteīnus veidojošās aminoskābes ir a-aminoskābes (karboksil- un amino- grupas ir pievienotas pie viena un tā paša oglekļa atoma, saukta par Ca) | H 3+N―Ca―H | R a-aminoskābe COO- | H 3+N―Ca―Cb―H | | R R’ | H 3+N―Ca―Cb―Cg―H | R | | R’ R’’ b- un g- aminoskābes (proteīnus neveido)
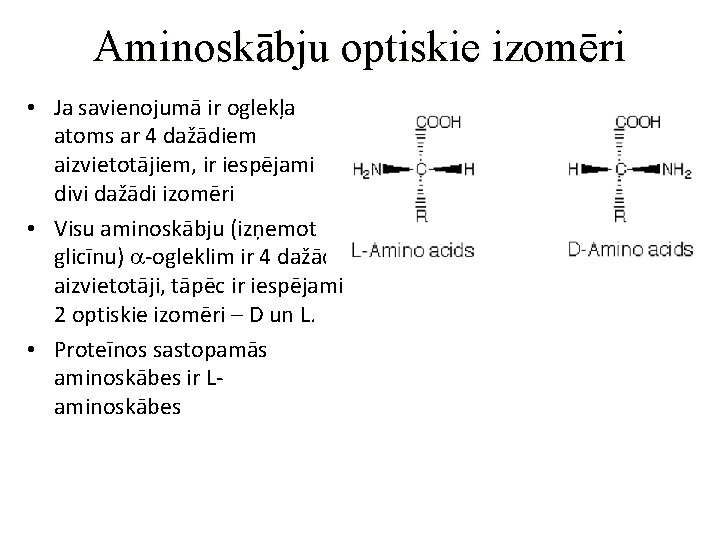
Aminoskābju optiskie izomēri • Ja savienojumā ir oglekļa atoms ar 4 dažādiem aizvietotājiem, ir iespējami divi dažādi izomēri • Visu aminoskābju (izņemot glicīnu) a-ogleklim ir 4 dažādi aizvietotāji, tāpēc ir iespējami 2 optiskie izomēri – D un L. • Proteīnos sastopamās aminoskābes ir Laminoskābes

Aminoskābju klasifikācija • Parasti aminoskābes klasificē pēc to sānu ķēžu polaritātes • Izdala nepolārās (hidrofobās), polārās un lādētās aminoskābes
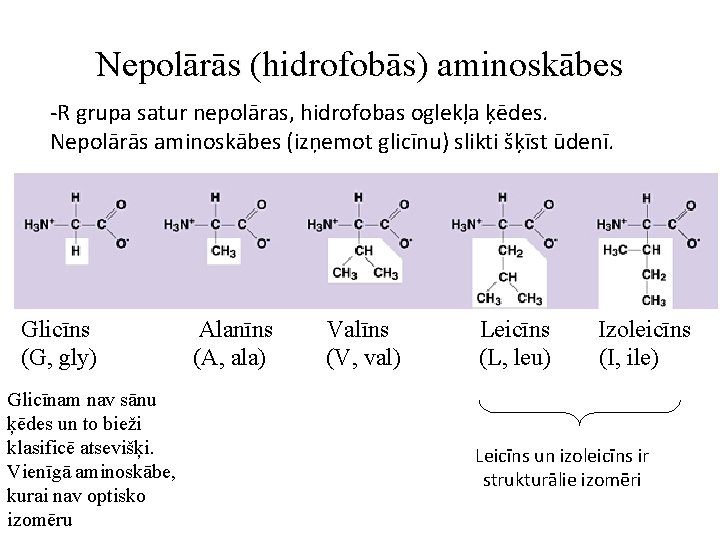
Nepolārās (hidrofobās) aminoskābes -R grupa satur nepolāras, hidrofobas oglekļa ķēdes. Nepolārās aminoskābes (izņemot glicīnu) slikti šķīst ūdenī. Glicīns (G, gly) Glicīnam nav sānu ķēdes un to bieži klasificē atsevišķi. Vienīgā aminoskābe, kurai nav optisko izomēru Alanīns (A, ala) Valīns (V, val) Leicīns (L, leu) Izoleicīns (I, ile) Leicīns un izoleicīns ir strukturālie izomēri
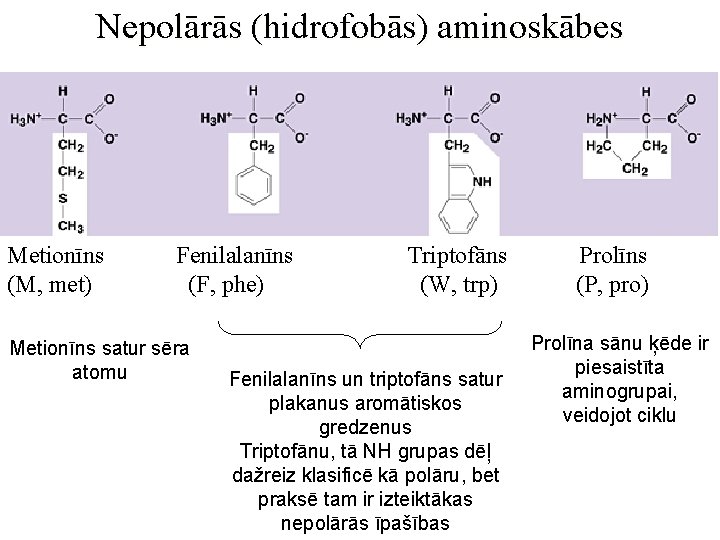
Nepolārās (hidrofobās) aminoskābes Metionīns (M, met) Fenilalanīns (F, phe) Metionīns satur sēra atomu Triptofāns (W, trp) Fenilalanīns un triptofāns satur plakanus aromātiskos gredzenus Triptofānu, tā NH grupas dēļ dažreiz klasificē kā polāru, bet praksē tam ir izteiktākas nepolārās īpašības Prolīns (P, pro) Prolīna sānu ķēde ir piesaistīta aminogrupai, veidojot ciklu

Polārās aminoskābes - R grupa sastāv no oglekļa, skābekļa, un skābekļa atomiem, kuri sānu ķēdi padara polārāku un tādejādi hidrofilāku. Polārās aminoskābes labi šķīst ūdenī. Serīns (S, ser) Treonīns (T, thr) Cisteīns (C, cys) Tirozīns (Y, tyr) Cisteīnam ir gan polāras, gan hidrofobas īpašības. Divi cisteīni var savienoties ar SH grupām Aspargīns Glutamīns (N, asn) (Q, gln)
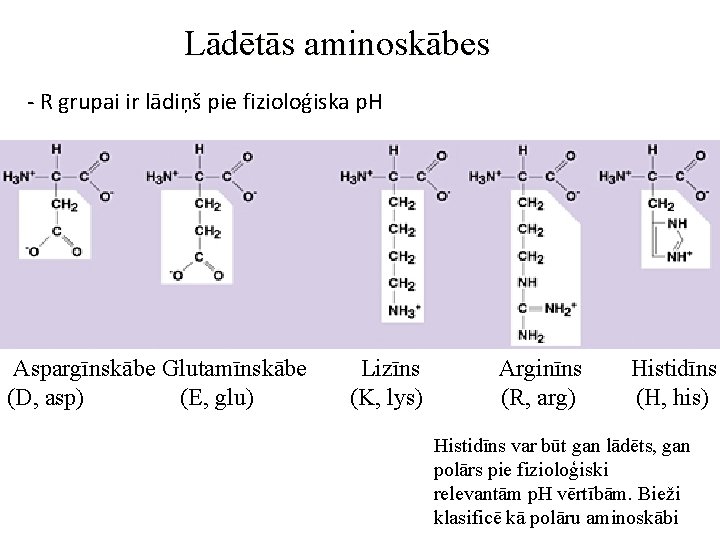
Lādētās aminoskābes - R grupai ir lādiņš pie fizioloģiska p. H Aspargīnskābe Glutamīnskābe (D, asp) (E, glu) Lizīns (K, lys) Arginīns (R, arg) Histidīns (H, his) Histidīns var būt gan lādēts, gan polārs pie fizioloģiski relevantām p. H vērtībām. Bieži klasificē kā polāru aminoskābi

Ogļhidrāti (ogļūdeņi, cukuri) • Vispārīgā ķīmiskā formula (CH 2 O)n = ogļhidrāti • Monosaharīdi: 3 – 6 C atomu ķēde + viena karbonil- un vairākas hidroksil- funkcionālās grupas • Monosaharīdu kondensācijas reakcijās veidojas di-, triun polisaharīdi 48

Monosaharīdu klasifikācija • Atkarībā no funkcionālās grupas, izšķir divus monosaharīdu veidus – aldozes un ketozes • Nosaukumos ietilpst arī oglekļa atomu skaits – piem. triozes (3 oglekļi), heksozes (6 oglekļi), u. c. • Līdzīgi aminoskabēm, monosaharīdiem ir D- un Lizomēri; dabā sastopama pārsvarā D- forma D-gliceraldehīds, aldotrioze Dihidroksiacetons, ketotrioze 49
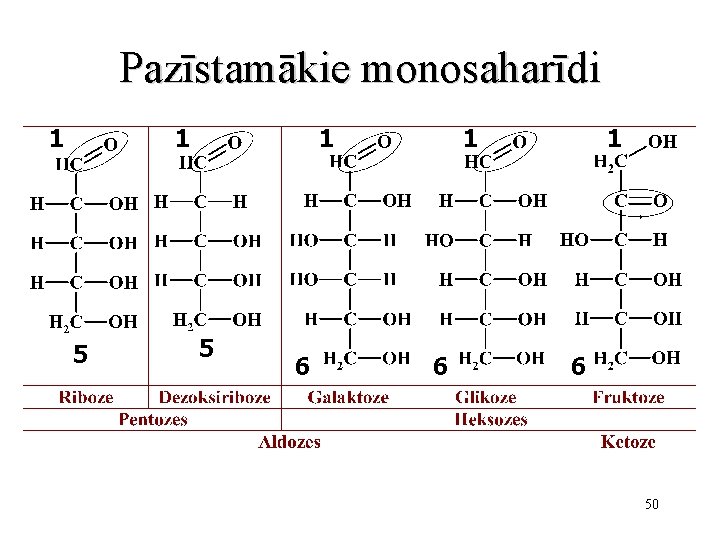
Pazīstamākie monosaharīdi 1 1 5 6 1 6 50
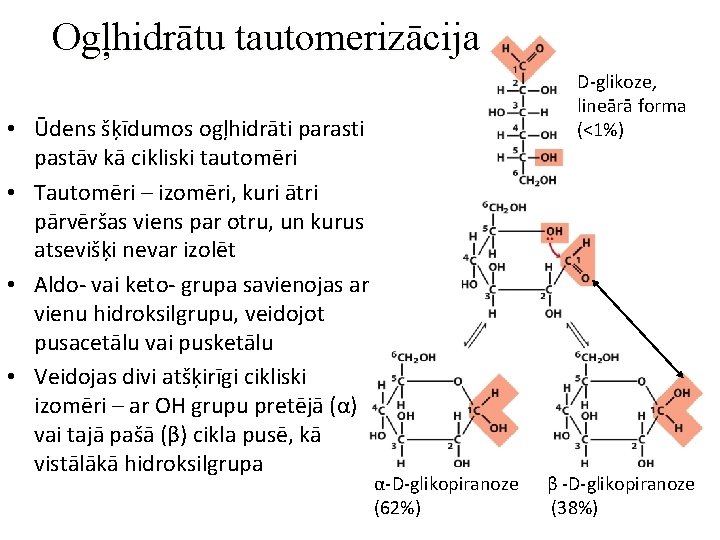
Ogļhidrātu tautomerizācija • Ūdens šķīdumos ogļhidrāti parasti pastāv kā cikliski tautomēri • Tautomēri – izomēri, kuri ātri pārvēršas viens par otru, un kurus atsevišķi nevar izolēt • Aldo- vai keto- grupa savienojas ar vienu hidroksilgrupu, veidojot pusacetālu vai pusketālu • Veidojas divi atšķirīgi cikliski izomēri – ar OH grupu pretējā (α) vai tajā pašā (β) cikla pusē, kā vistālākā hidroksilgrupa D-glikoze, lineārā forma (<1%) α-D-glikopiranoze (62%) β -D-glikopiranoze (38%)
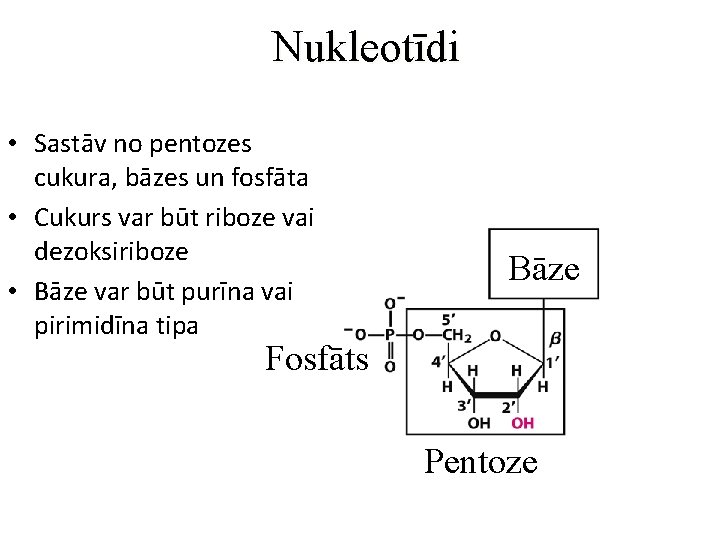
Nukleotīdi • Sastāv no pentozes cukura, bāzes un fosfāta • Cukurs var būt riboze vai dezoksiriboze • Bāze var būt purīna vai pirimidīna tipa Bāze Fosfāts Pentoze
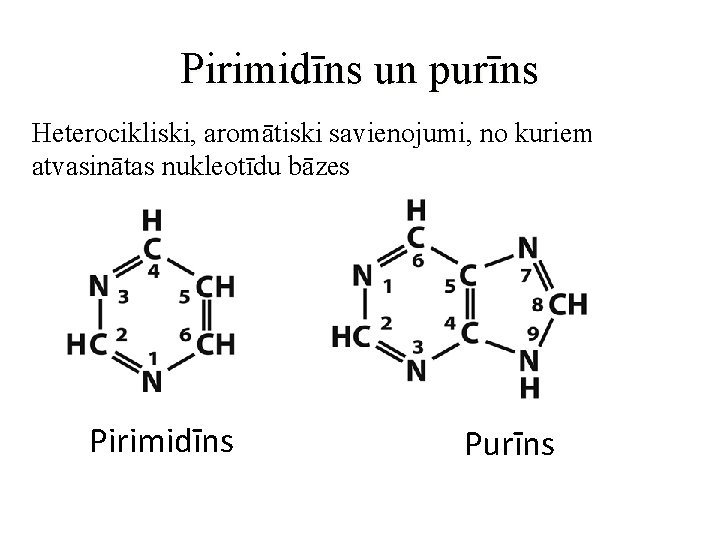
Pirimidīns un purīns Heterocikliski, aromātiski savienojumi, no kuriem atvasinātas nukleotīdu bāzes Pirimidīns Purīns
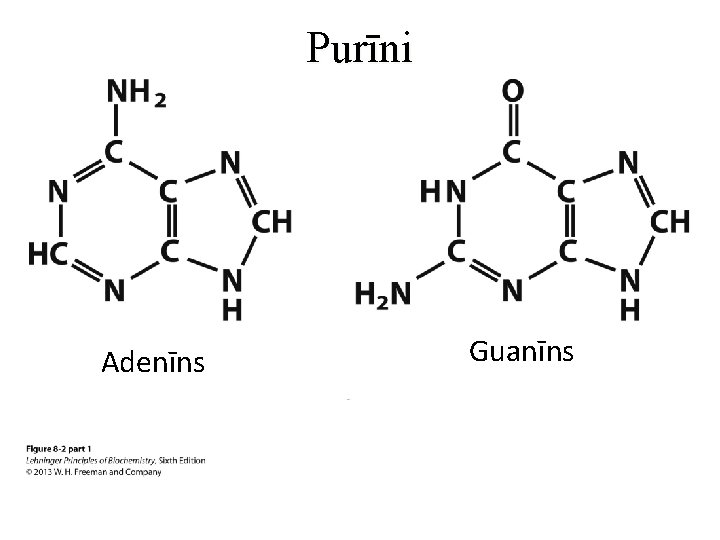
Purīni Adenīns Guanīns
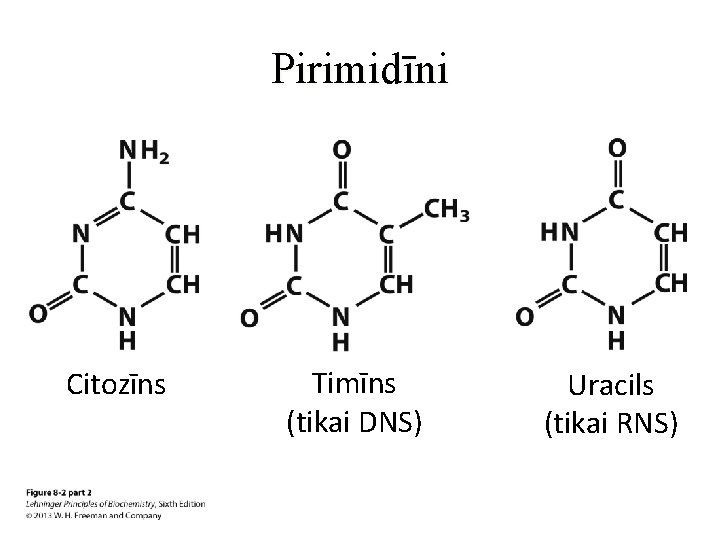
Pirimidīni Citozīns Timīns (tikai DNS) Uracils (tikai RNS)
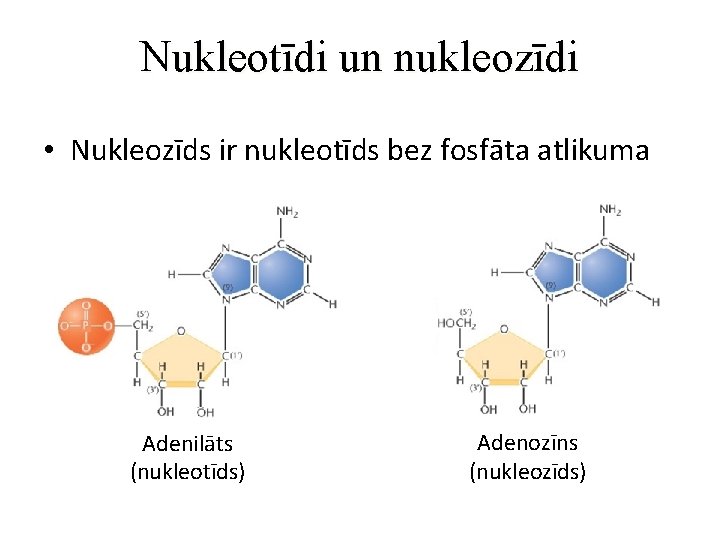
Nukleotīdi un nukleozīdi • Nukleozīds ir nukleotīds bez fosfāta atlikuma Adenilāts (nukleotīds) Adenozīns (nukleozīds)
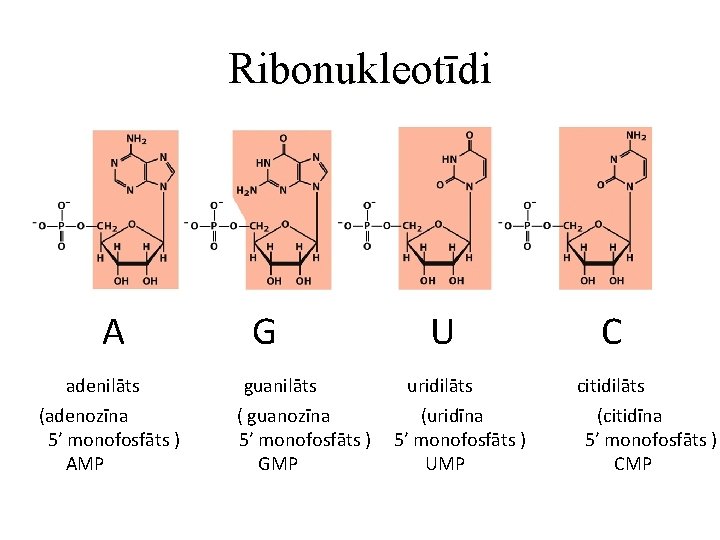
Ribonukleotīdi A adenilāts (adenozīna 5’ monofosfāts ) AMP G guanilāts ( guanozīna 5’ monofosfāts ) GMP U uridilāts (uridīna 5’ monofosfāts ) UMP C citidilāts (citidīna 5’ monofosfāts ) CMP
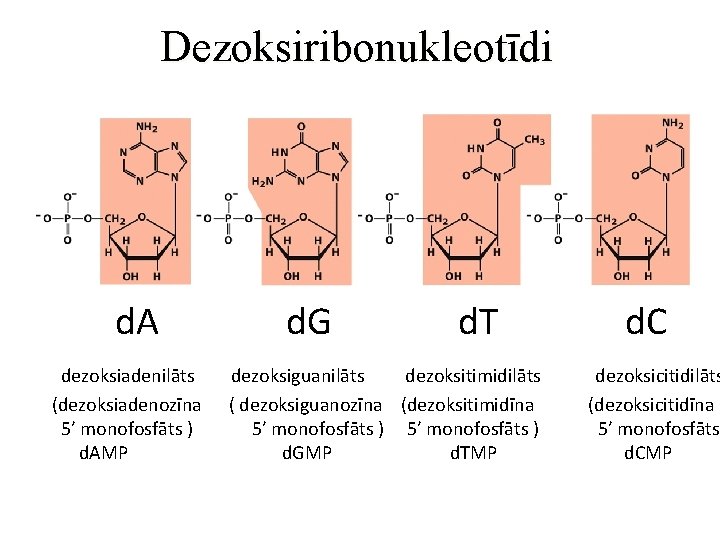
Dezoksiribonukleotīdi d. A dezoksiadenilāts (dezoksiadenozīna 5’ monofosfāts ) d. AMP d. G d. T dezoksiguanilāts dezoksitimidilāts ( dezoksiguanozīna (dezoksitimidīna 5’ monofosfāts ) d. GMP d. TMP d. C dezoksicitidilāts (dezoksicitidīna 5’ monofosfāts d. CMP
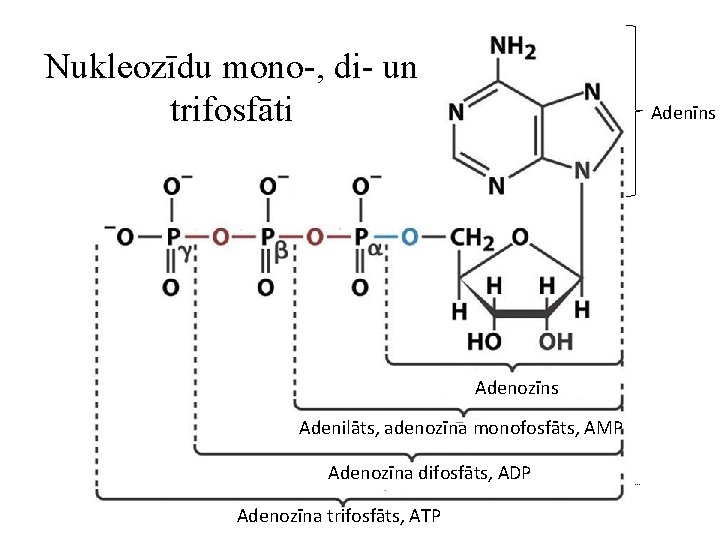
Nukleozīdu mono-, di- un trifosfāti Adenīns Adenozīns Adenilāts, adenozīna monofosfāts, AMP Adenozīna difosfāts, ADP Adenozīna trifosfāts, ATP
- Slides: 59