Analisis Kualitatif Kation Oleh Rezki Pratama02043 Yusuf00346 1212022
















- Slides: 18

Analisis Kualitatif Kation Oleh: Rezki Pratama/02043 Yusuf/00346 1/21/2022 1

Apa itu Analisis Kualitatif? o Analisa kualitatif merupakan suatu proses dalam mendeteksi keberadaan suatu unsur kimia dalam cuplikan yang tidak diketahui. Analisa kualitatif merupakan salah satu cara yang paling efektif untuk mempelajari kimia dan unsur-unsur serta ionionnya dalam larutan. 1/21/2022 2

Dalam metode analisis kualitatif kita menggunakan beberapa pereaksi diantaranya pereaksi golongan dan pereaksi spesifik, kedua pereaksi ini dilakukan untuk mengetahui jenis anion / kation suatu larutan. Regensia golongan yang dipakai untuk klasifikasi kation yang paling umum adalah asam klorida, hidrogen sulfida, ammonium sulfida, dan amonium karbonat. 1/21/2022 3

Berdasarkan Apakah Klasifikasi Itu? Klasifikasi ini didasarkan atas apakah suatu kation bereaksi dengan reagensia-reagensia ini dengan membentuk endapan atau tidak. Sedangkan metode yang digunakan dalam anion tidak sesistematik kation. Namun skema yang digunakan bukanlah skema yang kaku, karena anion termasuk dalam lebih dari satu golongan. 1/21/2022 4

Didalam kation ada beberapa golongan yang memiliki ciri khas tertentu diantaranya : 1/21/2022 5

1. Golongan I : Kation golongan ini membentuk endapan dengan asam klorida encer. Ion golongan ini adalah Pb, Ag, Hg. 1/21/2022 6

Reaksinya adalah : n Ag+ n 1. Ag+ + HCL → Ag. CL ↓ putih + Hn 2. 2 Ag+ + 2 Na. OH → 2 Ag. OH + 2 Na+ ↓ coklat n 3. 2 Ag+ + 2 NH 4 OH → 2 Ag. OH → NH+ n Pb 2+ n 1. Pb 2+ + 2 Na. OH → Pb(OH)2 ↓ putih + 2 Na+ n Pb(OH)2 + 2 Na. OH → Na 2 Pb(OH)4 n 2. Pb 2+ +2 NH 4 OH → Pb(OH)2 ↓ putih + 2 NH 4+ n 3. Pb 2+ + 2 KI → Pb. I 2 1/21/2022 7

2. Golongan II : Kation golongan ini bereaksi dengan asam klorida, tetapi membentuk endapan dengan hidrogen sulfida dalam suasana asam mineral encer. Ion golongan ini adalah Hg, Bi, Cu, cd, As, Sb, Sn. 1/21/2022 8

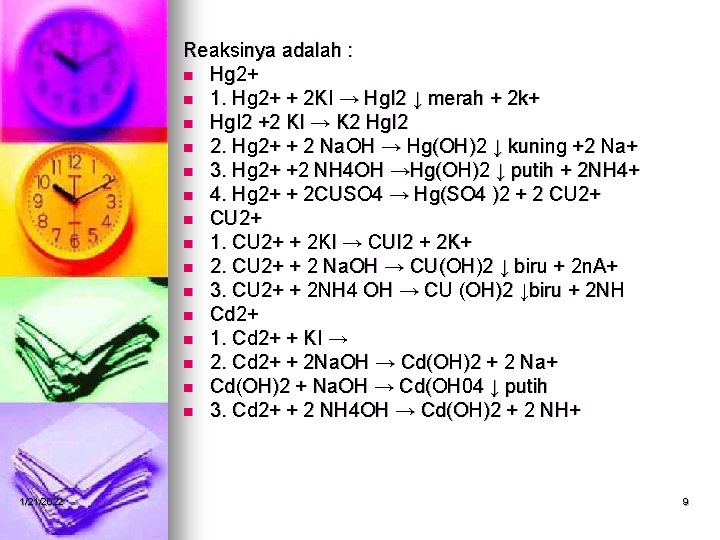
Reaksinya adalah : n Hg 2+ n 1. Hg 2+ + 2 KI → Hg. I 2 ↓ merah + 2 k+ n Hg. I 2 +2 KI → K 2 Hg. I 2 n 2. Hg 2+ + 2 Na. OH → Hg(OH)2 ↓ kuning +2 Na+ n 3. Hg 2+ +2 NH 4 OH →Hg(OH)2 ↓ putih + 2 NH 4+ n 4. Hg 2+ + 2 CUSO 4 → Hg(SO 4 )2 + 2 CU 2+ n 1. CU 2+ + 2 KI → CUI 2 + 2 K+ n 2. CU 2+ + 2 Na. OH → CU(OH)2 ↓ biru + 2 n. A+ n 3. CU 2+ + 2 NH 4 OH → CU (OH)2 ↓biru + 2 NH n Cd 2+ n 1. Cd 2+ + KI → n 2. Cd 2+ + 2 Na. OH → Cd(OH)2 + 2 Na+ n Cd(OH)2 + Na. OH → Cd(OH 04 ↓ putih n 3. Cd 2+ + 2 NH 4 OH → Cd(OH)2 + 2 NH+ 1/21/2022 9

3. Golongan III : Kation golongan ini tidak bereaksi dengan asam klorida encer, ataupun dengan hidrogen sulfida dalam suasana asam mineral encer. Namun kation ini membentuk endapan dengan ammonium sulfida dalam suasana netral / amoniakal. Kation golongan ini Co, Fe, Al, Cr, Co, Mn, Zn. 1/21/2022 10

Reaksinya adalah : n n n n 1/21/2022 Golongan III A Fe 2+ 1. Fe 2+ + 2 Na. OH → Fe(OH)2 ↓ hijau kotor + 2 Na+ 2. Fe 2+ + 2 NH 4 OH → Fe(OH)2 ↓ hijau kotor + 2 NH 4+ 3. Fe 2+ + 2 K 4 Fe(CN)6 → K 4 {Fe(CN)6} ↓ biru + 4 k+ 4. Fe 2+ + KSCN → Fe(SCN)2 + 2 K+ Fe 3+ 1. Fe 3+ + 3 Na. OH → Fe(OH)3 ↓ kuning + 3 Na+ 2. Fe 3+ + 3 NH 4 OH → Fe(OH)3 ↓ Kuning + 3 NH 4+ 3. Fe 3+ + 3 K 4 Fe(CN)6}2 → K 4{Fe(CN)6}2 ↓ biru +3 k+ 4. Fe 3+ + 3 KCNS → Fe(SCN)3 + 3 K+ Al 3+ 1. Al 3+ + 3 Na. OH → Al(OH)3 ↓ putih + 3 Na+ 2. Al 3+ + 3 NH 4 OH → Al(OH)3 ↓ putih + 3 NH 4+ 3. Al 3+ + KSCN → 11

n n n n 1/21/2022 Golongan III B Zn 21. Zn 2 - + Na. OH → Zn(OH)2 ↓ putih + 2 Na+ 2. Zn 2 - + Na 2 CO 3 → ZN(CO 3)2 ↓ putih + 2 Na+ 3. Zn 2 - + K 4 Fe(CN )6 → Zn 4{Fe(CN)6}2 tetap + 8 k+ Ni 2+ 1. Ni 2+ + 2 Na. OH → Ni(OH)2 ↓ hijau + 2 Na+ 2. Ni 2+ + NH 4 OH → Ni(OH)2 ↓ hijau + 2 NH 4+ 3. Ni 2+ + 2 Na 2 CO 3 → Ni(CO 3)2 ↓ hijau muda + 2 Na 4. Ni 2+ + K 4 Fe(CN)6 → Ni 4{Fe(CN)6}2 tetap + 8 k+ CO 21. CO 2 - + NH 4 OH → CO(OH)2 ↓ hijau + 2 NH 4 2. CO 2 - + 2 Na. OH → CO 9 OH)2 ↓ biru + 2 Na+ 3. CO 2 - + K 4 Fe(CN)6 → CO 4{Fe(CN)6}2 tetap + 8 k+ 4. CO 2 - + 2 Na 2 CO 3 → CO(CO 3)2 ↓ hijau muda + 2 Na 12

4. Golongan IV : Kation golongan ini bereaksi dengan golongan I, III. Kation ini membentuk endapan dengan ammonium karbonat dengan adanya ammonium klorida, dalam suasana netral atau sedikit asam. Ion golongan ini adalah Ba, Ca, Sr. 1/21/2022 13

Tes Nyala 1/21/2022 14

Reaksinya adalah : n n n n 1/21/2022 Ba 21. Ba 2 - + k 2 Cr. O 4 → Ba. Cr. O 4 ↓ kuning 2. Ba 2 - + Na 2 CO 3 → Ba. CO 3 ↓ putih Uji nyala Ba → kuning kehijaun Ca 2+ 1. Ca 2+ + K 2 Cr. O 4 → Ca. Cr. O 4 Lart. Kuning +2 K+ 2. Ca 2+ + Na 2 CO 3 → Ca. CO 3 + 2 Na+ Untuk uji nyala Ca → merah kekuningan. Sr 2+ 1. Sr 2+ + K 2 Cr. O 4 → Sr. Cr. O 4 Lart. Kuning + 2 K 2. Sr 2+ + Na 2 CO 3 → Sr. CO 3 + 2 Na+ Untuk uji nyala Sr → merah karmin 15

5. Golongan V : Kation-kation yang umum, yang tidak bereaksi dengan regensia-regensia golongan sebelumnya, merupakan golongan kation yang terakhir. Kation golongan ini meliputi : Mg, K, NH 4+. 1/21/2022 16

Reaksinya adalah : n Mg 2+ n 1. Mg 2+ + 2 Na. OH → Mg(OH)2 putih + 2 Na+ n 2. Mg 2+ + 2 NH 4 OH → Mg(OH)2 tetap + 2 NH 4+ n 3. Mg 2+ + Na 3 CO(NO 2)6 → Mg 3{CO(NO 2)6} Lart. Merah darah + 3 Na 1/21/2022 17

1/21/2022 18
 Cara menghitung nilai rf pada klt
Cara menghitung nilai rf pada klt Skema pemisahan kation golongan 1
Skema pemisahan kation golongan 1 Wiązanie jonowe polega na elektrostatycznym
Wiązanie jonowe polega na elektrostatycznym Uranil magnesium asetat
Uranil magnesium asetat Hexabromoseleničitan draselný
Hexabromoseleničitan draselný Kwasy lewisa
Kwasy lewisa Sulfonowanie benzenu reakcja
Sulfonowanie benzenu reakcja Retencja
Retencja Van der waals bindinger
Van der waals bindinger Tabulasi kation golongan 2
Tabulasi kation golongan 2 Teknik analisis data kualitatif dan kuantitatif
Teknik analisis data kualitatif dan kuantitatif Contoh analisis risiko kualitatif dan kuantitatif
Contoh analisis risiko kualitatif dan kuantitatif Pengolahan dan analisis data kualitatif
Pengolahan dan analisis data kualitatif Contoh analisis risiko kualitatif dan kuantitatif
Contoh analisis risiko kualitatif dan kuantitatif Analisis kualitatif senyawa obat
Analisis kualitatif senyawa obat Contoh analisis kualitatif
Contoh analisis kualitatif Contoh analisis isi kualitatif
Contoh analisis isi kualitatif Contoh analisis risiko kualitatif dan kuantitatif
Contoh analisis risiko kualitatif dan kuantitatif Koding kualitatif
Koding kualitatif