Aminy Budowa i klasyfikacja amin Nazewnictwo i izomeria

Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin

Budowa i klasyfikacja amin • Aminy – pochodne amoniaku (NH 3), w cząsteczce którego jeden lub kilka atomów wodoru zastąpiono podstawnikami węglowodorowymi (R lub Ar) • Klasyfikacja amin: ü Aminy I-rzędowe: R – NH 2 lub Ar – NH 2 ü Aminy II-rzędowe : R – NH – R ü Aminy III-rzędowe: R – N| – R • W zależności od podstawników węglowodorowych rozróżnia się aminy alifatyczne, aromatyczne, mieszane, jeżeli grupa aminowa nie jest związana bezpośrednio z pierścieniem aromatycznym, to aminy te należą do amin alifatycznych. • Ze względu na wolną parę elektronową na atomie N, aminy są elektronodonorami, czyli wykazują właściwości zasadowe.
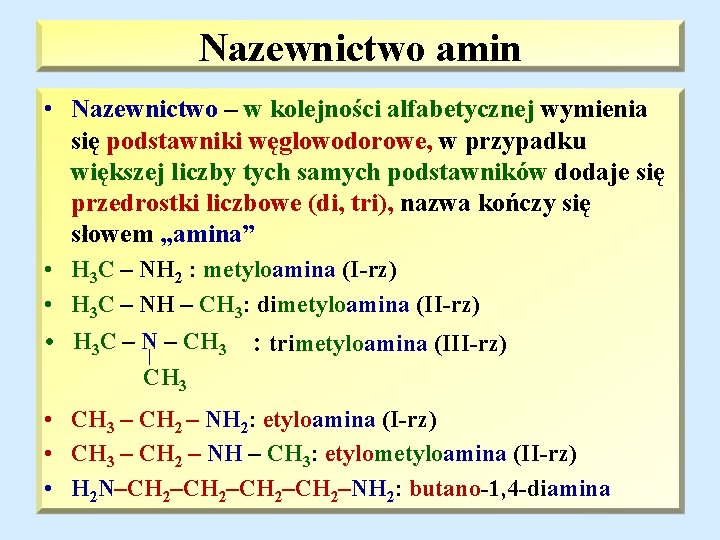
Nazewnictwo amin • Nazewnictwo – w kolejności alfabetycznej wymienia się podstawniki węglowodorowe, w przypadku większej liczby tych samych podstawników dodaje się przedrostki liczbowe (di, tri), nazwa kończy się słowem „amina” • H 3 C – NH 2 : metyloamina (I-rz) • H 3 C – NH – CH 3: dimetyloamina (II-rz) • H 3 C – N| – CH 3 : trimetyloamina (III-rz) CH 3 • CH 3 – CH 2 – NH 2: etyloamina (I-rz) • CH 3 – CH 2 – NH – CH 3: etylometyloamina (II-rz) • H 2 N–CH 2–CH 2–NH 2: butano-1, 4 -diamina
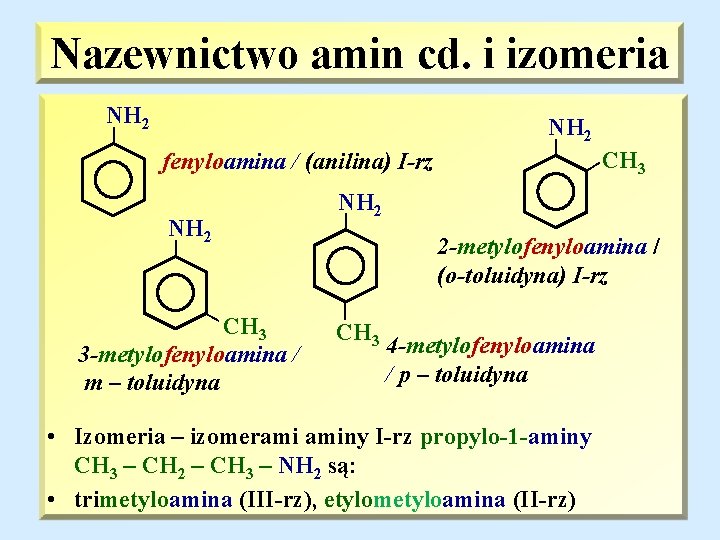
Nazewnictwo amin cd. i izomeria NH 2 | 2 -metylofenyloamina / (o-toluidyna) I-rz | | | CH 3 3 -metylofenyloamina / m – toluidyna CH 3 | fenyloamina / (anilina) I-rz | CH 3 4 -metylofenyloamina / p – toluidyna • Izomeria – izomerami aminy I-rz propylo-1 -aminy CH 3 – CH 2 – CH 3 – NH 2 są: • trimetyloamina (III-rz), etylometyloamina (II-rz)
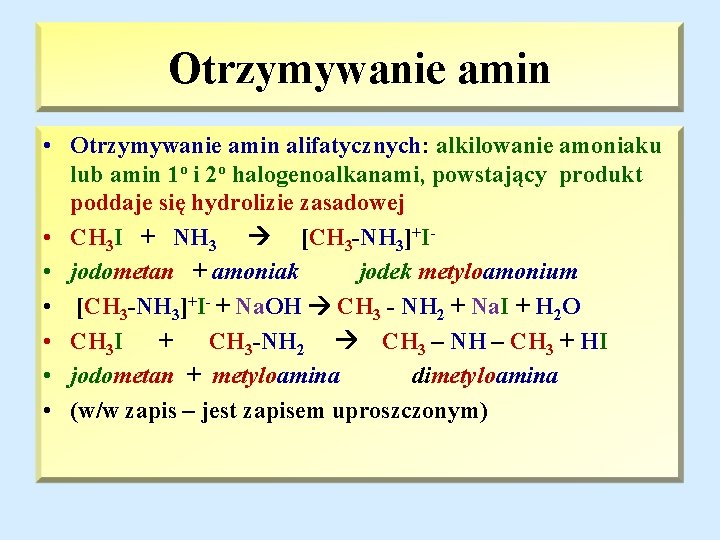
Otrzymywanie amin • Otrzymywanie amin alifatycznych: alkilowanie amoniaku lub amin 1 o i 2 o halogenoalkanami, powstający produkt poddaje się hydrolizie zasadowej • CH 3 I + NH 3 [CH 3 -NH 3]+I • jodometan + amoniak jodek metyloamonium • [CH 3 -NH 3]+I- + Na. OH CH 3 - NH 2 + Na. I + H 2 O • CH 3 I + CH 3 -NH 2 CH 3 – NH – CH 3 + HI • jodometan + metyloamina dimetyloamina • (w/w zapis – jest zapisem uproszczonym)

Otrzymywanie amin cd • Otrzymywanie amin aromatycznych: • redukcja nitrobenzenu wodorem wobec katalizatora • C 6 H 5 -NO 2 + 3 H 2 C 6 H 5 -NH 2 + 2 H 2 O nitrobenzen anilina • redukcja nitrobenzenu mieszaniną cynku (lub cyny, żelaza) i kwasu chlorowodorowego, w drugim etapie hydroliza w środowisku zasadowym • C 6 H 5 – NO 2 + 3 Zn + 7 HCl [C 6 H 5 -NH 3]+Cl- + 3 Zn. Cl 2 + 2 H 2 O nitrobenzen chlorek aniliny • [C 6 H 5 -NH 3]+Cl- + Na. OH C 6 H 5 -NH 2 + Na. Cl + H 2 O chlorek aniliny anilina

Właściwości fizyczne amin • Metyloamina i etyloamina są gazami o nieprzyjemnym zapachu, aminy aromatyczne (anilina) i aminy o dłuższych łańcuchach węglowych są cieczami, difenyloamina, p-toluidyna są ciałami stałymi. • Aminy mają niskie temp. wrzenia, ponieważ nie mają zdolności tworzenia wiązań wodorowych. • Aminy alifatyczne dobrze rozpuszczają się w wodzie, ponieważ mogą tworzyć wiązania wodorowe z cząsteczkami wody poprzez wolna parę elektronową na atomie azotu. • stała dysocjacji metyloaminy / Kb = 4, 265 ٠ 10 -4 ü CH 3 – NH 2 + H 2 O ↔ CH 3 – NH 3+ + OH •

Właściwości fizyczne amin • Aminy aromatyczne - anilina Ø trudno rozpuszcza się w wodzie, ponieważ wolna para elektronowa jest sprzężona z sekstetem elektronowym pierścienia aromatycznego, co obniża właściwości elektrodonorowe, Ø stała dysocjacji aniliny / Kb = 4, 266 ٠ 10 -10 ü C 6 H 5 – NH 2 + H 2 O ↔ C 6 H 5 – NH 3+ + OHØ wraz ze wzrostem liczby grup aminowych związanych z pierścieniem aromatycznym wzrasta rozpuszczalność ich w wodzie (wzrastają właściwości elektrodonorowe).

Właściwości chemiczne amin • Aminy wykazują właściwości zasadowe, podobnie jak amoniak (wolna para elektronowa na atomie azotu – elektronodoner) • dysocjacja elektrolityczna w roztworze wodnym • CH 3 – NH 2 + H 2 O ↔ CH 3 -NH 3+ + OH • reakcja z kwasami sól • CH 3 -NH 2 + HBr CH 3 -NH 3 Br metyloamina bromek metyloamonium • Aminy alifatyczne wykazują silniejsze właściwości zasadowe niż amoniak, natomiast anilina ma słabsze właściwości zasadowe niż amoniak i aminy alifatyczne. • Aminy, jako słabe zasady są wypierane z soli przez wodorotlenki litowców.

Właściwości chemiczne amin cd • Pozostałe reakcje amin: • aminy I i II-rzędowe ulegają alkilowaniu powstają odpowiedni aminy II i III- rzędowe, • utlenianie do grupy nitrowej, • halogenowaniu ( substytucji rodnikowej na alifatycznej części węlgowodorowej) • aminy aromatyczne – substytucja elektrofilowa na pierścieniu aromatycznym, grupa aminowa jest podstawnikiem I- rodzaju, kolejne podstawniki są kierowane w pozycje: ü orto (2 i 6). ü para (4)

Zastosowanie amin • Metyloamina CH 3 - NH 2: produkcja barwników, środków farmaceutycznych, jest dodatkiem do rozpuszczalników, zmywaczy, paliw, • Diaminy od 2 -ch do 6 at. C w cząsteczce stosowane są do produkcji włókien sztucznych (np. heksano-1, 6 -diamina jest półproduktem w produkcji nylonu) • Aminy III-rzędowe są stosowane jako utwardzacze żywic syntetycznych mających zastosowanie jako kleje (epidian), lakiery materiały izolacyjne.

Zastosowanie amin • Anilina właściwości i zastosowanie: ü bezbarwna ciecz brunatniejąca pod wpływem powietrza, ü słaby ale charakterystycznym zapachu, ü toksyczna, ü stosowana do produkcji barwników, ü farmaceutyków, ü materiałów wybuchowych, ü tworzyw sztucznych.
- Slides: 12