Treci multimedialne kodowanie przetwarzanie prezentacja Odtwarzanie treci multimedialnych

























![Właściwości chemiczne aldehydów PRÓBA TOLLENSA – etap IV metanal HCHO wodorotlenek diaminasrebra(I) [Ag(NH 3)2]+ Właściwości chemiczne aldehydów PRÓBA TOLLENSA – etap IV metanal HCHO wodorotlenek diaminasrebra(I) [Ag(NH 3)2]+](https://slidetodoc.com/presentation_image_h/9ababb30b7449af5835239a0e13182f8/image-53.jpg)

![Właściwości chemiczne aldehydów PRÓBA TOLLENSA – etap V + [Ag(NH ) ] 2 + Właściwości chemiczne aldehydów PRÓBA TOLLENSA – etap V + [Ag(NH ) ] 2 +](https://slidetodoc.com/presentation_image_h/9ababb30b7449af5835239a0e13182f8/image-56.jpg)



















- Slides: 81

Treści multimedialne - kodowanie, przetwarzanie, prezentacja Odtwarzanie treści multimedialnych Andrzej Majkowski informatyka + 1

JEDNOFUNKCYJNE POCHODNE WĘGLOWODORÓW: ALDEHYDY 2

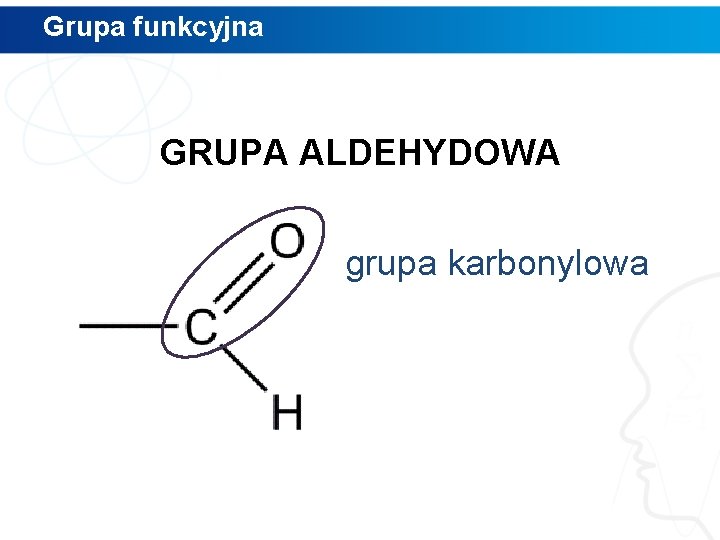
Budowa aldehydów ALDEHYDY – pochodne węglowodorów, zawierające w swej cząsteczce grupę aldehydową –CHO (w skład której wchodzi grupa karbonylowa)

Grupa funkcyjna GRUPA ALDEHYDOWA grupa karbonylowa

Grupa funkcyjna POWTÓRZMY

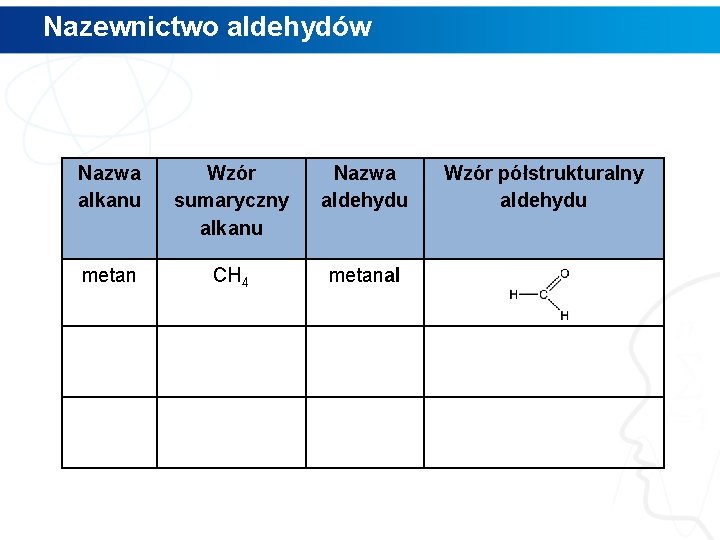
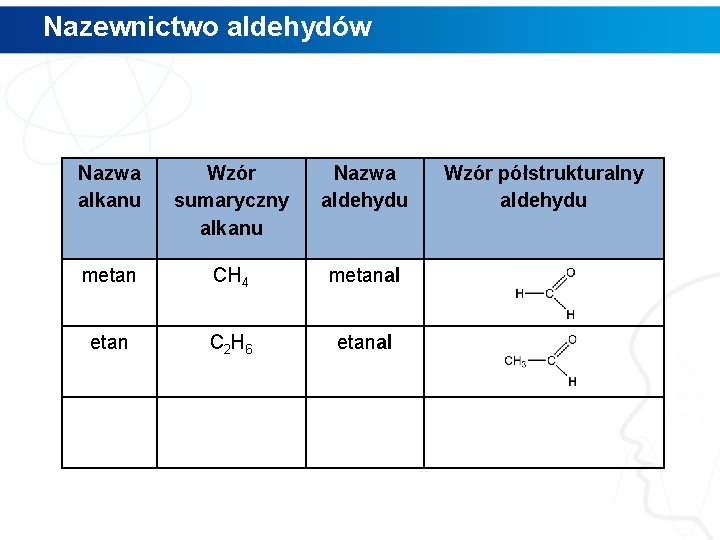
Nazewnictwo aldehydów Nazwa alkanu Wzór sumaryczny alkanu Nazwa aldehydu metan CH 4 metanal Wzór półstrukturalny aldehydu

Nazewnictwo aldehydów Nazwa alkanu Wzór sumaryczny alkanu Nazwa aldehydu metan CH 4 metanal etan C 2 H 6 etanal Wzór półstrukturalny aldehydu

Nazewnictwo aldehydów Nazwa alkanu Wzór sumaryczny alkanu Nazwa aldehydu metan CH 4 metanal etan C 2 H 6 etanal propan C 3 H 8 propanal Wzór półstrukturalny aldehydu

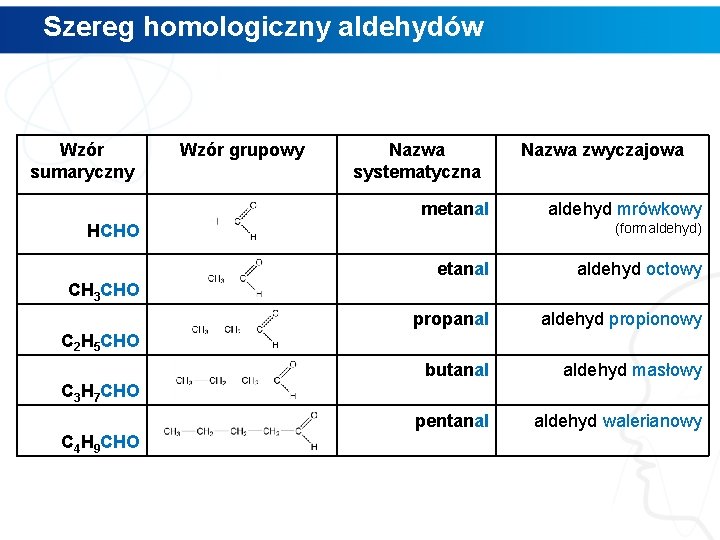
Szereg homologiczny aldehydów Wzór sumaryczny Wzór grupowy Nazwa systematyczna metanal Nazwa zwyczajowa aldehyd mrówkowy (formaldehyd) HCHO etanal aldehyd octowy propanal aldehyd propionowy butanal aldehyd masłowy pentanal aldehyd walerianowy CH 3 CHO C 2 H 5 CHO C 3 H 7 CHO C 4 H 9 CHO

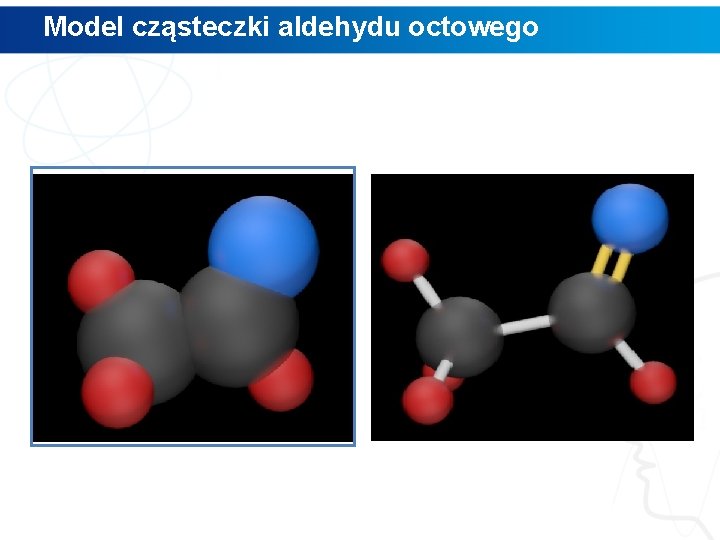
Model cząsteczki aldehydu octowego

Polecenie 1. Wskaż, gdzie w modelu aldehydu octowego znajduje się grupa aldehydowa. 2. Przeanalizuj, w jaki sposób łączą się ze sobą atomy węgla, tlenu oraz wodoru w tej grupie. 3. Za pomocą programu Chem. Skech narysuj wzór aldehydu benzoesowego oraz alkoholu, z którego możemy go otrzymać. 4. Obejrzyj narysowane przez Ciebie struktury w przestrzeni trójwymiarowej, wykorzystując funkcje programu Chem. Skech o nazwie 3 D Viewer.

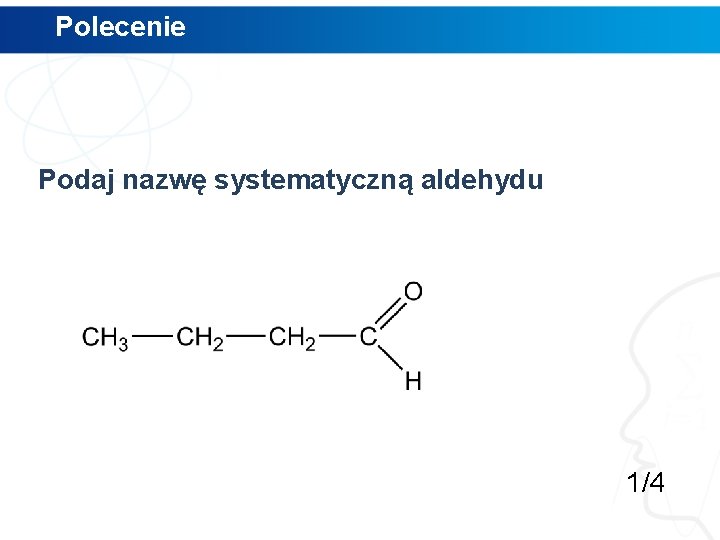
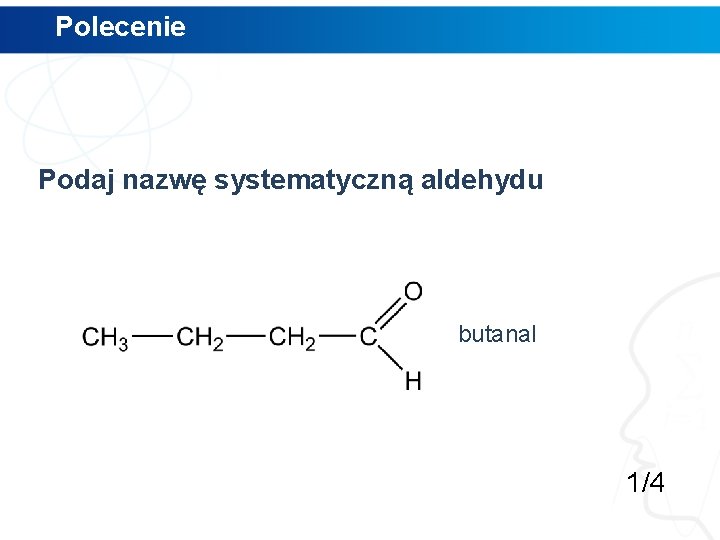
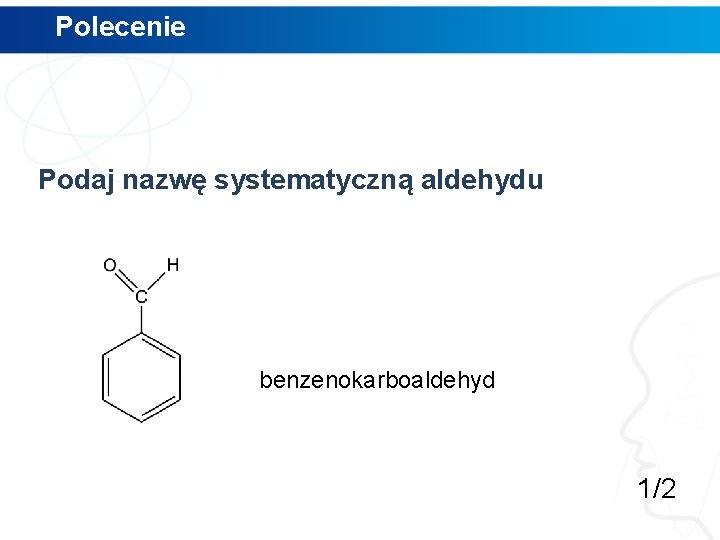
Polecenie Podaj nazwę systematyczną aldehydu 1/4

Polecenie Podaj nazwę systematyczną aldehydu butanal 1/4

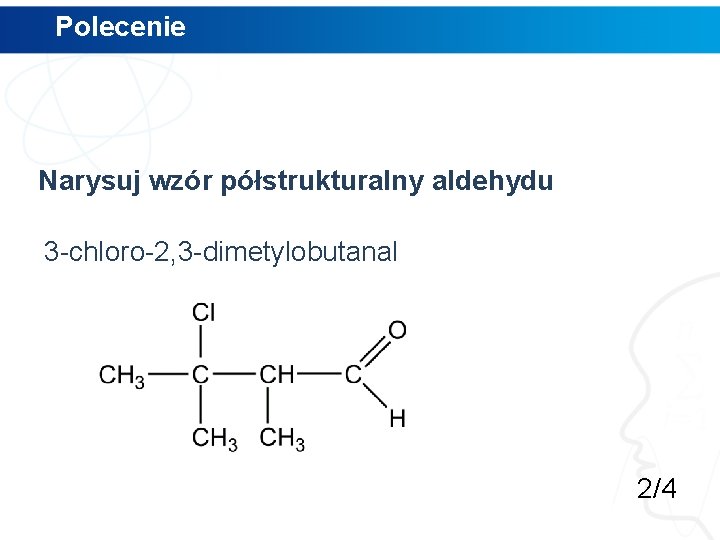
Polecenie Narysuj wzór półstrukturalny aldehydu 3 -chloro-2, 3 -dimetylobutanal 2/4

Polecenie Narysuj wzór półstrukturalny aldehydu 3 -chloro-2, 3 -dimetylobutanal 2/4

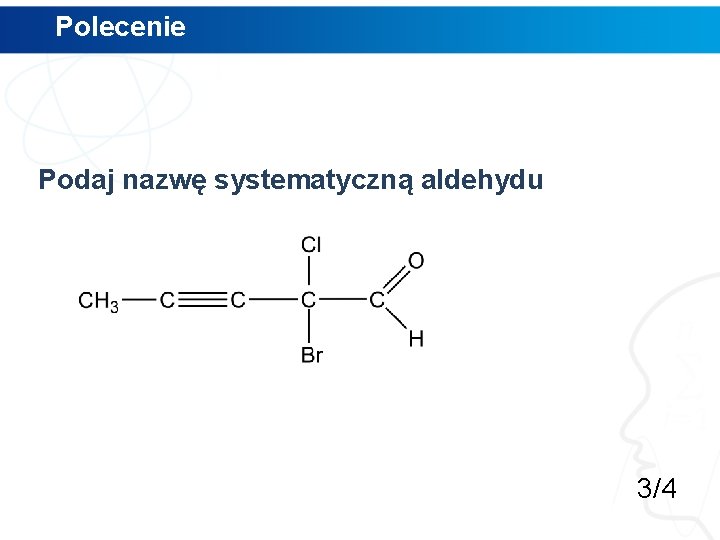
Polecenie Podaj nazwę systematyczną aldehydu 3/4

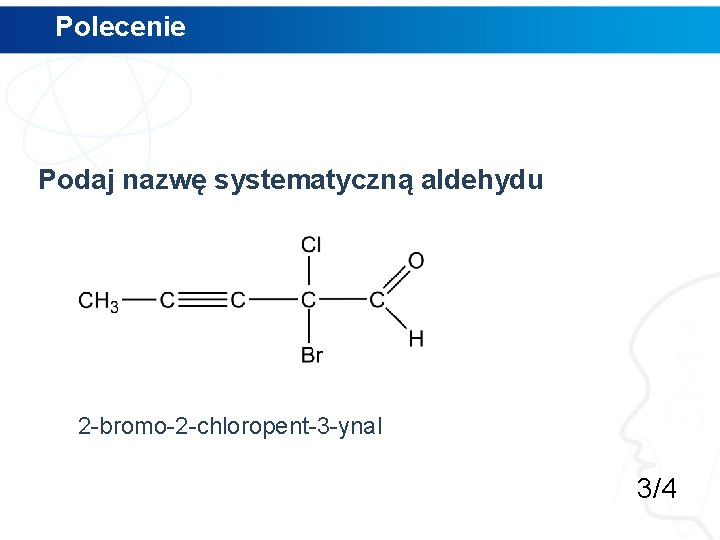
Polecenie Podaj nazwę systematyczną aldehydu 2 -bromo-2 -chloropent-3 -ynal 3/4

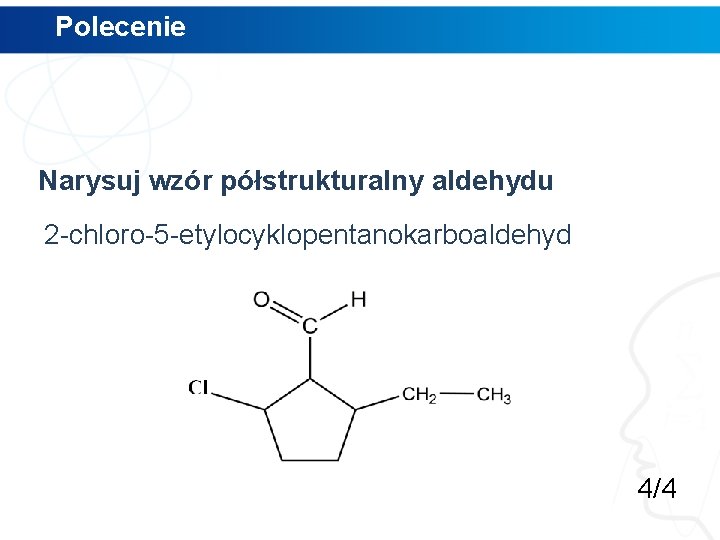
Polecenie Narysuj wzór półstrukturalny aldehydu 2 -chloro-5 -etylocyklopentanokarboaldehyd 4/4

Polecenie Narysuj wzór półstrukturalny aldehydu 2 -chloro-5 -etylocyklopentanokarboaldehyd 4/4

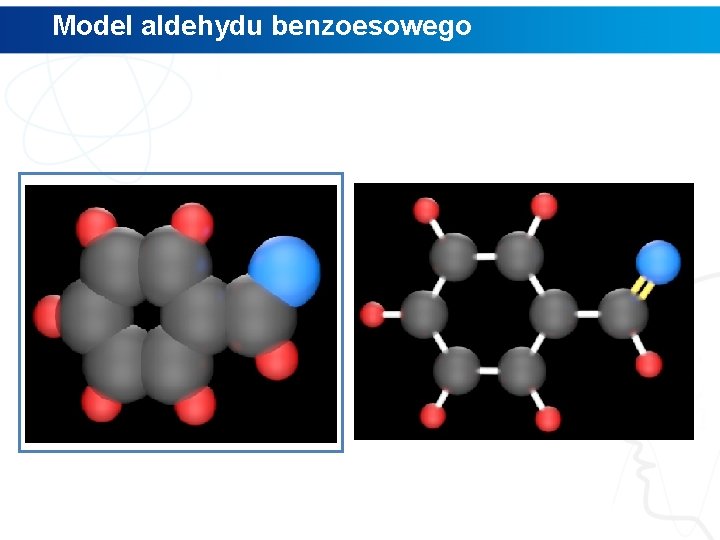
Model aldehydu benzoesowego

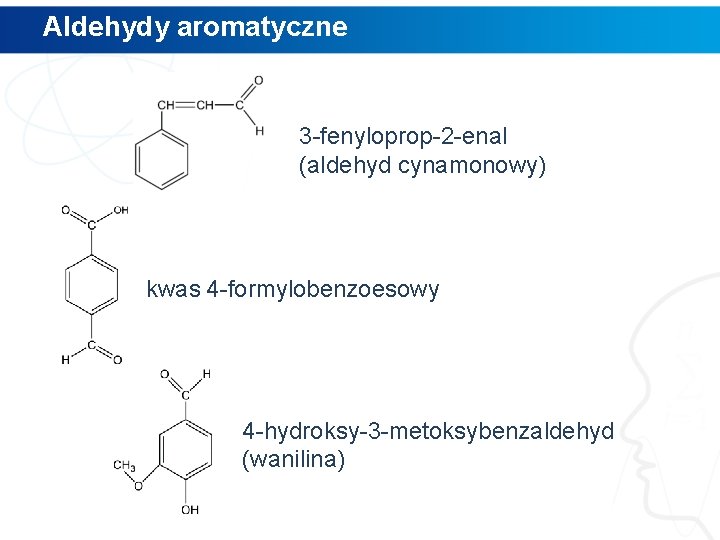
Aldehydy aromatyczne 3 -fenyloprop-2 -enal (aldehyd cynamonowy) kwas 4 -formylobenzoesowy 4 -hydroksy-3 -metoksybenzaldehyd (wanilina)

Polecenie 1. Wskaż, gdzie w modelu aldehydu benzoesowego znajduje się grupa aldehydowa. 2. Przeanalizuj, w jaki sposób łączą się ze sobą atomy węgla, tlenu oraz wodoru w tej grupie. 3. Za pomocą programu Chem. Skech narysuj wzór aldehydu benzoesowego oraz alkoholu, z którego możemy go otrzymać. 4. Obejrzyj narysowane przez Ciebie struktury w przestrzeni trójwymiarowej, wykorzystując funkcje programu Chem. Skech o nazwie 3 D Viewer.

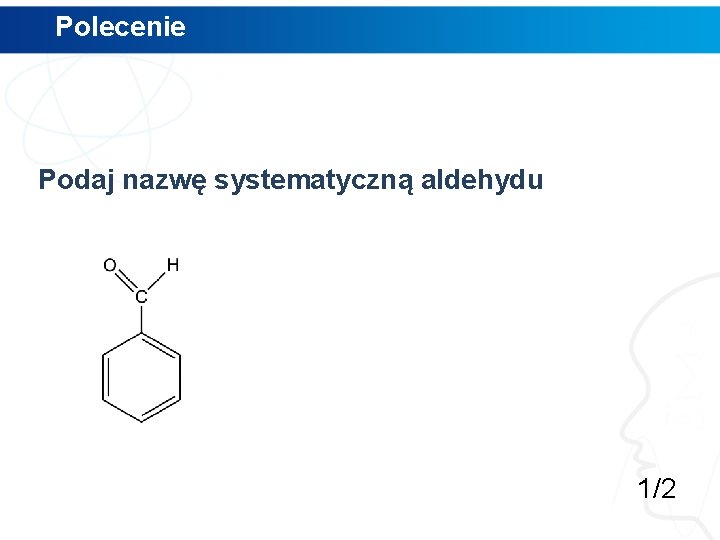
Polecenie Podaj nazwę systematyczną aldehydu 1/2

Polecenie Podaj nazwę systematyczną aldehydu benzenokarboaldehyd 1/2

Polecenie Narysuj wzór półstrukturalny aldehydu cykloheksanokarboaldehyd 2/2

Polecenie Narysuj wzór półstrukturalny aldehydu cykloheksanokarboaldehyd 2/2

Polecenie 1. Wyszukaj w zasobach Internetu temperatury wrzenia dziesięciu wybranych aldehydów. 2. Posortuj je w programie Excel. 3. Zrób odpowiedni wykres zależności temperatury wrzenia aldehydów od liczby atomów węgla w ich cząsteczkach.

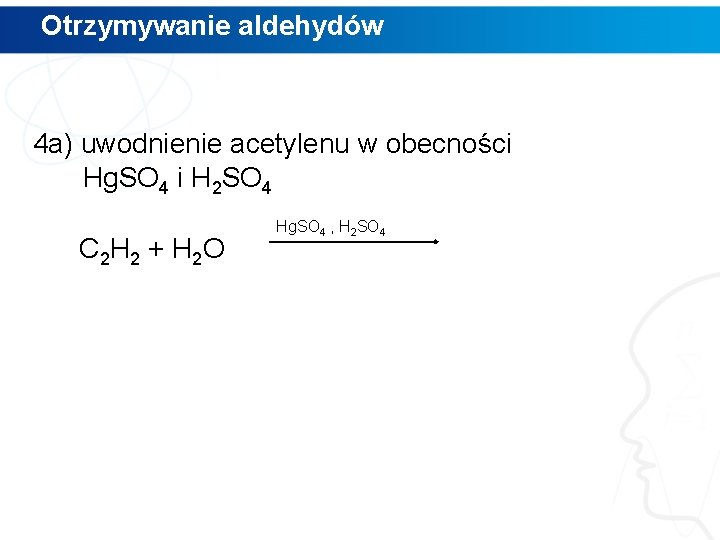
Otrzymywanie aldehydów 1. utlenianie alkoholi I-rzędowych z udziałem Cu. O, w obecności katalizatora 2. katalityczne utlenianie alkoholi (metoda przemysłowa) 3. odwodornienie alkoholi I-rzędowych 4. reakcje specyficzne: a) uwodnienie acetylenu w obecności Hg. SO 4 i H 2 SO 4 b) utlenienie etylenu w obecności katalizatorów

Otrzymywanie aldehydów 1. utlenianie alkoholi I-rzędowych z udziałem Cu. O, w obecności katalizatora CH 3 CH 2 OH + Cu. O

Otrzymywanie aldehydów 1. utlenianie alkoholi I-rzędowych z udziałem Cu. O, w obecności katalizatora CH 3 CH 2 OH + Cu. O CH 3 CHO + Cu + H 2 O etanal

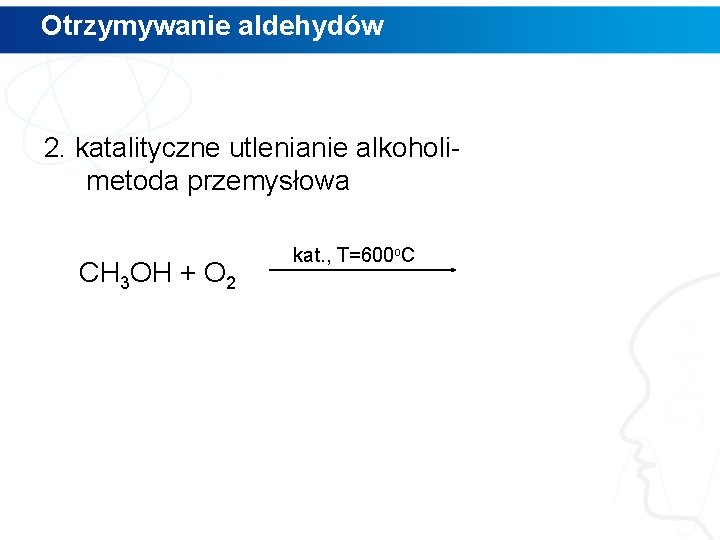
Otrzymywanie aldehydów 2. katalityczne utlenianie alkoholimetoda przemysłowa CH 3 OH + O 2 kat. , T=600 o. C

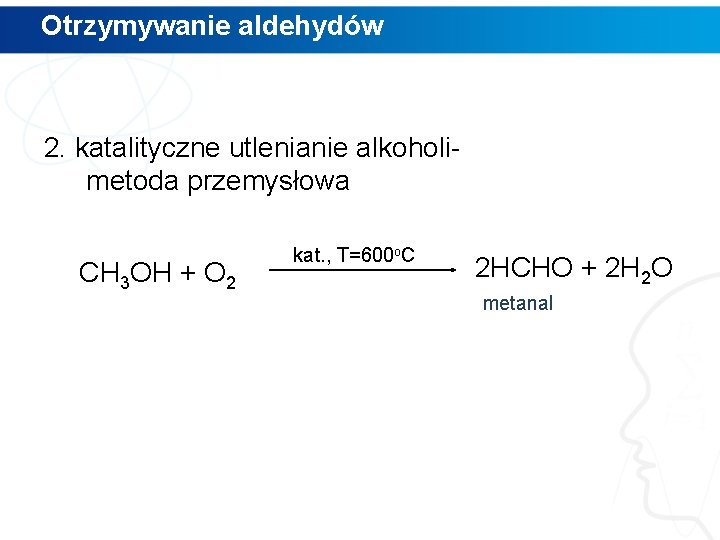
Otrzymywanie aldehydów 2. katalityczne utlenianie alkoholimetoda przemysłowa CH 3 OH + O 2 kat. , T=600 o. C 2 HCHO + 2 H 2 O metanal

Otrzymywanie aldehydów 3. odwodornienie alkoholi I-rzędowych CH 3 CH 2 OH kat.

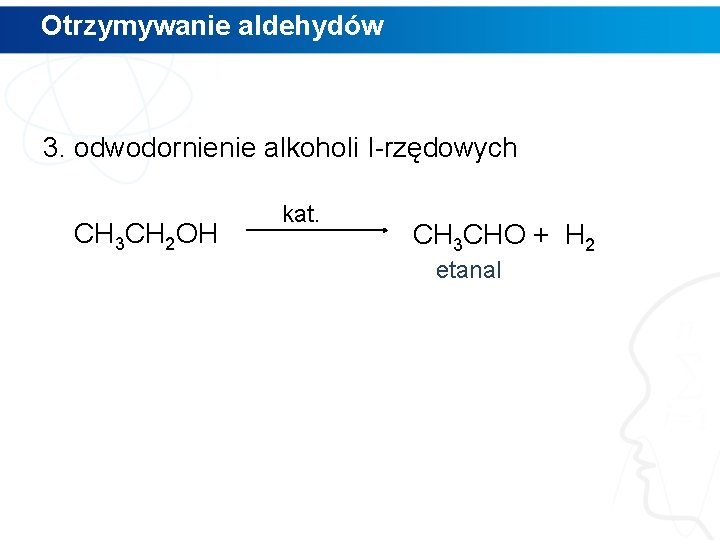
Otrzymywanie aldehydów 3. odwodornienie alkoholi I-rzędowych CH 3 CH 2 OH kat. CH 3 CHO + H 2 etanal

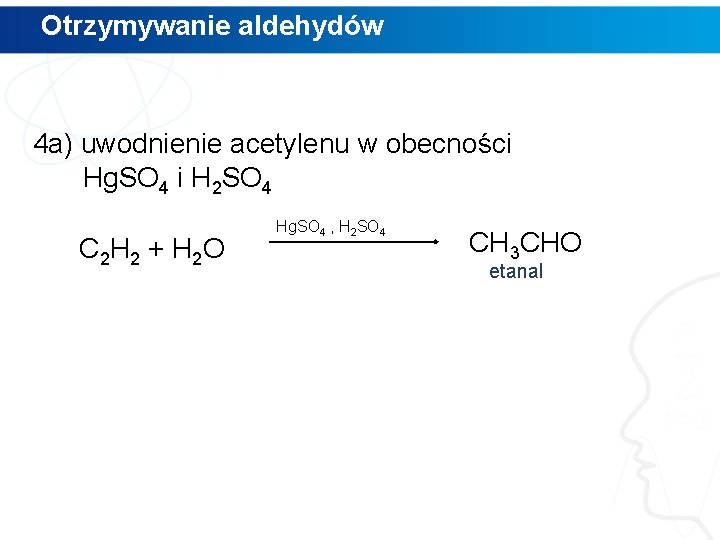
Otrzymywanie aldehydów 4 a) uwodnienie acetylenu w obecności Hg. SO 4 i H 2 SO 4 C 2 H 2 + H 2 O Hg. SO 4 , H 2 SO 4

Otrzymywanie aldehydów 4 a) uwodnienie acetylenu w obecności Hg. SO 4 i H 2 SO 4 C 2 H 2 + H 2 O Hg. SO 4 , H 2 SO 4 CH 3 CHO etanal

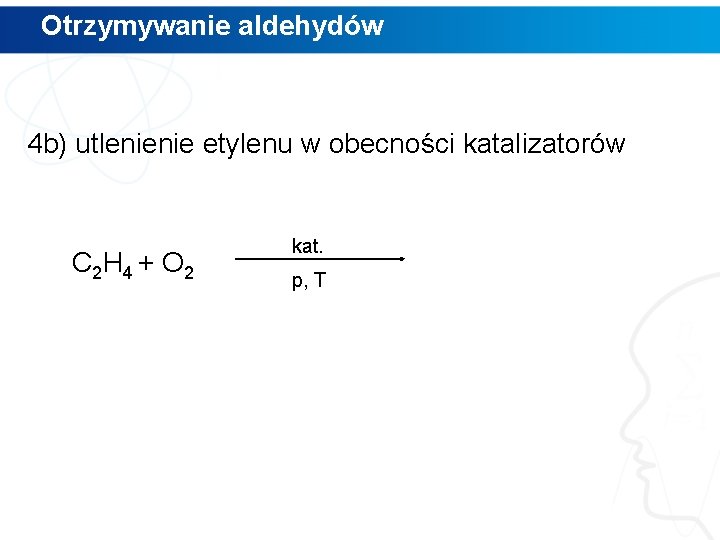
Otrzymywanie aldehydów 4 b) utlenienie etylenu w obecności katalizatorów C 2 H 4 + O 2 kat. p, T

Otrzymywanie aldehydów 4 b) utlenienie etylenu w obecności katalizatorów C 2 H 4 + O 2 kat. p, T 2 CH 3 CHO etanal

Otrzymywanie aldehydów Otrzymywanie aldehydu octowego 39

Właściwości fizyczne aldehydów METANAL → w warunkach normalnych gaz o ostrym, charakterystycznym zapachu → bardzo dobrze rozpuszcza się w wodzie → związek toksyczny → drażni błony śluzowe i powoduje łzawienie → roztwór 40% to formalina (bezbarwna, lotna ciecz o drażniącym zapachu) ETANAL → bezbarwna ciecz o drażniącym zapachu → dobrze rozpuszcza się w wodzie Kolejne aldehydy to również ciecze.

Właściwości fizyczne aldehydów Właściwości aldehydów zależą od: • rodzaju grupy węglowodorowej połączonej z grupą funkcyjną • obecności grupy karbonylowej

Polecenie 1. Wyszukaj w zasobach Internetu informacje na temat formaliny i jej zastosowań. 2. Utwórz krótką notatkę na ten temat korzystając z edytora tekstu i grafiki.

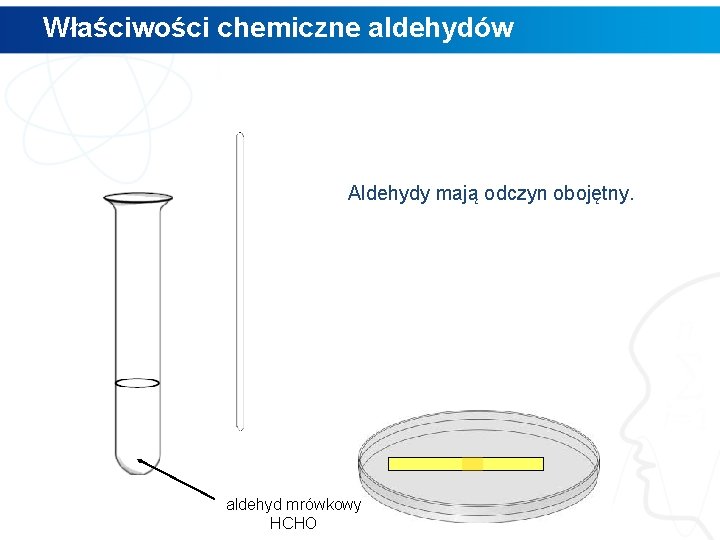
Właściwości chemiczne aldehydów Aldehydy mają odczyn obojętny. aldehyd mrówkowy HCHO

Właściwości chemiczne aldehydów Właściwości redukujące: • próba Tollensa • próba Trommera Właściwości utleniające: • redukcja do alkoholi I-rzędowych alkohol I-rzędowy utlenianie aldehyd redukcja kwas karboksylowy

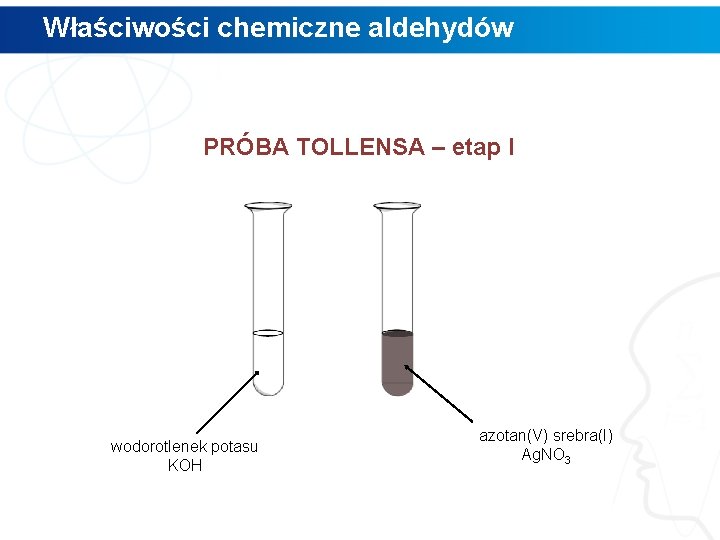
Właściwości chemiczne aldehydów PRÓBA TOLLENSA – etap I wodorotlenek potasu KOH azotan(V) srebra(I) Ag. NO 3

Właściwości chemiczne aldehydów PRÓBA TOLLENSA – etap I wodorotlenek srebra Ag. OH

Właściwości chemiczne aldehydów PRÓBA TOLLENSA – etap II wodorotlenek srebra(I) Ag. OH jest substancją nietrwałą i ulega rozkładowi do tlenku srebra(I) Ag 2 O woda destylowana

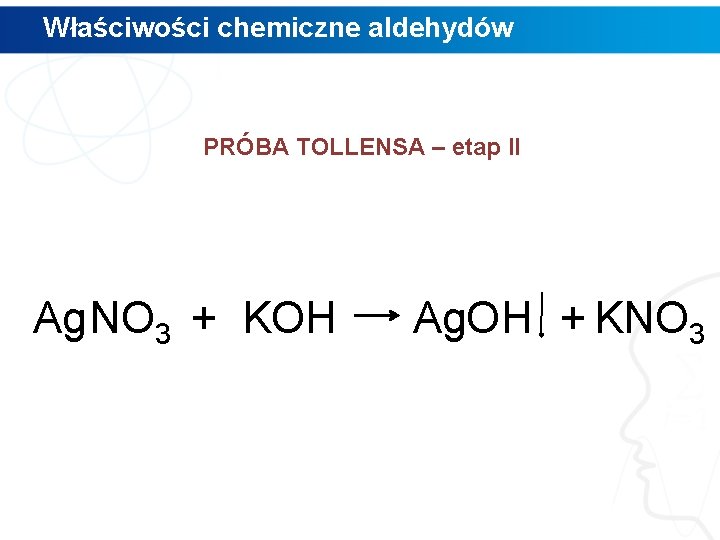
Właściwości chemiczne aldehydów PRÓBA TOLLENSA – etap II Ag. NO 3 + KOH Ag. OH + KNO 3

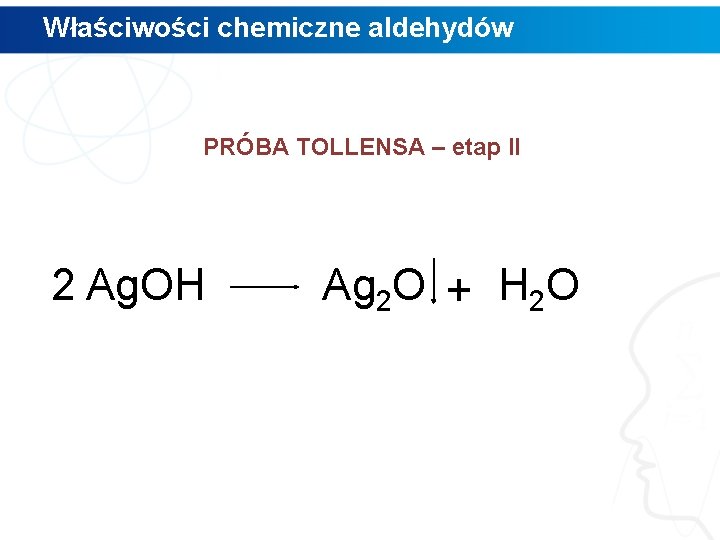
Właściwości chemiczne aldehydów PRÓBA TOLLENSA – etap II 2 Ag. OH Ag 2 O + H 2 O

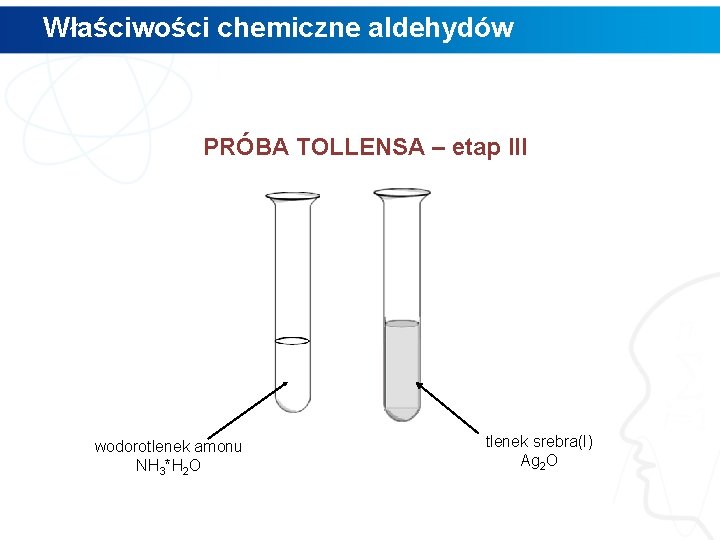
Właściwości chemiczne aldehydów PRÓBA TOLLENSA – etap III wodorotlenek amonu NH 3*H 2 O tlenek srebra(I) Ag 2 O

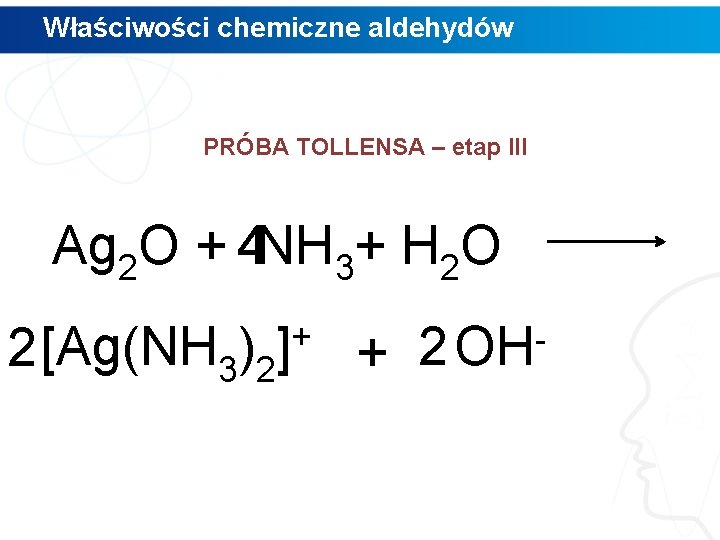
Właściwości chemiczne aldehydów PRÓBA TOLLENSA – etap III Ag 2 O + 4 NH 3+ H 2 O 2 [Ag(NH 3)2 + ] + 2 OH -

Polecenie Korzystając z informacji znalezionych w Internecie, przygotuj kartę charakterystyki aldehydu mrówkowego (substratu w kolejnym etapie doświadczenia)
![Właściwości chemiczne aldehydów PRÓBA TOLLENSA etap IV metanal HCHO wodorotlenek diaminasrebraI AgNH 32 Właściwości chemiczne aldehydów PRÓBA TOLLENSA – etap IV metanal HCHO wodorotlenek diaminasrebra(I) [Ag(NH 3)2]+](https://slidetodoc.com/presentation_image_h/9ababb30b7449af5835239a0e13182f8/image-53.jpg)
Właściwości chemiczne aldehydów PRÓBA TOLLENSA – etap IV metanal HCHO wodorotlenek diaminasrebra(I) [Ag(NH 3)2]+

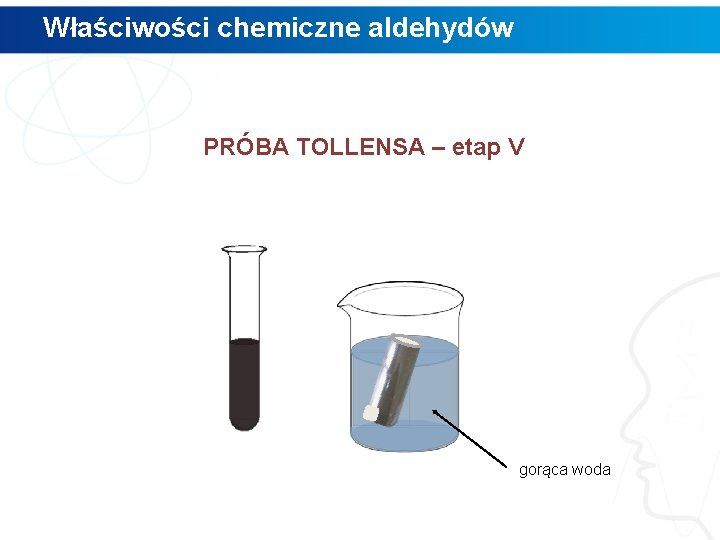
Właściwości chemiczne aldehydów PRÓBA TOLLENSA – etap V gorąca woda

Polecenie Sformułuj wnioski, ilustrując przebieg próby Tollensa odpowiednimi rysunkami (korzystaj z programów graficznych).
![Właściwości chemiczne aldehydów PRÓBA TOLLENSA etap V AgNH 2 Właściwości chemiczne aldehydów PRÓBA TOLLENSA – etap V + [Ag(NH ) ] 2 +](https://slidetodoc.com/presentation_image_h/9ababb30b7449af5835239a0e13182f8/image-56.jpg)
Właściwości chemiczne aldehydów PRÓBA TOLLENSA – etap V + [Ag(NH ) ] 2 + HCHO 3 2 2 Ag↓ + HCOO- + 4 NH 3 + 2 H 2 O

Zastosowanie próby Tollensa Próba Tollensa jest wykorzystywana przy produkcji luster oraz ozdób choinkowych.

Właściwości chemiczne aldehydów Właściwości redukujące: • próba Tollensa • próba Trommera Właściwości utleniające: • redukcja do alkoholi I-rzędowych alkohol I-rzędowy utlenianie aldehyd redukcja kwas karboksylowy

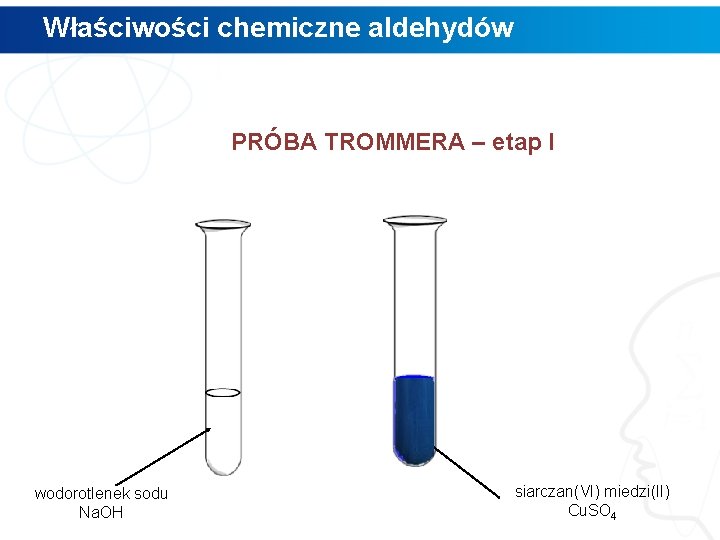
Właściwości chemiczne aldehydów PRÓBA TROMMERA – etap I wodorotlenek sodu Na. OH siarczan(VI) miedzi(II) Cu. SO 4

Właściwości chemiczne aldehydów PRÓBA TROMMERA – etap II formalina HCHO wodorotlenek miedzi(II) Cu(OH)2

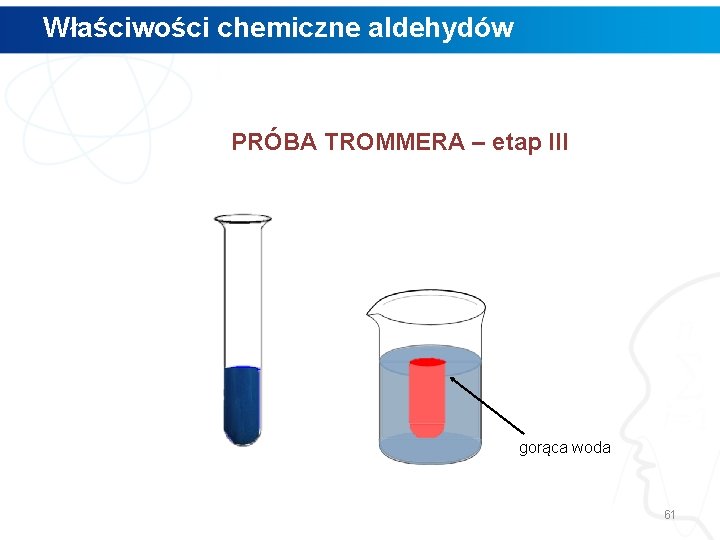
Właściwości chemiczne aldehydów PRÓBA TROMMERA – etap III gorąca woda 61

Polecenie Sformułuj wnioski, ilustrując przebieg próby Trommera odpowiednimi rysunkami (korzystaj z programów graficznych).

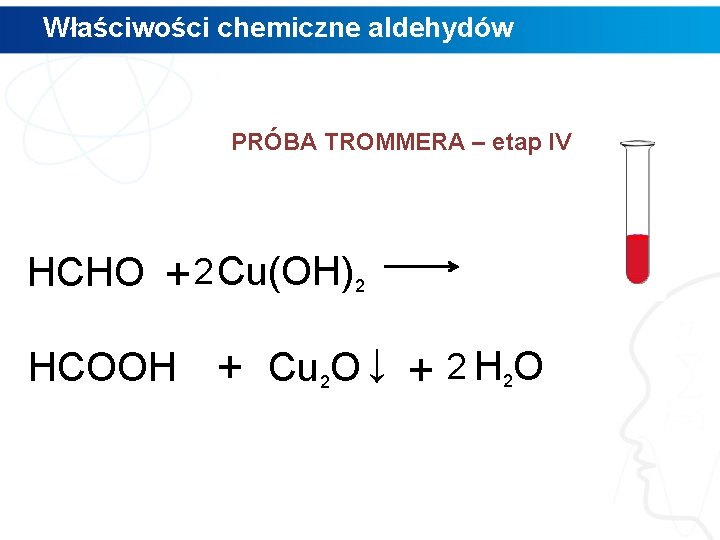
Właściwości chemiczne aldehydów PRÓBA TROMMERA – etap IV HCHO + 2 Cu(OH)2 HCOOH + Cu 2 O ↓ + 2 H 2 O

Właściwości chemiczne aldehydów I II metanal wodorotlenek miedzi(II) kwas mrówkowy tlenek miedzi(I) Metanal w reakcji z wodorotlenkiem miedzi(II) zredukował miedź ze stopnia utlenienia II do I, a sam utlenił się do kwasu mrówkowego.

Zastosowanie próby Trommera Próba Trommera jest wykorzystywana także do wykazania właściwości redukujących cukrów. przykład utlenienie glukozy do kwasu glukonowego

Próba Trommera Wykrywanie obecności glukozy w winogronach 66

Właściwości chemiczne aldehydów Właściwości redukujące: • próba Tollensa • próba Trommera Właściwości utleniające: • redukcja do alkoholi I-rzędowych alkohol I-rzędowy utlenianie aldehyd redukcja kwas karboksylowy

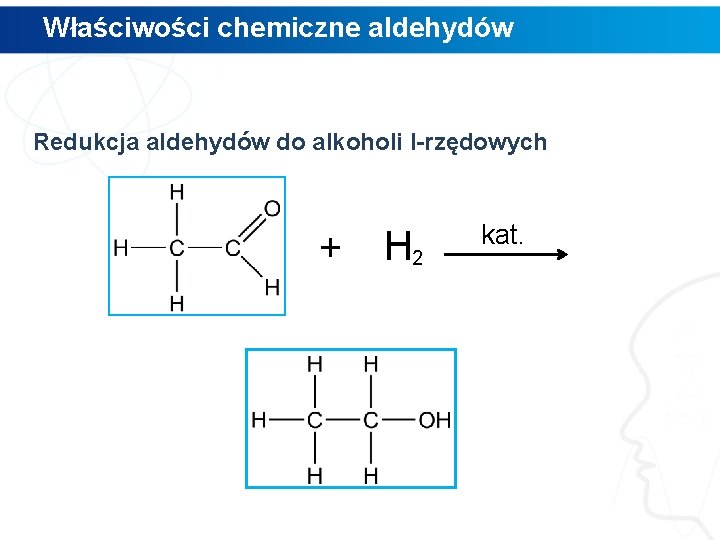
Właściwości chemiczne aldehydów Redukcja aldehydów do alkoholi I-rzędowych + H 2 kat.

Występowanie aldehydów q cytral Aldehyd, od którego pochodzi cytrynowy zapach olejku eterycznego, otrzymywanego z liści mirtu cytrynowego i trawy cytrynowej. Występuje w postaci mieszaniny izomerów cis (jako neral) i trans (jako geranial). q aldehyd cynamonowy Nadaje cynamonowy zapach i korzenny smak. Olejek ten występuje w korzeniach, liściach i korze cynamonowca.

Zastosowanie aldehydów qwanilina – w przemyśle spożywczym i cukierniczym, jako substancja zapachowa q cynamal – do aromatyzowania słodyczy, sosów i napojów q aldehyd glutarowy i aldehyd bursztynowy – do dezynfekcji narzędzi dentystycznych i chirurgicznych (właściwości wirusobójcze, bakteriobójcze i grzybobójcze)

Zastosowanie aldehydów q aldehyd mukonowy – w preparatach brązujących q aldehyd mrówkowy – jako substancja konserwująca w kosmetykach (właściwości bakteriobójcze), do produkcji tworzyw sztucznych, barwników i leków q aldehyd octowy– do produkcji kwasu etanowego

Polecenie Narysuj cząsteczkę aldehydu benzoesowego oraz butanalu. Skorzystaj z dowolnego programu do modelowania struktury związków chemicznych (na przykład ISIS Draw).

Przypomnijmy Co to jest reakcja dysproporcjonowania?

Przypomnijmy Dysproporcjonowanie typ reakcji chemicznej, w której jedno indywiduum ulega równoczesnemu utlenieniu i redukcji.

Reakcja Cannizzaro Aldehydy, które nie mają atomów wodoru przy drugim atomie węgla w szkielecie węglowym, w środowisku silnie zasadowym ulegają dysproporcjonowaniu. Są to tzw. reakcje Cannizzaro.

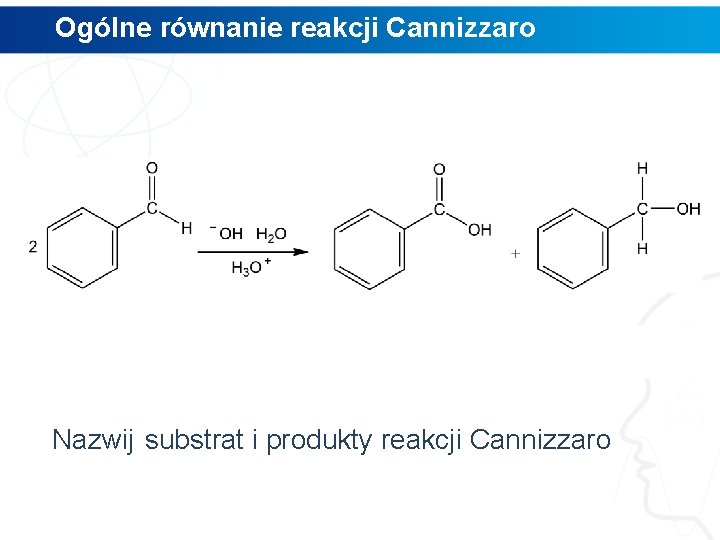
Ogólne równanie reakcji Cannizzaro Nazwij substrat i produkty reakcji Cannizzaro

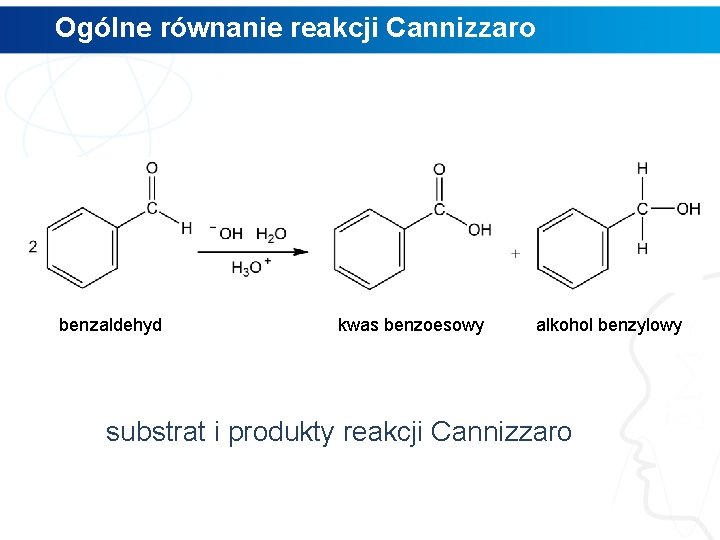
Ogólne równanie reakcji Cannizzaro benzaldehyd kwas benzoesowy alkohol benzylowy substrat i produkty reakcji Cannizzaro

Mechanizm reakcji Cannizzaro opis mechanizm

Mechanizm reakcji Cannizzaro Reakcja Cannizzaro zachodzi poprzez addycję nukleofilową jonu wodorotlenowego do aldehydu. Powstaje wówczas tetraedryczny produkt pośredni, z którego możliwe jest odczepienie jonu wodorkowego. Następnie druga cząsteczka aldehydu przyjmuje ten jon wodorkowy (w procesie addycji) – zachodzi reakcja dysproporcjonowania. W jednej cząsteczce aldehydu następuje podstawienie jonu wodorkowego przez jon wodorotlenowy i cząsteczka ta zostaje ona utleniona do kwasu. Druga cząsteczka aldehydu łączy się z jonem wodorkowym i w konsekwencji redukuje się do alkoholu.

Polecenie Powtórzmy budowę i nazewnictwo aldehydów GRA EDUKACYJNA MEMORY 1. Skorzystaj z gotowej gry Memory. Klikaj w zakryte karty i szukaj par. 2. Przygotuj samodzielnie podobną grę, korzystając z dowolnego programu (np. Scratch lub Flash).

 Zasady tworzenia prezentacji
Zasady tworzenia prezentacji Transakcyjna baza danych
Transakcyjna baza danych Gradient obrazu
Gradient obrazu Przetwarzanie rozproszone
Przetwarzanie rozproszone Prezentacja multimedialna program
Prezentacja multimedialna program Prawo autorskie prezentacja
Prawo autorskie prezentacja Prawo autorskie w szkole
Prawo autorskie w szkole Kodowanie informacji
Kodowanie informacji Kody huffmana
Kody huffmana Naturalny kod binarny
Naturalny kod binarny Kodowanie predykcyjne
Kodowanie predykcyjne Symetria kwiatów
Symetria kwiatów Danuta stanek
Danuta stanek Innowacja kodowanie w przedszkolu
Innowacja kodowanie w przedszkolu Delatnosti ljudi 3 razred
Delatnosti ljudi 3 razred Upravni i neupravni govor 3 razred kontrolni
Upravni i neupravni govor 3 razred kontrolni Obim pravougaonika kvadrata i trougla
Obim pravougaonika kvadrata i trougla Prvi keplerov zakon
Prvi keplerov zakon Kviz za 3 razred
Kviz za 3 razred Vodena zivotna zajednica
Vodena zivotna zajednica Sta su materijali priroda i drustvo
Sta su materijali priroda i drustvo Diktat za 3 razred osnovne skole
Diktat za 3 razred osnovne skole Třecí síla
Třecí síla Třecí síla
Třecí síla Rap muzika
Rap muzika Tradycyjny strój śląski
Tradycyjny strój śląski Zespół downa prezentacja
Zespół downa prezentacja Symetria w przyrodzie prezentacja
Symetria w przyrodzie prezentacja Moskiewskie metro prezentacja
Moskiewskie metro prezentacja Mózgowie ryby
Mózgowie ryby Organizacja pracy małych zespołów prezentacja
Organizacja pracy małych zespołów prezentacja Warstwy skóry właściwej
Warstwy skóry właściwej Podroby
Podroby Medycyna w starożytności prezentacja
Medycyna w starożytności prezentacja Tajga krajobraz
Tajga krajobraz Programy rezerwacyjne w hotelarstwie
Programy rezerwacyjne w hotelarstwie Budowa wnętrza ziemi prezentacja
Budowa wnętrza ziemi prezentacja Prezentacja ptaki
Prezentacja ptaki Grzyby prezentacja
Grzyby prezentacja Pacyficzny pierścień ognia prezentacja
Pacyficzny pierścień ognia prezentacja Zaczarowana zagroda prezentacja
Zaczarowana zagroda prezentacja Czas i miejsce akcji pinokia
Czas i miejsce akcji pinokia Klaudia hofman
Klaudia hofman Iii rozbiór polski
Iii rozbiór polski Agregaty prądotwórcze psp prezentacja
Agregaty prądotwórcze psp prezentacja Dziękuję za uwagę
Dziękuję za uwagę Hitler partia
Hitler partia Maria skłodowska curie ciekawostki
Maria skłodowska curie ciekawostki Historia mojej rodziny prezentacja
Historia mojej rodziny prezentacja Renesans ramy czasowe
Renesans ramy czasowe Wszyscy bogowie rzymscy
Wszyscy bogowie rzymscy Co to liternet
Co to liternet Nike z samotraki autor
Nike z samotraki autor Prezentacja rozmowa kwalifikacyjna
Prezentacja rozmowa kwalifikacyjna Mnemotechniki prezentacja
Mnemotechniki prezentacja Bryła geometryczna o kolistej podstawie z wierzchołkiem
Bryła geometryczna o kolistej podstawie z wierzchołkiem Liście pułapkowe funkcje
Liście pułapkowe funkcje Pojezierze wielkopolskie klimat
Pojezierze wielkopolskie klimat Adwent czas oczekiwania prezentacja
Adwent czas oczekiwania prezentacja Organizacje międzynarodowe tomaszewska prezentacja
Organizacje międzynarodowe tomaszewska prezentacja Formy wypukłe terenu
Formy wypukłe terenu Prezentacja past simple
Prezentacja past simple Historia hymnu polskiego prezentacja
Historia hymnu polskiego prezentacja Niewola babilońska prezentacja
Niewola babilońska prezentacja Imiona mozarta
Imiona mozarta Ochrona przyrody prezentacja
Ochrona przyrody prezentacja Pecha kucha prezentacja
Pecha kucha prezentacja Wypalenie zawodowe prezentacja
Wypalenie zawodowe prezentacja Aleksandra maksym
Aleksandra maksym Metanol wzór sumaryczny
Metanol wzór sumaryczny Zwierzęta w wielkopolskim parku narodowym
Zwierzęta w wielkopolskim parku narodowym Kodon definicja
Kodon definicja Armatura wodna prezentacja
Armatura wodna prezentacja Mądrość boża prezentacja
Mądrość boża prezentacja Zabytki anglii prezentacja
Zabytki anglii prezentacja Prezentacja o saturnie
Prezentacja o saturnie Pierwsze przykazanie boże prezentacja
Pierwsze przykazanie boże prezentacja Antyczne wzorce bohaterów
Antyczne wzorce bohaterów Bibliografia na prezentacji
Bibliografia na prezentacji Znak p8c
Znak p8c Pierwsza pralka na świecie
Pierwsza pralka na świecie Prezentacja dorobku zawodowego nauczyciela stażysty
Prezentacja dorobku zawodowego nauczyciela stażysty