200 Jahre Gesellschaft fr Natur und Heilkunde in
























![Entdeckung des Urans 1789 Pechblende in Salpetersäure gelöst [ UO 2(NO 3)2], Neutralisation mit Entdeckung des Urans 1789 Pechblende in Salpetersäure gelöst [ UO 2(NO 3)2], Neutralisation mit](https://slidetodoc.com/presentation_image_h2/6fdbf8169d7632356ff8327142f25c61/image-29.jpg)














- Slides: 43

200 Jahre Gesellschaft für Natur- und Heilkunde in Berlin Die Bedeutung Martin Heinrich Klaproths und Sigismund Friedrich Hermbstaedts für die moderne Chemie Prof. Dr. Jörn Müller Institut für Chemie Technische Universität Berlin 25. Februar 2010

Martin Heinrich Klaproth geb. 01. 12. 1743 in Wernigerode gest. 01. 1817 in Berlin Mitglied Nr. 1 Sigismund Friedrich Hermbstaedt geb. 14. 04. 1760 in Erfurt gest. 22. 10. 1833 in Berlin Mitglied Nr. 11

Die Gründungsmitglieder Gesellschaft für Natur- und Heilkunde in Berlin


Klaproths Lebensweg I Geboren am 01. 12. 1743 in Wernigerode als Sohn eines armen Schneiders. Bis Ende 1758 Schulbesuch in Wernigerode. Bis Ostern 1764 Lehrjunge der Rats-Apotheke Quedlinburg. Bis Ostern 1766 Geselle der Rats-Apotheke Quedlinburg. Bis Ostern 1768 Geselle der Hof-Apotheke Hannover. Bis 1770 Geselle der Mohren-Apotheke Berlin sowie Weiterbildung (Analytik) bei den Chemikern Johann Heinrich Pott (1692 1777) und Andreas Sigismund Marggraf (1709 1782). Bis 1771 Geselle der Rats-Apotheke Danzig. März bis Ende April 1771 Geselle in der Schwan-Apotheke Berlin, enge Freundschaft mit dem Besitzer Valentin Rose d. Älteren (1736 1771). Nach dessen Tod Provisor der Apotheke und Vormund des Sohnes Valentin Rose d. Jüngeren (1762 1807). 13. 02. 1780 Heirat mit der vermögenden Christiane Sophie Lehmann (eine Nichte Marggrafs). Valentin Rose d. Ä. verheiratet mit einer anderen Nichte Marggrafs; eine ihrer Töchter verheiratet mit Hermbstaedt; damit war Klaproth der angeheiratete Onkel von Hermbstaedt. Geburtsstätte Marggraf

Klaproths Lebensweg II 1780 Erwerb der Bären-Apotheke in Berlin (ursprünglich gegründet vom Vater A. S. Marggrafs, der Schwan-Apotheke in der Spandauer Straße benachbart). Ablegen des pharmazeutischen Examens. Einrichtung eines chemischen Laboratoriums. 1800 Veräußerung der inzwischen zu großem Ansehen gelangten Apotheke. Gedenktafel Spandauer Str. 25

Klaproths Lebensweg III Seit 1782 Dozentur am Collegium medico-chirurgicum. Seit 1783 Privatvorlesungen in Chemie. Seit 1784 Lehramt an der Bergakademie (Vorläufer der TU Berlin). Seit 1787 Dozentur an der Artillerieakademie. 1788 Wahl zum ordentlichen Mitglied der Akademie der Wissenschaften. 1800 Ernennung zum ordentlichen Chemiker der Akademie als Nachfolger von Franz Carl Achard (1753 1821; Errichter der ersten Rübenzuckerfabrik der Welt). 1803 Fertigstellung des neuen chemischen Laboratoriums der Akademie (Nutzungsrecht später an Universität). 1810 Berufung zum Professor der Chemie an der neugegründeten Berliner Universität auf Vorschlag von Alexander von Humboldt. F. C. Achard

Klaproths Lebensweg IV Klaproth nach 1811 1813 Erster Schlaganfall, dem weitere folgten. 1. Januar 1817 Todestag (73 Jahre alt). Grabrede von Hermbstaedt. Das chemische Laboratorium in der Dorotheenstraße 10 Gedenktafel am Dorotheenstädtischen Friedhof

Klaproths Nachfolge an der Universität Der Lehrstuhl von Klaproth blieb 5 Jahre vakant. Berzelius lehnte einen Ruf an die Universität ab, schlug stattdessen seinen Schüler Eilhard Mitscherlich (1794 1863) vor. 1822 Berufung von E. Mitscherlich als a. o. , 1825 als o. Professor.

Hermbstaedts Lebensweg I Geboren am 14. 04. 1760 in Erfurt als Sohn eines Actuarius und Stadtvoigts. Nach Schulbesuch 1774 Studium der Arzneiwissenschaft an der Universität zu Erfurt. Der Chemiker Wilhelm Bernhard Trommsdorf (1738 1782) weckt sein Interesse an Chemie und Pharmakologie. Nach Promotion zum Dr. phil. Übersiedlung nach Langensalza als Repetent der chemischen Vorlesungen von Johann Christian Wiegleb (1732 1800). Erweiterung der chemischen und pharmazeutischen Kenntnisse. 1782 1784 Officium in der Ratsapotheke in Hamburg. 1784 für 1 Jahr Provisor der Apotheke zum weißen Schwan in Berlin (4 Jahre nach Ausscheiden von Klaproth). Beginn der Freundschaft mit Klaproth. 1786 Studienreise u. a. nach Göttingen, Halle, Leipzig, Freiberg; Bekanntschaft mit namhaften Wissenschaftlern, darunter Johann Beckmann (1739 1811), Ökonom, Physiker und Naturforscher und Begründer Technologie; ferner Johann Friedrich Gmelin (1748 1804), bekannt durch sein Werk „Grundsätze der Technischen Chemie“ (1786). Beckmann Gmelin

Hermbstaedts Lebensweg II Seit 1787 Privatvorlesungen über Physik, Chemie, Technologie, Pharmazie. 1788 Eheschließung mit Magdalena Rose, Tochter von Valentin Rose d. Ä. 1790 96 Führung der Kgl. Hofapotheke. Seit 1790 Professor für pharmazeutische Chemie am Collegium medicochirurgicum. Seit 1794 Dozentur für Experimentalphysik an der Bergakademie. 1794 Titel Obersanitätsrat, Berufung in das Obercollegium sanitatis. Seit 1795 Chemie- und Physikvorlesungen für Schüler der Pépinière. 1796 Assessor beim Manufaktur- und Kommerzienkollegium und 1797 Mitglied der Technischen Deputation dieser dem Fabriken-Department unterstehenden Behörde. Beginn der Ausübung des späteren Spezialgebietes: Förderung der Gewerbe auf wissenschaftlicher Grundlage. 1797 Linderung der Atemnot des an „Brustwassersucht“ erkrankten Königs Friedrich Wilhelm II durch Behandlung mit „Lebensluft“ (Sauerstoff). 1798 1808 Kgl. Obermedizinalrat und Generalstabsapotheker für die preußische Armee.

Hermbstaedts Lebensweg III 1800 Wahl zum außerordentlichen, 1808 zum ordentlichen Mitglied in die physikalische Klasse der Akademie der Wissenschaften. 1802 Umzug in ein neu erbautes und großzügig ausgestattetes Arbeits- und Wohnhaus in der Georgenstraße 43; dort bis zum Tode gewohnt und Vorlesungen gehalten sowie experimentiert. 1810 Ernennung zum außerordentlichen, 1811 zum ordentlichen Professor der technologischen Chemie an der Universität Berlin. 1816 Tod der Gattin Magdalena. 1817 Übernahme der Chemievorlesungen Klaproths an der Bergakademie. 1820 Chemie-Unterricht an der Kgl. Allgemeinen Kriegsschule. 1821 Stiftung des „Vereins zur Beförderung des Gewerbefleißes in Preußen“ durch Christian Peter Wilhelm Beuth (1781 1853); Wahl Hermbstaedts zum Vorsteher der Sparte „Physik und Chemie“. 1826 Beteiligung an der Gründung der chemischen Fabrik Kunheim (seit 1928 Kali-Chemie AG). 22. 10. 1833 Plötzlicher und unerwarteter Tod (73 Jahre alt, „Nervenschlag“). Beisetzung auf dem Dorotheenstädtischen Friedhof.

Hermbstaedts Lebensweg IV Urteil eines Zeitgenossen: Hermbstaedt hat bis ins hohe Alter die geistige Kraft und Frische eines Jünglings bewahrt. C. P. W. Beuth Hermbstaedts Ordinariat blieb unbesetzt, da kein Nachfolger zu finden war, der die Technologie in vergleichbarer Breite zu vertreten vermochte. Erst 1873 Errichtung eines Extraordinariats für Technologie. Gedenkstele nach Entwurf Schinkel

Klaproth als Analytiker • Zitat Berzelius: „Klaproth ist der größte analytische Chemiker Europas. “ • Erkannte als erster die Notwendigkeit, quantitativ wichtige Niederschläge vor dem Wägen bis zur Gewichtskonstanz bei bestimmten Temperaturen zu trocknen bzw. zu glühen (u. a. durch Nutzung der Brennöfen bei KPM). • Forderung nach reinsten Reagenzien. Peinliche Vermeidung von Fehlerquellen, z. B. Einfluss von Arbeitsgeräten (Tiegelmaterial). • Einführung des Brauches, nicht nur die Endergebnisse, sondern auch die Einzelgewichte der erhaltenen Niederschläge anzugeben. • Verbesserung des Silikataufschlusses durch Alkalischmelze im Silbertiegel. Zum Nachweis von Alkalien in Mineralien Einführung des Silikataufschlusses mit Bariumnitrat, später mit Bariumcarbonat. • Nachweis von Phosphor als Ursache für die gefürchtete Kaltbrüchigkeit von Eisen. • • • Ausfällung und Abtrennung des Eisen(III) von Mangan durch Natriumsuccinat. Äußerst sorgfältige ebenso wie selbstkritische Arbeitsweise. Klaproth beendete den (den Wissenschaftsfortschritt hemmenden) Unfug, nach willkürlichen Vorstellungen korrigierte Resultate vorzulegen.

Klaproth als Mineraloge • Einige 100 quantitative Analysen an Mineralien aus aller Welt, die meisten vielmals durchgeführt. Jedoch keinerlei systematische Folgerungen an die Ergebnisse geknüpft. Klaproth verfügte auch nicht über das kristallographische Wissen seines Zeitgenossen René-Just Haüy (1743 1822). • Beispiele für Mineralanalysen: Alaun, Apatit, Rotkupfererz, Gelbbleierz, Basalt, Aragonit, Lepidolith, Dolomit, Smaragd, Topas, Granat, Kryolith. Diverse Steinund Metallmeteore. Weitere Mineralien im Zusammenhang mit der Entdeckung neuer Elemente behandelt. • Anlegen einer bedeutenden Mineraliensammlung mit 4831 Einzelstücken (3139 nichtmetallische, 1486 metallische Mineralien, 23 Meteoriten, 183 größere Stücke). Wurde nach Klaproths Tod von der Universität angekauft. • Entdeckung der Dimorphie am Beispiel Kalkspat/Aragonit. • „Beiträge zur chemischen Kenntnis der Mineralkörper“ (Band I 1795, Band VI 1815). War lange Zeit Standardwerk für exakte Mineralanalysen. • Darüber hinaus hatte Klaproth eine bedeutende Sammlung chemischer Präparate und ein umfassendes Herbarium (von Nicolai als Berliner Sehenswürdigkeit gerühmt).

Die Vier-Elemente-Lehre der Antike und des Mittelalters

Die Vier-Elemente-Lehre der Antike und des Mittelalters

Robert Boyle früher Wegbereiter der modernen Chemie 1627 1692 Physiker, Chemiker, Naturphilosoph. Gründungsmitglied und ab 1680 Präsident der Royal Society in London. Bedeutende Leistungen • Gesetz von Boyle und Mariotte (p · V = const) und andere Gaseigenschaften. • Ablehnung der 4 -Elemente Lehre des Aristoteles ebenso wie der 3 -Prinzipien. Lehre des Paracelsus (Salz, Schwefel, Quecksilber) zugunsten des modernen Elementbegriffs: chemisch unzerlegbare Bausteine der Materie. Verfolgte dennoch alchimistische Bestrebungen zur Elementumwandlung. • Mitbegründer Analytischen Chemie, vor allem nasschemische Analysentechnik. • Anhänger der Corpusculartheorie. • Befürworter gründlicher experimenteller Methoden (Empirie).

Die Phlogistontheorie Irrgarten der Chemie - brennbar Naturwissenschaftl. Versuch, den chemischen Prozess der Verbrennung zu erklären. Frühere Erklärungen nach der Vierelementen-Lehre (Antike, Alchemie) Empedokles: Der brennende Körper setzt Feuerteilchen frei (korpuskular). Aristoteles: Die Verbrennung führt als Prinzipienwechsel zu einer anderen elementaren Zusammensetzung der Materie (abstrakt). Paracelsus (1493 1541): Materie ist aus den Elementen Schwefel, Salz und Quecksilber zusammengesetzt. Bei der Verbrennung eines Körpers werden Schwefelteilchen frei. Basierend auf Vorarbeiten von Johann Joachim Becher (1635 1682) wurde die Phlogiston-Theorie von Georg Ernst Stahl (1659 1734) zu Beginn des 18. Jhr. ausgearbeitet. Einige Kernaussagen: Ein Stoff kann nur verbrennen, wenn er Phlogiston enthält, das bei der Verbrennung entweicht und von der Luft aufgenommen wird. Die entweichenden, unsichtbaren Phlogiston-Partikel setzen andere Partikel in Drehbewegung, die Stoffe erhitzen sich, es entsteht eine Flamme (Phlogiston auch als „Wärmestoff“). Brennende Körper in geschlossenen Gefäßen erlöschen nach einiger Zeit, da die Luft dann mit Phlogiston gesättigt ist.

Die Phlogistontheorie Irrgarten der Chemie Holz + dephlogistierte Luft Asche + phlogistierte Luft Metall + dephlogistierte Luft Rest + phlogistierte Luft Erz + Holzkohle (Phlogiston) Metall + gebundene Luft G. E. Stahl Verbrennung (so auch das Atmen und Rosten) und Reduktion sind also wechselseitige Prozesse: Verbrennung: Stoff A gibt Phlogiston ab, Stoff B nimmt es auf Reduktion: Stoff B gibt das aufgenommene Phlogiston wieder an Stoff A ab Stärke der Theorie: Erste Systematisierung wichtiger chemischer Prozesse aufgrund allgemeingültiger innerer Zusammenhänge, losgelöst von äußeren Stoffmerkmalen. Schwächen: Qualitative Arbeitsweise und Vernachlässigung gasförmiger Reaktionsprodukte führte zu offensichtlichen Widersprüchen. Z. B. wurde die Massenzunahme bei der Metallverbrennung mit negativer Phlogistonmasse erklärt, was wiederum im Widerspruch zur Massenabnahme bei der Holzverbrennung stand.

Phlogistiker, die zum Verfall der Theorie beitrugen 1 Joseph Black 1728 1799 2 Henry Cavendish 3 Carl Wilhelm Scheele 4 Joseph Priestley 1731 1810 1742 1786 1733 1804 1: Reindarstellung von „gebundener Luft“ (CO 2) aus Mg. CO 3 + Säure. Dieses Gas entsteht auch bei der Atmung, Gärung und Verbrennung von Holzkohle. 2: 1766 Darstellung von „brennbarer Luft“ (H 2) (Phlogiston? ) aus Eisen + Säure. Bei der Verbrennung mit „dephlogistierter Luft“ entsteht Wasser (dieses also kein Element!). 3: 1771 Entdeckung von „Feuerluft“ (O 2) über versch. Verfahren. Das „Element“ Luft besteht aus „Feuerluft“ und „verdorbener Luft“ (N 2). Publikation erst 1776. 4: 1774 Isolierung von „dephlogistierter Luft“ (O 2) durch Erhitzen von Hg. O, jedoch nicht als Element erkannt. Priestley-Versuche mit Mäusen.

Antoine Laurent de Lavoisier: Die Widerlegung der Phlogistontheorie 1743 1794 Lavoisier mit seiner Frau Marie 1788 Traité élémentaire de chimie (1789) • Exakte quantitative Arbeitsweise (Messen, Wiegen, Dokumentieren); Entwicklung geeigneter Apparate für volumetrische und gravimetrische Gasanalyse. • Oxidationstheorie (1772 1785): Beim Verbrennen eines Stoffes erfolgt Massezunahme, die dem Verbrauch an „Feuerluft“ (Oxygenium) entspricht. Bei der Reduktion eines Metalloxids mit Kohle wird der Sauerstoff auf das Reduktionsmittel übertragen. • Wiederholung der Cavendish-Versuche: Wasser ist kein Element! • Gesetz von der Erhaltung der Masse. Begründer Stöchiometrie. Bestimmung der %ualen elementaren Zusammensetzung vieler Stoffe. • Neue Namensliste der Elemente und Reformierung der lateinischen Namensgebung.

Akzeptanz der Oxidationstheorie in Deutschland Hermbstaedt hat als erster deutscher Chemiker die Oxidationstheorie von Lavoisier 1791 in seinem Lehrbuch „Systematischer Grundriß der allgemeinen Experimentalchemie“ übernommen. 1792 veröffentlichte er dessen „Traité élémentaire de chimie” unter dem Titel „System der antiphlogistischen Chemie” in deutscher Übersetzung. Klaproth war theoretischen Neuerungen gegenüber grundsätzlich skeptisch und zunächst „weit entfernt, Lavoisiers Theorie zu adoptieren“. 1786 Wiederholung des Lavoisierschen Versuchs der Zerlegung von Wasserdampf (Durchleiten durch glühendes Eisenrohr), jedoch phlogistische Deutung: „Die sich dabei bildende brennbare Luft ist reines (aus dem Eisen stammendes) Phlogiston, gemischt mit Wasserdünsten“. Erst nach eingehender experimenteller Überprüfung (Mittel der Akademie der Wissenschaften) machte sich Klaproth nach 1792 die Anschauungen Lavoisiers vollkommen zu eigen. Im ersten preußischen Arzneibuch (Pharmacopoea Borussica, 1799) führte er sie einschließlich der neuen Nomenklatur auch für den Bereich der Pharmazie als allein gültig ein. Dank seiner inzwischen gewonnenen Autorität wurde Klaproth so zum Vorbild für die junge Generation und Wegbereiter für die moderne Chemie.

Klaproth vs. Proust, Berthollet, Dalton Joseph Louis Proust (1754 1826), Apotheker und Chemiker und einer der führenden Analytiker seiner Zeit (u. a. H 2 S-Trennung). Sein Gesetz der konstanten Proportionen stützte sich auf eigene und vor allem auf Klaproths analytische Methoden und Befunde. Geriet darüber in einen langjährigen Streit mit Claude-Louis Berthollet (1748 1822), Mediziner und Chemiker. Begriff der chemischen Affinität. Lehnt die Proust‘sche Theorie ab. Stattdessen existiert Vielzahl von Verbindungen zweier Stoffe in beliebigen Gewichtsverhältnissen. Klaproth würdigt Berthollets Anschauungen ausgiebig, ohne auf Prousts Gedankengänge einzugehen! John Dalton (1766 1844), Metereologe und Chemiker. Wichtige Gasgesetze. 1808 „A New System of Chemical Philosophy“: Quantitative Atomhypothese und Gesetz der multiplen Proportionen (z. B. CH 4 u. C 2 H 4). Bestimmung einer Reihe relativer Atom- und Molekülmassen. Daltons bahnbrechende Arbeiten fanden bei Klaproth keine erkennbare Resonanz.

Klaproth als Entdecker bzw. Mitentdecker von Elementen Gedenkstele von Ralf Sander (1996) auf dem Campus der TU Berlin. Cer (1803) Uran (1789) Titan (1795) Strontium (1793) Tellur (1798) Zirkonium (1789) Zusätzlich: Chrom (1797) Beryllium (1798) Yttrium (1800)

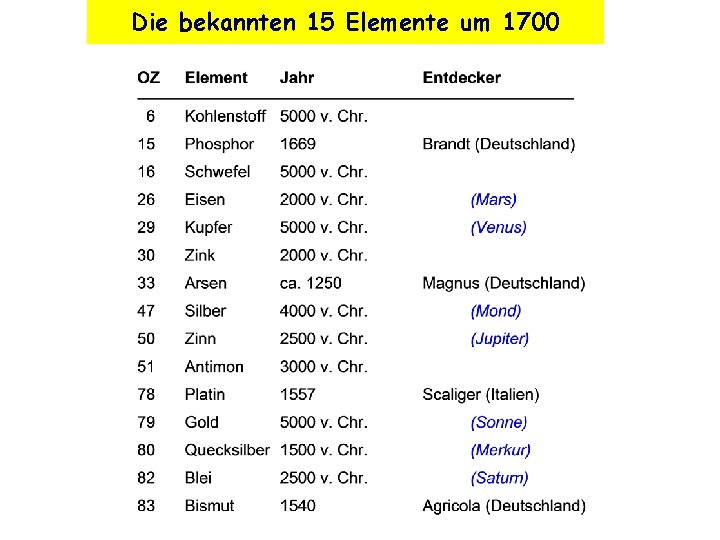
Die bekannten 15 Elemente um 1700

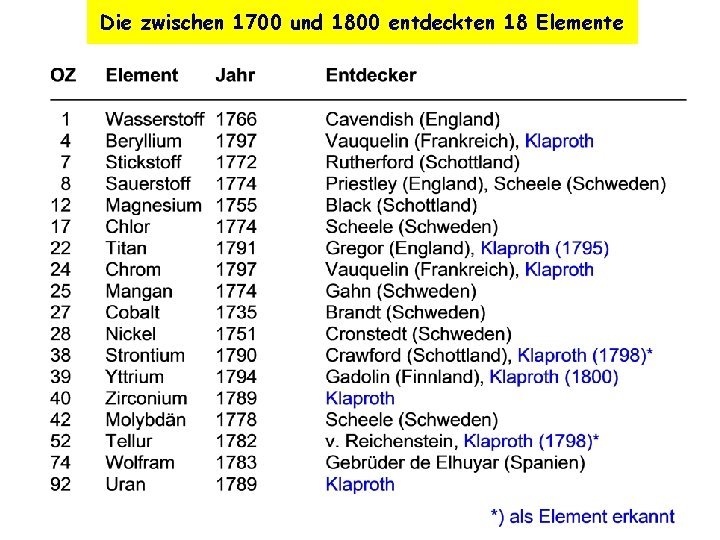
Die zwischen 1700 und 1800 entdeckten 18 Elemente

Entdeckung des Urans 1789 Klaproth fand das Uran in der Pechblende (heute Uraninit, UO 2 bis U 3 O 8). Wurde ursprünglich für ein Zink- oder Wolframerz gehalten. Namensgebung Uranit, später Uranium, nach dem von Herschel 1781 gefundenen Planeten Uranus. Grube Georg Wagsfort bei Johanngeorgenstadt Niederschlema
![Entdeckung des Urans 1789 Pechblende in Salpetersäure gelöst UO 2NO 32 Neutralisation mit Entdeckung des Urans 1789 Pechblende in Salpetersäure gelöst [ UO 2(NO 3)2], Neutralisation mit](https://slidetodoc.com/presentation_image_h2/6fdbf8169d7632356ff8327142f25c61/image-29.jpg)
Entdeckung des Urans 1789 Pechblende in Salpetersäure gelöst [ UO 2(NO 3)2], Neutralisation mit Natronlauge Ausfällung eines gelben „Metallkalkes“ [Na 2 U 2 O 7]. Starkes Erhitzen mit Kohlepulver unter Luftabschluss im Porzellanofen Sintermasse aus metallisch glänzenden Körnchen [UO 2!!!], von Klaproth für metallisches Uran gehalten. 24. 09. 1789 Vorstellung des neuen Elementes vor der Preußischen Akademie der Wissenschaften. Nachfolgend mehrfache Revision der Anschauung über die Natur der Pechblende; erst 1797 als oxidisches Uranerz bezeichnet. Erste Darstellung von reinem Uran: 1841 durch Eugène Péligot in Paris (Reduktion von UCl 4 mit K). Frühe Verwendung von Uranoxiden: Färbung von Glas und Porzellan (gelb, grün). Entdeckung der Radioaktivität: 1896 durch Antoine Henri Becquerel. Ein Uranpräparat erzeugte auf einer Photoplatte unter Lichtausschluss eine Schwärzung.

Entdeckung des Zirconiums 1789 Aus Ceylon (Sri Lanka) stammende Mineralproben von Zirkon (1789) und Hyacinth (1795), Zr[Si. O 4], wurden von Klaproth in eine neue „Erde“, Zr. O 2, überführt, die er Zirkonerde nannte. Die Darstellung von metallischem Zirconium gelang erst 1824 Berzelius durch Erhitzen von K 2 Zr. F 6 mit Kalium im Eisenrohr. Verunreinigung durch Hafnium! Jöns Jakob Berzelius 1779− 1848

Klaproths Definition von „Erden“ „Trockene, unentzündliche, feuerbeständige, der Metallisierung widerstehende Körper, teils in Säuren, teils in Alkalien, teils in bloßem Wasser löslich. “ „Einfache Erden können nicht in ungleichartige Bestandteile zerlegt werden, haben also elementaren Charakter. “ Sie wurden von Klaproth nicht eindeutig als Metalloxyde erkannt bzw. nicht immer widerspruchsfrei von „Metallischen Erden oder Metalloxyden“ abgegrenzt. Bis ca. 1790 kannte man 6 „einfache Erden“: Kalkerde (Ca. O) Baryterde (Ba. O) Beryllerde (Be. O) Kieselerde (Si. O 2) Talkerde (Mg. O) Tonerde (Al 2 O 3)

Entdeckung des Strontiums 1793 Strontianit (Sr. CO 3), benannt nach dem schottischen Dorf Strontian. 1790 erkennt Adair Crawford (1749 1795), dass der von ihm erstmalig beschriebene Strontianit von Calcit (Ca. CO 3) und Witherit (Ba. CO 3) zu unterscheiden sei. Thomas Hope (1766 1844) unterscheidet die 3 Elemente 1792 anhand ihrer Flammenfärbungen (Publikation 1793). Unabhängig davon weist Klaproth 1793 im Strontianit eine neue „einfache Erde“ nach: Strontinerde, später Strontianerde genannt (Sr. O). 1808 erstmalige Gewinnung von (unreinem) metallischem Strontium (Name!) durch Sir Humphry Davy (1778 1829) auf elektrolytischem Wege an einer Quecksilber-Kathode.

Entdeckung des Titans 1795 Der englische Geistliche und Chemiker William Gregor (1761− 1817) entdeckte 1791 in einem aus Cornwall stammenden, Ilmenit (Fe. Ti. O 3) enthaltenden Sand ein neues Element in Form seines Oxids. Ilmenit Unabhängig davon fand Klaproth 1795 im „Roten Schörl“ (Rutil, Ti. O 2) aus Boinik (Ungarn), der damals für eine Art Granat oder Turmalin gehalten wurde, eine „weiße Erde“ und benannte das zugrundeliegende Metall nach den „Ursöhnen der Erde“ Titanium. Rutil Das Metall (unrein) stellte erstmals J. J. Berzelius 1825 durch Reduktion von Titandioxid mit Natrium dar.

Entdeckung des Chroms 1797 Rotbleierz bzw. Krokoit, Pb. Cr. O 4 Die Entdeckung des Chroms im sibirischen Krokoit wird allgemein dem französischen Chemiker Louis Nicolas Vauquelin (1763 1829) zugeschrieben. Benennung nach der Farbigkeit der Verbindungen: χρώμα = Farbe. Vauquelin wandelte Krokoit mit Salzsäure in Chrom(III)oxid um: 2 Pb. Cr. O 4 + 10 HCl 2 Pb. Cl 2 + 5 H 2 O + Cr 2 O 3 + 3 Cl 2 Anschließend Reduktion des Oxids mit Holzkohle zum (unreinen) Metall. Klaproth entdeckte und publizierte das Element jedoch unabhängig im selben Jahr! Erstmalige (elektrolytische) Reindarstellung von Chrom 1854 durch Robert Wilhelm Bunsen (1811 1899).

Entdeckung des Tellurs 1797 Tellur wurde 1782 zunächst von dem österreichischen Chemiker Franz Joseph Müller von Reichenstein (1740 1825) in Golderzen aus der Grube Mariahilf (Rumänien) entdeckt. Er vermutete darin ein neues Halbmetall und nannte es Nagyagit „metallum problematicum“. [Pb 3(Pb, Sb)3 S 6](Au, Te)3 1797 erhielt Klaproth Proben der Erze von Müller von Reichenstein und bestätigte nach sorgfältigen Untersuchungen das neue Element, das er Tellurium nannte (lat. tellus = „Erde“). Vortrag vor der Akademie der Wiss. am 25. 01. 1798 unter Würdigung von Reichensteins. Tellur war das einzige von ihm (mit-)entdeckte Metall, das Klaproth auch elementar in Händen hielt. Sylvanit (Au, Ag)Te 2 Museum f. Naturkunde

Entdeckung des Cers 1803 Das Element wurde in Form seiner „Erde“ 1803 von Klaproth bei der Analyse von Cerit aus Bastnäs (Schweden) entdeckt. Wegen der Ockerfarbe benannte er die neue Erde Ochroiterde. Cerit aus Bastnäs Fast gleichzeitig und unabhängig fanden auch J. J. Berzelius und Wilhelm Hisinger (1766 1852) in Stockholm diese Erde und benannten das zugrundeliegende Metall nach dem gerade entdeckten Planetoiden Ceres „Cerium“. 1825 Herstellung von metallischem Cer über Reduktion von Ce. Cl 3 mit Na durch Carl Gustav Mosander (1797 1858) in Stockholm. 1839 Nachweis, dass die Ochroiterde von Klaproth eine Mischung mehrerer Erden darstellte.

Zur Entdeckung des Berylliums und Yttriums Vauquelin isolierte erstmalig die Beryllerde (Be. O) 1798 aus Beryll und Smaragd (Be 3 Al 2[Si 6 O 18]) und nannte das Element Glycinium. Klaproth bestätigte wenig später die Natur der Beryllerde, die er aus sibirischem Beryll gewonnen hatte; er führte den heute gebräuchlichen Namen Beryllium ein. Beryll Gadolinit 1794 hatte der finnische Chemiker Johan Gadolin (1760 1852) in einem bei Ytterby in Schweden gefundenen Mineral, das den Namen Gadolinit erhielt, eine neue Erde (Y 2 O 3) gefunden, die vom Schweden Ekeberg 1798 als Yttererde bezeichnet wurde. Klaproth und Vauquelin stellten 1800 diesen Befund durch genaue Analysen sicher. Sowohl Beryllium als auch Yttrium wurden in metallischer Form erst 1828 von Friedrich Wöhler (1800 1882) durch Schmelzen der Chloride mit Kalium gewonnen. F. Wöhler J. Gadolin

Entdeckung des „mineralischen“ Kaliums 1797 Nach herkömmlicher Ansicht wurden folgende „fixe Laugensalze“ unterschieden: „Alcali vegetabile“ (K 2 CO 3), ausschließlich in Pflanzenasche gefunden. „Alkali minerale“ (Na 2 CO 3), vorrangig aus Mineralien gewonnen. „Alkali volatile“ ([NH 4]2 CO 3 bzw. [NH 4]HCO 3). Die entsprechenden Hydroxide hießen „ätzende oder caustische Laugensalze“. Bei eingehenden analytischen Untersuchungen des Leucits (K[Al. Si 2 O 6], ein Zeolith) stellte Klaproth regelmäßig einen Substanzverlust von ca. 20 % fest. Er fand schließlich die folgende Erklärung (1797 veröffentlicht): „Höchst unerwartet bin ich durch Auffindung eines Bestandteils überrascht worden, welcher in einem Stoffe besteht, dessen Dasein wohl noch niemand innerhalb der Grenzen des Mineralreiches, und am wenigsten in der natürlichen Mischung eines festen, mineralogisch einfachen Fossils je vermutet hat. Dieser gegenwärtig in der Eigenschaft einer oryktognostischen Substanz auf den Schauplatz tretende Bestandteil des Leucits ist kein anderer, als das bisher dem Pflanzenreiche ausschließlich eigen geglaubte und deswegen auch nach selbigem also benannte Pflanzenalkali!“ Klaproth führte daraufhin neue Namen ein: „Alcali vegetabile“ = „Kali“ ( Kalium) „Alcali minerale“ = „Natron“ (ältere Bezeichnung), später „Natrum“ ( Natrium)

Entdeckung der „Honigsteinsäure“ 1802 1789 erstmalige Beschreibung des aus Braunkohlegruben in Thüringen stammenden seltenen Minerals Honigstein (Mellit) durch A. G. Werner und C. A. S. Hoffmann. Diverse Analysen verschiedener Autoren mit deutlich voneinander abweichenden Ergebnissen veranlassten Klaproth 1802 zu eigenen Untersuchungen. Ergebnis: „…dass der Honigstein aus einer natürlichen Verbindung der Alaunerde mit einer Säure bestehe; dass aber diese Säure keine einfache Mineralsäure, sondern von der Natur der Pflanzensäuren sei. . Da nun „ Säure des Honigsteins sich als eine, aus Sauerstoff, Kohlenstoff und Wasserstoff zusammengesetzte die und daher durch Feuer leicht zerstörbare, Säure zu erkennen giebt, dabei aber in ihrem Verhalten mit keiner der jetzt bekannten Säuren übereinkömmt: so würde sie diesemnach unter den vegetabilischen Säuren als eine Säure von eigener Natur, und zwar vorerst noch unter dem Namen Honigsteinsäure (Acidum melilithicum) aufzuführen seyn. “ Heutige Kenntnis: Mellit ist das Aluminiumsalz der Benzolhexacarbonsäure Al 2 C 6(COO)6 · 16 H 2 O

Wichtige Schriften Klaproths „ • Zahlreiche Publikationen über experimentelle Arbeiten und zusammenfassende Herausgabe in den 6 Bänden „Beiträge zur chemischen Kenntnis der Mineral. Körper“, 1795 1815; französische und englische Übersetzung. • „Pharmacopoea Borussica“, gemeinsam mit Formey, Hermbstaedt und Rose; 1799 1. , 1804 2. , 1813 3. Auflage. • 1806/07 Herausgabe der völlig umgearbeiteten Auflage von Grens „Systematisches Handbuch der gesamten Chemie“. • 1807 1819 gemeinsam mit Wolff „Chemisches Wörterbuch“ in 9 Bänden; enzyklopädische Behandlung des gesamten chemischen Wissens der damaligen Zeit; französische und italienische Übersetzung. • Klaproth zeichnete auch als Mitherausgeber diverser Periodika, u. a. „Neues allgemeines Journal der Chemie“ (1803 1805). „Neues allgemeines Journal für die Chemie, Physik und Mineralogie“ (1806 1809).

Leistungen Hermbstaedts Chemiker 1782 Herstellung von Oxalsäure durch Oxidation von Weinsäure mit Salpetersäure. 1785 Untersuchung der Chinarinde-Inhaltsstoffe, Auffindung des Calciumsalzes der Chinasäure. 1792 Propagierung der antiphlogistischen Lehre Lavoisiers und Verbreitung der neuen chemischen Nomenklatur. Technologe Verbreitung und Fortentwicklung des vorhandenen chemisch-technologischen Praxiswissens der verschiedensten Gewerbe durch eine Fülle von Vorträgen, Vorlesungen, Abhandlungen und Lehrbüchern sowie eigene Laboruntersuchungen. Gewerbeförderung durch Vermittlung naturwiss. Grundlagen von Produktion und Verarbeitung, Einführung neuer Verfahren, Beratung bei Firmengründungen. Ausgewählte Tätigkeitsfelder: Zuckerfabrikation; Textilherstellung und –verarbeitung; Färberei; Gerberei; Brauerei; Branntweinproduktion; Veredelung von Flachs und Hanf; BleiweißHerstellung; Drucktechnik; Tabakanbau; Schießpulverproduktion; Alaunund Seifensiederei; Bleicherei; Papierherstellung; Agrikulturchemie; Soda. Herstellung; Arzneimittel. Neben technologischen spielten auch kameralistische und juristische Aspekte stets eine Rolle.

Wichtige Schriften Hermbstaedts I „ • „Physikalisch-chemische Versuche und Beobachtungen“ (1786 Bd. 1, 1789 Bd. 2) • „Magazin der Technologie“ (1789) • „Bibliothek der neuesten physikalischen, chemischen, metallurgischen und pharmazeutischen Literatur“ (4 Bde. 1787 95) • • • „Systematischer Grundriß der Allgemeinen Experimentalchemie“ (3 Bde. 1791) • • • „Grundriß der Experimentalpharmazie“ (2 Bde. 1792/3) „Katechismus der Apothekerkunst, oder die ersten Grundsätze der Pharmazie für Anfänger“ (1792) „Grundriß der Färbekunst“ (3 Aufl. 1802/06/25) „Theoretisch-praktisches Handbuch der allgemeinen Fabrikenkunde“ (1807) „Grundsätze der experimentellen agronomischen Chemie“ (1808) „Grundriß der Technologie“ (2 Aufl. 1814/30) „Kompendium der Technologie“ (als Leitfaden zum Gebrauch akademischer Vorlesungen) (1831)

Wichtige Schriften Hermbstaedts II