11 12 HAFTA Ntralleme Titrasyonlarnn lkeleri AsitBaz Titrasyonlar

11 -12 HAFTA Nötralleşme. Titrasyonlarının İlkeleri ü Asit/Baz Titrasyonları için Çözeltiler ve İndikatörler ü Kuvvetli Asitler ve Kuvvetli Bazlar için Titrasyon Eğrileri ü Zayıf Asitlerin Titrasyon Eğrileri ü Zayıf Asit ve Bazların İyonlaşma Sabitlerinin. Tayini ü Zayıf Bazların Titrasyon Eğrileri ü Asit/Baz Titrasyon Dönüm Noktalarının p. H Ölçerek Belirlenmesi

Nötralleşme titrasyonları Kuvvetli asit ve bazların standart çözeltileri, asit veya bazların veya kimyasal işlemlerle asit veya baz haline dönüştürülebilen maddelerin tayininde çok geniş bir şekilde kullanılır.

ASİT/BAZ TİTRASYONLARI İÇİN ÇÖZELTİLER VE İNDİKATÖRLER Standart Çözeltiler Nötralleşme reaksiyonlarında kullanılan standart çözeltiler kuvvetli asitler veya kuvvetli bazlardır. Asitlerin standart çözeltileri: v. Der. HCl. O 4 v. Der. H 2 SO 4 v. Der. HNO 3

Bazların standart çözeltileri: v. Katı Na. OH v. KOH v. Ba(OH)2 (nadiren)

Zayıf asitler ve bazlar, analit ile tamamen reaksiyona girmediği için hiçbir zaman standart reaktif olarak kullanılmaz.

Asit/Baz İndikatörleri Sentetik ve doğal maddelerin birçoğu, bulundukları çözeltilerin p. H’sına bağlı olarak farklı renkler gösterirler. Bir asit/baz indikatörü, iyonlaşmamış türünün rengi konjüge asitinin veya konjüge bazının renginden farklı olan zayıf bir organik asit veya zayıf bir organik bazdır.
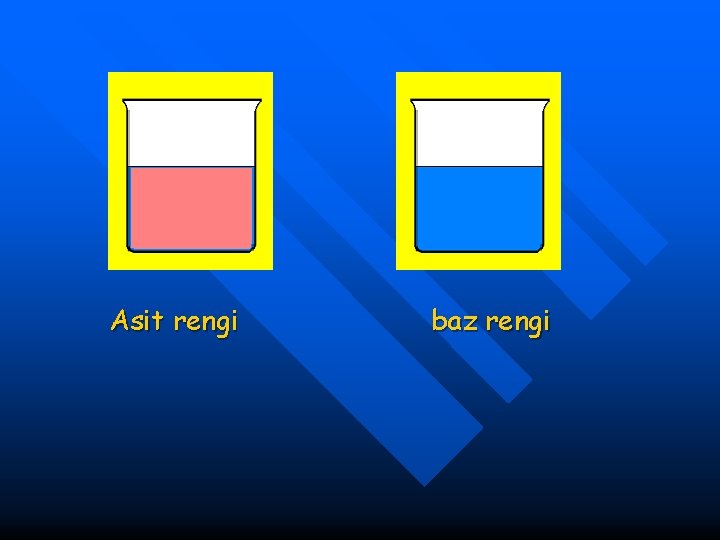
Asit rengi baz rengi
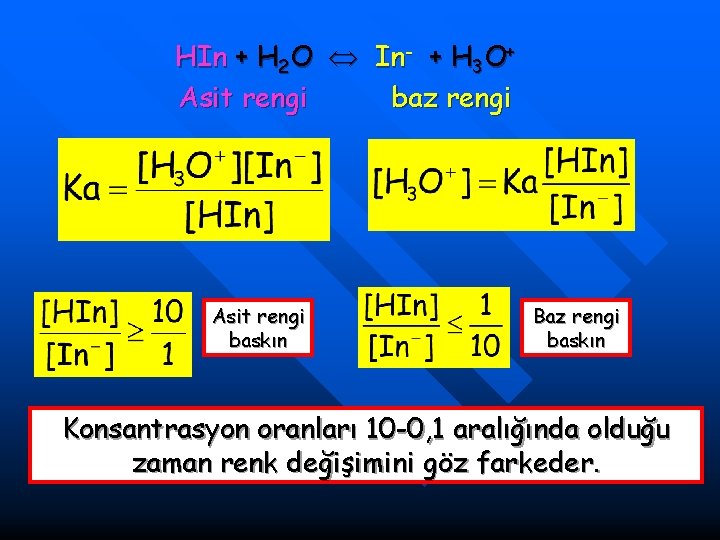
HIn + H 2 O In- + H 3 O+ Asit rengi baz rengi Asit rengi baskın Baz rengi baskın Konsantrasyon oranları 10 -0, 1 aralığında olduğu zaman renk değişimini göz farkeder.
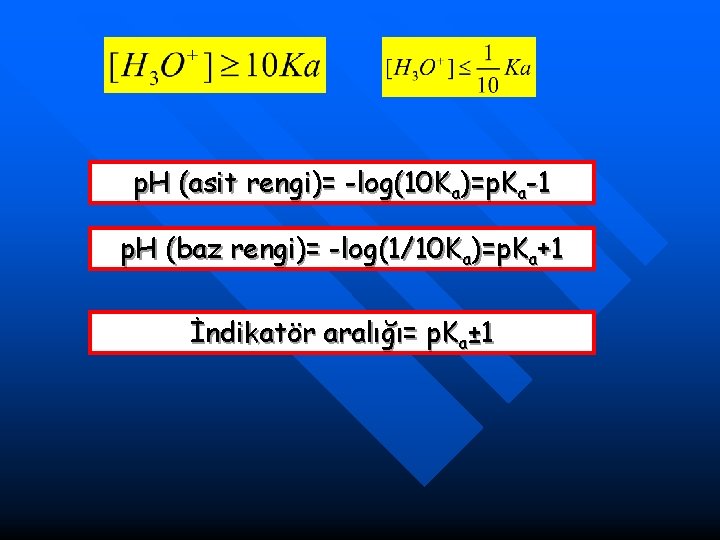
p. H (asit rengi)= -log(10 Ka)=p. Ka-1 p. H (baz rengi)= -log(1/10 Ka)=p. Ka+1 İndikatör aralığı= p. Ka± 1

İndikatör aralığı= p. Ka± 1 Asit iyonlaşma sabiti 1 x 10 -5 (p. Ka=5) olan bir indikatör, çözündüğü çözeltinin p. H’ı 4’ den 6’ya değiştirirse, bu indikatör tam bir renk dönüşümüne uğrar.

Asit/Baz İndikatörlerinden kaynaklanan Titrasyon Hataları 1. Uygun indikatörler seçilememesi, 2. İndikatör renk değişim aralığı farklı kişilerce farklı olabilir.

KUVVETLİ ASİTLER VE KUVVETLİ BAZLAR İÇİN TİTRASYON EĞRİLERİ Kuvvetli asitlerin sulu çözeltilerindeki hidronyum iyonunun 2 kaynağı vardır: 1. Asitin su ile reaksiyonu 2. Suyun iyonlaşması

Seyreltik çözeltilerin çoğunda bile asitten gelen hidronyum iyonu, çözücüden gelene göre çok fazladır. Bu nedenle konsantrasyonu 1 x 10 -6 M dan büyük olan HCl çözeltileri için aşağıdaki eşitlik yazılabilir: [H 3 O+]= CHCl + [OH-] CHCl
![Sodyum hidroksit gibi kuvvetli bir baz çözeltisi için benzer eşitlik ise şöyledir: [OH-] = Sodyum hidroksit gibi kuvvetli bir baz çözeltisi için benzer eşitlik ise şöyledir: [OH-] =](http://slidetodoc.com/presentation_image_h/a733bffc43e9f1ff20e314ab73547c2f/image-14.jpg)
Sodyum hidroksit gibi kuvvetli bir baz çözeltisi için benzer eşitlik ise şöyledir: [OH-] = CNa. OH + [H 3 O+] CNa. OH

Kuvvetli Bir Asitin Kuvvetli Bir Bazla Titrasyonu Kuvvetli bir asit çözeltisinin, kuvvetli bir bazla titrasyon grafiğini çizmek için, üç türlü hesaplama yapmak gerekir. Bu hesaplamaların herbiri titrasyonun farklı basamakları için yapılır:

Kuvvetli bir asit çözeltisinin, kuvvetli bir bazla titrasyon grafiğini çizmek için, üç türlü hesaplama yapmak gerekir. Bu hesaplamaların herbiri titrasyonun farklı basamakları için yapılır: v Eşdeğerlik noktası öncesi, (asit konsantrasyonu, asitin başlangıç konsantrasyonu ile eklenen bazın konsantrasyonu yardımıyla yapılır) v Eşdeğerlik noktasında, ([OH-] = [H 3 O+] bu noktada hidronyum iyonu konsantrasyonu doğrudan suyun iyonlar çarpımı sabitinden hesaplanır) v Eşdeğerlik noktası sonrası, (ortamda fazla miktarda bulunan bazın analitik konsantrasyonu hesaplanır. Hidroksit iyonu konsantrasyonu, bazın analitik konsantrasyonuna eşittir)
Örnek 50, 00 m. L 0, 0500 M HCl ‘nin 0, 100 M Na. OH ile titrasyonu için titrasyon eğrisini çiziniz. DN: 25 ml 1. 2. 3. 4. Başlangıç noktası, 10 m. L baz (Na. OH) ilavesinde (asidik bölge), Eşdeğerlik noktası, 25, 10 m. L baz (Na. OH) ilavesinde (bazik bölge),

Örnek 50, 00 m. L 0, 0500 M HCl ‘nin 0, 100 M Na. OH ile titrasyonu için titrasyon eğrisini çiziniz. DN: 25 ml 1. 2. Başlangıç noktası, p. H=-log[H 3 O+] 10 m. L baz (Na. OH) ilavesinde (asidik bölge), 3. Eşdeğerlik noktası, [H 3 O+] [HO-]= Ksu 4. 25, 10 m. L baz (Na. OH) ilavesinde (bazik bölge),

Kuvvetli Bir Bazın Kuvvetli Bir Asit ile Titrasyonu Örnek 50, 00 m. L 0, 0500 M Na. OH ‘nin 0, 100 M HCl ile titrasyonu için titrasyon eğrisini çiziniz. 1. Başlangıç noktası, p. OH=-log[OH-] = -log 0, 05 = 1, 3 2. 10 m. L asit (HCl) ilavesinde (bazik bölge) p. H = 12, 70 p. OH=-log[OH]- = -log 0, 025 = 1, 60 p. H=12, 40 3. Eşdeğerlik noktası, [H 3 O+] [HO-]= Ksu p. OH=-log[OH-] = -log 1 x 10 -7 = 7 p. H = 7 4. 25, 50 m. L asit (HCl) ilavesinde (asidik bölge), p. H=3, 18

ZAYIF ASİTLERİN TİTRASYON EĞRİLERİ Bir zayıf asitin (veya bir zayıf bazın) titrasyon eğrisini elde etmek için birbirinden tamamen farklı dört çeşit hesaplama yapmak gerekir. 1. Başlangıçta, çözelti yalnız asit veya baz ihtiva eder ve p. H bu türlerin konsantrasyonu ve iyonlaşma sabiti yardımıyla hesaplanır. 2. Her titrant ilavesi ile ortamda bir seri tampon çözelti oluşur (eşdeğerlik noktasından önce) ve her tampon çözeltinin p. H’sı asit veya baz ile bunların konjüge bazı veya asitinin analitik konsantrasyonları yardımıyla hesaplanır. 3. Eşdeğerlik noktasında ortamda, titre edilen asit veya bazın yalnız konjüge türü bulunur (yani tuz) ve p. H bu ürünün konsantrasyonu yardımıyla hesaplanır. 4. Eşdeğerlik noktasından sonra kuvvetli asit veya baz titrantın aşırısı, reaksiyon ürününün asidik veya bazik özelliğini baskı altına alır ve p. H aşırısı titrantın konsantrasyonu kullanılarak hesaplanır.
Örnek 50, 00 m. L 0, 100 M asetik asitin (Ka=1, 75 10 -5) 0, 1000 M sodyum hidroksit ile titrasyonu için titrasyon grafiğini çiziniz. DN: 50 ml 1. Başlangıç: CH 3 COOH + H 2 O CH 3 COO- + H 3 O+ 2. 10 m. L Na. OH ilavesinde CH 3 COOH + Na. OH CH 3 COONa + H 2 O Tampon çözelti 3. Eşdeğerlik noktasında CH 3 COOH CH 3 COONa p. H hesaplanır. 4. Eşdeğerlik noktasından sonra ortam bazik CH 3 COONa + Na. OH var

ZAYIF BAZLARIN TİTRASYON EĞRİLERİ Hesaplamalar benzer tarzda yapılır.

ÇOK KULLANILAN ASİT/BAZ İNDİKATÖRLERİ Ftalein İndikatörleri Sülfonftalein İndikatörleri Azo İndikatörleri
- Slides: 23