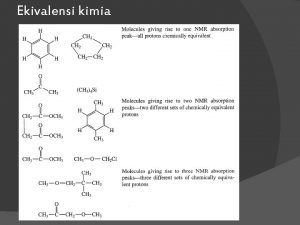
Wykad 7 Sprzenie spinspin Przesunicie chemiczne Sprzenie spinspin











![Aromatyczność - przykłady [18]-anulen [10]-paracyklofan Aromatyczność - przykłady [18]-anulen [10]-paracyklofan](https://slidetodoc.com/presentation_image_h/e6de0f195f1101baefa9ae181e47b789/image-40.jpg)
- Slides: 40

Wykład 7 Sprzężenie spin-spin Przesunięcie chemiczne

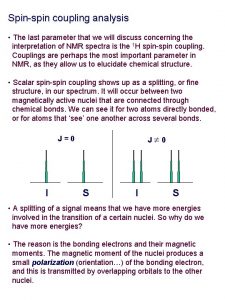
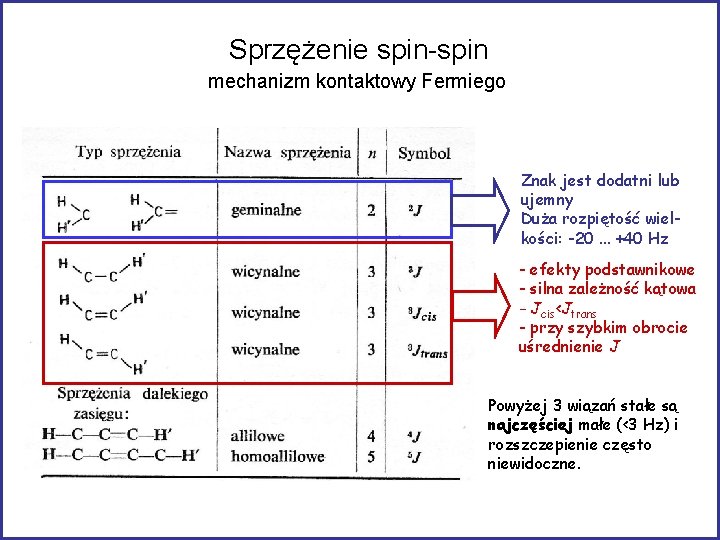
Sprzężenie spin-spin mechanizm kontaktowy Fermiego Znak jest dodatni lub ujemny Duża rozpiętość wielkości: -20. . . +40 Hz - efekty podstawnikowe - silna zależność kątowa - Jcis<Jtrans - przy szybkim obrocie uśrednienie J Powyżej 3 wiązań stałe są najczęściej małe (<3 Hz) i rozszczepienie często niewidoczne.

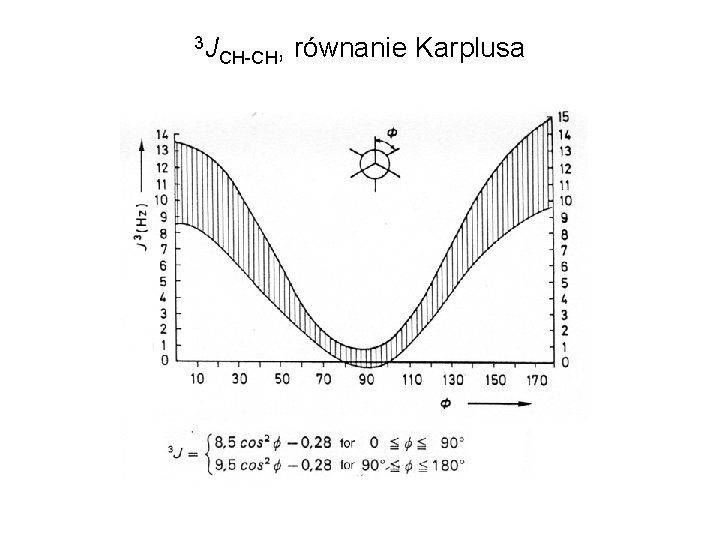
3 J CH-CH, równanie Karplusa

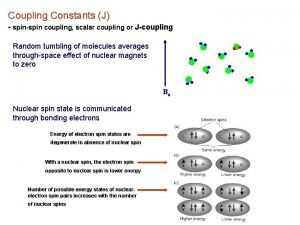
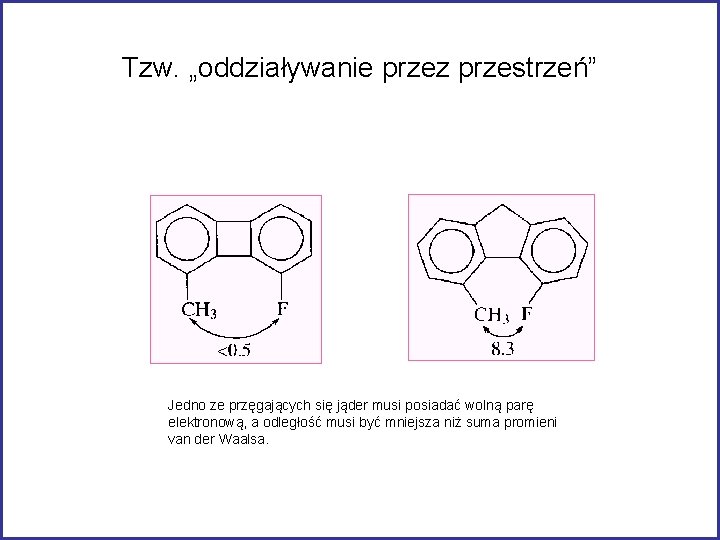
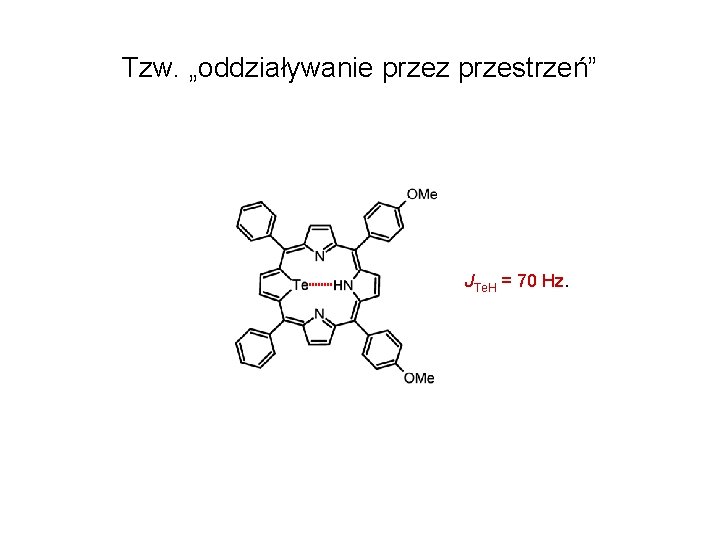
Tzw. „oddziaływanie przez przestrzeń” Jedno ze przęgających się jąder musi posiadać wolną parę elektronową, a odległość musi być mniejsza niż suma promieni van der Waalsa.

Tzw. „oddziaływanie przez przestrzeń” JTe. H = 70 Hz.

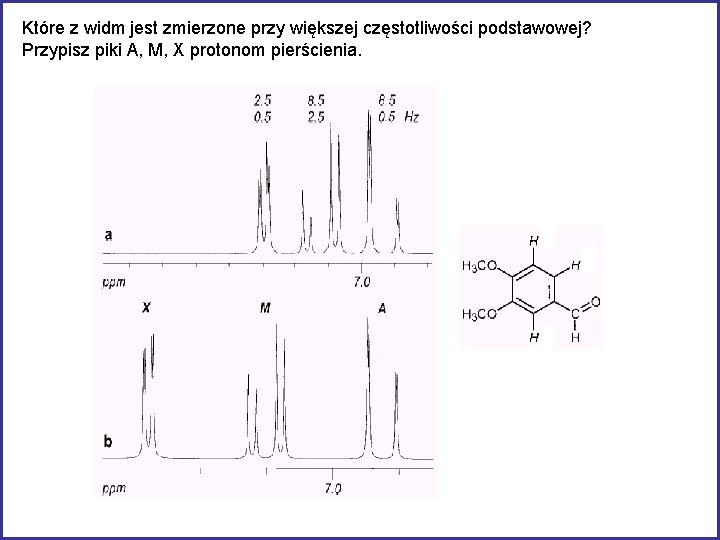
Które z widm jest zmierzone przy większej częstotliwości podstawowej? Przypisz piki A, M, X protonom pierścienia.

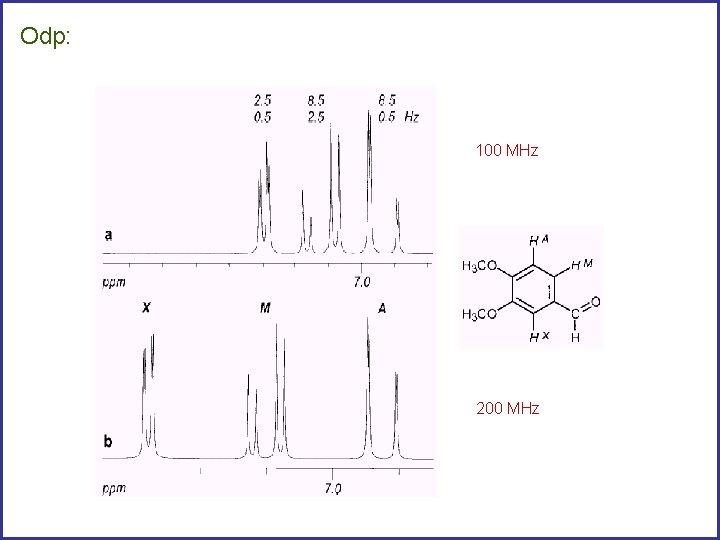
Odp: 100 MHz 200 MHz

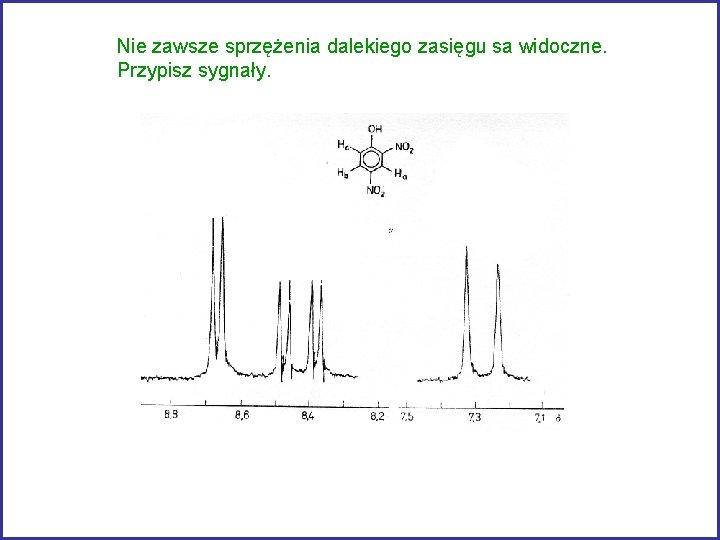
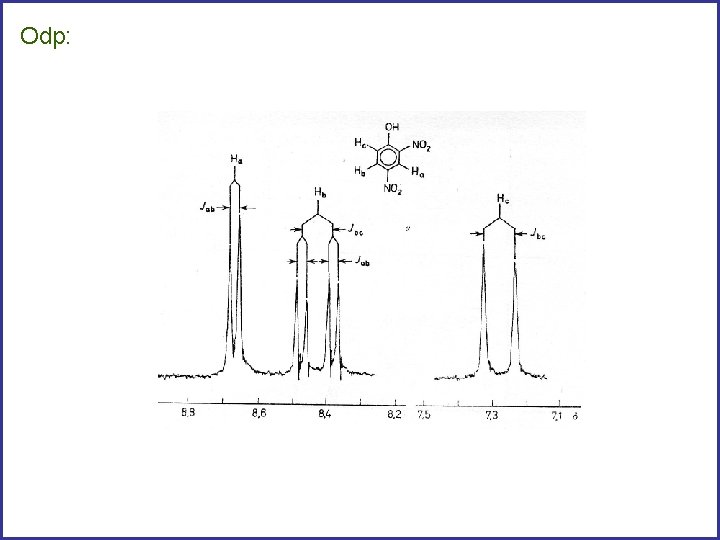
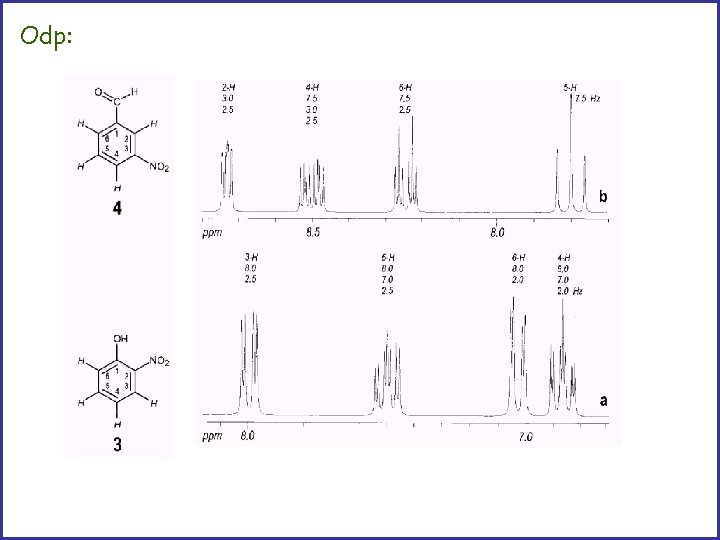
Nie zawsze sprzężenia dalekiego zasięgu sa widoczne. Przypisz sygnały.

Odp:

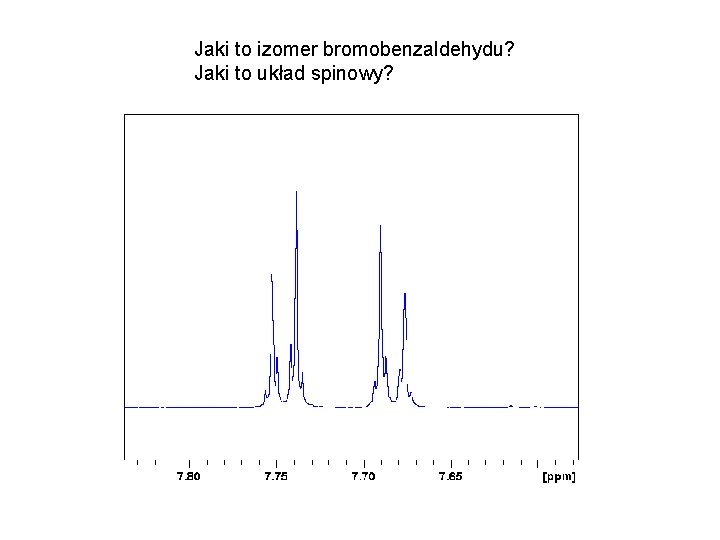
Jaki to izomer bromobenzaldehydu? Jaki to układ spinowy?

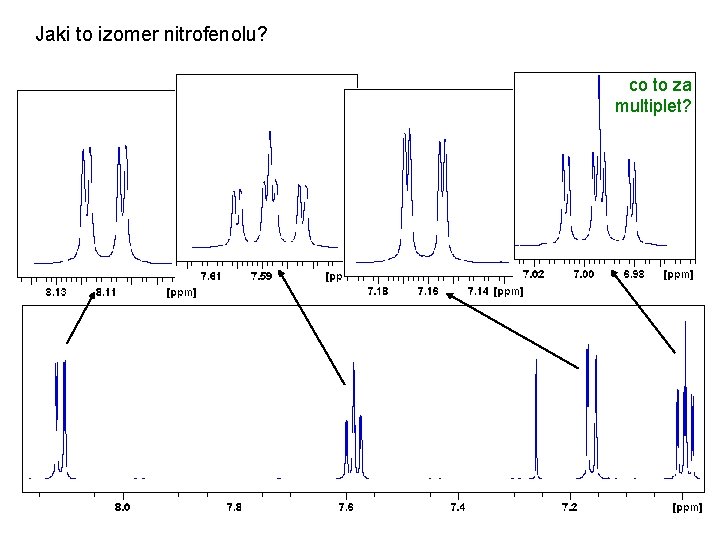
Jaki to izomer nitrofenolu? co to za multiplet?

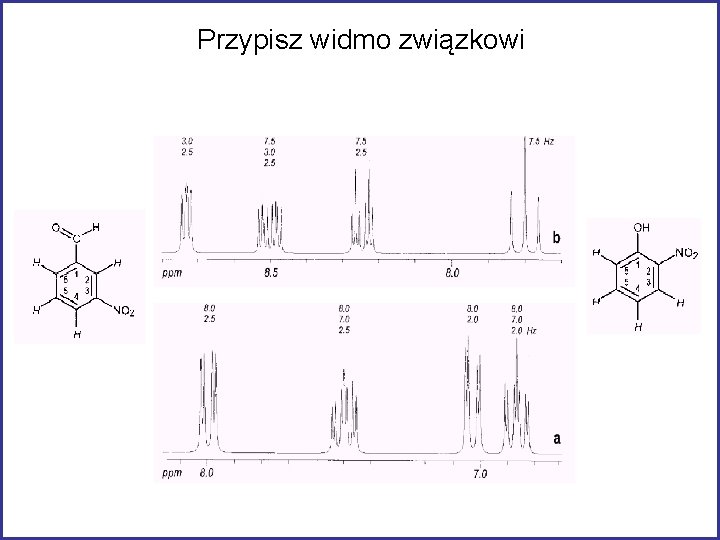
Przypisz widmo związkowi

Odp:

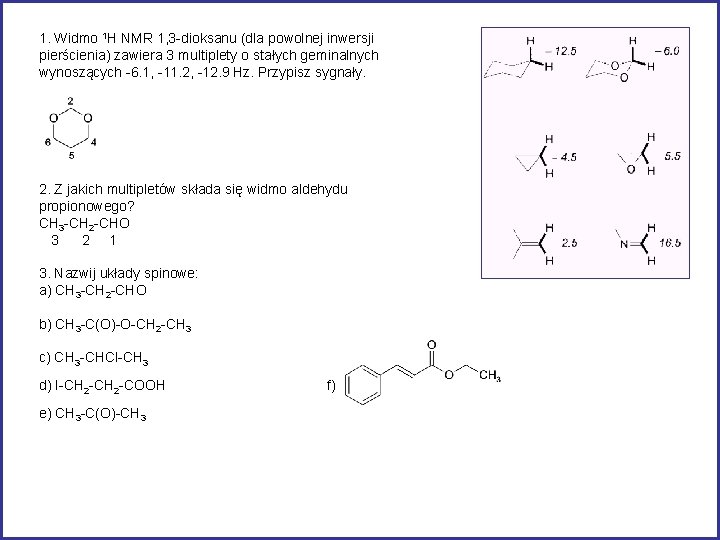
1. Widmo 1 H NMR 1, 3 -dioksanu (dla powolnej inwersji pierścienia) zawiera 3 multiplety o stałych geminalnych wynoszących -6. 1, -11. 2, -12. 9 Hz. Przypisz sygnały. 2. Z jakich multipletów składa się widmo aldehydu propionowego? CH 3 -CH 2 -CHO 3 2 1 3. Nazwij układy spinowe: a) CH 3 -CH 2 -CHO b) CH 3 -C(O)-O-CH 2 -CH 3 c) CH 3 -CHCl-CH 3 d) I-CH 2 -COOH e) CH 3 -C(O)-CH 3 f)

Stałe sprzężenia 13 C-1 H i 13 C-13 C

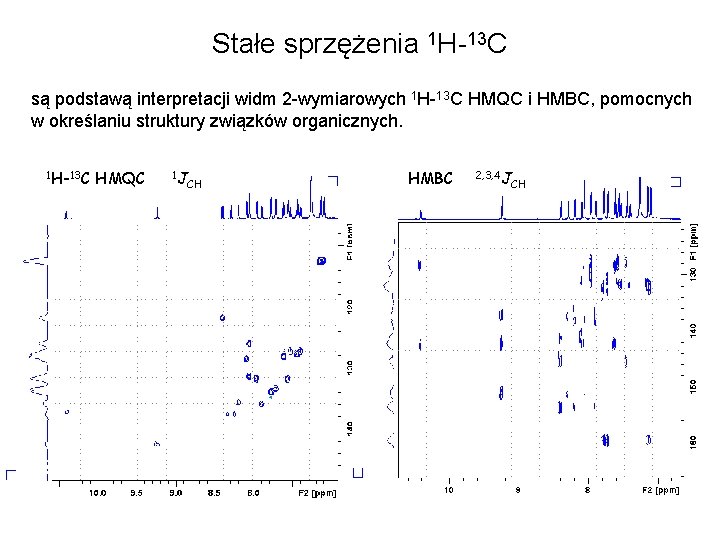
Stałe sprzężenia 1 H-13 C są podstawą interpretacji widm 2 -wymiarowych 1 H-13 C HMQC i HMBC, pomocnych w określaniu struktury związków organicznych. 1 H-13 C HMQC 1 J CH HMBC 2, 3, 4 J CH

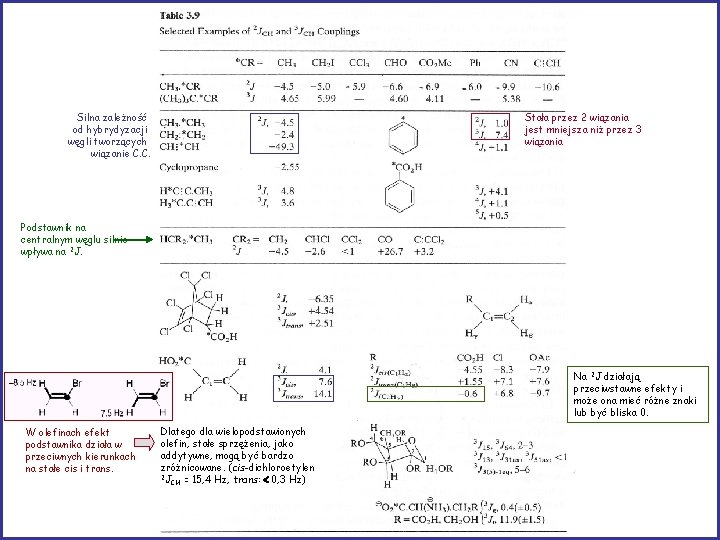
Stałe sprzężenia 1 H-13 C UWAGA! Nie zawsze stała sprzężenia JCH maleje wraz ze wzrostem odległości (liczonej jako ilość wiązań). Na 2 J działają przeciwstawne efekty i może ona mieć różne znaki lub być bliska 0. Związki aromatyczne: zazwyczaj 2 JCH < 3 JCH (zazwyczaj trans) benzen: 1 7. 4 Hz

Stałe sprzężenia 1 JHC • zależność od hybrydyzacji węgla (większy udział s wzrost J) 1 J CH = 1 J CH 125 Hz 167 Hz 250 Hz = 162 Hz w cyklopropanie • efekty podstawników – addytywność; podstawnik elektroujemny wzrost 1 J. Dla węgli sp 2 efekty podstawników są większe (podobnie aromatyczne) - dla podstawnika F w HFC=CH 2 DJ = 44 Hz, inny wpływ cis vs trans w CH 3 F DJ = 24 Hz B. duży jest efekt a w aldehydach:

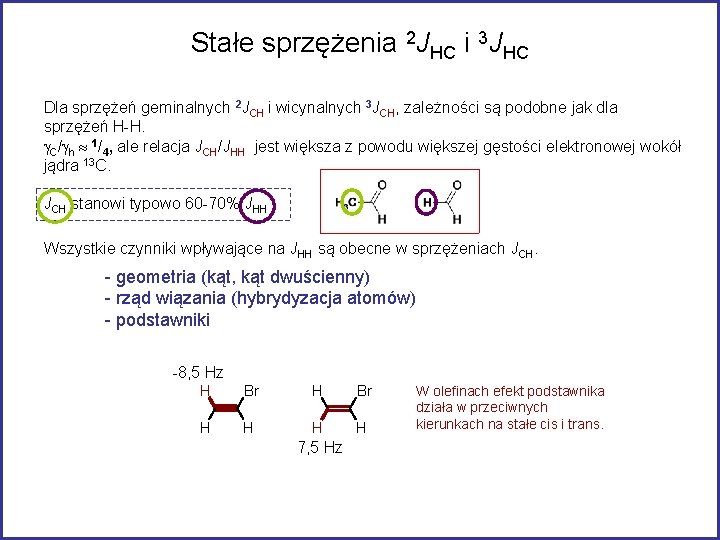
Stałe sprzężenia 2 JHC i 3 JHC Dla sprzężeń geminalnych 2 JCH i wicynalnych 3 JCH, zależności są podobne jak dla sprzężeń H-H. g. C/gh 1/4, ale relacja JCH/JHH jest większa z powodu większej gęstości elektronowej wokół jądra 13 C. JCH stanowi typowo 60 -70% JHH Wszystkie czynniki wpływające na JHH są obecne w sprzężeniach JCH. - geometria (kąt, kąt dwuścienny) - rząd wiązania (hybrydyzacja atomów) - podstawniki -8, 5 Hz H Br H H 7, 5 Hz W olefinach efekt podstawnika działa w przeciwnych kierunkach na stałe cis i trans.

Stałe sprzężenia 13 C-13 C Do wyznaczenia potrzebne wzbogacenie 13 C. Znaczne zróżnicowanie 1 JCC w zależności od rzędowości wiązania. Zachowuje się podobnie jak 1 JCH lecz jest mniejsze (bo g 13 C < g 1 H). Korelacja z 1 JCH: 1 1 J 1 C-CH 3 0, 27 JCH (g. C/gh /4) jest spełniona dla szerokiej gamy związków. C C 35 -40 Hz C C 65 -75 C C 170 -175 CN 80. 3 Uwaga - wiązanie pojedyncze, ale pomiędzy węglami o hybrydyzacjach sp i sp 2 (np. benzonitryl) nie będzie typowe dla wiązania pojedynczego sp 3 -sp 3. Podobnie dla 2 JCH i 3 JCH

Silna zależność od hybrydyzacji węgli tworzących wiązanie C. C. Stała przez 2 wiązania jest mniejsza niż przez 3 wiązania Podstawnik na centralnym węglu silnie wpływa na 2 J. Na 2 J działają przeciwstawne efekty i może ona mieć różne znaki lub być bliska 0. W olefinach efekt podstawnika działa w przeciwnych kierunkach na stałe cis i trans. Dlatego dla wielopodstawionych olefin, stałe sprzężenia, jako addytywne, mogą być bardzo zróżnicowane. (cis-dichloroetylen 2 J CH = 15, 4 Hz, trans: < 0, 3 Hz)

d

Wkłady w stałą ekranowania 1 H: Bpróbki = B 0 -s. B 0 = (1 − s)Bo σ = σlok + σel. + σmagn. . + σW + σrozp sąsiadów 1. Lokalny - dla protonu tylko diamagnetyczny. σlok = σdia + σpara 2. Sąsiadów: a) zmiany gęstości elektronowej dzięki efektom σel i) indukcyjnemu ii) mezomerycznemu b) cyrkulacje elektronów sąsiednich grup pod wpływem pola Bo, zmieniające lokalne pole Blok. σmagn 3. Wpływ pola elektrycznego i efekty Van der Waalsa σW 4. Wpływ rozpuszczalnika σrozp

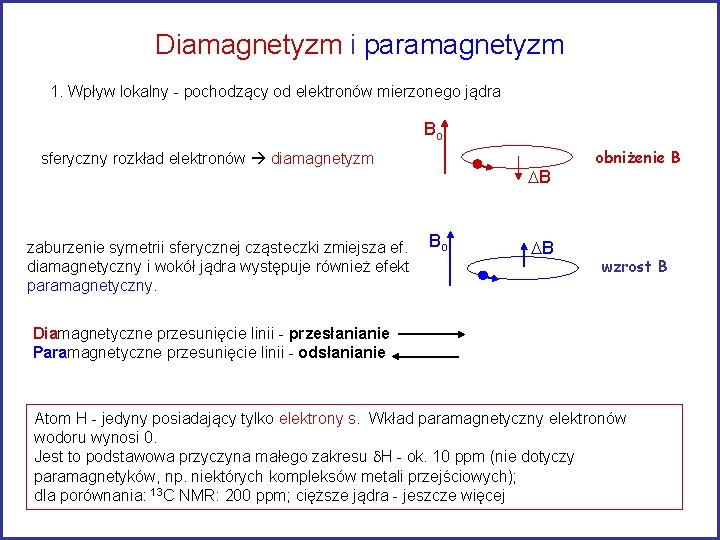
Diamagnetyzm i paramagnetyzm 1. Wpływ lokalny - pochodzący od elektronów mierzonego jądra Bo sferyczny rozkład elektronów diamagnetyzm zaburzenie symetrii sferycznej cząsteczki zmiejsza ef. diamagnetyczny i wokół jądra występuje również efekt paramagnetyczny. DB Bo DB obniżenie B wzrost B Diamagnetyczne przesunięcie linii - przesłanianie Paramagnetyczne przesunięcie linii - odsłanianie Atom H - jedyny posiadający tylko elektrony s. Wkład paramagnetyczny elektronów wodoru wynosi 0. Jest to podstawowa przyczyna małego zakresu d. H - ok. 10 ppm (nie dotyczy paramagnetyków, np. niektórych kompleksów metali przejściowych); dla porównania: 13 C NMR: 200 ppm; cięższe jądra - jeszcze więcej

Wkłady w stałą ekranowania 1 H: 1. Lokalny - dla protonu tylko diamagnetyczny. σlok = σdia + σpara 2. Sąsiadów: a) zmiany gęstości elektronowej dzięki efektom σel i) indukcyjnemu ii) mezomerycznemu b) cyrkulacje elektronów sąsiednich grup pod wpływem pola Bo, zmieniające lokalne pole Blok. σmagn 3. Wpływ pola elektrycznego i efekty Van der Waalsa σW 4. Wpływ rozpuszczalnika σrozp

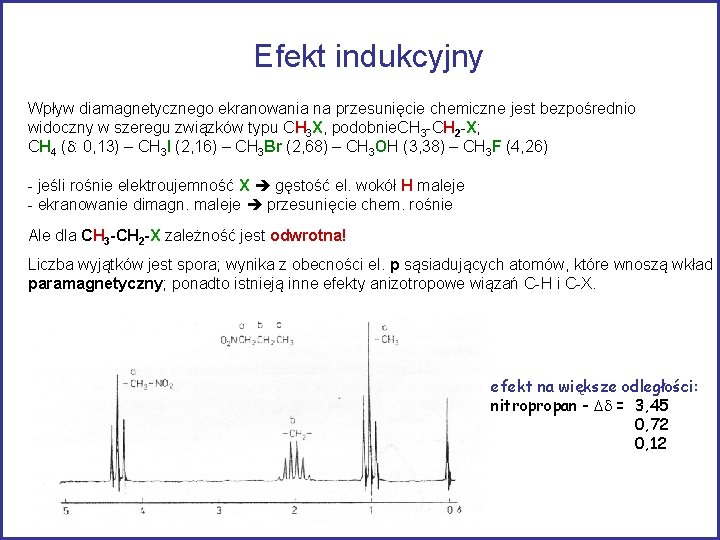
Efekt indukcyjny Wpływ diamagnetycznego ekranowania na przesunięcie chemiczne jest bezpośrednio widoczny w szeregu związków typu CH 3 X, podobnie. CH 3 -CH 2 -X; CH 4 (d: 0, 13) – CH 3 I (2, 16) – CH 3 Br (2, 68) – CH 3 OH (3, 38) – CH 3 F (4, 26) - jeśli rośnie elektroujemność X gęstość el. wokół H maleje - ekranowanie dimagn. maleje przesunięcie chem. rośnie Ale dla CH 3 -CH 2 -X zależność jest odwrotna! Liczba wyjątków jest spora; wynika z obecności el. p sąsiadujących atomów, które wnoszą wkład paramagnetyczny; ponadto istnieją inne efekty anizotropowe wiązań C-H i C-X. efekt na większe odległości: nitropropan - Dd = 3, 45 0, 72 0, 12

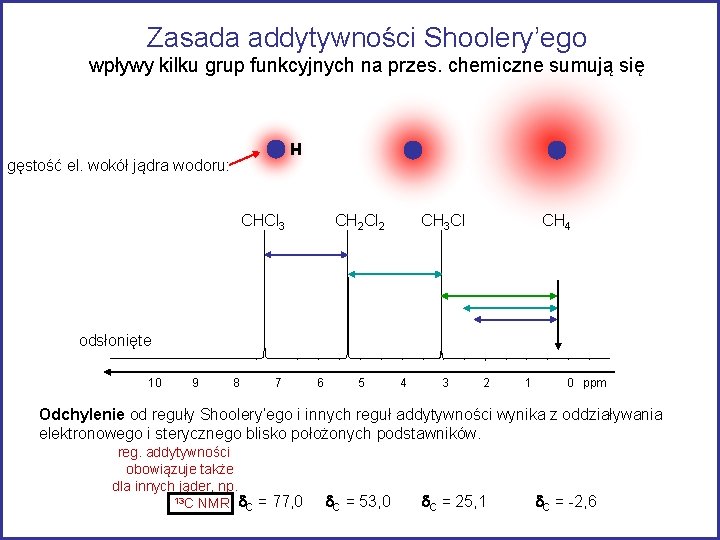
Zasada addytywności Shoolery’ego wpływy kilku grup funkcyjnych na przes. chemiczne sumują się H gęstość el. wokół jądra wodoru: CHCl 3 CH 2 Cl 2 CH 3 Cl CH 4 odsłonięte 10 9 8 7 6 5 4 3 2 1 0 ppm Odchylenie od reguły Shoolery’ego i innych reguł addytywności wynika z oddziaływania elektronowego i sterycznego blisko położonych podstawników. reg. addytywności obowiązuje także dla innych jąder, np. 13 C NMR: d = 77, 0 C d. C = 53, 0 d. C = 25, 1 d. C = -2, 6

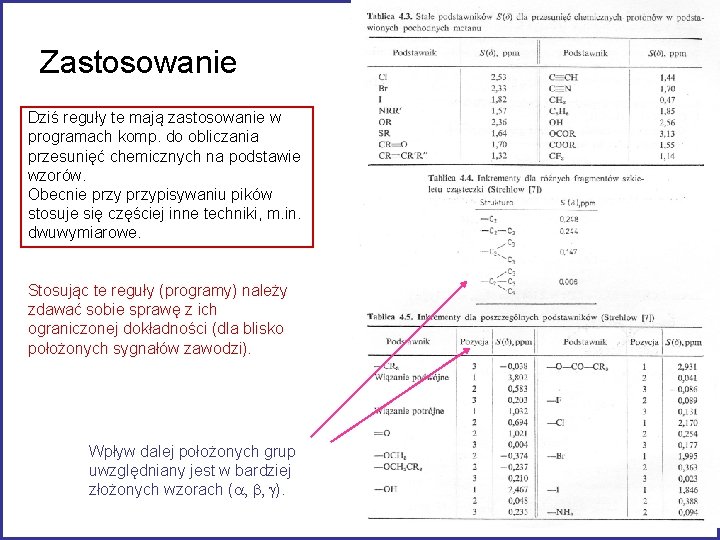
Efekt przesłaniania można rozłożyć na udziały poszczególnych atomów i grup atomów. Ilościowy wpływ podstawnika - doświadczalna stała podstawnika czyli inkrement - różnica między przesunięciem protonu w związku niepodstawionym a przesunięciem w związku podstawionym tym podstawnikiem. dla związków typu CH 2 XY oraz CHXYZ: d. H = 0, 23 + S inkr. (d. CH 4) Shooleery 1959 rok Dokładność ok. 0, 3 ppm dla CH 2 XY, gorzej dla CHXYZ. dla olefin d. H : Zcis H d. C=C-H= 5, 25 + Zgem + Zcis + Ztrans C=C Ztrans Zgem (d. C 2 H 4) różny wpływ na d w zależności od położenia: wyciąganie el. vs. donacja el. inne efekty dominują na bliskie odl. (wyciąganie indukcyjne) lub dalsze odległości (dominuje koniugacja). podstawnik Zgem Zcis Ztrans OR (R alif. ) Ar Cl F 1. 22 1. 38 1. 08 1. 54 – 1. 07 0. 36 0. 18 – 0. 40 – 1. 21 – 0. 07 0. 13 – 1. 02

Zastosowanie Dziś reguły te mają zastosowanie w programach komp. do obliczania przesunięć chemicznych na podstawie wzorów. Obecnie przypisywaniu pików stosuje się częściej inne techniki, m. in. dwuwymiarowe. Stosując te reguły (programy) należy zdawać sobie sprawę z ich ograniczonej dokładności (dla blisko położonych sygnałów zawodzi). Wpływ dalej położonych grup uwzględniany jest w bardziej złożonych wzorach (a, b, g).

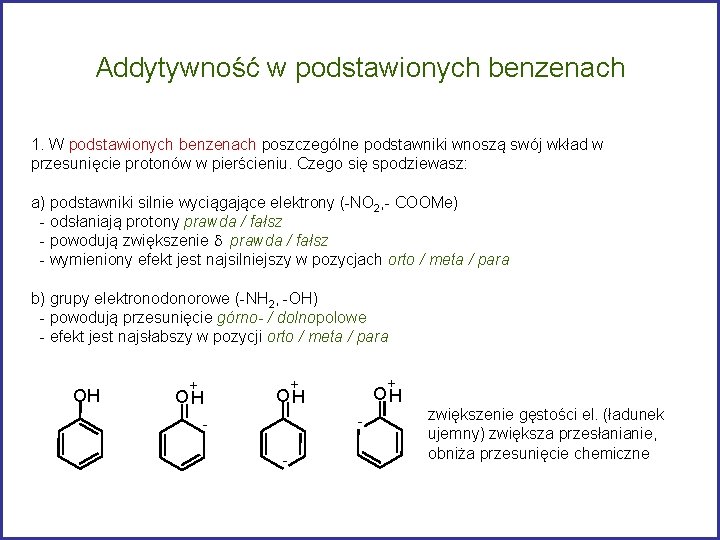
Addytywność w podstawionych benzenach 1. W podstawionych benzenach poszczególne podstawniki wnoszą swój wkład w przesunięcie protonów w pierścieniu. Czego się spodziewasz: a) podstawniki silnie wyciągające elektrony (-NO 2, - COOMe) - odsłaniają protony prawda / fałsz - powodują zwiększenie d prawda / fałsz - wymieniony efekt jest najsilniejszy w pozycjach orto / meta / para b) grupy elektronodonorowe (-NH 2, -OH) - powodują przesunięcie górno- / dolnopolowe - efekt jest najsłabszy w pozycji orto / meta / para OH + + OH OH - - zwiększenie gęstości el. (ładunek ujemny) zwiększa przesłanianie, obniża przesunięcie chemiczne

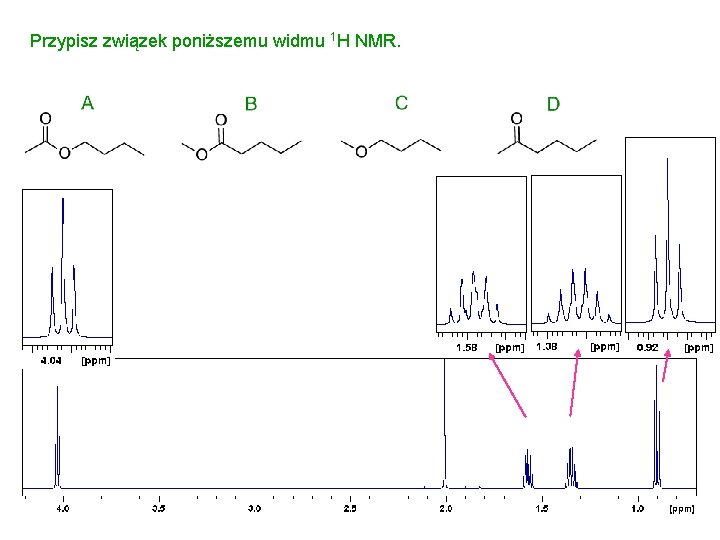
Przypisz związek poniższemu widmu 1 H NMR.

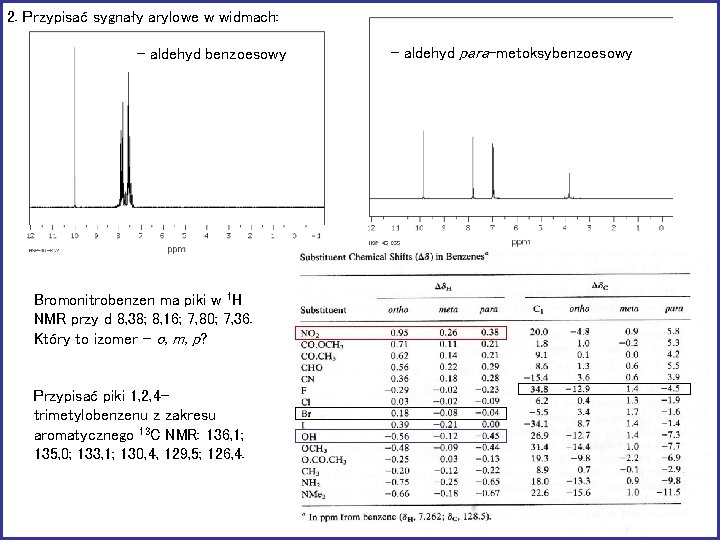
2. Przypisać sygnały arylowe w widmach: - aldehyd benzoesowy Bromonitrobenzen ma piki w 1 H NMR przy d 8, 38; 8, 16; 7, 80; 7, 36. Który to izomer - o, m, p? Przypisać piki 1, 2, 4 trimetylobenzenu z zakresu aromatycznego 13 C NMR: 136, 1; 135, 0; 133, 1; 130, 4, 129, 5; 126, 4. - aldehyd para-metoksybenzoesowy

Wkłady w stałą ekranowania 1 H: Blok = Bo-DB = (1 − s)Bo σ = σlok + σel. + σmagn. . + σW + σrozp sąsiadów 1. Lokalny - dla protonu tylko diamagnetyczny. σlok = σdia + σpara 2. Sąsiadów: a) zmiany gęstości elektronowej dzięki efektom σel i) indukcyjnemu ii) mezomerycznemu b) cyrkulacje elektronów sąsiednich grup pod wpływem pola Bo, zmieniające lokalne pole Blok. σmagn 3. Wpływ pola elektrycznego i efekty Van der Waalsa σW 4. Wpływ rozpuszczalnika σrozp

Aromatyczność

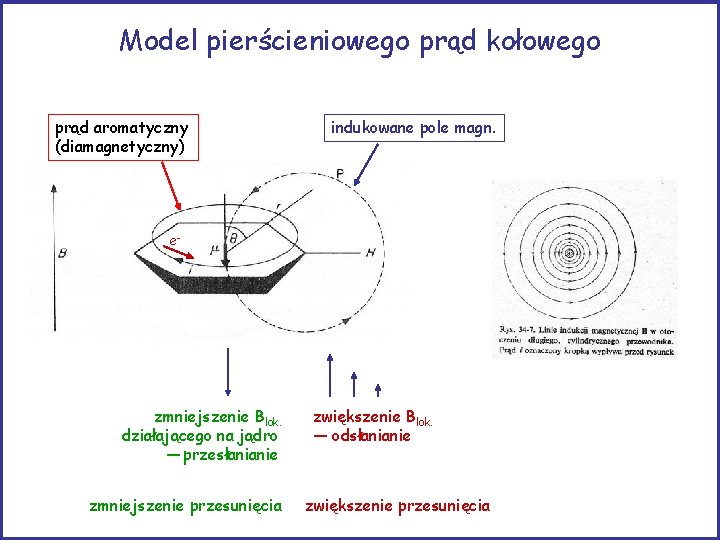
Model pierścieniowego prąd kołowego prąd aromatyczny (diamagnetyczny) indukowane pole magn. e- zmniejszenie Blok. działającego na jądro — przesłanianie zmniejszenie przesunięcia zwiększenie Blok. — odsłanianie zwiększenie przesunięcia

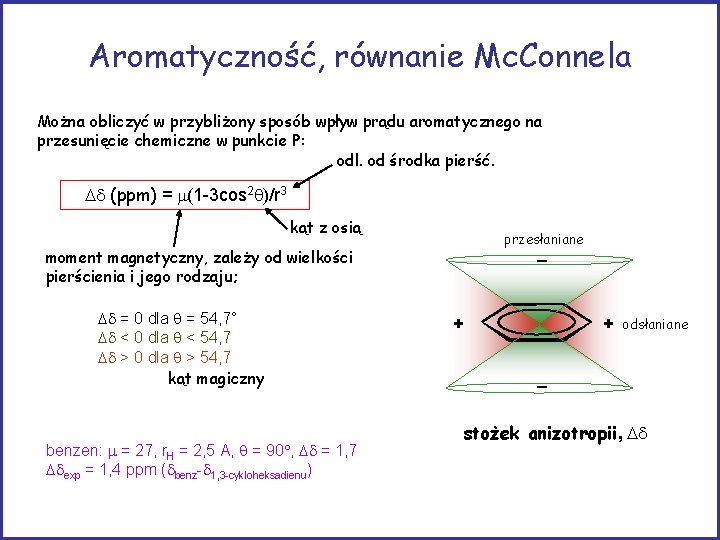
Aromatyczność, równanie Mc. Connela Można obliczyć w przybliżony sposób wpływ prądu aromatycznego na przesunięcie chemiczne w punkcie P: odl. od środka pierść. Dd (ppm) = m(1 -3 cos 2 )/r 3 kąt z osią przesłaniane _ moment magnetyczny, zależy od wielkości pierścienia i jego rodzaju; Dd = 0 dla = 54, 7° Dd < 0 dla < 54, 7 Dd > 0 dla > 54, 7 kąt magiczny benzen: m = 27, r. H = 2, 5 A, = 90 , Dd = 1, 7 Ddexp = 1, 4 ppm (dbenz-d 1, 3 -cykloheksadienu) + + odsłaniane _ stożek anizotropii, Dd

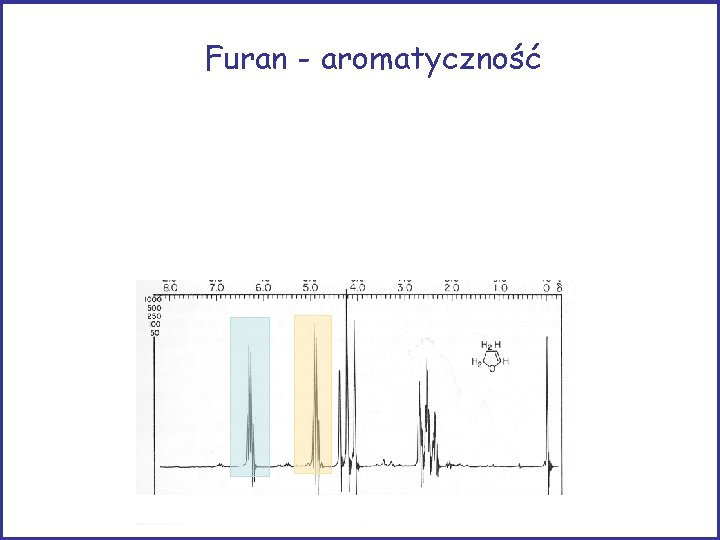
Furan - aromatyczność

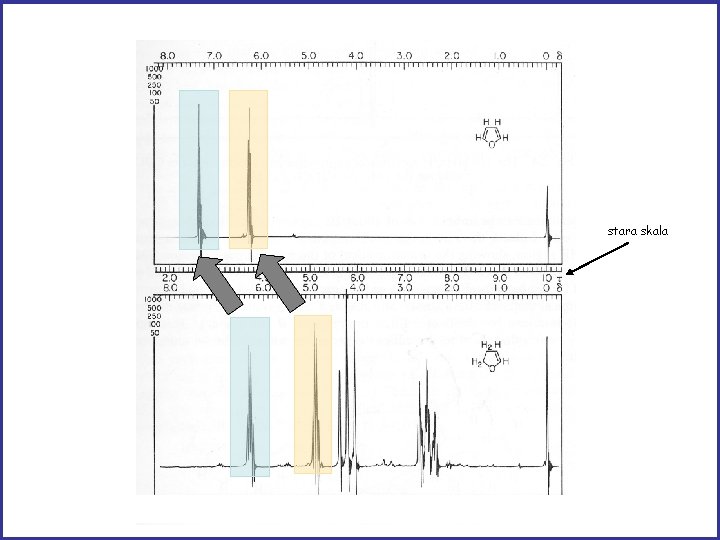
stara skala

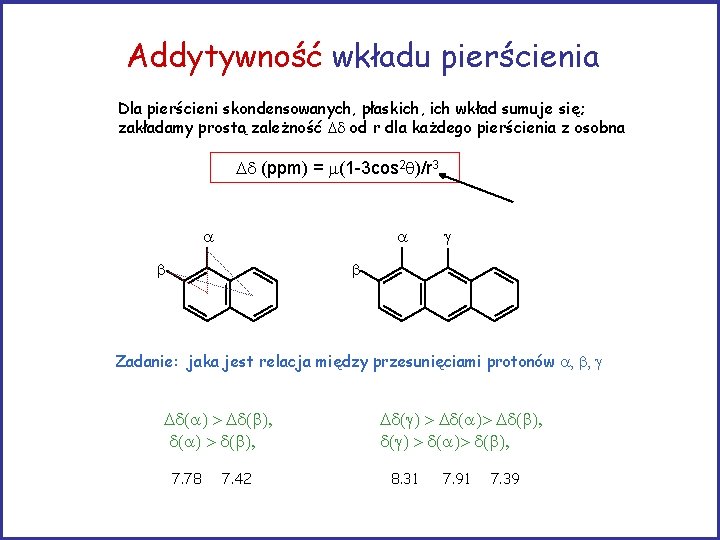
Addytywność wkładu pierścienia Dla pierścieni skondensowanych, płaskich, ich wkład sumuje się; zakładamy prostą zależność Dd od r dla każdego pierścienia z osobna Dd (ppm) = m(1 -3 cos 2 )/r 3 a a b g b Zadanie: jaka jest relacja między przesunięciami protonów a, b, g Dd(a) > Dd(b), d(a) > d(b), 7. 78 7. 42 Dd(g) > Dd(a)> Dd(b), d(g) > d(a)> d(b), 8. 31 7. 91 7. 39
![Aromatyczność przykłady 18anulen 10paracyklofan Aromatyczność - przykłady [18]-anulen [10]-paracyklofan](https://slidetodoc.com/presentation_image_h/e6de0f195f1101baefa9ae181e47b789/image-40.jpg)
Aromatyczność - przykłady [18]-anulen [10]-paracyklofan