UNIDADES DE CONCENTRACIN PARTE II 11 MO GRADO











- Slides: 16

UNIDADES DE CONCENTRACIÓN PARTE II 11 MO GRADO QUIMICA

CONCENTRACIÓN Y PROPIEDADES COLIGATIVAS §Son las propiedades que dependen de la cantidad de soluto pero no del tipo de soluto presente en una solución. §Estas son: § Disminución en la presión de vapor § Elevación en el punto de ebullición § Disminución en el punto de congelación § Presión osmótica

DISMINUCIÓN EN LA PRESIÓN DE VAPOR §La adición de un soluto no volátil a un solvente lleva a una disminución en la presión de vapor de la solución resultante en comparación con el solvente puro. §Ley de Raoult PA = P°A XA §Donde: § PA = presión parcial de la solución § P°A = presión parcial del solvente puro § XA = fracción molar del solvente

EJERCICIO A 25ºC la presión de vapor del agua es 23. 76 mm. Hg. Determine la presión de vapor a 25ºC de la solución que se prepara añadiendo 5. 67 g de C 6 H 12 O 6 (Mmolar=180 g/mol) en 25. 2 g H 2 O (Mmolar=18. 02 g/mol).

ELEVACIÓN EN EL PUNTO DE EBULLICIÓN Y DISMINUCIÓN EN EL PUNTO DE CONGELACIÓN

EJERCICIO Determine el punto de ebullición y el punto de congelación de una solución que contiene 4. 76 g de etilenglicol (Mmolar=62. 07 g/mol) en 202 g H 2 O. Kb. H 2 O = 0. 52ºC/m y Kf. H 2 O = 1. 86ºC/m

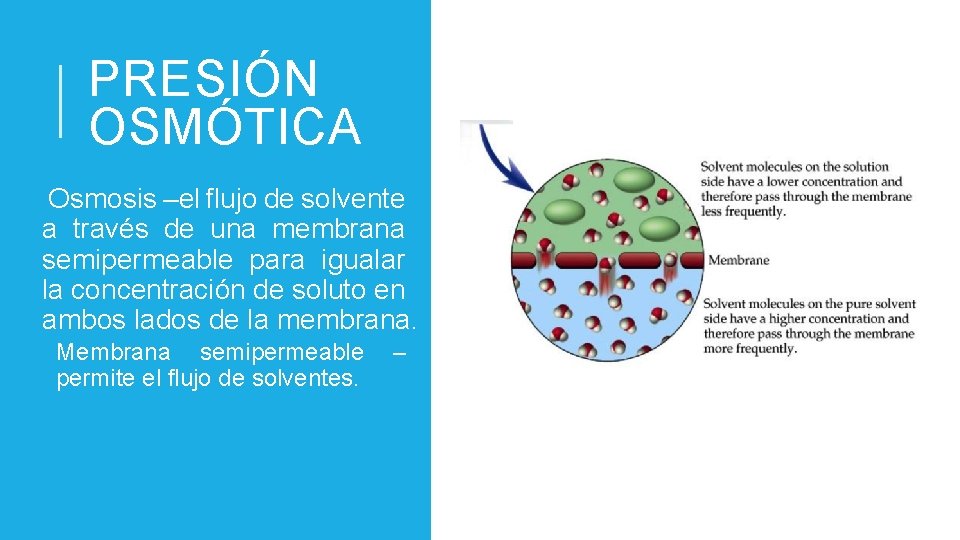
PRESIÓN OSMÓTICA §Osmosis –el flujo de solvente a través de una membrana semipermeable para igualar la concentración de soluto en ambos lados de la membrana. §Membrana semipermeable permite el flujo de solventes. –


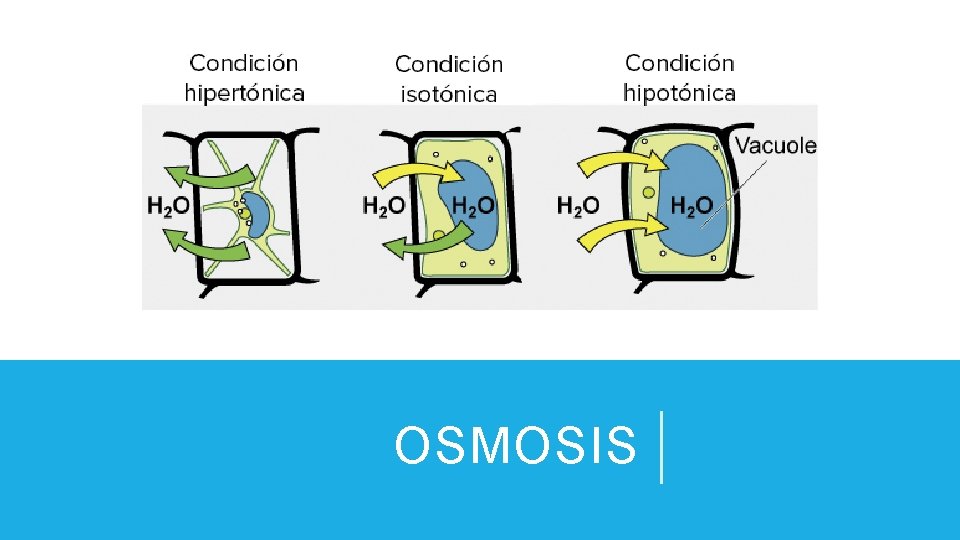
OSMOSIS

COLOIDES §Dispersión de partículas de una sustancia en otra sustancia o solución. §Dos fases: § Fase dispersa § Fase continua §Efecto Tyndall – reflejo de la luz por las partículas coloides. § Coloide hidrofílico - son coloides que se dispersan fácilmente en agua. § Coloide hidrofóbico – no son coloides que se dispersan fácilmente en agua.

TIPOS DE COLOIDES 1. Aerosol - gotas de líquido o sólido disperso en un gas. Ej. niebla, humo. 2. Emulsión - Emulsión-gotas de líquido dispersas en otro líquido o sólido. Ej. leche, mayonesa, mantequilla. 3. Sólidos - partículas sólidas dispersas en líquido o sólido. Ej. pintura, vidrio, rubí.

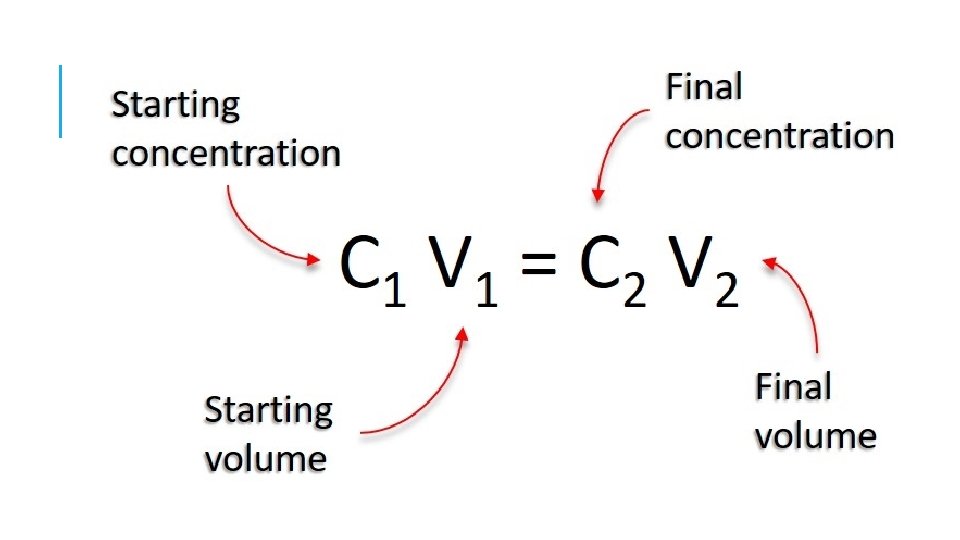
CALCULAR DILUCIONES §Utilizando conjuntos proporcionales; utilizadas para calcular un desconocido donde dos soluciones son mezclas proporcionales. §C 1 v 1 = concentración inicial y volumen inicial §C 2 V 2 = concentración final y volumen final


Step 2: Transpose for x and solve Example 2 3. Substitute Quantities If a 15 m. L dose of a product contains 300 mg of ingredient B, how much will be contained in 500 m. L ? Calculate the quantity of a concentration needed to produce a different final desired concentration and volume (a serial dilution). Method Example 1 Step 1: Use c 1/v 1= c 2/v 2 How much 10% solution is needed to make up 500 m. L of a 2% solution? Method NB: In this case we use C 1 x V 1 = C 2 x V 2 Step 2: Transpose for x and solve Step 1: Use c 1 x v 1= c 2 x v 2 2. Equivalent Strengths Converting from one measure of strength to another. Step 2: Transpose for x and solve Example 1 What is 1 part in 20 expressed as a percentage? Method Example 2 Step 1: Use c 1/v 1= c 2/v 2 How much 5% solution is needed to make up 80 ml of a 0. 4% solution? Method Step 1: Use c 1 x v 1= c 2 x v 2 Step 2: Transpose for x and solve Example 2 What is 0. 25% expressed as a ratio strength? Method Step 1: Use c 1/v 1= c 2/v 2 Step 2: Transpose for x and solve

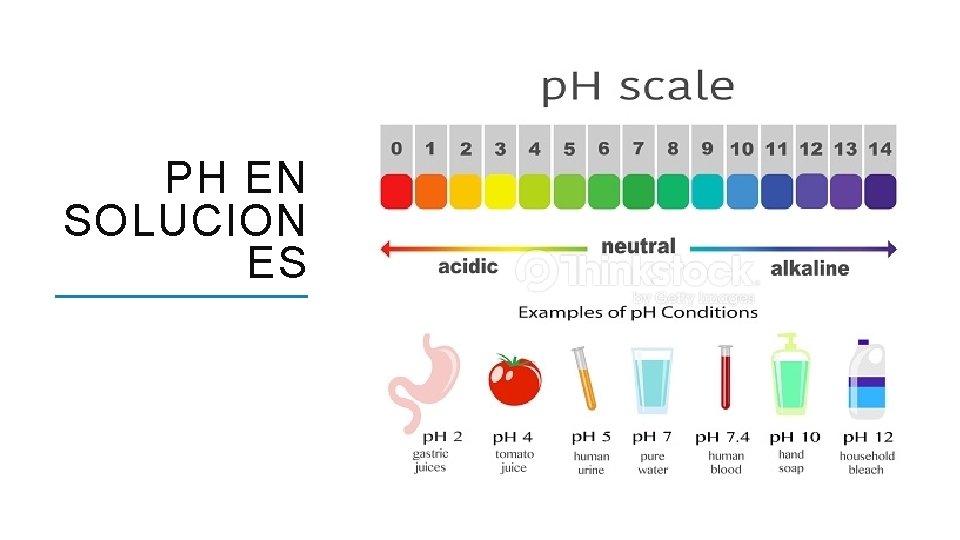
PH EN SOLUCION ES

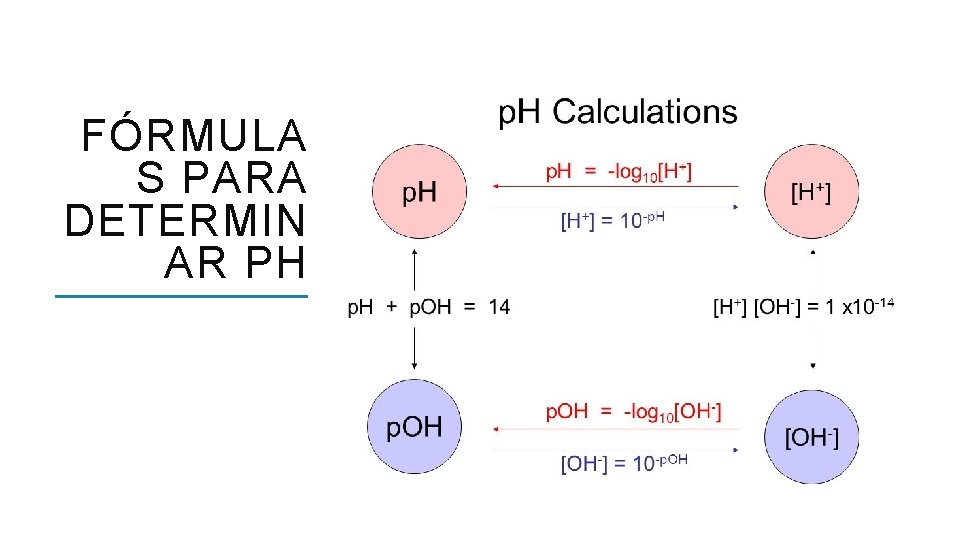
FÓRMULA S PARA DETERMIN AR PH