Semana 8 Concentracin de Soluciones Primera Parte Unidades





















- Slides: 23

Semana 8 Concentración de Soluciones -Primera Parte. Unidades Relativas: • Diluido • Concentrado • Insaturado • Sobresaturados Unidades Físicas: • Porcentaje % (p/p. v/v, p/v) • Partes por millón (ppm) • Dilución de Soluciones

UNIDADES RELATIVAS: Solución Insaturada o no saturada: Cuando un solución contiene menos soluto que el límite de solubilidad. Solución Saturada: Es una solución en el que disolvente es incapaz de solubilizar más soluto (se encuentra en el límite de solubilidad)

Solución Sobresaturada: Es aquella solución en la que la cantidad de soluto está por arriba del límite de solubilidad.

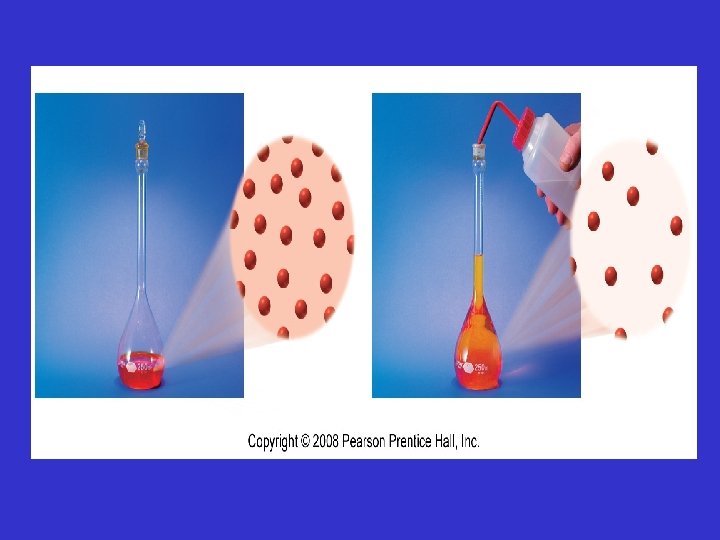
Concentrado: Una solución concentrada es aquella que contiene una cantidad relativamente grande de soluto. Diluido: Una solución diluida contiene una cantidad relativamente pequeña de soluto



concentración: Es la cantidad de solutos disueltos en una cantidad dada de disolvente o de solución.


PORCENTAJE EN MASA: %P/P Es la masa de soluto (gramos) que hay en 100 g de solución (solvente + soluto) Número de gramos de soluto en 100 g de solución. % P/P = Masa del soluto x 100 Masa de solución

Ejercicio: 1. Cúanto soluto se necesita para preparar 125 g de una solución de Na. Cl al 10% p/p 2. ¿Cuál es el % p/p de una solución que contiene 15 g de KCl disueltos en 110 g de solución? 3. ¿Cuántos gramos de solvente se necesitan agregar para preparar 100 g de solución de Ca. Cl 2 al 8% p/p?

Ejemplo: Cuál es la cantidad de gramos de soluto disuelto en 150 mililitros de una solución al 3% p/p y densidad igual a 1. 19 gr/ml Sabemos que: D=m/v

-PORCENTAJE EN VOLUMEN: 1. PORCENTAJE VOLUMEN/VOLUMEN (%V/V): Es el número de unidades de volumen de soluto por 100 unidades de volumen de solución. % v/v= Volumen del soluto x 100 Volumen de solución

Ejercicio: 1. ¿Cuál es % v/v de una solución de alcohol preparada mezclando 15. 5 ml de alcohol con agua suficiente para completar un volumen total de 200 ml? 2. ¿Cuánto alcohol hay que agregar para preparar 150 ml una solución hidroalcohólica al 16% V/V? 3. Una solución de vinagre tiene una concentración de 12% V/V de ácido acético ¿Cuánto ácido acético tiene una botella de 250 ml?

2. PORCENTAJE PESO/VOLUMEN (%P/V): Número de gramos de soluto en 100 ml de solución. % P/V = Masa del soluto x 100 Volumen de solución

Las cantidades muy pequeñas de soluto se expresan mejor como mg / dl, es usada para expresar concentraciones de solutos en sangre Ejemplo: ácido úrico : 3 a 7 mg/dl calcio : 8. 5 a 10. 3 mg/dl creatinina : 0. 7 a 1. 5 mg/dl

Ejemplo: Cuál es la cantidad en gramos de soluto disuelto en 125 gramos de una solución al 5% p/v y densidad igual a 1. 17 gr/ml. Sabemos que D=m/v

EJERCICIO: 1. ¿Cómo se prepara 100 ml de una solución de Na. Cl al 12 % p/v?

Partes por millón (ppm): Se utiliza para soluciones diluidas. Las soluciones muy diluidas, pueden expresarse también como partes por billón (ppb) Para soluciones acuosas: 1 ppm= 1 miligramo/litro (mg/L) 1 ppb= 1 microgramo/litro (μg/L) 1 ppm =1000 ppb ppm= Mg de soluto Litro

Es frecuente el uso de estas unidades para expresar niveles extremadamente bajos de sustancias tóxicas. Una concentración 1 ppm significa que hay una parte en un millón de partes.

EJERCICIO: 1. Una muestra de agua contiene 7 mg de iones sulfato en 150 ml de agua. ¿ Cuál es su concentración en ppm? 2. Calcule cuántos mg de cloruro hay en 1. 5 litros de agua que tiene 1. 2 ppm 3. 4 litros de agua contienen 12 ppm de hipoclorito Cl. O- ¿ Cuántos gramos de Cl. O - tiene la muestra?


Dilución: Proceso de añadir solvente a una solución con el objeto de disminuir su concentración. Se puede calcular la concentración final de la dilución a partir de las concentración y volumen inicial y del volumen final. C 1 x V 1 = C 2 X V 2

1. Calcule cuantos ml de HCl concentrado 14% p/v se necesitan para preparar 125 ml de una solución de HCl 3. 5% p/v. 2. Cual sería el % p/v de una solución que se preparó diluyendo 25 ml de una solución 58 % p/v, hasta un volumen de 150 ml